Реферат Бутадиен. Реферат по дисциплине Химия и технология основного органического и нефтехимического синтеза
 Скачать 138.01 Kb. Скачать 138.01 Kb.
|
|
Федеральное государственное бюджетное образовательное учреждение высшего образования «Казанский национальный исследовательский технологический университет» (ФГБОУ ВО «КНИТУ») Кафедра «Технология основного органического и нефтехимического синтеза» Реферат по дисциплине «Химия и технология основного органического и нефтехимического синтеза» на тему «Бутадиен» Выполнил: Магистр кафедры ТООНС, группы 417-М11 Ишмухаметова Л.А. Казань 2017 Содержание Введение……………………………………………………………………….…3
Список использованной литературы………………………………………..…15 Введение Бутадиен-1,3 (дивинил) СН2=СН—СН=СН2 – бесцветный газ с характерным неприятным запахом с темп. кип. 268,59 К. Бутадиен – типичный диеновый углеводород с сопряженными двойными связями, легко полимеризуется и сополимеризуется со стиролом, нитрилами или эфирами акриловой или метакриловой кислот, винил- и метилвинилпиридинами, винил- и винилиденхлоридами, изобутиленом, изопреном и др. Бутадиен является основным мономером, применяемым в современном промышленном производстве синтетических каучуков. На бутадиене базируется производство подавляющего большинства синтетических каучуков общего назначения: стереорегулярные 1,4,-цис-бутадиеновые, бутадиен-стирольные, бутадиен-метилстирольные, ряд синтетических каучуков специального назначения – бутадиен-нитрильные, бутадиен- метилвинилпиридиновые и др. Помимо производства синтетических каучуков, бутадиен применяется в промышленном масштабе для производства синтетических смол, адиподинитрила (в производстве полиамидов) и себациновой кислоты.
Бутадиен-1,3 (дивинил) C4 H6 представляет собой при обычных условиях бесцветный газ, конденсирующийся в жидкость при 268,7 К (-4,3°С), с температурой кипения -4,4°С, температурой плавления - 108,9°С и плотностью в жидком состоянии 0, 645 т/м3 (при 0°С). Не растворим в воде, плохо растворим в спиртах, хорошо — в бензоле, диэтиловом эфире, хлороформе; с некоторыми растворителями образует азеотропные смеси. Критическая температура бутадиена 152°С. С воздухом бутадиен образует взрывчатые смеси с пределами воспламеняемости 2,0 и 11,5% об. Температура вспышки бутадиена составляет -40°С, температура самовоспламенения 420"С. Бутадиен легко полимеризуется: nC4H6→[-CH2-CH=CH-CH2-]n Полимеризация инициируется пероксидами, образующимися при контакте бутадиена с воздухом. Тепловой эффект полимеризации зависит температуры и составляет от 72, 8 до 125,6 кДж/моль. Вследствие этого бутадиен хранится в присутствии ингибиторов, например, п-оксидифениламина или п-трет-бутилпирокатехина, которые удаляются промывкой гидроксидом натрия перед полимеризацией. При радикально-цепной сополимеризации бутадиена со стиролом, а-метилстиролом или акрилонитрилом образуются сополимеры, в макромолекуле которых беспорядочно чередуются звенья исходных веществ. Бутадиен в высоких концентрациях обладает наркотическим действием; в малых концентрациях раздражает дыхательные пути и слизистую оболочку глаз. ПДК составляет 100 мг/м3 .
Бутадиен является основным мономером, применяемым в современном промышленном производстве синтетических каучуков. На бутадиене базируется производство подавляющего большинства синтетических каучуков общего назначения: стереорегулярные 1,4,-цис-бутадиеновые, бутадиен-стирольные, бутадиен-метилстирольные, ряд синтетических каучуков специального назначения – бутадиен-нитрильные, бутадиен- метилвинилпиридиновые и др. Помимо производства синтетических каучуков, бутадиен применяется в промышленном масштабе для производства синтетических смол, адиподинитрила (в производстве полиамидов) и себациновой кислоты.
Впервые дивинил был получен французским химиком Ж.Б. Каванту в 1862 году пиролизом сивушного масла. Первое промышленное производство его в СССР было организовано по методу Лебедева из этилового спирта. Этим методом является каталитическое превращение этилового спирта. Он был открыт в 1931 году. Метод Лебедева был заложен в основу промышленного синтеза дивинила в нашей стране. Однако в настоящее время данный метод не находит широкого применения. В 1949 году В. Реппе открыл метод получения бутадиена-1,3 взаимодействием ацетилена с формальдегидом. С 1940 года начались исследования метода получения дивинила каталитическим дегидрированием н-бутана и н-бутилена Н.Д. Зелинским и А.А. Баладиным, впоследствии успешно внедренного в практику. Одностадийное дегидрирование н-бутана освоено с 1947 года. В 1980 году в Перми построили установку по выделению бутанов и пентанов из попутных нефтяных газов. Эта установка позволяет получать 50% дивинила из нефтяного сырья.
На первых заводах синтетического каучука, построенных в Советском Союзе еще в начале 30-х годов, бутадиен получали по способу С.В. Лебедева путем каталитического разложения этилового спирта. На основе этого процесса в СССР впервые в мире было создано промышленное производство синтетического каучука. Процесс проводили в одну стадию: 2C2H5OH → C4H6 + H2 +2H2O – 84,8 кДж Из уравнения видно, что суммарная реакция представляет собой сочетание конденсации, дегидрирования и дегидратации. Этим требованиям отвечает предложенный Лебедевым полифункциональный окисный катализатор, обеспечивающий протекание реакции получения дивинила в одну стадию с технически приемлемым выходом. Превращение этанола складывается из следующих реакций: Дегидрирование спирта в ацетальдегид: CH3CH2OH → CH3CHO + H2 Конденсация ацетальдегида в альдольм с последующим отщеплением воды и образованием кротонового альдегида: 2CH3CHO → CH3CH(OH)CH2CHO →CH3CH = CHCHO + H2O Восстановление карбонильной группы кротонового альдегида с использованием молекулы этанола в качестве гидрирующего агента (последний при этом превращается в ацетальдегид): CH3CH = CHCHO + C2H5OH → CH3CH = CHCH2OH + CH2CHO Дегидратация кротилового спирта, сопровождающаяся образованием сопряженной системы двойных связей: CH3CH = CHCH2OH →CH2 = CH-CH = CH2 + H2O Превращение спирта в бутадиен протекает при 360-380°С на неподвижном оксидном катализаторе. В качестве побочных продуктов образуются органические соединения различных классов: углеводороды, спирты, эфиры, альдегиды и др. Теоретический выход бутадиена составляет 58,7%, однако, вследствие протекания побочных реакций он обычно бывает несколько ниже, но остается близким к теоретическому. Основным недостатком процесса является низкая селективность. Достоинство способа - сравнительная простота аппаратурного оформления технологического процесса. В настоящее время этот процесс в основном потерял промышленное значение.
Первая стадия процесса получения бутадиена заключается в каталитическом гидрировании 35% - го водного раствора бутиндиола до 1,4 – бутиленгликоля при 180 - 2000С и 280 атм. Катализатором служит смесь 90% никеля, 9% меди и 1% хрома на силикагеле. В трубе, рассчитанной на высокое давление, при 2600С и 70 атм можно осуществить отщепление воды от бутиленгликоля (в водном растворе) под действием свободной фосфорной кислоты. При последующей перегонке под давлением почти с количественным выходом получается 94%-ный тетрагидрофуран – очень хороший растворитель. Его недостатками являются: относительно легкое окисление на воздухе с образованием перекиси и главным образом недостаточная физиологическая безвредность. Затем при 260-2700С в присутствии водяного пара и фосфата натрия(катализатор) на коксе или кусковом графите от тетрагидрофурана снова отщепляют воду; в результате получается бутадиен. Его можно получать и непосредственно отщеплением двух молекл воды от 1,4 – бутиленгликоля в присутсвии фосфорнокислого катализатора, но при этом протекают побочные реакции и получаются худшие выходы, чем при двухступенчатом процессе. 
Производство бутадиена из углеводородов С4 методам каталитического дегидрирования является основным направлением в современной технологии получения бутадиена. Дегидрирование н-бутана до бутадиена-1,3 представляет обратимый гетерогенно-каталитический процесс, протекающий с поглощением тепла через стадию образования изомеров бутилена по схеме:  В промышленности используют различные технологические варианты получения бутадиена дегидрированием углеводородов С4. Применяемые процессы можно условно разделить на следующие группы: дегидрирование бутана в бутены, дегидрирование бутенов; одностадийное и двухстадийное дегидрирование бутана в бутадиен. Характерной особенностью реакций дегидрирования с образованием олефинов является ограничение степени превращения условиями равновесия. Реакции дегидрирования всегда являются эндотермическими и, следовательно, равновесие в сторону образования ненасыщенных углеводородов должно сдвигаться с повышением температуры. Степень превращения углеводородов возрастает с повышением температуры и понижением давления. На практике при температурах выше 773-823 К даже в отсутствие катализаторов предельные углеводороды претерпевают реакции изомеризации, крекинга и др. Поэтому процесс дегидрирования бутана проводят при температурах до 923-973 К, т.е. при температурах более низких, чем термодинамические оптимальные. Применение катализаторов позволяет достигнуть высокой скорости процесса при относительно низкой температуре, когда еще не существенен вклад побочных реакций. Ввиду обратимости реакций дегидрирования – гидрирования и, следовательно, способности катализаторов ускорять обратимые реакции в обоих направлениях, эти реакции катализируются одними и теми же соединениями. При дегидрировании вследствие отщепления водорода всегда происходит увеличение объема газа, и понижение давления благоприятствует повышению степени конверсии. По этой причине процессы дегидрирования проводят при давлении, близком к атмосферному, а в некоторых случаях процесс осуществляют в вакууме. Иногда вместо применения вакуума предпочтительнее разбавлять реакционную массу газом, инертным в условиях реакции, или паром, что также приводит к снижению парциальных давлений реагентов и возрастанию равновесной степени конверсии. Снижение парциального давления позволяет также понизить температуру реакции и, следовательно, уменьшить образование побочных продуктов. Важным параметром при проведении реакции дегидрирования является время контакта реакционной смеси с катализатором. Работы по каталитическому дегидрированию н-бутана по двухстадийному варианту: н-бутан → н-бутен → бутадиен были начаты в США в 1920-х годах. В Советском Союзе фундаментальные исследования в этой области проводили С.В. Лебедев, Н.И. Шуйкин, А.А. Баландин, Б.А. Казанский и др.
Одностадийный процесс дегидрирования алканов C4H10 ↔ C4H6 + 2H2 + ∆H, ∆H= 247 кДж имеет очевидные преимущества перед двухстадийным процессом ввиду отсутствия необходимости разделения газовых смесей после каждой стадии и более низких энерго и капитальных затрат. 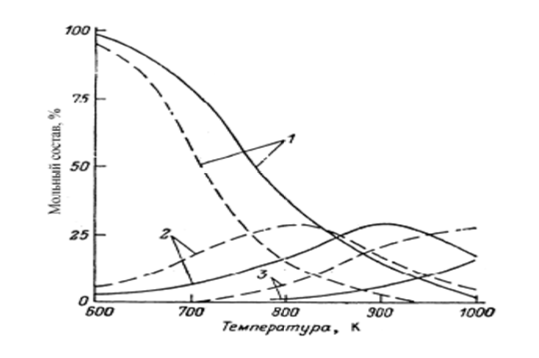 Рис. 2 - Зависимость состава равновесной смеси при дегидрировании бутана в бутены и бутадиен от температуры и давления. Сплошные линии - 0,1 МПа, штриховые-0,01 МПа. 1 – бутан; 2 – бутены; 3 – бутадиен Термодинамические расчеты показывают, что равновесный выход диена существенно возрастает с повышением температуры и с уменьшением парциального давления алкана. Поскольку повышение температуры связано с потерей селективности реакции, одностадийное получение диенов из алканов было реализовано в условиях вакуумного дегидрирования. В одностадийном процессе дегидрирования используют алюмохромовые катализаторы, содержащие 18-30% оксида хрома. Фирма « Гудри» (США) впервые реализовала процесс получения бутадиена из бутана в одну стадию (аналогично процессу получения изопрена из изопентана). В присутствии алюмохромового катализатора протекают побочные превращения бутана, бутенов и бутадиена. Применение алюмохромового катализатора исключает использование водяного пара в качестве разбавителя.
Большинство промышленных установок получения дивинила из бутана работает по двухстадийной схеме. Первая стадия дегидрирования бутана заключается в превращении его в бутилен, а вторая - это процесс получения дивинила из бутилена дегидрирование бутана в бутилен на хромо-оксидном промотированном катализаторе, нанесенном на оксид алюминия, протекает по реакции: С4Н10 ↔ С4Н8+Н2; ΔН= 131 кДж. В промышленных реакторах протекают и побочные реакции: обратная реакция гидрирования бутилена, крекинг бутана и бутилена, изомеризация бутана и бутилена, реакции углеобразования. На советских промышленных установках по дегидрированию бутана применяют системы с кипящим слоем мелкозернистого алюмохромового катализатора марки К-5. В процессе дегидрирования бутана катализатор покрывается углеродистыми отложениями и изменяет свой химический состав. Активность катализатора при этом резко снижается. С целью реактивации катализатор непрерывно отводят из реактора и обжигают в токе воздуха в регенераторе с кипящим слоем. Углеродистые соединения при этом выгорают, а низшие оксиды хрома окисляются до Сr2О3. Дегидрирование бутилена до дивинила протекает на хром-кальций-фосфатном катализаторе по реакции: С4Н8 ↔ С4Н6 + Н2, ΔН= 119 кДж. Бутадиен при повышенных температурах разлагается, поэтому для сохранения достаточно высокой селективности по бутадиену на практике приходится прибегать к снижению парциального давления реакционных газов за счет применения перегретого водяного пара или вакуума. Оптимальная температура сырья на входе в реактор 860-910К. Двухстадийный процесс позволяет создать на каждой стадии оптимальные условия ее протекания, обеспечивающие максимальный выход продуктов и селективность. Для проведения первой стадии широко используются аппараты кипящего слоя. Такие аппараты отличаются целым рядом преимуществ в сравнении с аппаратами, в которых катализатор неподвижно располагается на нескольких тарелках:1)изотермичность слоя, которая достигается благодаря активному перемешиванию; 2) текучесть слоя, в результате которой появляется возможность транспортировки закоксованного катализатора из реактора в регенератор и обратно; 3) высокая поверхность межфазного обмена, обусловленная малым размером частиц катализатора, в результате высокие скорость теплообмена и массопередачи; 4) низкое гидравлическое сопротивление слоя, обеспечивающее уменьшение энерго затрат и повышающее скорость процесса. Таким образом, в конструкции реактора КС соблюдены все закономерности проведения гетерогенно-каталитических реакций. Процессы дегидрирования и регенерации осуществляются в разных аппаратах одинаковой конструкции. В отличие от первой, вторая стадия протекает в адиабатических реакторах с неподвижным слоем катализатора. Необходимое для реакции тепло подводится с перегретым паром, смешиваемым с сырьем. Достоинство этих аппаратов простота конструкции, недостатки неравномерность распределения температуры в слое, высокое гидравлическое сопротивление аппарата, ухудшение показателей эффективности работы реактора по мере закоксовывания катализатора, периодичность работы аппарата, попеременно работающего то в режиме дегидрирования, то в режиме регенерации. Стадия осуществляется при более высокой температуре и пониженном парциальном давлении, которое достигается при разбавлении бутенов водяным паром. Температура для разных типов катализатора колеблется от 580 до 677 , разбавление паром в соотношении 20:1. Охлаждение контактного газа (закалка) осуществляется впрыскиванием водяного конденсата, дальнейшее охлаждение газа происходит в котле-утилизаторе, затем газ направляется на промывку в скруббер и далее на разделение. Выход бутадиена от массы исходного бутена составляет 20-35%. Селективность колеблется от 73 до 94 %. Достоинствами одностадийного процесса дегидрирования н-бутана до бутадиена-1,3 являются: значительное сокращение расхода технологического пара; использование теплоты регенерации катализатора и проведение реакции дегидрирования в адиабатическом режиме и, как следствие, простота конструкции реактора и отсутствие сложного теплообменного оборудования; исключение второй стадии дегидрирования и операций разделения бутанбутиленой фракции. За счет этого относительно невысокие выход бутадиена-1,3 (12-14%) и степень конверсии н-бутана (не превышающая 0,2) компенсируются меньшими капитальными затратами и энергоемкостью производства и, как следствие, более низкой, чем в двухстадийном методе, себестоимостью бутадиена-1,3. Соответственно, проанализировав выше написанное, можно увидеть, что метод двухстадийного дегидрирования бутана энергоемкий и требует сложной технологической схемы. Для промышленной реализации это невыгодно, так как потребуются значительные энергозатраты. Поэтому появилась необходимость поиска альтернативного способа дегидрирования. Оказалось, что этот процесс может быть осуществлён и по одностадийной схеме, хотя термодинамика процесса устанавливает четкий предел выхода целевого продукта. Но при повышении температуры и понижении давлении можно достичь хороших результатов и по этой схеме. В данной статье как вариант решения проблемы рассмотрен способ дегидрирования под вакуумом, изобретенным в США в фирме Гудри. Как оказалось, данный метод имеет ряд преимуществ и дает хороший выход продукта. Для увеличения выхода целевых продуктов, увеличения селективности и снижения материальных затрат, необходимо проведение дальнейших исследований влияния глубины вакуума на процессы дегидрирования бутанов и бутиленов.
Основное направление потребления бутадиена в России – производство каучуков различных марок (дивинилстирольные, бутадиеннитрильные, полибутадиеновые и др.); незначительное количество бутадиена используется в производстве акрилонитрилбутадиенстирольных пластиков (АБС-пластиков), дивинилстирольных термоэластопластов, латексов. Практически каждый крупный производитель имеет собственную сырьевую базу на основе фракционирования. Процессы, разработанные для получения бутадиена как целевого продукта, - это дегидрирование бутана или бутена, а также выделение бутадиена из фракции С4 крекинг-газов (БДФ). Основные производители бутадиена методом выделения целевого продукта – ОАО «Нижнекамскнефтехим», ОАО «Омский каучук», ООО «Тольяттикаучук» и ЗАО «Каучук» (г. Стерлитамак). Метод дегидрирования бутана внедрен на двух предприятиях в России – в ОАО «Тобольский НХК» и ООО «НКНХ-Дивинил». Реализованная технология, несмотря на свою историческую зрелость, крайне востребована на российском рынке. Обусловлено это двумя основными факторами: устойчивой тенденцией роста производства сжиженных газов – сырьевой базой, и положительной тенденцией роста производства синтетических каучуков – потребителей бутадиена. Таким образом, «НКНХ-Дивинил» является не только производителем одного из ключевых мономеров в нефтехимическом ряду «сжиженные газы» – резины, но и значительным потребителем (до 175 тыс. т/год) бутана нормального. Кроме того, технологические мощности установок ЦГФУ, входящих в состав «Нижнекамскнефтехима», позволяют осуществлять выделение целевого вида сырья (бутана нормального) из фракций бутана технического и др. В 2007 году в России было произведено 404,1 тыс. т бутадиена: 54% по методу одностадийного дегидрирования н-бутана, 46% - извлечением из пиролизной фракции. В 2009 г было выработано 409,7 тыс. т, а в 2011, за счет увеличения мощностей практически на всех российских предприятиях удалось достигнуть значения 483,9 тыс.т/г бутадиена. Но даже при такой выработке ежегодный дефицит бутадиена в 2012 году составляло около 200 тыс.т/г, что сказалось на производстве всех видов бутадиенсодержащих продуктов. В условиях сложившегося сырьевого кризиса в индустрии бутадиена цены на бутадиен выросли более чем в 2 раза. Цена реализации бутадиен – 1,3 производства ОАО «Тобольск-Нефтехим» по состоянию на март 2012 г. составляла не менее 100 тыс. руб./тонна. Остальные российские производители не имели товарной выработки бутадиена, весь получаемый ими продукт расходовался на собственное потребление.
За рубежом широко применяют процессы получения бутадиена из н-бутана и/или бутан-бутиленовой фракции, а изопрена - из изопентана и/или изопентанизоамиленовой фракции, что является процессом каталитического дегидрирования углеводородов - процессом «Катадиен» фирмы-разработчика «Air Products and Chemicals» (США). Модификации процесса «Катадиен» проведены фирмой «ABB Lummus Crest» (США). Наибольшими мощностями в 2003 г. обладали следующие страны (тыс. т/г.): США - 2592, Япония - 1012, Китай - 768, Южная Корея - 724, Германия - 505, Франция - 420. Крупнейшим заводом бутадиена в мире является предприятие фирмы «Хантсман» в г. Хьюстон (США) - 544 тыс. т. в год. Ожидается, что в течение 2001-2006 гг. в Северо-Восточной Азии войдет в строй свыше 580 тыс. т новых мощностей.
Очищенная бутановая фракция из сепаратора 9 поступает в испаритель 10. Пары углеводорода перегреваются сначала в пароперегревателях 8 до 2750С, а затем – трубчатой печи 2 – до 530 – 5500С. Из печи перегретые пары бутана при давлении 1,5 ат направляются в реактор 7 с кипящим слоем катализатора. Дегидрирование проводят при 580 С. Для достижения этой температуры из регенератора 6 в реактор непрерывно подают катализатор, нагретый до 640 — 650°С. Температуру в реакционной зоне регулируют, изменяя кратность циркуляции катализатора (обычно кратность циркуляции колеблется в пределах 14—20). Таким образом, в данном процессе катализатор является и теплоносителем. Контактные газы из реактора, пройдя пароперегреватели 8 и испарители 10, промываются водой в скруббере 11 и охлаждаются. В сепараторе 13 контактный газ отделяют от тяжелых углеводородов и направляют на разделение. Отработанный катализатор на выходе из нижней части реакторатобрабатывают азотом для десорбции углеводородов. По пневмотранспортной трубе мелкозернистый катализатор с помощью воздуха направляют в регенератор б. В регенераторе углистые отложения на поверхности катализатора выжигаются кислородом воздуха в кипящем слое. Однако тепла, выделяющегося при сгорании углистых отложений, недостаточно для подогрева катализатора до требуемой температуры (≈650° С). Поэтому в регенератор через форсунки вводят топливный газ, при сгорании которого выделяется дополнительное тепло. Регенерированный катализатор проходит десорбер, где продувается бутаном для удаления адсорбированного кислорода и дополнительного восстановления шестивалентного хрома в трехвалентный. Для этих целей расходуют от 3 до 5% подаваемого на процесс бутана; бутан из десорбера используют как топливо, подаваемое на сжигание в регенератор. Физическое тепло отходящих из регенератора газов используют в котле—утилизаторе 5 для получения водяного пара. Катализаторная пыль, увлекаемая газами из регенератора, увлажняется в аппарате 4 и оседает в электрофильтре 3. 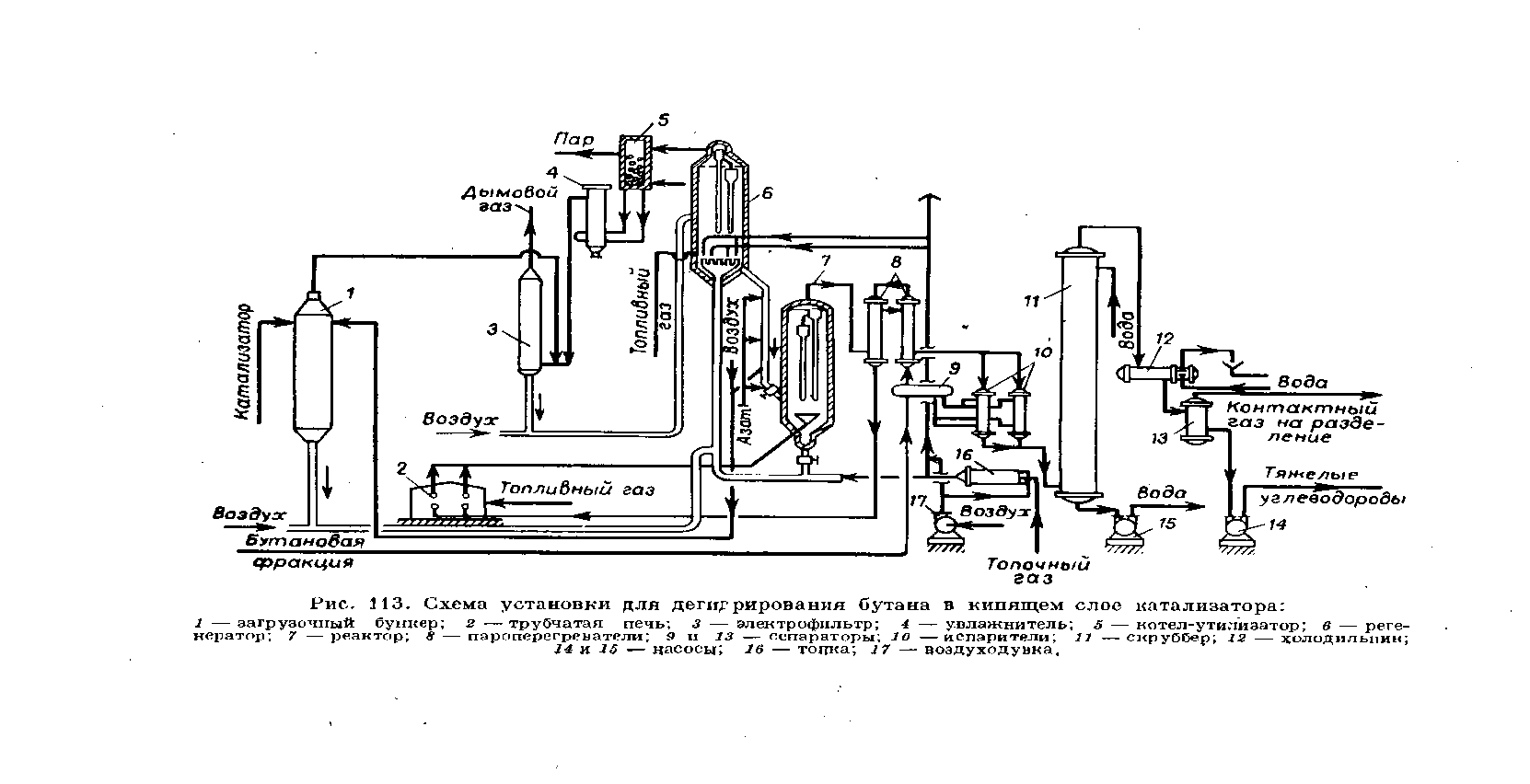 Список использованной литературы
|
