теория горения и взрыва. Решение Дано Запишем уравнение реакции горения бензола Количество бензола составит
 Скачать 66.47 Kb. Скачать 66.47 Kb.
|
|
Определить объем воздуха, необходимого для сгорания 15 кг бензола (С6Н6) при температуре 100С и давлении 730 мм. Рт. Ст. Решение Дано: 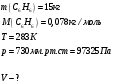 Запишем уравнение реакции горения бензола: 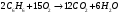 Количество бензола составит: 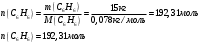 Тогда для сгорания 15 кг бензола необходимо количество кислорода: 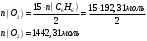 Масса кислорода составит: 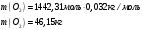 Поскольку в воздухе кислород составляет только 23,15%, то масса воздуха составит: 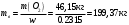 И на основании уравнения Менделеева-Клапейрона можно рассчитать объем воздуха при Т = 283 К и давлении 97325 Па: 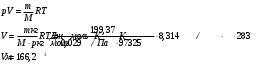 Ответ: объем воздуха для сгорания 15 кг бензола составит 166,2 м.куб. Определить низшую теплоту сгорания сухого газа общего состава: 40% [CH4], 20% [C2H6], 20% [CO], 20% [C2H4]. Решение Дано: 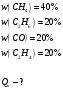 Допустим нам дано 1 м. куб. газа. Тогда в нем будет содержаться 400 л метана CH4, 200 л этана C2H6, 200 л СО и 200 л C2H4. Тогда количества этих газов составят: 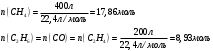 Запишем уравнения горения и энтальпии процессов горения отдельных газов. Запишем уравнение горения метана в кислороде воздуха: 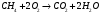 Вычислим значение изменения энтальпии реакции горения метана: 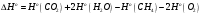 Тогда: 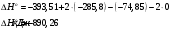 Тепловой эффект горения 1 моля метана равен: 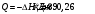 Для этана уравнение примет вид: 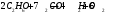 Энтальпия сгорания этана составит: 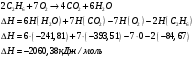 Для СО уравнение горения примет вид: 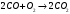 Энтальпия процесса равна: 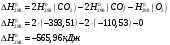 Для этена уравнение горения примет вид: 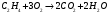 А энтальпия процесса составит: 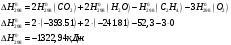 Тогда в данном случае мы получим, что теплота сгорания газов составит: 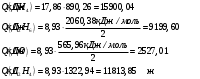 Суммируем теплоты: 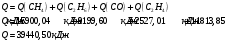 В результате вычисления видно, что низшая теплота сгорания 1 м.куб смеси газов составит: 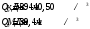 Ответ: 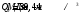 . . |
