психология. Решение Определяем общую массу пленочного покрытия. 134343,312г 130430,4г 3912,912г
 Скачать 134.05 Kb. Скачать 134.05 Kb.
|
|
ФЦ-С-О-171В Манагаров Юрий Аблякимова Диана Задача 4 Определить массу покрытия на одну таблетку, если 434768 шт. таблеток тикагрелор таблетки, покрытые пленочной оболочкой, средняя масса таблетки без покрытия составила 130430,4г., а после покрытия 134343,312 г. Решение 1. Определяем общую массу пленочного покрытия. 134343,312г - 130430,4г = 3912,912г 2. Определяем массу пленочного покрытия на одну таблетку. 3912,912г/434768шт = 0,009г 3. Рабочая пропись (для 200кг таблеток готового продукта) Рабочая пропись Состав 1 таблетки без оболочки:
Состав оболочки:
Материальный баланс Состав таблеток «Тикагрелол» · Тикаглерол 60 · Маннитол 84 · Кальция гидрофосфат 42 · Карбоксиметилкрахмал натрия 6 · Гипролоза 6 · Магния стеарат 2 200=60+84+42+6+6+2 Красх=200/193=1.03 Nтех.выхода=193/200*100%=96,5% Тикаглерол 1,03=x/60 x=61,8 Маннитол 1,03=x/84 x=86,52 Кальция гидрофосфат 1,03*42= 43,26 Карбоксиметилкрахмал натрия 1,03*6=6,18 Гипролоза 1,03*6= 6,18 Магния стеарат 1,03*2=2,06
Спецификация Таблетки покрыты пленочной оболочкой желтого цвета, круглые, двояковыпуклые. Вспомогательные вещества: маннитол, кальция гидрофосфат, карбоксиметилкрахмал натрия, магния стеарат Фармакологическое действие антиагрегатное Показания: профилактика атеротромбических осложнений у взрослых, инфаркт миокарда Побочные эффекты: кровотечение, отдышка, головокружение, обморок Блок – схема согласно технологического процесса 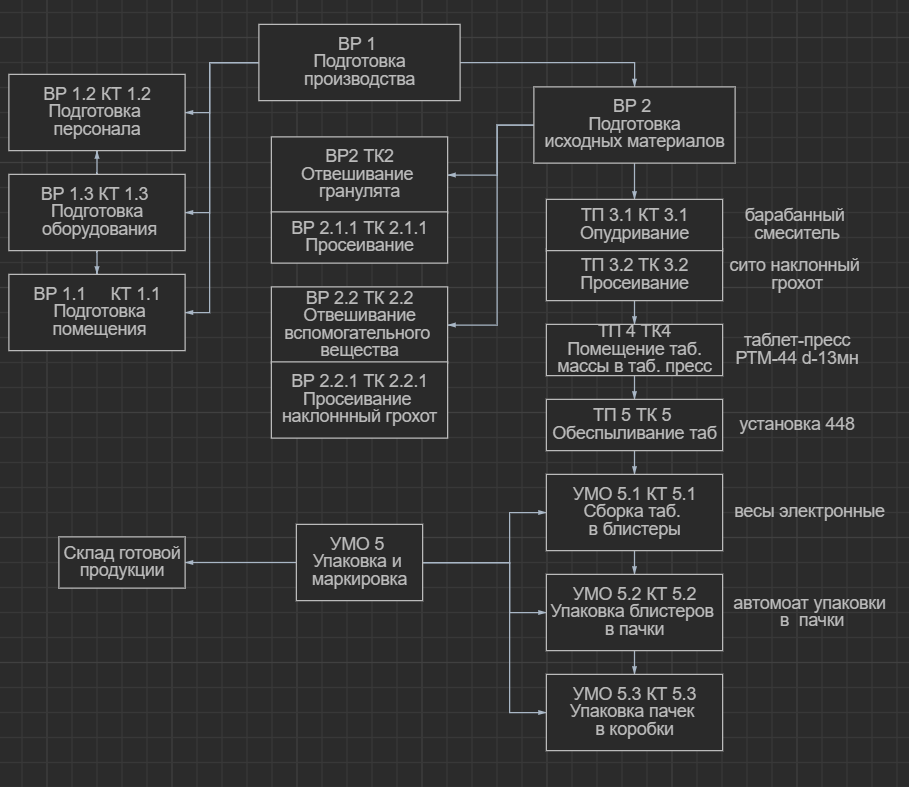 Указать, возможность избирательной растворимости таблеток в желудке или кишечнике. Таблетки в пленочной оболочке — распространенная позиция аптечного ассортимента. Пленочные покрытия регулируют скорость абсорбции биологически активных веществ, позволяют совмещать в одной таблетке несовместимые вещества. Они обеспечивают избирательную растворимость таблеток в желудке или кишечнике. Покрытие сохраняет физические, химические и механические свойства таблеток. Оболочка защищает таблетки от истирания и поддерживает первоначальные геометрические параметры, форму и маркировку. Пленочные покрытия бывают растворимыми в воде, желудочном соке, содержимом кишечника и нерастворимыми. Водорастворимые покрытия улучшают внешний вид лекарственной формы, корригируют вкус и запах. Они предохраняют таблетки от механических повреждений, однако не защищают от влаги, которая содержится в воздухе. Водорастворимые и растворимые в желудочном соке покрытия исчезают в желудке за 10-30 минут. Кишечнорастворимые покрытия выдерживают воздействие желудочного сока в течение 2-4 ч. Но в нейтральной и щелочной среде кишечника их диссоциация занимает не более часа. Растворимые в кишечнике пленочные покрытия предохраняют слизистую оболочку желудка от раздражающего действия лекарственных веществ и демонстрируют выраженный влагозащитный эффект. Меняя полимеры и толщину пленки, фармакологи добиваются распада таблетки в определенном отделе кишечника. Лекарство доходит до места назначения и только там освобождается от оболочки и всасывается. Пленочные покрытия регулируют скорость абсорбции биологически активных веществ, позволяют совмещать в одной таблетке несовместимые вещества. Тикагрелор характеризуется линейной фармакокинетикой; экспозиция тикагрелора и активного метаболита (AR-C124910XX) примерно пропорциональна дозе вплоть до 1260 мг. После приема внутрь тикагрелор быстро абсорбируется со средним значением Tmax примерно 1.5 ч. Формирование основного циркулирующего в крови метаболита AR-C124910XX (также активного) из тикагрелора происходит быстро со средним Tmax примерно 2.5 ч. После приема натощак тикагрелора в дозе 90 мг Сmах составляет 529 нг/мл, AUC - 3451 нг×ч/мл. Средняя абсолютная биодоступность тикагрелора составляет 36%. Прием жирной пищи не влияет на Сmах тикагрелора или AUC активного метаболита, но приводит к повышению на 21% AUC тикагрелора и снижению на 22% Сmах активного метаболита. Эти небольшие изменения имеют минимальную клиническую значимость; поэтому, тикагрелор можно назначать вне зависимости от приема пищи. Связывание с белками плазмы тикагрелора и его активного метаболита высокое (> 99%). Vd тикагрелора в равновесном состоянии составляет 87.5 л. CYP3A4 является основным изоферментом, отвечающим за метаболизм тикагрелора и формирование активного метаболита, и их взаимодействия с другими субстратами CYP3А варьируют от активации до ингибирования. Тикагрелор и активный метаболит являются слабыми ингибиторами Р-гликопротеина. Основным метаболитом тикагрелора является AR-C124910XX, который также активен, что подтверждается результатами оценки связывания с Р2Y12 АДФ-рецептором тромбоцитов in vitro. Системная экспозиция активного метаболита составляет примерно 30-40% от экспозиции тикагрелора. Основной путь выведения тикагрелора - печеночный метаболизм. При введении меченного изотопом тикагрелора в среднем примерно 57.8% радиоактивности выделяется с калом, 26.5% - с мочой. Выведение тикагрелора и активного метаболита с мочой составляет менее 1% дозы. В основном активный метаболит выводится с желчью. Средний T1/2 тикагрелора и активного метаболита составлял 7 и 8.5 ч соответственно. Средняя биодоступность препарата у пациентов-азиатов на 39% выше, чем у европеоидов. Биодоступность тикагрелора на 18% ниже у пациентов негроидной расы по сравнению с больными европеоидной расы. Экспозиция тикагрелора и активного метаболита примерно на 20% ниже у пациентов с тяжелой почечной недостаточностью (КК <30 мл/мин) по сравнению с пациентами с нормальной функцией почек. Стах и AUC тикагрелора были на 12% и 23% выше у пациентов с печеночной недостаточностью легкой степени по сравнению со здоровыми добровольцами. Не проводились исследования тикагрелора у пациентов с умеренной или тяжелой печеночной недостаточностью. Расписать условия, регулирование скорости адсорбции лекарственных веществ Скорость абсорбции зависит от: • пути введения лекарственного препарата, • состояния центральной гемодинамики, • состояния регионарного кровотока, • физико-химических свойств самого препарата. Распределение ЛС определяется: • скоростью кровотока и степенью кровоснабжения тканей; • степенью связывания препарата с белками плазмы; • растворимостью в липидах; • способностью депонироваться в жировых или других депо; • скоростью метаболизма и выведения; • выделением из организма (почками, печенью, легкими, с калом). • Хорошо васкуляризированные ткани: мозг, сердце, печень, почки, эндокринные железы – составляют около 10% массы тела, доля сердечного выброса около 75%. • Мышцы, кожа – составляют около 50% МТ, доля сердечного выброса около 19%. • Жировая ткань – составляет около 20% МТ, доля сердечного выброса около 6%. • Слабо васкуляризированные: кости, связки, хрящи – составляют около 20% МТ, доля сердечного выброса 0%. •препараты с кислой и основной реакцией находятся в плазме в ионизированной и неионизированной формах, это соотношение зависит от рН и определяется уравнением Хендерсона-Хассельбаха; • только неионизированная форма препарата способна проникать через липидные мембраны клеток или растворяться в жировых соединениях, поэтому именно ее считают активной диффундирующей фракцией Связывание с белками плазмы Лекарственные вещества поступая в кровь связываются с белками плазмы, главным образом с альбуминами, в меньшей степени с кислыми альфагликопротеинами и липопротеидами. Связанная с белком форма не способна диффундировать в органы и ткани и, следовательно, оказывать фармакологический эффект. Для связывания характерно насыщение! Указать в ответе, возможность совмещения в одной лекарственной форме несовместимых лекарственных веществ. Одним из преимуществ пленочных покрытий является возможность совмещения в одной лекарственной форме несовместимых лекарственных веществ. Расписать условия, сохранение физических, химических и механических свойств ядер таблеток при нанесении пленочных покрытий. Сохранение физических, химических и механических свойств ядер таблеток при нанесении пленочных покрытий – одно из преимуществ, которое осуществляется при соблюдении условий нанесения пленочных покрытий. Пленочное покрытие незначительно увеличивает массу таблеток. Благодаря применению летучих органических растворителей, исключается длительная стадия сушки оболочек. Написать, возможность сохранение первоначальных геометрических параметров таблеток, их формы, маркировки, фирменных обозначений. Сохранение первоначальных геометрических параметров таблеток, их формы, маркировки, фирменных обозначений можно добиться, используя тонкую (порядка 0,05— 0,2 мм) оболочку, образующую на таблетке после высыхания нанесенного на ее поверхность раствора плёнкообразующее вещество (пленочное покрытие) Дать пояснение о возможности, уменьшения массы объема пленочного покрытия по сравнению с дражировочным. Дражированная таблетка состоит из таблетки-ядра, содержащей лекарственное вещество и покрытия, содержащего комплекс вспомогательных веществ. Таблетка-ядро должна быть механически прочной. Это обусловлено тем, что на таблетку при дражировании действуют четыре фактора: суммарная масса таблеток, зависящая от величины загрузки котла (с увеличением загрузки и скорости вращения котла возрастает возможность разрушения таблеток); свободное падение таблеток с верхней точки вращающегося котла на нижнюю (эта сила прямо пропорциональна массе таблеток и высоте, с которой они падают); кинетическая энергия вращающихся таблеток в котле (таблетка не просто произвольно падает, а создается вращательный момент, сила которого зависит от массы таблетки и скорости вращения котла); расклинивающий эффект жидкостей, применяемых при дражировании. Таблетки, подлежащие дражированию, не должны иметь плоскую форму, во избежания их возможного слипания. Расписать, возможность автоматизации процесса покрытия, интенсификации производства и сокращение производственных площадей. Разработка методов нанесения оболочек на таблетки путем прессования,а также использование ряда других технологических принципов, значительно расширили проблему таблетирования и открыли пути для совершенствования таблеток как лекарственной формы и создания новых препаратов пролонгированного действия. |
