Физико-химические и металлургические процессы при обработке материалов КПЭ”. Исходные данные для задания. Решение Сталь 20Х2Н4 Si 0,27 содержание кремния Mn 0,45 содержание марганца
 Скачать 35.72 Kb. Скачать 35.72 Kb.
|
|
Исходные данные для задания:
Решение: Сталь 20Х2Н4 Si = 0,27 % - содержание кремния Mn = 0,45 % - содержание марганца Cr = 1,45 % - содержание хрома Cu = 0,3% - содержание меди Ni = 3,45 % - содержание никеля Fe = 94 % - содержание железа Расчет температуры кипения сплава Tкип при давлении среды Pс = 0,01 Па, Pс = 1 Па и Pс = 105 Па; Данную температуру можно получить из уравнения Клайперона – Клазиуса: 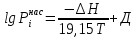 где 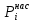 – упругость насыщенного пара, Па; – упругость насыщенного пара, Па; 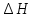 – энергия испарения, Дж/моль; – энергия испарения, Дж/моль;19,15T=2,3RT=2,3  8,31 8,31 T, Дж/моль T, Дж/моль К; Д – коэффициент К; Д – коэффициентТ – температура, К. Для существования пузырька нужно, чтобы упругость насыщенного пара в нём была не менее суммы давлений: 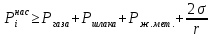 где Piнас – упругость насыщенного пара; 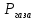 – давление газа; – давление газа;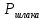 – давление шлака; – давление шлака; 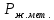 – металлостатическое давление; – металлостатическое давление;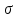 – поверхностное натяжение; – поверхностное натяжение; 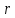 – радиус поры. – радиус поры. Процесс кипения возможен, если выполняется данное неравенство. Давление насыщенного пара определяется температурой. Ввиду того, что у нас электронно-лучевая сварка, то 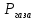 = = 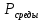 ; ; 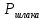 =0 (сварка электронным лучом не требует наличия флюса или другого шлака в качестве защитной среды); =0 (сварка электронным лучом не требует наличия флюса или другого шлака в качестве защитной среды); 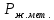 =0, так как наши свариваемые детали имеет толщину =2 мм; а =0, так как наши свариваемые детали имеет толщину =2 мм; а 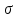 и и 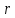 можно пренебречь из-за слишком маленьких размеров данных параметров. можно пренебречь из-за слишком маленьких размеров данных параметров. Итого имеем Расчет при Pс = 0,01 Па 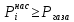 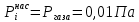 Значит, можем рассчитать температуру кипения 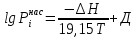 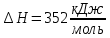 , Д = 10,847 для Fe; , Д = 10,847 для Fe;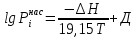 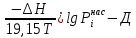  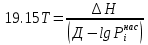 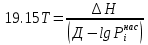 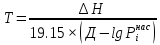 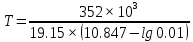 = 1431 K = 1431 KTкип = 1431 К 2) Расчет при Pс = 1 Па 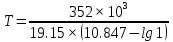 = 1695 K = 1695 KTкип = 1695 К 3) Расчет при Pс = 105 Па 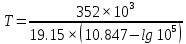 = 3144 K = 3144 KTкип = 3144 К Расчет энтальпии Нi сплава во всем интервале температур существования сплава в жидком состоянии. Расчет приведен для железа, хрома и никеля, поскольку остальные элементы практически не вносят вклад в теплоемкость ввиду их низкого содержания в сплаве. 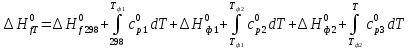 f – индекс, указывающий на образование вещества. Для чистых элементов при температуре 298 К 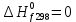 Теплоемкость при постоянном давлении обычно представляют в виде степенного ряда 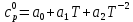 Используем табличные данные для теплоемкости и приращения энтальпии при фазовых превращениях из справочников 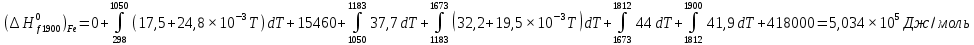 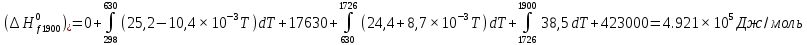 Рассчитать при заданной температуре энтальпию образования 35ХГ2 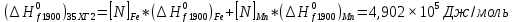 Расчет состав сплава в мольных долях 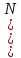 Где, ni – количество моль данного компонента, Ai – атомный вес, где gi – массовая доля i-го компонента. Распишем атомные весы и массовые доли для каждых составляющих элементов стали: Si: 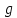 = 0.27, A=28.085; = 0.27, A=28.085; Mn: 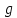 = 0.45, A= 54.938; = 0.45, A= 54.938; Cr: 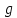 = 1.45, A=51.996; = 1.45, A=51.996; Cu: 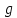 = 0.3, A=63.546; = 0.3, A=63.546;Ni: 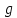 = 3.45, A=58.693; = 3.45, A=58.693; Fe: 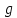 = 94, A=55.845; = 94, A=55.845;Значения атомных весов каждого из элементов взяты из таблицы химических элементов Дмитрия Ивановича Менделеева. 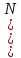 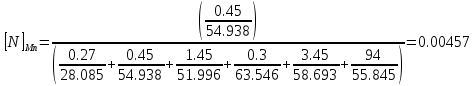 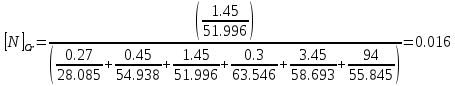 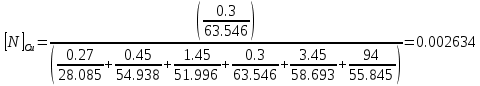 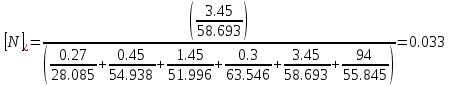 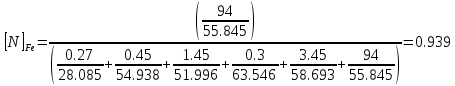 Проведём расчёт упругости насыщенного пара каждого компонента по уравнению Клайперона-Клазиуса при температуре плавления Tпл , 1.3 Tпл , Tкип Оно применительно к равновесию системы «конденсат – пар» для области небольших давлений, далеких от критических. При некоторых допущениях и с учетом аппроксимации опытных данных получено уравнение для определения равновесного давления пара над чистым элементом при различной температуре. Расчеты при Tпл 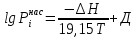 Si: 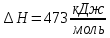 , Д = 12.681, Т=1811 К: , Д = 12.681, Т=1811 К: 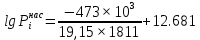 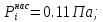 Mn: 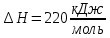 , Д = 9.98, Т=1811 К , Д = 9.98, Т=1811 К 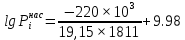 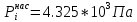 ; ; Cr: 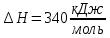 , Д = 11.309, Т=1811 К: , Д = 11.309, Т=1811 К: 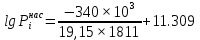 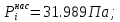 Сu:  , Д = 10.587, Т=1811 К: , Д = 10.587, Т=1811 К: 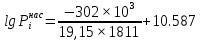 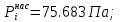 Ni: 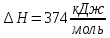 , Д = 11.174, Т=1811 К: , Д = 11.174, Т=1811 К: 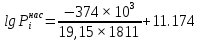 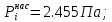 Fe: 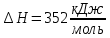 , Д = 10.847, Т=1811 К: , Д = 10.847, Т=1811 К: 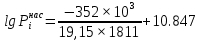 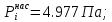 Расчеты при 1.3 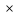 Tпл Tпл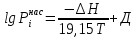 Si: 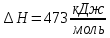 , Д = 12.681, Т=2354 К: , Д = 12.681, Т=2354 К: 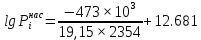 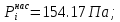 Mn: 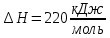 , Д = 9.98, Т=2354 К: , Д = 9.98, Т=2354 К: 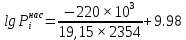 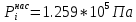 ; ; Cr: 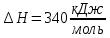 , Д = 11.309, Т=2354 К: , Д = 11.309, Т=2354 К:  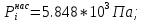 Сu:  , Д = 10.587, Т=2354 К: , Д = 10.587, Т=2354 К:  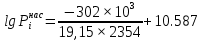 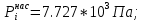 Ni: 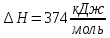 , Д = 11.174, Т=2354 К: , Д = 11.174, Т=2354 К: 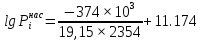 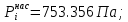 Fe: 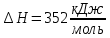 , Д = 10.847, Т=2354 К: , Д = 10.847, Т=2354 К: 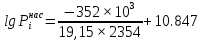 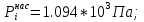 Расчеты при Ткип 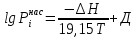 Si: 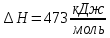 , Д = 12.681, Т=3135 К: , Д = 12.681, Т=3135 К: 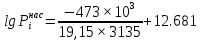 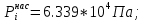 Mn: 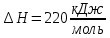 , Д = 9.98, Т=3135 К: , Д = 9.98, Т=3135 К: 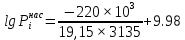 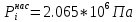 ; ; Cr: 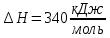 , Д = 11.309, Т=3135К: , Д = 11.309, Т=3135К: 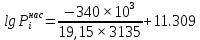 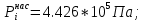 Сu:  , Д = 10.587, Т=3135 К: , Д = 10.587, Т=3135 К: 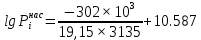 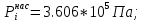 Ni: 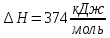 , Д = 11.174, Т=3135 К: , Д = 11.174, Т=3135 К: 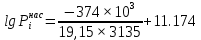 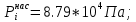 Fe: 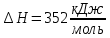 , Д = 10.847, Т=3135 К: , Д = 10.847, Т=3135 К: 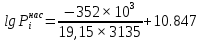 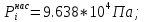 Расчёт давления пара каждого компонента над раствором по уравнению Рауля: Расчет давления паров над жидкостью можно произвести по закону Рауля: давление пара любого компонента идеального раствора (растворителя сильноразбавленного раствора) в условиях равновесия равно произведению давления насыщенного пара этого компонента на его мольную долю в концентрате: 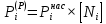 где 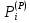 – давление пара компонента i над раствором (парциальное давление); – давление пара компонента i над раствором (парциальное давление); 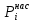 – упругость насыщенного пара чистого компонента; – упругость насыщенного пара чистого компонента;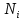 – мольная доля компонента i. – мольная доля компонента i. 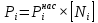 Давление, которое оказывает компонент газовой смеси, называется парциальным, Pi Si: 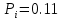 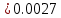 = 0.0003 Па; = 0.0003 Па; Mn: 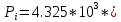 0.0045 = 19.4625 Па; 0.0045 = 19.4625 Па;Cr: 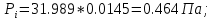 Cu: 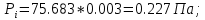 Ni: 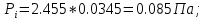 Fe: 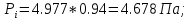 Расчет мольной доли в паре каждого компонента 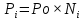 => => 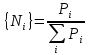 Общее давление смеси газов равно сумме парциальных давлений компонентов: 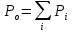 – закон Дальтона – закон Дальтона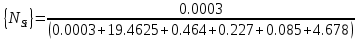 = 1.474*10-5 ; = 1.474*10-5 ; 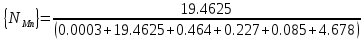 = 0.956; = 0.956; 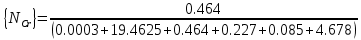 = 0.023; = 0.023;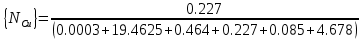 = 0.011 = 0.011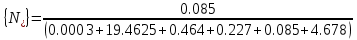 4.176*10-3; 4.176*10-3;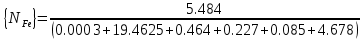 = 5.601*10-3 = 5.601*10-3Расчет летучести компонентов сплава f: 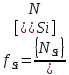 = =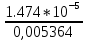 = 2.748*10-3 = 2.748*10-3 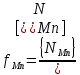 = =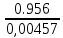 = 209.19 = 209.19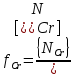 = =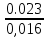 = 1.438 = 1.438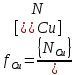 = =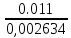 = 4.176 = 4.176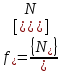 = =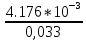 = 0.127 = 0.127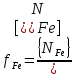 = =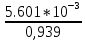 = 5.965*10-3 = 5.965*10-3Расчет плотности энергии q0: 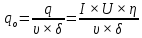 , ,где q0 – плотность энергии, Дж/см2; q – эффективная тепловая мощность, Вт; υ – скорость сварки, см/с; δ – толщина пластины, см; I – ток сварки, А; U – ускоряющее напряжение, В; η – эффективный КПД при ЭЛС. V = 36 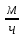 = 0,778 = 0,778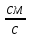 ; ;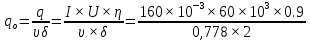 = 5553 = 5553 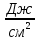 ; ; Расчет размеров зоны термического влияния b1 при заданных параметрах источника теплоты: b1 – часть ширины, зависящая от теплофизических свойств материала, плотности энергии источника теплоты, скорости источника теплоты, толщины пластины. 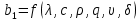 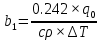 cρ = 3.622 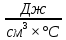 - объёмная теплоёмкость - объёмная теплоёмкость 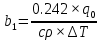 = = 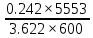 = 0.618 см; = 0.618 см; Выбор коэффициента K’2 в соответствие с механическими свойствами обрабатываемых материалов: 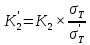 Для определения 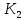 используем таблицу только при σт=180 МПа, используем таблицу только при σт=180 МПа,
К2 = 0.21 Для 35ХГ2 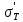 =1080 Мпа =1080 Мпа 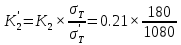 = 0.035 = 0.035Расчет размерного параметра b2: 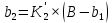 , где , где В-полуширина пластины. 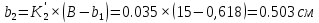 Определение ширины зоны пластических деформаций bпл 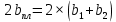 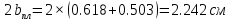 Определение площади зоны пластических деформаций 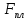 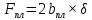 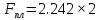 = 4.484см2; = 4.484см2; Расчет значений реактивных напряжений 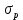 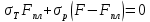 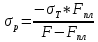 , , где σт – предел текучести; F – площадь поперечного сечения пластины; Fпл – площадь зоны пластической деформации. 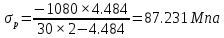 Определение деформаций 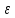 и расчет укорочения пластины и расчет укорочения пластины 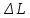 : : 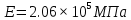 – модуль упругости для 35ХГ2 – модуль упругости для 35ХГ2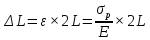 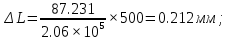 Пластина укоротилась на 0.212 мм 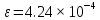 | ||||||||||||||||||||||||||||||||||||||||||