Решение Существенное влияние на скорость коррозии оказывает концентрация растворенного в среде кислорода. Кислород может выступать либо в роли пассиватора, либо в роли деполяризатора.
 Скачать 30.62 Kb. Скачать 30.62 Kb.
|
|
ВУЗ Вид работы По дисциплине «» Тема/Вариант «» Выполнил: ФИО ___________________ Рецензент: ФИО ___________________ подпись___________________ г. 2022 1. Влияние концентрации растворенного кислорода на скорость коррозии. Решение Существенное влияние на скорость коррозии оказывает концентрация растворенного в среде кислорода. Кислород может выступать либо в роли пассиватора, либо в роли деполяризатора. Если кислород выступает в роли пассиватора, то сначала скорость коррозии возрастает из-за потерь металла вызванного образованием окисной пленки, а затем при некоторой концентрации кислорода, когда вся поверхность покроется окисной пленкой, скорость коррозии будет падать. Если кислород выступает в роли деполяризатора, то скорость коррозии будет расти по линейной зависимости с увеличением количества растворенного кислорода. Источником кислорода в подавляющем большинстве случаев является воздух. Кислород может оказывать положительное и отрицательное влияние на скорость коррозии. Растворенный кислород в электролитах, выступающий в качестве деполяризатора, усиливает коррозионное разрушение, причем скорость коррозии возрастает по линейной зависимости с ростом концентрации растворенного кислорода. Если же кислород выступает в роли пассиватора, то прямая зависимость наблюдается до тех пор, пока слишком высокая концентрация кислорода не приводит к пассивации поверхности металла, после чего происходит снижение скорости коррозии. На рисунке 1 показана зависимость скорости коррозии железа от концентрации растворенного в воде кислорода. Из графика видно, что при малых и средних концентрациях кислорода скорость коррозии резко возрастает, а при больших концентрациях понижается вследствие образования защитных пленок. Следует отметить, что кислород способствует уменьшению числа коррозионных центров на поверхности металла, на которых может возникнуть коррозионный процесс, но вместе с тем увеличивает скорость коррозии в точке, начавшей корродировать. 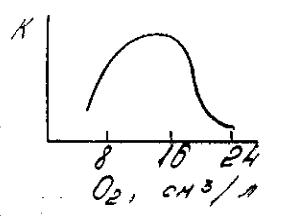 Рис. 1 — Зависимость скорости коррозии железа от концентрации кислорода в воде 2. При окислении меди с кислородом с образованием оксида CuO положительный массовый показатель составит K+m = 9,8 мг/(м2*ч). Рассчитать отрицательный массовый показатель К-m. Решение 3. Определить удовлетворяют ли условиям сплошности пленка CuS на меди, если плотность Cu = 8,95 г/см3, а его сульфида 4,6 г/см3. Решение 4. В кислой среде (рН = 4) контактируют никель и железо. Написать уравнения электродных процессов, рассчитать ЭДС и энергию Гиббса образовавшегося гальванического элемента. Решение 5. На основании ниже приведенных данных: - определить закон роста пленки на металле; - найти уравнение зависимости толщины пленки от времени окисления; - привести примеры металлов, окисляющихся по этому закону.
Решение 6. Найти энергию активации окисления металла в следующем интервале температур:
|
