Контрольная 9 вариантrd. Решение Вычисляем 0 х р. и S 0 х р. для первой реакции со(г) зн 2 (г) сн 4 (г) Н
 Скачать 172.68 Kb. Скачать 172.68 Kb.
|
9. На основании стандартных теплот образования и абсолютных стандартных энтропии соответствующих веществ вычислите ∆G0298 реакций, протекающих по уравнениям: СО(г) + ЗН2(г) = СН4(г) + Н2О(г) N2 (г) + 3Н2(г) = 2NH3(г). Возможна ли эта реакция при стандартных условиях? Решение Вычисляем 0х.р. и S0х.р. для первой реакции: СО(г) + ЗН2(г) = СН4(г) + Н2О(г)
Изменение энтальпии: 0х.р. = (f0CН4 + f0Н2О) – (3f0Н2+ f0 CО) 0х.р.= [(–74,5) +(–241,82)] – [(–110,5) + 3·0] = –205,82 кДж < 0. Реакция экзотермическая. Изменение энтропии: S0х.р. = (fS0CН4 + fS0Н2О) – (3fS0Н2+ fS0 CО) = 186,19 + 188.72 - 3*130,6-197,54 = - 214,43 Дж/моль*К < 0 Энергию Гиббса при соответствующих температурах находим из соотношения G0х.р=0х.р – ТS0х.р G0298 = –205,82*1000 – 298214,43 = -141919,86кДж Так как G0298 < 0, то, значит, прямая реакция может протекать самопроизвольно при нормальных условиях (298К) Вычисляем 0х.р. и S0х.р. для второй реакции: N2 (г) + 3Н2(г) = 2NH3(г). 0х.р. = 2*f0NН3 = 2*(–46,19) = -92,38 кДж/моль < 0 Реакция экзотермическая S0х.р. = 2*fS0 NН3 – 3fS0Н2 - fS0 N2 = 2*192,50 - 3*130,6-191,49= - 198,29 Дж/моль*К < 0 Энергию Гиббса при соответствующих температурах находим из соотношения G0х.р = 0х.р – ТS0х.р G0298 = -92,38 *1000+ 298204,34= -33289,58Дж/моль < 0. Так как G0298 < 0, то, значит, прямая реакция может протекать самопроизвольно при нормальных условиях (298К) Задание 20 20. К какой аналитической группе (согласно кислотно-основного метода классификации) относится катион Hg22+? Какие еще катионы относятся к данной группе? Групповой и специфические реагенты на катионы данной группы (подтвердить уравнениями реакций). Особые условия проведения реакций (если есть). Ответ Ко второй группе катионов относят катионы серебра Ag+, ртути (1) Hg22+ и свинца Рb2+. Групповым реагентом на катионы второй аналитической группы является водный раствор хлороводородной кислоты (обычно с концентрацией 2 моль/л НС1); реже — растворы растворимых хлоридов. Групповой реагент осаждает из водных растворов катионы второй аналитической группы в виде осадков малорастворимых в воде хлоридов серебра AgCl, ртути (1) Hg2Cl2 и свинца PbCl2: Hg22+ +2 НСl = Hg2Cl2↓ + 2H+ При действии группового реагента катионы свинца осаждаются из водного раствора не полностью — частично они остаются в растворе. Реакции катиона ртути (I) Hg22+ 1.Хлороводородная кислота HCl и растворимые хлориды из растворов солей ртути (I) осаждают хлорид ртути (I), или каломель, - осадок белого цвета: Hg2(NO3)2 + HCl = Hg2Cl2↓ + 2HNO3 Hg22+ +2Cl- = Hg2Cl2↓ Водный раствор аммиака окрашивает осадок в черный цвет, обусловленный образованием черной мелкораздробленной ртути: Hg2Cl2 + 2 NH3 = Hg2(NH2)Cl↓ + Hg↓ + NH4Cl С помощью этой реакции открывают ион Hg22+, добавляют 3 капли раствора аммиака. Наблюдают почернение осадка. 2. Иодид калия KI из растворов солей ртути (I) осаждает иодид ртути (I) – осадок болотно-зеленого цвета: Hg2(NO3)2 + 2KI = 2KNO3 + Hg2I2↓ Осадок довольно легко распадается на иодид ртути (II) и металлическую ртуть; при этом цвет осадка изменяется: Hg2I2 = HgI2↓ + Hg↓ 3. Хромат калия K2CrO4 образует с солями ртути (I) при нагревании красно-бурый осадок Hg2CrO4. Hg2(NO3)2 + K2CrO4 = Hg2CrO4 ↓ + 2KNO3 2Hg+ + CrO42- = Hg2 CrO4↓ Осадок не растворяется в щелочах и разбавленной уксусной кислоте. Реакции катиона свинца Pb2+ 1. Хлороводородная кислота HCl и растворимые хлориды осаждают из умеренно концентрированных растворов солей свинца (II) белый хлопьевидный осадок хлорида свинца (II), легко растворимый в горячей воде: Pb(NO3)2+ 2HCl = PbCl2↓ + 2 HNO3 Pb2+ + 2Cl- = PbCl2↓ 2.Едкие щелочи из растворов солей свинца (II) осаждают гидроксид свинца (II) – осадок белого цвета: Pb(NO3)2 + 2KOH = Pb(OH)2↓ + 2KNO3 Pb2+ + 2OH- = Pb(OH)2↓ Гидроксид свинца (II) обладает амфотерными свойствами, поэтому он растворяется в разбавленной азотной или уксусной кислотах и в избытке щелочи: Pb(OH)2 + 2KOH = K2[Pb(OH)4] 3. Серная кислота H2SO4 и растворимые сульфаты выделяют из свинцовых солей труднорастворимый сульфат свинца – осадок белого цвета: Pb(NO3)2+ H2SO4 = PbSO4↓ + 2 HNO3 Pb2+ + SO42- = PbSO4↓ Осадок растворим при нагревании в растворах щелочей (10-15%): PbSO4+ 4NaOH = Na2[Pb(OH)4] + Na2SO4 4. Иодид калия KI, взаимодействуя со свинцовыми солями, дает желтый осадок иодида свинца (II): Pb(NO3)2 + KI = PbI2↓ + 2KNO3 Pb2+ + 2I- = PbI2↓ Реакция часто применяется для открытия ионов Pb2+. Растворившийся при нагревании осадок иодида свинца вновь выпадает в виде красивых золотистых чешуек. 5. Хромат калия K2CrO4 или хромат натрия Na2CrO4 выделяет из раствора соли свинца желтый осадок соли свинца (II): Pb(NO3)2 + K2CrO4 = PbCrO4↓ + 2KNO3 Pb2+ + CrO42- = PbCrO4↓ Осадок не растворяется в уксусной кислоте, но растворяется в азотной кислоте и щелочах. Реакция чувствительна и является характерной для ионов Pb2+. Реакции катиона серебра Ag+ 1. Хлороводородная кислота HCl и растворимые хлориды осаждают из нейтральных и кислых растворов солей серебра в виде белого творожистого осадка хлорида серебра: AgNO3 + HCl = AgCl↓ + HNO3 Ag+ + Cl- = AgCl↓ Осадок легко растворяется в избытке аммиака с образованием комплексной соли: AgCl + 2 NH3 = [Ag(NH3)2]Cl При подкислении аммиачного раствора концентрированной азотной кислотой эта соль разрушается и вновь выпадает осадок хлорида серебра [Ag(NH3)2]Cl + 2HNO3 = AgCl↓ + 2NH4NO3 Эту реакцию обычно используют для открытия иона Ag+ 2. Иодид калия KI образует с ионом Ag+ светло-желтый осадок AgI: AgNO3 + KI = Agl↓ + KNO3 Ag+ + l- = Agl↓ Иодид серебра не растворяется в растворе аммиака в отличие от хлорида серебра. 3.Хромат калия K2CrO4 из растворов солей серебра осаждает кирпично-красный хромат серебра: 2AgNO3 + K2CrO4 = Ag2CrO4↓ + 2KNO3 2Ag+ + CrO42- = Ag2CrO4↓ Осадок растворяется в растворе аммиака и азотной кислоте. 4.Едкие щелочи из растворов солей серебра осаждают грязно-коричневый осадок оксида серебра: 2AgNO3+ 2KOH = Ag2O↓ + H2O + 2KNO3 2Ag+ + 2OH- = Ag2O↓ + H2O 5. Тиосульфат натрия Na2S2O3 из растворов солей серебра выделяет белый осадок, который быстро желтеет, затем буреет и переходит в черный: 2AgNO3 + Na2S2O3 = Ag2 S2O3↓ + 2NaNO3 Ag2S2O3+ H2O = Ag2S↓ + H2SO4 Осадок Ag2S2O3растворяется в избытке тиосульфата с образованием комплексных солей, поэтому осадок образуется при избытке ионов серебра. Задание 21 21. К какой аналитической группе относится анион SO42-? Какие еще анионы относятся к данной группе? Групповой и специфические реагенты на анионы данной группы (подтвердить уравнениями реакций). Особые условия проведения реакций (если есть). Ответ: При аналитической классификации анионов по группам, основанной на образовании малорастворимых солей бария и серебра, анионы делят по данной классификации на три группы. К I группе относят анионы, образующие малорастворимые в воде (в нейтральной или слабо - щелочной среде) соли с катионами Ba2+. Групповым реагентом является раствор BaCl2. К данной группе относят анионы: SO42−, SO32−, CO32−, PO43−. 1. Анионы сульфата при взаимодействии с катионами Ba2+ образует белый мелкокристаллический осадок BaSO4: Ba2+ + SO42− → BaSO4↓. белый осадок. Осадок не растворяется в минеральных кислотах, за исключением концентрированной серной кислоты: BaSO4↓ + H2SO4 → Ba(HSO4)2 Если в растворе присутствует перманганат калия KMnO4, то осадок сульфата бария окрашивается в фиолетово-красный цвет за счет адсорбции анионов MnO4− на осадке. 2.Реакция с катионами свинца Pb2+. Сульфат-ион образует с катионами свинца белый кристаллический осадок PbSO4: Pb2+ + SO42− → PbSO4↓ белый осадок Осадок частично растворяется в минеральных кислотах; щелочах и в водных растворах ацетатов (CH3COONH4 или CH3COONa) с образованием комплексных соединений. Растворение осадка в щелочах: PbSO4↓ + 4 NaOH → Na2[Pb(OH)4] + Na2SO4. 3.Реакция с карбонатом бария. К исследуемому раствору (рН 7) добавляют несколько капель суспензии BaCO3. Смесь выпаривают на водяной бане, сухой остаток обрабатывают раствором фенолфталеина. Если в растворе присутствовали ионы SO42−, то фенолфталеин окрашивается в малиновый цвет вследствие протекания реакций: BaCO3↓ + SO42− = BaSO4↓ + CO32−; CO32− + H2O = HCO3− + OH−; HCO3− + H2O = H2CO3 + OH−. Сульфит-ионы при взаимодействии с 1. катионами бария образуют белый кристаллический осадок BaSO3: Ba2+ + SO32− → BaSO3↓. белый осадок. Осадок растворяется в разбавленных кислотах: HCl и HNO3 c выделением оксида серы (IV): BaSO3↓ + 2 HCl → SO2↑ + BaCl2 + H2O. 2.Реакция разложения сульфитов сильными кислотами. Все сульфиты разлагаются под действием сильных кислот с выделением газообразного оксида серы (IV): SO32− + 2 Н+ → SO2↑ + H2O 3. Реакция с раствором йода. Анионы сульфита в нейтральных или слабокислых растворах окисляются йодом до анионов сульфата. Желтый раствор йода при этом обесцвечивается: SO32− + I2 + H2O → SO42− + 2 I− + 2 H+. Анион карбоната при взаимодействии с катионами Ba2+ образует белый мелкокристаллический осадок ВаСО3: Ba2+ + CO32− → BaCO3↓белый осадок. Осадок растворяется в кислотах: HCl, HNO3, CH3COOH. Анионы карбоната при взаимодействии с сильными кислотами образуют нестойкую угольную кислоту, разлагающуюся с выделением углекислого газа. Выделение пузырьков газа – аналитический признак данной реакции: СO32− + 2 H3O+ → H2CO3 + 2 H+; H2CO3 → CO2↑ + H2O Анион PO43− образует при взаимодействии с катионами Ва2+ осадок белого цвета: 1. 2 PO43− + 3 Ва2+ → Ba3(PO4)2↓ белый осадок растворяется в кислотах: HCl, HNO3, CH3COOH. 2.Реакция с нитратом серебра. Анионы фосфата и гидрофосфата образуют с катионами серебра в нейтральной среде желтый осадок фосфата серебра: PO43− + 3 Ag+ → Ag3PO4↓ желтый осадок HPO42− + 3 Ag+ → Ag3PO4↓ + H+ Осадок фосфата серебра растворяется в азотной кислоте и избытке раствора аммиака. 3.Реакция с магнезиальной смесью (MgCl2 + NH4Cl + NH4OH). Анион фосфата при взаимодействии с данной смесью образует белый мелкокристаллический осадок двойного фосфата NH4MgPO4: Mg2+ + PO43− + NH4+ → NH4MgPO4↓ белый осадок Осадок двойной соли растворим в кислотах. 4.Реакция с молибдатом аммония. Анионы фосфата взаимодействуют с молибдатом аммония (NH4)2MoO4 при нагревании. В результате реакции образуется желтый кристаллический осадок комплексной аммонийной соли фосфоромолибденовой кислоты: (NH4)3[PO4(MoO3)12] или (NH4)3[PMo12O40]: PO43− + 3 NH4+ + 12 MoO42− + 24 H+ = (NH4)3[PO4(MoO3)12]↓ + 12 H2O. желтый осадок Осадок фосфоромолибдата аммония растворим в азотной кислоте; в растворах щелочей и аммиака; в избытке анионов фосфата с образованием желтого раствора (поэтому реакцию проводят с использованием избыточного количества реактива Задание 32 32. В процессе очистки промышленных сточных вод происходит образование коллоидных растворов. Для их разрушения и коагуляции обычно применяются растворы электролитов. Если исходные сточные воды содержали поверхностно-активные вещества на основе солей триалкиламмония общей формулы
Решение Исходные сточные воды содержали поверхностно-активные вещества на основе солей триалкиламмония общей формулы (R3NH+ )2SO4-2 ↔ 2 R3NH+ + SO4-2 Коагулирующее действие оказывает ион, заряд которого противоположен заряду коллоидной частицы. Правило Шульце – Гарди: величина порога коагуляции данного коллоидного раствора зависит от заряда иона–коагулятора, причем, чем выше заряд этого иона, тем ниже величина порога коагуляции. Значения порогов коагуляции для одно-, двух- и трехзарядных ионов примерно обратно пропорциональны 6–й степени их зарядности.
Наибольший заряд имеет анион PO4-3 ,следовательно, раствор кислоты H3PO4 будет обладать наибольшей коагулирующей способностью Задание 43 43. Для осаждения большинства ионов тяжелых металлов из сточных растворов часто применяется гидроксид кальция (гашеная известь). Если годовой объем очищаемой воды равен 3000 м3, а содержание в нем ионов Fe3+ составляет 140 мг/дм3, то с учетом 10%-го избытка реагента, необходимого для полного осаждения, расход гидроксида кальция составит __916____ кг в год. (Ответ привести с точностью до целых; Ar(Fe) = 56.) Решение Уравнение реакции осаждения катионов железа Fe3+ будет следующее: 2Fe3+ + 3Ca(OH)2 = 2Fe(OH)3↓ + 3Ca+2 М(Ca(OH)2 = 40+ 17*2 = 74 г/моль По уравнению реакции на осаждение 112 г железа Fe3+ расходуется 3*74 г гашенной известиCa(OH)2 На (140*3000*1000/1000) * 110(%) г ----------------- х г Х = 140*3000*3*74*1,1/112*1000 = 915,75кг Задание 54 54. Наиболее технологичным и эффективным способом выделения металлов из растворов является электролиз. Если годовой объем очищаемой воды равен 1000 м3, а содержание в нем ионов Pd3+ в виде анионных комплексов составляет 7,8 мг/дм3, то время, необходимое для выделения всего палладия электролизом при силе тока 11,9 А и выходе по току 100 %, составит __21___ суток. (Ответ привести с точностью до целых; Ar(Pd) = 106; F = 96500 Кл/моль.) Решение Количественная характеристика процессов электролиза определяется законами, установленными Фарадеем. Закон Фарадея выражается следующим уравнением: m = Э*I*t/F. Здесь m— масса образовавшегося или подвергшегося превращению вещества; Э — его эквивалентная масса (г/моль); I — сила тока (а); t — время (сек); F — постоянная Фарадея (96500 Кл/моль), т. е. количество электричества, необходимое для осуществления электрохимического превращения одного эквивалента вещества. Pd3+ + 3e = Pd0 Э(Pd3+) = M(Pd3+)/3=106/3 = 35,3г/моль m (Pd) = 7,8 мг/дм3* 1000*1000м3/1000 =7800(г) m (Pd) = Э*I*t/F = 35,3*11,9*t/ 96500 = 7800(г) t = 7800*96500/35,3*11,9*60*60 = 497,7 час. t= 497,7 час/24 = 20,7 суток Задание 65 65. Какой из катионов: Fe3+, Ca2+, Al3+ или Hg2+, содержится в растворе, если: в ходе реакции взаимодействия его раствора с карбонатом натрия образуется осадок, исчезающий при добавлении раствора кислоты; при взаимодействии его раствора с гидроксидом калия раствор мутнеет; при взаимодействии его раствора с ортофосфорной кислотой выпадает осадок белого цвета; при взаимодействии его раствора с бихроматом калия раствор мутнеет и становится желтоватым. Для выполнения эксперимента в каждую пробирку добавляли только один из реагентов, находящихся в склянках. Подтвердите наличие иона соответствующими уравнениями реакций (если возможно - в молекулярном и ионном виде). Решение Рассмотрим 2-ой признак: при взаимодействии раствора катиона с ортофосфорной кислотой выпадает осадок белого цвета. Так как фосфаты катионов Fe3+ и Hg2+ имеют желтую Hg3(PO4)2 и слабо-желтую окраску(FePO4), то, видимо, эти катионы отсутствуют. Ca2+ + PO4-3 = Ca3(PO4)2 ↓ осадок белого цвета Al3+ + PO4-3 = AlPO4 ↓ осадок белого цвета Согласно 1-ому признаку: в ходе реакции взаимодействия его раствора с карбонатом натрия образуется осадок, исчезающий при добавлении раствора кислоты, определяемый катион не может быть Al3+ , поскольку карбонат алюминия в растворе не существует, а гидролизуется полностью с выделением углекислого газа. Ca2+ + СO3-2 = CaСO3 ↓ осадок белого цвета Образуется осадок, исчезающий при добавлении раствора кислоты: в молекулярном и ионном виде: 2CaСO3 ↓ +2 HCl = Ca(HСO3)2 + CaCl2 осадок CaСO3 ↓ растворяется при добавлении кислоты, например, HCl. Образуется кислая растворимая соль кальция Ca(HСO3)2 в ионном виде: 2CaСO3 ↓ + 2 H+ = 2 HСO3- + 2 Ca+2 Остается Ca2+. Этот катион образует при взаимодействии его раствора с бихроматом калия осадок желтого цвета, и раствор становится желтоватым (соответствует 3-ему признаку). Ca2+ + CrO4-2 = CaCrO4 ↓ Растворимость CaCrO4 в воде низкая — около 2,27 % (при 19 °С), кристаллическое вещество желтого цвета. Ответ: Ca2+ Задание 76 76. В чем заключается особенность прямого титрования в сравнении с другими типами титрования? При проведении кислотно-основного титрования 15 мл раствора гидроксида натрия неизвестной концентрации раствором соляной кислоты с молярной концентрацией эквивалента 0,10 моль/л экспериментально определили объем титранта. Он составил 10,5 мл. Рассчитайте массу гидроксида натрия, содержащуюся в 1 л этого раствора. (Ответ приведите в г с точностью до десятых, например 4,2.) Решение В любом методе титриметрического анализа существует несколько способов титрования. Различают прямое титрование, обратное титрование и титрование по замещению. При прямом титровании к раствору определяемого вещества добавляют по каплям титрант до достижения точки эквивалентности. Схема титрования: X + R = P. Прямое титрование предполагает непосредственное прибавление титранта к раствору пробы. νХ = νR где νХ и νR – количества молей эквивалентов Х и R. 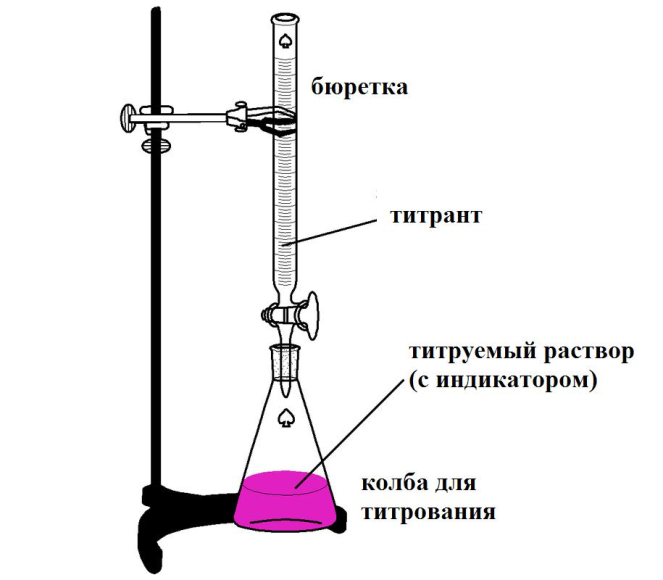 Прямое титрование - удобный и самый распространенный вариант титриметрии. Он более точен, чем другие. Ведь случайные погрешности в основном возникают при измерении объема растворов, а в данном способе титрования объем измеряют только один раз. Однако прямое титрование возможно далеко не всегда. Многие реакции между Х и R идут недостаточно быстро, и после добавления очередной порции титранта в растворе не успевает установиться равновесие. Иногда прямое титрование невозможно из-за побочных реакций или ввиду отсутствия подходящего индикатора. В подобных случаях применяют более сложные схемы обратного или заместительного титрования. Закон эквивалентов для прямого титрования: C(1/z) Х VХ = C(1/z) RVR Количество (массу) определяемого вещества, содержащееся в исследуемом растворе, вычисляют, используя закон эквивалентов (для прямого титрования) mХ= C(1/z)R VR M(1/z)Х ٠10-3 , (3) где C(1/z)R – молярная концентрация эквивалента[1] титранта, моль/дм3; VR – объем титранта, см3; M(1/z) Х – молярная масса эквивалента определяемого вещества; C(1/z)Х – молярная концентрация эквивалента определяемого вещества, моль/дм3; VХ – объем определяемого вещества, см3 Задача NaOH + HCl = NaCl + H2O C(1/z) Х VХ = C(1/z) RVR 15 мл*Х = 10,5*0,10 См(NaOH) = 10,5*0,10 /15 = 0,07моль/л Э(NaOH) = M(NaOH) = 40г/моль m(NaOH) = 0,07*40г/моль = 2,8 г Ответ: 2,8 г Задание 87 87. В процессе получения железа в промышленности возможно использование реакции угля с оксидом железа (III) Fe2O3 + 3C = 2Fe + 3CO Теплота, необходимая для осуществления процесса, обеспечивается горением углерода. Если энтальпии образования оксида железа (III), угарного и углекислого газов равны: –822,16, –111 и –394 кДж/моль соответственно, то для получения 1120 кг железа потребуется _509___ кг углерода. (Потерями углерода на побочные процессы пренебречь; ответ привести с точностью до целого значения; Ar(Fe) = 56.) Решение Горение угля, реакция: С + О2 = СО2, при этом выделяется такое количество тепла: 0(СО2). = -394 кдж/моль Реакция Fe2O3 + 3C = 2Fe + 3CO +Q идет с поглощениемтепла 0х.р. = 3 f0CO - fFe2O30 = - 3*111+ 822,16 = +489,16 кдж/моль Q =-0х.р= -489,16 кдж/моль Термохимическое уравнение: Fe2O3 + 3C = 2Fe + 3CO -489,16 кдж/моль Для получения 112 г железа необходимо 489,16 кдж тепла, а для получения 1120 кг железа -------------------------- х Х = 1120*489,16/0.112 = 489,16 *104кдж Это количество тепла выделяется следующим количеством угля: 489,16 *104кдж /394= 1,24 *104 моль угля или m1= M(c)* 1,24 *104 моль = 12г/моль*1,24 *104 моль/1000 =148,98 кг Также необходимо учесть количество углерода, которое расходуется на саму реакцию восстановления железа: Fe2O3 + 3C = 2Fe + 3CO Из уравнения реакции видно, что на 2 моля железа требуется 3 моля углерода. N (Fe) =1120 кг/56 = 20*103 моль Углерода понадобится N(С) =1,5*20*103 моль =30*103 моль; m2(C ) = 12г/моль*30*103 моль =360 кг Итого углерода потребуется для получения 1120 кг железа: m(C ) = m1(C ) + m2(C ) = 149 + 360 =509 кг Задание 98 98. Какие из предложенных соединений при прокаливании образуют только сложные вещества? Записать соответствующие уравнения реакций.
Решение Реакции разложения при прокаливании: NH4Cl =NH3 + HCl 2CuSO4 (650oC) =2CuO + 2SO2 + O2 CrPO4 tпл.=1800оС, практически не разлагается. NH4NO2 =N2 + H2O Одно только соединение из предложенных при прокаливании образует только сложные вещества: хлористый аммоний NH4Cl =NH3 + HCl Задание 101 Напишите уравнения диссоциации солей K3[Fe(CN)6] и NH4Fe(SO4)2 в водном растворе. К каждой из них прилили раствор щелочи. В каком случае выпадает осадок гидроксида железа (Ш)? Напишите молекулярные и ионно-молекулярные уравнения реакций. Какие комплексные соединения называют двойными солями Решение Двойные соли [NH4Fe(SO4)2] образуются при соединении нейтральных молекул разных веществ друг с другом: (NH4)2SO4 + Fe2(SO4)3= (NH4)2SO4▪Fe2(SO4)3 [2NH4Fe (SO4)2] Комплексные соли {K3[Fe(CN)6]} образуются в результате взаимодействия иона – комплексообразователя (ион металла) с лигандами, противоположно заряженными ионами или нейтральными молекулами. Ион – комплексообразователь и лиганды образуют внутреннюю сферу комплексного соединения, которую обозначают квадратными скобками. Ионы, не вошедшие во внутреннюю сферу, образуют внешнюю сферу. Если ион – комплексообразователь – катион, то во внешней сфере находятся анионы: [Ag(NH3)2]+OH- Если ион – комплексообразователь – анион, то во внешней сфере находятся катионы: 4К+ [Fe(CN)6]4─ Число лигандов (аддендов), которые координируются вокруг центрального иона – комплексообразователя, называют координационным числом. Уравнения диссоциации соли K3[Fe(CN)6]: K3[Fe(CN)6] ↔ 3K+ + [Fe(CN)6]-3 После добавления раствора щелочи в первом растворе не произойдет изменений. Двойные соли отличаются от комплексных характером диссоциации в водных растворах. Двойные соли диссоциируют в одну ступень на катионы обоих металлов и анион кислотного остатка: NH4Fe(SO4)2↔ NH4+ +Fe+3 + 2SO4-2 После добавления раствора щелочи в втором растворе произойдет следующая реакция: NH4Fe(SO4)2+ 4NaOH = NH3 + Fe(OH)3 + H2O + 2Na2SO4 NH4+ +Fe+3 + 4OH- = NH3 + Fe(OH)3 + H2O Список использованной литературы 1. Коровин Н.В. Общая химия: учебник. – М.: Высшая школа, 2011. – 559 с. 2. Ахметов Н.С. Общая и неорганическая химия: учебник. – СПб.: Лань, 2014. – 752 с. 3. Карапетьянц М.Х., Дракин С.И. Общая и неорганическая химия: учебник. – М.: Либроком, 2015. – 592 с. 4. Глинка Н.В. Химия: учебник. – М.: КноРус, 2014. – 752 с. 5. Глинка Н.Л. Задачи и упражнения по общей химии: учеб. пособие. – М.: КноРус, 2012. – 240 с. 6. Батаева Е.В., Буданова А.А. Задачи и упражнения по общей химии: учеб. пособие. – М.: Академия, 2012 . – 156 с. 7. Ю.Я.Харитонов Аналитическая химия М., «Высшая школа», т.1, 2003 -614с. 8. Ю.Я.Харитонов Аналитическая химия М., «Высшая школа», т.2, 2003 -559с. 9. https://helpiks.org/6-44412.html |
