Сложные эфиры и жиры. Сложные эфиры Определение, номенклатура и изомерия сложных эфиров
 Скачать 298.5 Kb. Скачать 298.5 Kb.
|
|
Сложные эфиры 1. Определение, номенклатура и изомерия сложных эфиров. Производные карбоновых кислот, в которых атом водорода карбоксильной группы замещен на углеводородный радикал, называют сложными эфирами. Общая формула сложных эфиров RCOOR', где R и R' — углеводородные радикалы (для эфиров муравьиной кислоты R — атом водорода). В химии используют несколько номенклатур для названия сложных эфиров. Самые длинные названия состоят из четырех слов и происходят от наименования соответствующей кислоты с указанием углеводородного заместителя, например метиловый эфир уксусной кислоты, этиловый эфир муравьиной кислоты. В русском языке приняты названия, состоящие из двух слов: уксусно-метиловый эфир, муравьино-этиловый эфир. Еще более кратко химики называют сложные эфиры подобно солям кислот, только вместо металла в названии указывают углеводородный радикал. Те же эфиры можно назвать метилацетат и этилформиат:  Сложные эфиры являются межклассовыми изомерами карбоновых кислот и для насыщенных R и R' имеют общую формулу СпН2пО2. Структурная изомерия может быть связана с длиной углеродной цепи в заместителях (приведенные выше метилацетат и этилформиат изомерны) и строением углеродного скелета. Упражнение. Написать все возможные изомеры состава С4Н8О2. Назвать полученные вещества 2. Свойства и получение сложных эфиров. Сложные эфиры низших карбоновых кислот представляют собой летучие жидкости, многие из которых обладают приятным фруктовым или цветочным запахом. Например: уксусноизопентиловый эфир – запах груш; маслянобутиловый эфир – запах ананасов. Сложные эфиры содержатся в цветах, фруктах, ягодах, придавая им специфический запах. Они практически не растворимы в воде и имеют более низкие температуры кипения, чем изомерные им карбоновые кислоты. Это связано с нем, что в молекулах сложных эфиров отсутствуют межмолекулярные водородные связи. В основе получения сложных эфиров лежит реакция этерификации между карбоновой кислотой и спиртом: 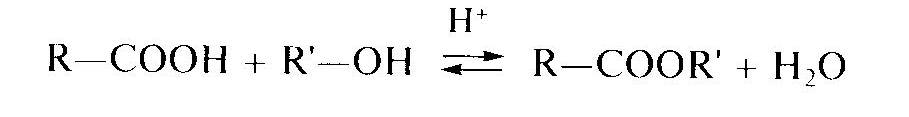 Реакция катализируется сильными кислотами. Например, при взаимодействии уксусной кислоты с этиловым спиртом получается сложный эфир, который называют этиловым эфиром уксусной кислоты, или этилацетатом (написать уравнение реакции самостоятельно) Обратимость реакции этерификации серьезно осложняет ее практическое использование. Равновесие смещают вправо, удаляя из реакционной смеси воду. Химические свойства сложных эфиров. Сложноэфирный фрагмент достаточно устойчив к действию различных реагентов. Легко протекают лишь реакции горения (до углекислого газа и воды) и гидролиза.  Жиры. 1. Определение, состав и классификация жиров. К сложным эфирам природного происхождения относятся жиры. Люди начали использовать жиры в повседневной жизни гораздо раньше, чем изучили их химическое строение. Животные и растительные жиры являются одним из основных компонентов пищи, их используют в качестве смазки, косметического средства, топлива для освещения улиц и жилищ. Жиры играют важную роль в природе. Они являются одним из источников энергии живых организмов, которая выделяется при окислении этих соединений. У китов подкожный слой жира достигает 1 метра, а самое жирное молоко у дельфинов – 40 %. Помимо употребления в пищу жиры используют для изготовления мыла, смазочных материалов, косметических средств, жирных кислот, свечей, глицерина, олифы. Жирами называют сложные эфиры трехатомного спирта глицерина и высших карбоновых кислот. Общая формула жиров: 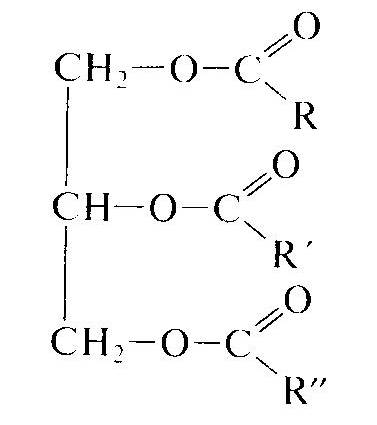 В состав природных жиров входят остатки предельных и непредельных кислот, содержащих четное число углеродных атомов и неразветвленный углеродный скелет. Перечислим некоторые из них: масляная кислота С3Н7СООН, пальмитиновая кислота C15H31COOH, стеариновая кислота C17H35COOH, олеиновая кислота C15H31COOH. Жиры, образованные предельными кислотами (масляной, пальмитиновой, стеариновой и др.), имеют, как правило, твердую консистенцию. Исключение – рыбий жир. Это жиры преимущественно животного происхождения. С увеличением длины углеводородного радикала температура плавления жира увеличивается. Если в состав жира входят остатки непредельных кислот (например, олеиновой), жиры представляют собой вязкие жидкости; их часто называют маслами. Масла — это жидкие жиры преимущественно растительного происхождения. Исключение кокосовое масло и какао. Природные жиры, как правило, являются смешанными сложными эфирами, т.е. в состав их молекул входят остатки разных кислот. Жиры не растворимы в воде, но хорошо растворяются в органических растворителях: бензоле, тетрахлорметане, гексане. 2. Химические свойства и переработка жиров в технике. Щелочной гидролиз жиров приводит к образованию глицерина и солей высших карбоновых кислот, называемых мылами. Поэтому реакцию сложных эфиров со щелочами называют омылением. Например, при нагревании тристеарата глицерина с водным раствором гидроксида натрия образуется стеарат натрия — твердое мыло: 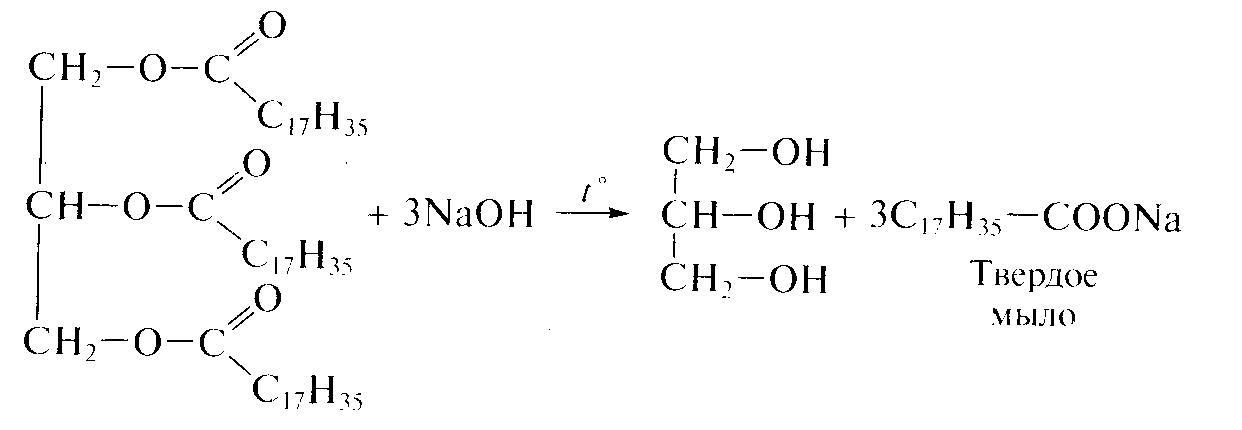 В незначительной степени гидролиз протекает и при хранении жира под действием влаги, света и тепла. Жир прогоркает — приобретает неприятный вкус и запах, обусловленный образующимися кислотами. Остатки непредельных кислот в жирах сохраняют свойства алкенов. Например, растительное масло обесцвечивает бромную воду и окисляется водным раствором перманганата калия, также его обесцвечивая. Эти свойства обусловлены присутствием в молекуле двойных углерод-углеродных связей. Важным промышленным процессом является гидрирование растительных жиров, т.е. присоединение водорода по кратным связям с образованием предельных жиров. Например, жидкий триолеат глицерина при гидрировании превращается в твердый тристеарат: 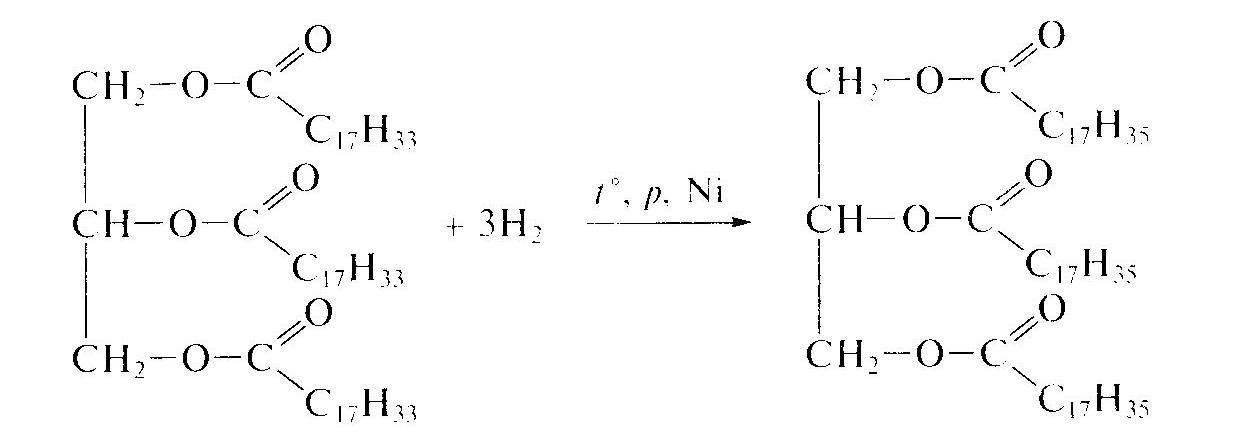 Гидрированием растительных масел получают твердый продукт, называемый саломасом. Он идет на изготовление маргарина и других продуктов питания. Двойные связи непредельных кислот в жидких жирах сохраняют способность к полимеризации под влиянием кислорода воздуха с образованием твердых полимерных пленок. Это свойство используют при изготовлении олифы и лаков из льняного и конопляного масел. Задание 1. Приведите примеры применения сложных эфиров и жиров
|
