Содержание Введение Глава Сущность экстракционнофотометрических методов Глава Примеры использования метода для определения тяжелых металлов в природных водах Глава Современное оборудование Литература Введение
 Скачать 123.76 Kb. Скачать 123.76 Kb.
|
|
«Экстракционно-фотометрический метод определения тяжелых металлов в природных водах» Содержание Введение Глава 1. Сущность экстракционно-фотометрических методов Глава 2. Примеры использования метода для определения тяжелых металлов в природных водах Глава 3. Современное оборудование Литература Введение Для определения загрязняющих веществ используют инструментальные методы современной аналитической химии, основанные на измерении различных физических свойств определяемых веществ или продуктов их химических превращений (аналитических реакций) с помощью физических и физико-химических приборов. Результат измерения, несущий химико-аналитическую информацию, часто называют аналитическим сигналом. Спектроскопические методы анализа основаны на использовании взаимодействия атомов или молекул определяемых веществ с электромагнитным излучением широкого диапазона энергий. Это могут быть (в порядке уменьшения энергии) гамма-кванты, рентгеновское излучение, ультрафиолетовое и видимое, инфракрасное, микроволновое и радиоволновое излучение. Сигналом может быть испускание или поглощение излучения. Важнейшими для экологического мониторинга, по-видимому, являются нейтронно-активационный, рентгеноспектральный, атомно-абсорбционный и атомно-эмиссионный анализ, спектрофотометрический и флуориметрический методы, инфракрасная спектрометрия. Данная курсовая работа посвящена экстракционно-фотометрическим методам анализа и их роли в определении тяжелых металлов в природных водах. Глава 1. Сущность экстракционно-фотометрических методов Эти методы применяют в аналитической химии очень даже широко, причем определение анализируемого компонента в экстракте может производиться как фотометрическим, так и другим методом: полярографическим, спектральным. Вместе с тем существуют некоторые группы экстракционных методов, в которых фотометрическое окончание является наиболее эффективным, обеспечивая необходимую быстроту и точность определения. Эти методы называются экстракционно-фотометрическими. Весьма распространенной является методика, по которой определенный микроэлемент переводят в растворимое в воде окрашенное соединение, экстрагируют его и экстракт фотомоделируют. Такая методика позволяет устранить мешающее влияние посторонних компонентов и увеличивает чувствительность определения, так как при экстракции происходит концентрирование микропримесей. Например, определение примесей железа в солях кобальта или никеля проводят экстракцией его тиоцаинатных комплексов амиловым спиртом.1 ФОТОМЕТРИЧЕСКАЯ ТЕХНОЛОГИЯФотометрическая технология - основная технология для определения концентраций многих жидкостей и газов, используемых в промышленности, на ppm и процентном уровнях. Приборы, основанные на данной технологии, называют фотометрами. Каждый газ или жидкость обладают своим характерным спектром поглощения электромагнитного излучения. Можно подобрать такой диапазон длин волн, на котором спектр поглощения измеряемого компонента будет кардинально отличаться от спектров поглощения остальных компонентов. Если пропускать излучение необходимой длины волны через ячейку с пробой, то по изменению спектра поглощения можно узнать концентрацию измеряемого компонента. В зависимости от длины волны источника излучения анализаторы могут работать в инфракрасном, ультрафиолетовом или оптическом диапазоне.
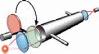
Измерительная ячейка состоит из следующих основных частей2, 5: широкополосного источника излучения, одного или нескольких фильтров и приемника излучения. Излучение от источника направляется через соответствующий светофильтр в измерительную кювету. После прохождения луча через фильтр в излучении остаются только те длины волн, которые поглощаются измеряемым веществом и не поглощаются другими компонентами пробы. Такой пучок света проходит через пробу газа и поглощается исследуемым компонентом пропорционально его концентрации. Далее оставшееся излучение попадает на приемник излучения, при помощи которого оценивается его интенсивность и определяется концентрация исследуемого компонента. При необходимости контроля концентрации нескольких веществ одновременно, приборы комплектуются несколькими ячейками (обычно число фотометрических ячеек не превышает четырех в одном приборе) или в самой ячейке устанавливается несколько светофильтров, переключение которых позволяет измерять концентрации нескольких веществ. При необходимости измерения таких веществ, как кислород, водород и других, дополнительно монтируются внутрь корпуса, соответственно, электрохимические, парамагнитные, циркониевые и кондуктометрические измерительные ячейки. 3-5 Глава 2. Примеры использования метода для определения тяжелых металлов в природных водах Экстракционно-фотометрический метод определения хрома16 На протекание естественных процессов в воде большое влияние оказывает содержание в ней тяжелых металлов. Были проведены исследования, целью которых являлась количественная оценка загрязнения реки Кальмиус тяжелыми металлами. Результаты данного исследования показали, что одним из тяжелых металлов, требующих оперативного контроля, является Сr+6, поступающий в водоемы со сточными водами гальванических цехов машиностроительных, авиационных, автомобильных заводов, предприятий химической, кожевенной промышленности и пр. В речных загрязненных и слабозагрязненных водах концентрация Сr+6 колеблется от нескольких десятых долей мг/дм3 до нескольких мг/дм3. Из-за высокой токсичности содержание Сr+6 в водоемах нормировано и не должно превышать ПДК, равной 0,05 мг/дм3. Одним из обязательных условий контроля содержания Сr+6 в природных водах является оперативность его определения, так как хранение проб невозможно в связи с переходом +6 в анаэробных условиях в Сr+3.6,7 Широкое распространение получил метод фотометрического определения Сr+6 с применением дифенилкарбазида, позволяющий оперативно определять содержание Сr+6 в пробах природной воды. Однако, согласно метрологическим характеристикам данного метода, минимально определяемая концентрация Сr+6 составляет лишь 30 мг/дм3. Поэтому для существенного повышения чувствительности (в 30 раз) применяют экстракционно-фотометрический метод, который заключается в экстракции определяемого вещества с его последующим фотометрическим определением. Этот метод применяется при анализе сложных смесей, когда нужно определить малые количества одних веществ в присутствии больших количеств других, при определении примесей в присутствии основных компонентов, а также в тех случаях, когда непосредственное определение интересующего элемента в смеси связано с большими трудностями. При экстракции малых количеств примесей происходит не только их выделение, но и концентрирование. Поэтому экстракционно-фотометрический метод приобретает особо важное значение в связи с определением малых количеств примесей в веществах высокой степени чистоты, широко применяемых в атомной и полупроводниковой технике. Экстракционно-фотометрические методы анализа являются высокочувствительными методами, они быстро развиваются и очень перспективны. Следовательно, экстракционно-фотометрический метод позволяет определять содержание Сr+6 в поверхностных водах на уровне 1-30 ПДК и может быть использован при оперативном контроле, в том числе в условиях работы передвижной гидрохимической лаборатории. При этом методе можно проводить измерения в потоке воды, проба может последовательно проходить несколько различных кювет, где можно измерить другие параметры, может использоваться установка на участке сброса вод, измерения могут проводится периодически, не нужен постоянный контроль, для определения концентрации хрома в воде впрыскивается избыточное количество экстракта, которое связывает почти 100% ионов хрома, что позволяет более точно провести измерения.8-12 Так как в качестве экстракта была выбрана суспензия, то прошедший через нее поток быстро затухает, и поэтому в качестве информативного параметра был выбран отраженный поток, который зависит от длины волны источника излучения и концентрации ионов хрома (рис. 1). 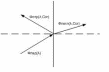 Рисунок 1 – Движение потока излучения Так как источник излучения частотно зависим и спектр поглощения ограничен, то в качестве источника излучения выбирается светоизлучающий диод (СИД) с длиной волны l=540 нм, что соответствует максимуму спектра поглощения и обеспечивает избирательность метода. Функцию избирательности можно усилить введением дополнительно оптического фильтра на длине волны l=540 нм с полосой пропускания 25±10 нм. Фотометр представляет собой прибор для канала измерительной автоматизированной системы контроля сточных вод (такие системы обслуживаются раз в 2 недели), в котором измеряется концентрация ионов хрома Сr+6. Также в данной системе могут быть каналы измерения других величин. Например, на измерение Сr+6 оказывает влияние уровень рН (учет данного фактора позволяет уменьшить погрешность с 6-7% до 3-4%). Для учета и оптимизации уровня рН при измерении концентрации ионов хрома Сr+6 целесообразно вводить в пробу необходимое (дозированное) количество кислоты Н2SO4. На измерение рН в свою очередь влияет температура. Поэтому уровень рН и температуры необходимо измерять. В результате имеем многоканальную систему, состоящую, как минимумом, из трех каналов измерения: рН, температуры и концентрации ионов хрома Сr+6. Влияние рН на результаты фотометрического измерения. При уменьшении кислотности среды, т. е. при повышении рН раствора, катионы металла, как правило, взаимодействуют с ОН-ионами, образуя в конечном счете малорастворимые гидроксиды или основные соли. Окрашенное соединение при этом разрушается. Малорастворимое соединение может и не образоваться, тем не менее участие определяемых катионов в сопряженном комплексообразовании с ОН-ионами значительно уменьшает условную константу устойчивости окрашенного комплекса и, следовательно, приводит к уменьшению степени связанности определяемого иона в окрашенное соединение. Особенно сильное влияние наблюдается для малопрочных комплексов, которые при увеличении рН раствора могут быть разрушены полностью. Поэтому реакции образования окрашенных соединений ионов металлов с анионами сильных кислот целесообразно проводить в достаточно кислых средах, где условная константа устойчивости окрашенного комплекса сохраняет свое наибольшее значение. Окрашенные комплексы с анионами слабых кислот. Когда в качестве реагентов используют слабые органические кислоты HR (салициловая кислота, ализарин, диметилглиоксим и др.), изменение рН раствора оказывает очень сильное, хотя внешне и не всегда заметное, влияние. Полнота связывания иона М в окрашенное соединение MRn зависит от концентрации в растворе анионов реагента R– которая в свою очередь зависит от концентрации Н+ в растворе. В кислых растворах концентрация R– бывает невелика, так как равновесие ионизации слабой кислоты HR сильно смещено в сторону недиссоциированной (кислотной) формы реагента. Увеличить концентрацию R– путем повышения общей концентрации реагента не всегда удается, поскольку слабые органические кислоты часто имеют ограниченную растворимость. В этом случае концентрацию увеличивают повышением рН раствора, которое смещает равновесие ионизации кислоты в сторону его солевой формы R– . Таким образом, реакции образования окрашенных соединений ионов металлов с анионами слабых кислот следует проводить по возможности в менее кислых средах. Однако уменьшение концентрации Н+ необходимо осуществлять очень осторожно, так как при повышении рН раствора может происходить образование основных солей или гидроксидов определяемых металлов; может изменяться состав окрашенного соединения вследствие ступенчатости комплексообразования. В некоторых случаях, когда влияние конкурирующего комплексообразования ОН-ионов преобладает над влиянием депротонирования реагента, повышение рН раствора может привести к противоположным результатам, т. е. к уменьшению степени связанности иона М в окрашенное соединение. Поэтому максимальный выход светопоглощающего комплекса будет наблюдаться только в определенном интервале значений рН раствора. 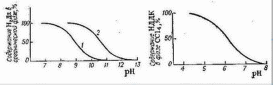 Рисунок 2 - Распределение дитизона в зависимости от рН водной фазы: 1 - CCl4; 2 - CHCl3 Диэтилдитиокарбаминовая кислота в кислых растворах разлагается на диэтиламин и сероуглерод, поэтому при хранении растворы Na-ДДК слегка подщелачивают (примерно до рН = 9). Распределение реагента между водной и органической фазами зависит от рН среды (рис. 2). При рН до 4 реагент в виде кислоты полностью переходит в органическую фазу, а. при рН выше 8 практически количественно остается в водном слое, что показано на рисунке 3:  Выяснение зависимости светопоглощения раствора от времени и температуры Фотометрический анализ обычно проводят при одинаковой комнатной температуре, так как изменение температуры раствора во многих случаях вызывает соответствующее изменение светопоглощения. Если даже небольшое изменение температуры (на 2—3 °С) приводит к значительному изменению оптической плотности фотометрируемого раствора, то измерения последней производят после предварительного термостатирования. Для выяснения устойчивости светопоглощения фотометрируемого соединения во времени измеряют оптическую плотность раствора через некоторые промежутки времени и строят график зависимости оптической плотности от времени. Для последующей работы выбирают такой интервал времени, в течение которого максимальное значение оптической плотности раствора сохраняется неизменным или меняется незначительно. Кроме того, на протяжении всех измерений строго выдерживают время между измерением оптической плотности и приготовлением фотометрируемого раствора.12-14 Связь концентрации ионов хрома Сr+6 с параметрами, влияющими на ее измерение можно представить в виде системы (1). 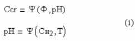 где Ссr – концентрация хрома; Ф – отраженный поток; рН – уровень рН; Сн2 – концентрация водорода; Т – значение температуры. Чтобы обеспечить метод экстракции необходима подсистема подготовки проб, которая должна периодически, дозируя экстракт, обеспечивать дополнение его в рабочую кювету. Необходимо установить наиболее благоприятные условия образования окрашенного соединения, то есть стабилизировать температуру, расход жидкости, расход экстракта, времени. Установление концентрации происходит спустя интервал времени, равный восьмикратному обновлению жидкости кюветы (3-5 мл3). Объем пробы – не более 50 мл. Предполагается производить измерения с интервалом в 1 час. В результате построена конструктивная схема измерительной автоматизированной системы контроля сточных вод, имеющей 3 канала измерения: - канал измерения температуры; - канал измерения рН; - канал измерения концентрации ионов хрома Сr+6. Данная конструктивная схема представлена на рисунке 4. 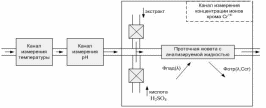 Рисунок 4 – Конструктивная схема измерительной автоматизированной системы контроля сточных вод. Для реализации используемого метода создается световой поток (поток излучения), часть которого проходит через кювету с заранее подготовленной окрашенной жидкостью, а часть отражается и преобразуется в электрический сигнал. Также предусмотрена возможность обработки полученного сигнала и выдачи результатов контроля объекта для их дальнейшего анализа. Вся система обеспечена питанием.14-16 Экстракционное концентрирование фенола и крезолов с применением бутиловых спиртов17 Фенол и крезолы в больших количествах содержатся в очищенных сточных водах коксохимических и нефтехимических предприятий. Предельно допустимые концентрации фенола и крезолов в водах находятся на уровне (1-4).10-3 мг/л, их определение в природных и очищенных сточных водах включает стадию экстракционного концентрирования. В качестве экстрагентов нами применены частично и неограниченно растворимые в воде бутиловые спирты - н. бутиловый, изобутиловый, вторбутиловый и третбутиловый. Для наиболее полного выделения органического растворителя в самостоятельную фазу вводили высаливатель (сульфат аммония). Концентрация фенола, м- и п-крезолов в исходных водных растворах 0,005-0,50 мг/мл. Равновесную концентрацию фенолов в водной фазе после экстракции (Св) находили спектрофотометрически по реакции с диазотированным 4-нитроанилином. Концентрацию фенолов в органической фазе (Со) вычисляли по разности (Сисх-Св). Коэффициент распределения D рассчитывали по формуле: D=(Со/Св).r, где r- соотношение равновесных объемов водной и органической фаз. Установлены коэффициенты распределения фенола и крезолов между бутиловыми спиртами и водно-солевыми растворами. Положение алкильного радикала (крезолы) существенно влияет на D гомологов вследствие индукционного эффекта и эффекта сопряжения. п-Крезол характеризуется большими коэффициентами D, чем м-изомер в системах с частично растворимыми в воде спиртами. При экстракции неограниченно растворимым в воде третбутиловым спиртом максимальный коэффициент D получен для фенола. Рекомендованы системы, обеспечивающие практически полное (92-95 %-ное) извлечение фенола и крезолов из водно-солевых растворов.15, 17 Экстракция 1-нафтолмоносульфокислот из водных растворов смесями углеводородов с бутанолом-118 1-Нафтолмоносульфокислоты (НМСК) - продукты многотоннажного производства, применяемые в синтезе реагентов, красителей, при получении кино- и фотоматериалов. Контроль содержания НМСК в природных объектах, в том числе в водных бассейнах, - актуальная задача, решение которой осложняется содержанием НМСК в водах на уровне микроконцентраций. Изучена экстракция 1-нафтол-4-сульфокислоты и 1-нафтол-5-сульфокисло-ты смесями гидрофобного (гексан-нонан) и гидрофильного (бутанол-1) растворителей. Для снижения гидротропного эффекта спирта экстракцию проводили в присутствии соли (хлорид натрия, сульфат калия). Независимо от природы распределяемого соединения, высаливателя и инертного растворителя (углеводород) при экстракции наблюдается синергетический эффект. Изотермы имеют четко выраженный максимум, соответствующий содержанию в смеси растворителей 0,1 мол. доли углеводорода и 0,9 мол. доли бутанола-1. Коэффициенты распределения (D) изомера, содержащего сульфогруппу в 5-положении (OH- и SO3H-группы расположены в сопряженных кольцах нафталинового ядра), в 1,8 - 2 раза выше, чем для 1-нафтол-4-сульфокислоты (оба заместителя находятся в одном кольце). НМСК в отличие от нафтолов хорошо растворимы в воде, поэтому их экстракция из водных растворов затруднена. При экстракции смесями углеводородов с бутанолом-1 коэффициенты D на 2-3 порядка меньше, чем при экстракции 1-нафтола. Природа соли не оказывает существенного влияния на экстракцию НМСК, незначительное уменьшение коэффициентов D в присутствии K2SO4 объясняется различной степенью высаливания гидрофильного спирта. Изучена экстракция НМСК смесями гексан - бутанол-1 и нонан - бутанол-1 (по 0,5 мол. доли каждого компонента) при разных значениях рН водного раствора. На графиках зависимости коэффициентов D от рН для каждой экстракционной системы имеется параллельный оси абсцисс участок, где коэффициенты D практически постоянны (рН 3-5). Коэффициенты распределения НМСК при рН 3-5 в среднем в 3-4 раза выше, чем при рН 2. Исследование процессов комплексообразования и применение мышьяксодержащих азореагентов для фотометрического определения pB(ii), cU(ii) И fE(ii, iii) 19 В настоящее время одним из направлений в аналитическом контроле содержания элементов является разработка методов анализа с использованием окрашенных органических соединений, обладающих высокой контрастностью реакций и низким пределом обнаружения. Такими реагентами являются азосоединения, в состав которых входят одна или несколько арсогрупп. Исследована возможность определения свинца(II), меди(II), кадмия(II) и железа(II, III) с применением арсеназо I, III и сульфарсазена. Найдены оптические характеристики металлоиндикаторов в водных растворах с =0,1 (NаCI), а также исследованы процессы комплексообразования с исследуемыми ионами металлов. Установлены значения оптимальных длин волн, изучена зависимость оптической плотности растворов от кислотности среды и от концентрации компонентов. Определен мольный состав образующихся комплексных соединений: для свинца(II), меди(II) и кадмия(II) - 1:1, для железа (II, III) - 1:2. С помощью дифференциальных кривых зависимости А=f(рН) рассчитаны константы равновесий процессов комплексообразования и константы устойчивости образующихся комплексов с использованием разработанной программы SFKOMML.BAS. Образование яркоокрашенных комплексов с изученными реагентами позволило рекомендовать их в качестве проявителей в методе тонкослойной бумажной хроматографии. Предложены системы растворителей для совместного обнаружения таких ионов как медь(II) и кадмий(II), железо(II) и железо(III). Построены градуировочные зависимости, позволяющие обнаруживать низкие содержания ионов этих металлов в водных растворах. |