Справочный материал. Глава 22 – Пищеварительная система. Справочный материал по Физиологии. Глава 22 Пищеварительная система
 Скачать 399 Kb. Скачать 399 Kb.
|
|
Моторика желудочно-кишечного тракта Электрические свойства миоцитов. Ритм сокращений желудка и различных отделов кишечника определяется частотой медленных волн гладких мышц (рис. 22–3А). Эти волны — медленные, волнообразные изменения МП, на гребне которых генерируются потенциалы действия (ПД), которые и вызывают мышечное сокращение. Сокращение возникает тогда, когда МП уменьшается до –40 мВ (МП гладких мышц в покое колеблется от –60 до –50 мВ). 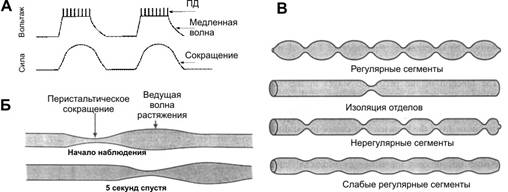 Рис. 22–3. Перистальтика. А. Сверху — медленные волны деполяризации с многочисленными ПД, внизу — запись сокращений [5]. Б. Распространение волны перистальтики. В. Сегментации тонкой кишки. Деполяризация. Факторы, деполяризующие мембрану ГМК: растяжение мышцы, ацетилхолин, парасимпатическая стимуляция, гастроинтестинальные гормоны. Гиперполяризация мембраны миоцитов. Её вызывают адреналин, норадреналин и стимуляция постганглионарных симпатических волокон. Виды моторики. Различают перистальтику и перемешивающие движения. Перистальтические движения — продвигающие (пропульсивные) движения. Перистальтика — основной вид двигательной активности, продвигающей пищу (рис. 22–3Б,В). Перистальтическое сокращение — результат выполнения местного рефлекса — перистальтический рефлекс, или миоэнтеральный рефлекс. В норме волна перистальтики продвигается в анальном направлении. Перистальтический рефлекс вместе с анальным направлением движения перистальтики получил название закон кишки. Перемешивающие движения. В некоторых отделах перистальтические сокращения выполняют функцию перемешивания, особенно там, где продвижение пищи задерживается сфинктерами. Могут возникать локальные чередующиеся сокращения, пережимающие кишку от 5 до 30 сек, затем новые пережатия в другом месте и т.д. Перистальтические и пережимающие сокращения приспособлены для продвижения и перемешивания пищи в различных частях пищеварительного тракта. Моторная функция пищеварительного тракта Жевание Жевание — комбинированное действие жевательных мышц, мышц губ, щёк и языка. Движения этих мышц координируют черепные нервы (V, VII, IX–XII пары). В контроле жевания участвуют не только ядра ствола мозга, но и гипоталамус, миндалина и кора больших полушарий. Жевательный рефлекс участвует в произвольно контролируемом акте жевания (регуляция растяжения жевательных мышц). Зубы. Передние зубы (резцы) обеспечивают режущее действие, задние зубы (коренные) — перемалывающее. Жевательные мышцы развивают при сжатии зубов силу для резцов в 15 кг и для коренных зубов в 50 кг. Поскольку пищеварительные ферменты действуют только на поверхностях пищевых частиц, темп пищеварения определяется общей поверхностью пищевых частиц, подвергнутых измельчению. Измельчение пищи до консистенции очень тонких частиц предотвращает повреждения пищевода и увеличивает лёгкость прохождения пищи из желудка в тонкую кишку и во все остальные сегменты кишечника. Глотание Глотание подразделяют на произвольную, глоточную и пищеводную фазы. Произвольная фаза начинается с завершения жевания и определения момента готовности пищи к проглатыванию. Пищевой комок продвигается в глотку, надавливая сверху на корень языка и имея сзади мягкое нёбо. С этого момента глотание становится непроизвольным, почти полностью автоматическим. Глоточная фаза. Пищевой комок стимулирует рецепторные зоны глотки, нервные сигналы поступают в ствол мозга (центр глотания), вызывая последовательный ряд сокращений мышц глотки. Мягкое нёбо подтягивается вверх и закрывает вход в полость носа, предупреждая рефлюкс (поступление пищи в обратном направлении) пищи в носовую полость. Нёбно–глоточные складки с обеих сторон сдвигаются, образуя сагиттальную щель. Эта щель свободно пропускает хорошо разжёванную пищу и препятствует быстрому прохождению более крупных частиц из глотки в пищевод. Голосовые связки смыкаются, шейные мышцы подтягивают гортань вперёд и вверх; надгортанник поворачивается назад и сверху закрывает вход в гортань. Подъём гортани подтягивает пищевод и расширяет вход в него. В это же время верхний пищеводный сфинктер (глоточно-пищеводный сфинктер) расслабляется, позволяя пище свободно передвигаться из заднего отдела глотки в верхний отдел пищевода. Между глотаниями сфинктер сильно сокращён, перекрывая пищевод от поступления воздуха во время дыхания и возможности попадания пищи в трахею. Одновременно с подъёмом гортани и расслаблением верхнего пищеводного сфинктера сокращается мускулатура гортани и продвигает пищу в пищевод. Пищеводная фаза глотания отражает основную функцию пищевода — быстрое проведение пищи из глотки в желудок. В норме пищевод имеет два вида перистальтики — первичную и вторичную. Первичная перистальтика — продолжение волны перистальтики, которая начинается в глотке Волна проходит от глотки до желудка в течение 5–10 с. Жидкость проходит быстрее. Вторичная перистальтика. Если первичная перистальтическая волна не может продвинуть всю пищу из пищевода в желудок, то возникает вторичная перистальтическая волна, вызванная растяжением стенки пищевода оставшейся пищей. Вторичная перистальтика продолжается до тех пор, пока вся пища не перейдёт в желудок. Нижний сфинктер пищевода (желудочно-пищеводный гладкомышечный сфинктер) располагается около места соединения пищевода с желудком. В норме происходит тоническое сокращение, предотвращающее попадание содержимого желудка (рефлюкса) в пищевод. В момент движения перистальтической волны по пищеводу сфинктер расслабляется (рецептивное расслабление). Нарушения глотания могут возникать при повреждении V, IX, X черепных нервов. При полиомиелите и энцефалите возможно нарушение центра глотания. Мышечная дистрофия и отравление ботулиническим токсином нарушают процесс нормального глотания. Утрата рефлекса «рецептивного расслабления» приводит к спазму желудочно-пищеводного сфинктера — ахалазии. Моторика желудка В стенке всех отделов желудка (рис. 22–4А) сильно развита мышечная оболочка, особенно в привратниковой (пилорической) части. Более того, циркулярный слой мышечной оболочки в месте перехода желудка в двенадцатиперстную кишку образует пилорический сфинктер, постоянно находящийся в состоянии тонического сокращения. Именно мышечная оболочка обеспечивает двигательные функции желудка — накопление пищи, перемешивание пищи с желудочными секретами и превращение её в полурастворённую форму (химус) и опорожнение химуса из желудка в двенадцатиперстную кишку. 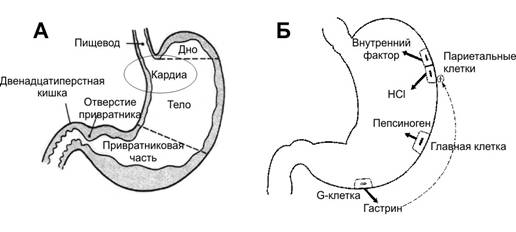 Рис. 22–4. Физиологическая анатомия желудка [5] А. Отделы. Б. Некоторые типы секреторных клеток. Голодные сокращения желудка возникают, когда желудок в течение нескольких часов остаётся без пищи. Голодные сокращения — ритмические перистальтические сокращения тела желудка — могут сливаться в непрерывное тетаническое сокращение, которое продолжается 2–3 мин. Выраженность голодных сокращений увеличивается при низком уровне сахара в плазме крови. Депонирование пищи. Пища поступает в кардиальный отдел отдельными порциями. Новые порции оттесняют предыдущие, что оказывает давление на стенку желудка и вызывает ваго–вагальный рефлекс, уменьшающий тонус мышечной оболочки. В результате создаются условия для поступления новых и новых порций, вплоть до полного расслабления стенки желудка, которое наступает при объёме полости желудка от 1,0 до 1,5 л. Перемешивание пищи. В наполненном пищей и расслабленном желудке на фоне медленных спонтанных колебаний МП гладких мышц возникают слабые перистальтические волны — перемешивающие волны. Они распространяются по стенке желудка в направлении привратниковой части каждые 15–20 с. Эти медленные и слабые перистальтические волны на фоне появления ПД сменяются более мощными сокращениями мышечной оболочки (перистальтические сокращения), которые, проходя до пилорического сфинктера, также перемешивает химус. Опорожнение желудка. В зависимости от степени переваривания пищи и формирования жидкого химуса перистальтические сокращения становятся всё более сильными, способными не только перемешивать, но и продвигать химус в двенадцатиперстную кишку (рис. 22–5). По мере прогрессирующего опорожнения желудка перистальтические выталкивающие сокращения начинаются от верхних отделов тела и дна желудка, добавляя их содержимое к химусу привратникового отдела. Интенсивность этих сокращений в 5–6 раз больше, чем сила сокращений перемешивающей перистальтики. Каждая сильная волна перистальтики выдавливает несколько миллилитров химуса в двенадцатиперстную кишку, оказывая пропульсивное насосное действие (пилорический насос). 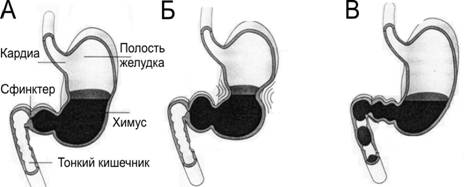 Рис. 22–5. Последовательные фазы опорожнения желудка. А, Б — пилорический сфинктер закрыт, В — пилорический сфинктер открыт. Регуляция опорожнения желудка Темп опорожнения желудка регулируется сигналами из желудка и двенадцатиперстной кишки. Увеличение объёма химуса в желудке способствует интенсивному опорожнению. Это происходит не из-за повышения давления в желудке, а вследствие реализации местных рефлексов и усиления активности пилорического насоса. Гастрин, выделяющийся при растяжении стенки желудка, усиливает работу пилорического насоса и потенцирует перистальтическую активность желудка. Эвакуация содержимого желудка тормозится кишечно-желудочными рефлексами из двенадцатиперстной кишки. Факторы, вызывающие тормозные кишечно-желудочные рефлексы: кислотность химуса в двенадцатиперстной кишке, растяжение стенки и раздражение слизистой оболочки двенадцатиперстной кишки, возрастание осмоляльности химуса, увеличение концентрации продуктов расщепления белков и жиров. Холецистокинин, желудочный ингибирующий пептид тормозят опорожнение желудка. нарушения двигательных функций пищеварительного тракта Проходимость пищеварительного тракта может быть нарушена в различных его отделах. Наиболее общие причины обструкции: злокачественные опухоли, фиброзные сужения, параличи отдельных сегментов кишечника. При обструкции в пилорическом отделе желудка возникает постоянная рвота желудочным содержимым, а потеря водородных ионов приводит к алкалозу. Если обструкция располагается дистальнее желудка, то антиперистальтический рефлюкс забрасывает кишечное содержимое в желудок и вместе с рвотой выводится наружу. Потеря жидкости и электролитов ведет к дегидратации организма. Поскольку в этом случае потеря оснований и кислот примерно одинакова, нарушений КЩР не происходит. Если обструкция располагается в нижнем отделе тонкой кишки, то в рвотных массах преобладают основания и развивается ацидоз. Проксимальнее места обструкции тонкая кишка растягивается за счёт увеличения секреции жидкости и электролитов. Если обструкция имеется в конце толстой кишки, то кал может накапливаться в ней в течение нескольких недель, вызывая в конечном итоге обезвоживание и шок из-за тяжёлой рвоты. Секреторная функция пищеварительного тракта Экзокринные железы пищеварительной системы секретируют пищеварительные ферменты от ротовой полости до дистального отдела тощей кишки и выделяют слизь на всём протяжении ЖКТ. Секрецию регулируют вегетативная иннервация и многочисленные гуморальные факторы. Парасимпатическая стимуляция, как правило, стимулирует секрецию, а симпатическая — подавляет. Таблица 22–2. Влияние различных отделов вегетативной нервной системы на секрецию в пищеварительном тракте
«+» — усиление секреции, «–» — подавление секреции Секреция слюны. Три пары слюнных желёз (околоушные, нижнечелюстные, подъязычные), а также много щёчных желёз ежедневно секретируют от 800 до 1500 мл слюны. Гипотоничная слюна содержит серозный компонент, содержащий -амилазу для переваривания крахмала и слизистый компонент, содержащий муцин для обволакивания пищевого комка и предохранения слизистой оболочки ротовой полости от механического повреждения. Околоушные железы выделяют серозный секрет, нижнечелюстные и подъязычные — слизистый и серозный, щёчные железы — только слизистый. pH слюны колеблется от 6,0 до 7,0. Слюна содержит большое количество факторов, подавляющих рост бактерий (лизоцим, лактоферрин, ионы тиоцианата) и связывающих Аг (секреторный IgA). Слюна предохраняет слизистую оболочку ротовой полости и глотки от повреждающего действия эффекта кислого желудочного содержимого, попадающего в ротовую полость при забросе из желудка. Слюна смачивает пищу, обволакивает пищевой комок для более лёгкого прохождения по пищеводу, осуществляет начальный гидролиз крахмала (-амилаза) и жиров (лингвальная липаза). Стимуляцию секреции слюны осуществляет импульсация, поступающая по парасимпатическим нервным волокнам от верхнего и нижнего слюноотделительных ядер ствола мозга. Эти ядра возбуждаются вкусовыми и тактильными стимулами от языка и других областей ротовой полости и глотки, а также рефлексами, возникающими в желудке и верхнем отделе кишечника. Парасимпатическая стимуляция также усиливает кровоток в слюнных железах. Симпатическая стимуляция влияет на кровоток в слюнных железах двухфазно: вначале снижает, вызывая сужение сосудов, а затем увеличивает его. Секреторная функция пищевода. Стенка пищевода содержит простые слизистые железы по всему протяжению; а ближе к желудку и в начальной части пищевода — сложные слизистые железы кардиального типа. Секрет желёз предохраняет пищевод от повреждающего действия поступающей пищи и от переваривающего действия забрасываемого желудочного сока. Секреторная функция желудка Внешнесекреторная функция желудка направлена на защиту стенки желудка от повреждений (в том числе самопереваривания) и на переваривание пищи. Поверхностный эпителий слизистой оболочки желудка вырабатывает муцины (слизь) и бикарбонат и выполняет защитную функцию путём формирования слизисто-бикарбонатного барьера, находящегося на поверхности эпителия. Слизистая оболочка в различных отделах желудка содержит кардиальные, фундальные и пилорические железы (рис. 22–4Б). Кардиальные железы вырабатывают преимущественно слизь, фундальные (80% всех желёз желудка) — пепсиноген, соляную кислоту, внутренний фактор Касла и некоторое количество слизи; пилорические железы секретируют слизь и гастрин. Слизисто-бикарбонатный барьер Слизисто–бикарбонатный барьер защищает слизистую оболочку от действия кислоты, пепсина и других потенциальных повреждающих агентов. Слизь постоянно секретируется на внутреннюю поверхность стенки желудка. Бикарбонат (ионы HCO3–), секретируемый поверхностными слизистыми клетками (рис. 22–7,I), имеет нейтрализующее действие. pH. Слой слизи имеет градиент pH. На поверхности слоя слизи pH равен 2, а в примембранной части более 7. Н+. Проницаемость плазмолеммы слизистых клеток желудка для Н+ различна. Она незначительна в мембране, обращённой в просвет органа (апикальной), и достаточно высока в базальной части. При механическом повреждении слизистой оболочки, при воздействии на неё продуктов окисления, алкоголя, слабых кислот или жёлчи концентрация H+ в клетках возрастает, что приводит к их гибели и разрушению барьера. 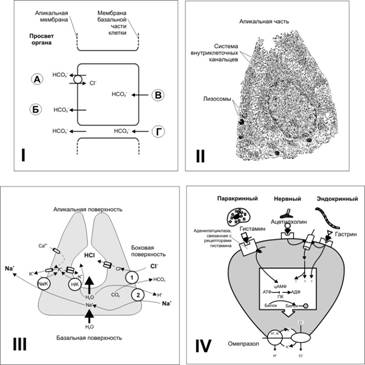 Рис. 22–7. ЖЕЛУДОЧНАЯ СЕКРЕЦИЯ. I —. Механизм секреции HCO3— эпителиальными клетками слизистой оболочки желудка и двенадцатиперстной кишки: А — выход HCO3– в обмен на Cl– стимулируют некоторые гормоны (например, глюкагон), и подавляет блокатор транспорта Cl– фуросемид. Б — активный транспорт HCO3–, не зависящий от транспорта Cl–; В и Г — транспорт HCO3– через мембрану базальной части клетки внутрь клетки и по межклеточным пространствам (зависит от гидростатического давления в подэпителиальной соединительной ткани слизистой оболочки). II — Париетальная клетка. Система внутриклеточных канальцев значительно увеличивает площадь поверхности плазматической мембраны. В многочисленных митохондриях вырабатывается АТФ для обеспечения работы ионных насосов плазматической мембраны.. III — Париетальная клетка: транспорт ионов и секреция HCl. Na+,К+ АТФаза участвует в транспорте K+ внутрь клетки. Cl– входит в клетку в обмен на HCO3– через мембрану боковой поверхности (1), а выходит через апикальную мембрану; 2 — обмен Na+ на H+. Одно из важнейших звеньев — выход H+ через апикальную мембрану по всей поверхности внутриклеточных канальцев в обмен на K+ при помощи H+,К+ АТФазы.. IV — Регуляции активности париетальных клеток. Стимулирующее влияние гистамина опосредуется через цАМФ, тогда как эффекты ацетилхолина и гастрина — через увеличение притока Са2+ в клетку. Простагландины снижают секрецию HCl, ингибируя аденилатциклазу, что приводит к уменьшению уровня внутриклеточного цАМФ. Блокатор H+,K+ АТФазы (например, омепразол) снижает выработку HCl. ПК — протеинкиназа, активируемая цАМФ; фосфорилирует мембранные белки, усиливая работу ионных насосов. [11]. Регуляция. Секрецию бикарбоната и слизи усиливают глюкагон, простагландин Е, гастрин, эпидермальный фактор роста. Для предупреждения повреждения и для восстановления повреждённого барьера применяют антисекреторные агенты (например, блокаторы гистаминовых рецепторов), простагландины, гастрин, аналоги сахаров (например, сукральфат). Разрушение барьера. При неблагоприятных условиях барьер разрушается в течение нескольких минут, происходят гибель клеток эпителия, отёк и кровоизлияния в собственном слое слизистой оболочки. Известны факторы, неблагоприятные для поддержания барьера: нестероидные противовоспалительные препараты (например, аспирин, индометацин); этанол, соли жёлчных кислот, Helicobacter pylori — грамотрицательная бактерия, выживающая в кислой среде желудка. H. pylori поражает поверхностный эпителий желудка и разрушает барьер, способствуя развитию гастрита и язвенного дефекта стенки желудка. Этот микроорганизм выделяют у 70% больных язвенной болезнью желудка и 90% больных язвой двенадцатиперстной кишки или антральным гастритом. Регенерация эпителия, формирующего слой бикарбонатной слизи, происходит за счёт стволовых клеток, расположенных на дне желудочных ямок; время обновления клеток — около 3 суток. Стимуляторы регенерации: гастрин из эндокринных клеток желудка, гастрин-рилизинг гормон из эндокринных клеток и окончаний волокон блуждающего нерва, эпидермальный фактор роста, поступающий из слюнных, пилорических желёз, желёз двенадцатиперстной кишки и других источников. Слизь. Помимо поверхностных клеток слизистой оболочки желудка, слизь секретируют клетки практически всех желёз желудка. Пепсиноген. Главные клетки фундальных желёз синтезирует и секретирует предшественники пепсина (пепсиноген), а также небольшое количество липазы и амилазы. Пепсиноген не обладает пищеварительной активностью. Под влиянием соляной кислоты и особенно ранее образованного пепсина пепсиноген превращается в активный пепсин. Пепсин — протеолитический фермент, активный в кислой среде (оптимум pH от 1,8 до 3,5). При pH около 5 он практически не имеет протеолитической активности и за короткое время полностью инактивируется. Внутренний фактор. Для всасывания витамина B12 в кишечнике необходим (внутренний) фактор Касла, синтезируемый париетальными клетками желудка. Фактор связывает витамин B12 и защищает его от разрушения ферментами. Комплекс внутреннего фактора с витамином B12 в присутствии ионов Ca2+ взаимодействует с рецепторами эпителиальной клетки дистального отдела подвздошной кишки. При этом витамин B12 поступает в клетку, а внутренний фактор высвобождается. Отсутствие внутреннего фактора приводит к развитию анемии. Соляная кислота Соляную кислоту (HCl) вырабатывают париетальные клетки, имеющие мощную систему внутриклеточных канальцев (рис. 22–7,II), существенно увеличивающих секреторную поверхность. Клеточная мембрана, обращённая в просвет канальцев, содержит протонный насос (H+,K+-ATФaза), выкачивающий из клетки Н+ в обмен на К+. Хлорно–бикарбонатный анионообменник встроен в мембрану боковой и базальной поверхности клеток: Cl– входит в клетку в обмен на HCO3– через этот анионообменник и выходит в просвет канальцев. Таким образом, в просвете канальцев оказываются оба компонента соляной кислоты: и Cl–, и H+. Все остальные молекулярные компоненты (ферменты, ионные насосы, трансмембранные переносчики) направлены на сохранение ионного баланса внутри клетки, прежде всего — на поддержание внутриклеточного pH. Таким образом, механизм образования соляной кислоты (рис. 22–7,II) складывается из следующих этапов. Ионы хлора активно транспортируются из цитоплазмы обкладочных клеток в просвет внутриклеточных канальцев, а ионы натрия переносятся наружу. Эти два эффекта создают в канальцах потенциал (от –40 до –70 мВ), приводящий к диффузии большого количества ионов калия и некоторого количества ионов натрия внутрь канальцев. В цитоплазме клетки вода диссоциирует на водородные и гидроксильные ионы. Водородные ионы посредством активного транспорта секретируются внутрь канальцев в обмен на ионы калия. Этот процесс катализирует H+, K+ АТФаза. В результате ионы калия и натрия, которые диффундировали внутрь канальцев, реабсорбируются в цитоплазму клеток, а ионы водорода занимают их место в канальцах, создавая там раствор концентрированной соляной кислоты, который через секреторные канальцы поступает наружу, т.е. на поверхность эпителия желудка. Вода проходит внутрь канальцев под воздействием осмоса. В результате секрет канальцев содержит соляную кислоту в концентрации 150–160 ммоль/л, хлорид калия в концентрации 15 ммоль/л и небольшое количество хлорида натрия. На заключительным этапе углекислота, образующаяся в ходе метаболизма клетки, под влиянием карбоангидразы соединяется с гидроксильными ионами, образуя бикарбонатные ионы. Бикарбонатные ионы диффундируют из цитоплазмы во внеклеточную жидкость в обмен на ионы хлора, входящие в клетку и в дальнейшем секретируемые в канальцы париетальных клеток. В покое клетка секретирует хлор. При стимуляции усиливается работа Н+,К+ АТФазы, в результате чего возрастает транспорт Н+ из клетки. Одновременно в 2–3 раза увеличивается транспорт Cl– в обмен на HCO3–. В итоге внутриклеточный pH остаётся неизменным. Стимуляция обкладочных клеток вызывает выделение кислого раствора, изотоничного внеклеточной жидкости, содержащего 160 ммоль/л соляной кислоты с величиной pH раствора около 0,8. Содержание водородных ионов в этом растворе в 3 млн раз выше, чем в артериальной крови. |
