синтетика 1. Стероидные соединения
 Скачать 0.94 Mb. Скачать 0.94 Mb.
|
|
АО «Южно-Казахстанская медицинская академия» Кафедра фармацевтической и токсикологической химии.  Реферат Тема: Стероидные соединения. Выполнила: Агзамова Д.Б Приняла: Джанаралиева К.С. Группа: В-ТФПОА- «06-19» Шымкент 2022г. План: Введение. Основная часть: Стероидные гормоны и их классификация Гестагенные гормоны. Кортикостероиды и их полусинтетические аналоги Андрогенные и эстрогенные гормоны Заключение. Литература. СТЕРОИДЫ, группа природных и синтетических химических соединений – производных частично или полностью гидрированного 1,2-циклопентенофенантрена типа 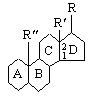 в молекулярном скелете которых 17 атомов углерода образуют 4 сочлененных кольца A, B, C, D. Стероиды широко распространены в природе, они участвуют в осуществлении самых разнообразных биологических функций. Стероидную природу имеют половые гормоны, витамин D, гормоны надпочечников, желчные кислоты, гормоны линьки и метаморфоза членистоногих, репелленты насекомых, отпугивающие хищников, и яды в коже жаб. И природные, и синтетические стероиды при сходном строении проявляют сильно различающееся физиологическое действие, поэтому они широко применяются в медицине в качестве противовоспалительных, сердечных, противозачаточных и других средств. Стероиды подразделяют на стерины, желчные кислоты, стероидные гормоны, стероидные сапонины, сердечные гликозиды и стероидные алкалоиды. Стероидные гормоны и их полусинтетические аналоги Стероидные гормоны являются производными ряда углеводородов, главным образразом: прегниана, андростана, эстрана. Производные прегнана: 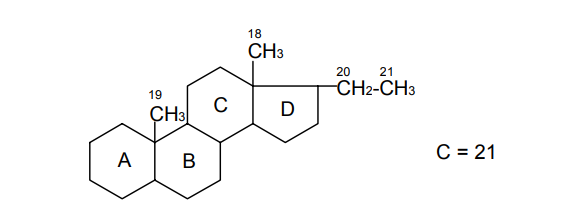 - гестагенные гормоны (гормоны желтого тела) и их синтетические аналоги: прогестерон, прегнин, норэтистерон (норколут), медроксипрогестерона ацетат (депо-провера); - кортикостероиды: дезоксикортона ацетат (дезоксикортикостерона ацетат), кортизона ацетат, гидрокортизон, преднизолон, фторзамещенные вещества (дексаметазон и др.). Производные андростана: 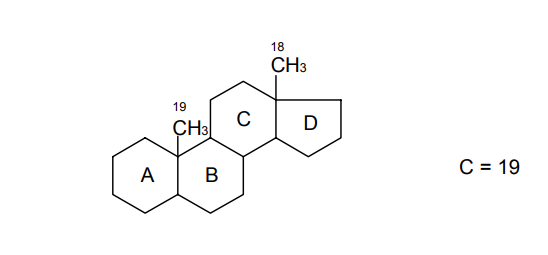 -Андрогенные гормоны и полусинтетические производные, обладающие анаболическим действием (анаболические стероиды): тестостерона пропионат, метилтестостерон, метандиенон (метандростенолон), метандриол (метиландростендиол), нандролона фенилпропионат (феноболин), нандролона деканоат (ретаболил), ципротерона ацетат (андрокур), пипекурония бромид. Производные эстрана: 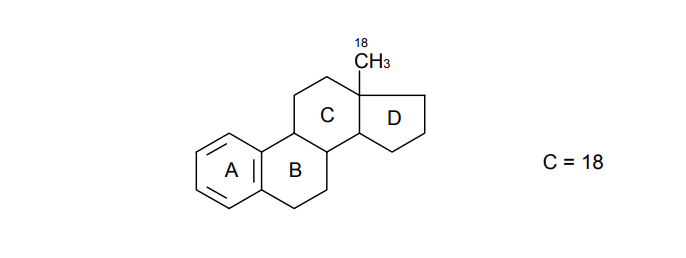 -эстрогенные гормоны: этинилэстрадиол, эфиры эстрадиола. Они сходны между собой по химической структуре. Отличие от андростана состоит лишь в том, что прегнан имеет в молекуле этильный радикал, а эстран - ароматическое ядро и у него отсутствует одна из метильных групп. Структурной основой стероидных гормонов является гидрированный скелет углеводорода циклопентанпергидрофе-нантрена. Общая формула стероидных гормонов может быть представлена следующим образом: Гестагенные гормоны В основе химического строения лежит углеводород прегнан (С = 21): 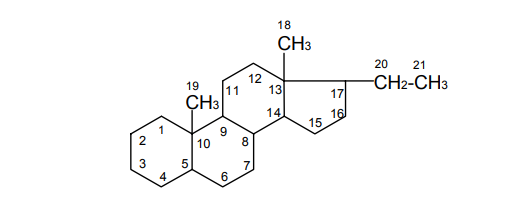 В ГФ включены препараты естественного гормона прогестерона и его полусинтетического аналога прегнина. Прогестерон может быть получен из гормонов желтого тела свиней и полусинтетическим способом из саласодина как промежуточный продукт синтеза кортизона. Прогестерон является гормоном, вырабатывающимся желтым телом и плацентой. Прогестерон подготавливает эндометрий к имплантации яйцеклетки, предупреждает овуляцию, способствует увеличению железистой ткани молочных желез. Прогестерон считается гормоном беременности, поскольку вырабатывается в течение всего периода беременности, уменьшает возбудимость и сократимость матки и одновременно препятствует созреванию новых яйцеклеток. Этот эффект равносилен временной стерильности женщин и применяется для предупреждения беременности. В медицине прогестерон применяется при различных нарушениях менструального цикла, при функциональных маточных кровотечениях разной этиологии, в качестве контрацептивов. Получение Исходными продуктами промышленного синтеза прогестерона могут быть холестерин, диосгенин, 17-кетостероиды. Из холестерина получают прегненолон, который подвергают микробиологическому дегидрированию до прогестерона: 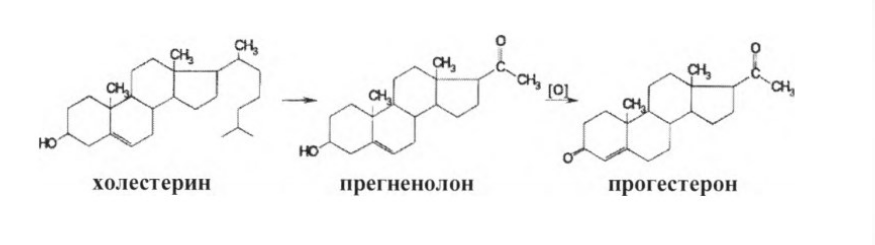 Физические свойства Белые с желтоватым оттенком мелкокристаллические порошки, практически нерастворимые в воде, растворимы в маслах и хлороформе. Оба вещества имеют общий хромофор: карбонильная группа в 3-м положении и двойная связь в положении 4-5. За счет этого хромофора они поглощают в УФ-области спектра и имеют λmax = 240 нм + 2 нм. Метод УФ-спектрофотометрии применяется для оценки качества лекарственных веществ по величине удельного показателя поглощения (Е 1% 1см), в частности для количественного определения веществ относительно стандартных образцов. Прогестерон и прегнин обладают оптической активностью, так как содержат центры хиральности. В оценке качества предусмотрено определение удельного вращения. Химические свойства и методы анализа 1. Концентрированная кислота серная является общим внутригрупповым специфическим реактивом, подтверждающим наличие стероидного цикла. При взаимодействии с ней образуются окрашенные в желтый (прогестерон) или малиновый (прегнин) цвет флуоресцирующие растворы. Специфичность данной реакции низкая. Для более надежной идентификации веществ применяют ИК-спектроскопию. 2. Гестагенные гормоны содержат в 3-м положении карбонильную группу, поэтому способны к взаимодействию с аминопроизводными, образуя окрашенные продукты или продукты с характерными температурами плавления (подлинность). 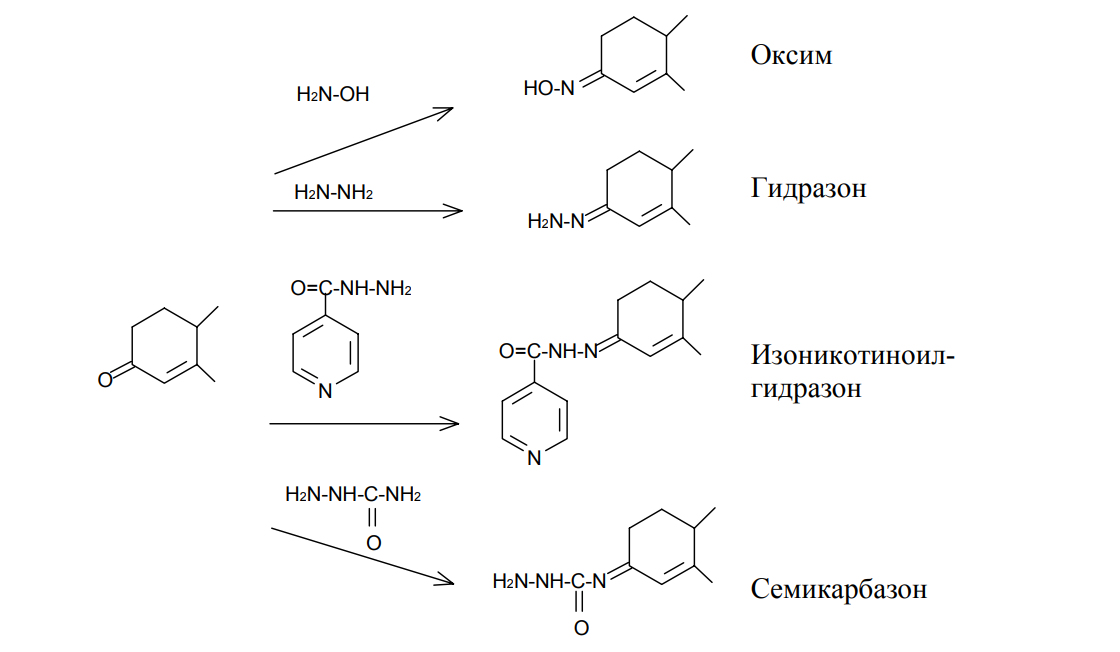 Эти продукты могут служить гравиметрической формой для количественного определения (прогестерон в масляном растворе). Реакцию образования оксима ГФ рекомендует для испытания подлинности прегнина (Т.пл. – 226-232 о С): 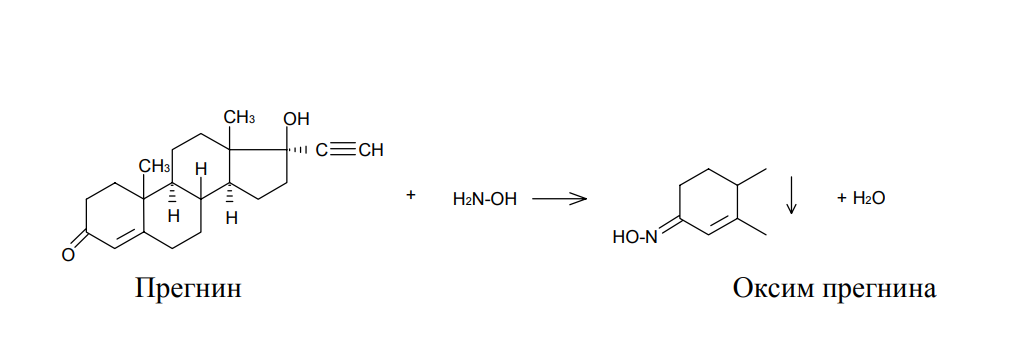 Прогестерон и прегнин отличаются по заместителям в 17-ом положении. Прогестерон содержит ацетильный фрагмент. При нагревании с иодом в щелочной среде образуется желтый осадок с характерным запахом – иодоформ (СНI3). Для прегнина отличительной особенностью строения является наличие этинильной группы (остаток ацетилена), который сохраняет кислотные свойства и взаимодействует с серебра нитратом: 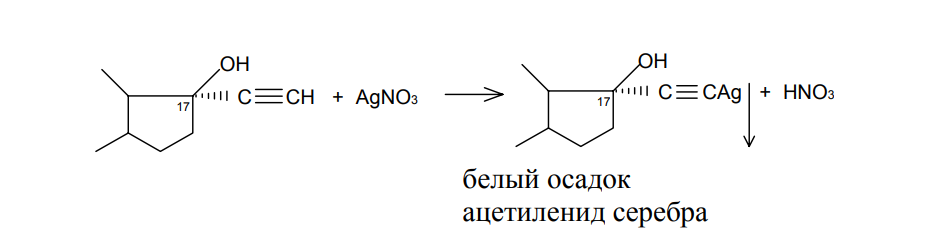 Кислота азотная выделяется в количестве, эквивалентном прегнину, что может использоваться для количественного алкалиметрического определения: HNO3 + NaOH → NaNO3 + H2O Методы количественного определения 1. Прегнин в порошке и таблетках определяют спектрофотометрически при длине волны 241 нм (по отношению к 0.001 % раствору стандартного образца прегнина): 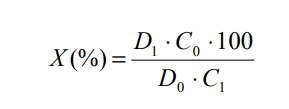 2. Реакцию образования 2,4-динитрофенилгидразона используют по ГФ для количественного определения прогестерона (весовой метод): 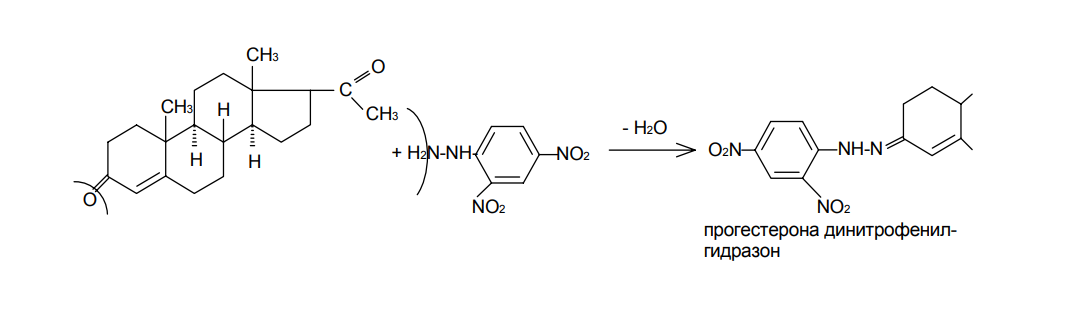 Хранение и применение Лекарственные вещества светочувствительны, поэтому их хранят в темном месте в хорошо укупоренной таре, по списку Б. Прогестерон и прегнин применяют в качестве гестагенных препаратов при нарушениях функции яичников, связанных с недостаточностью желтого тела. Прогестерон назначают в виде 1% или 2,5%-ных растворах в масле для инъекций. Прегнин в 5-6 раз менее активен, чем прогестерон, но, в отличие от него, сохраняет активность при пероральном введении, особенно при подъязычном применении КОРТИКОСТЕРОИДЫ Гормоны коркового слоя надпочечных желез (кортикостероиды) являются производными кортикостерона, структура которого включает стероидный цикл – прегнан: 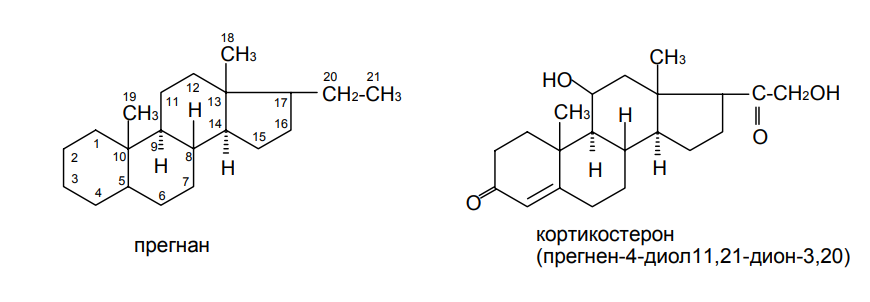 По действию на организм кортикостероиды условно делят на две группы: минералокортикостероиды и глюкокортикостероиды. Минералокортикостероиды активно регулируют минеральный обмен и слабо влияют на углеводный и белковый обмен. Глюкокортикостероиды активно регулируют углеводный и белковый обмен и слабо влияют на минеральный. 297 Лекарственные средства – производные глюкокортикостероидов – по своей активности превосходят природные соединения, могут применяться внутрь и имеют меньше побочных реакций. Источниками получения кортикостероидов служат либо надпочечные железы убойного скота, либо природные вещества стероидной структуры, в частности, холестерин, который считают предшественником кортикостероидов в организме. Физические и химические свойства препаратов кортикостероидов и их полусинтетических аналогов сходны между собой. Это обусловлено общностью химической структуры. Являясь производными прегнана, все они имеют карбонильную (кетонную) группу в положении 3, гидроксильную или кетонную группу в положении 11. В положении 17 все кортикостероиды содержат лабильную α-кетольную группировку, отличающуюся высокой восстановительной способностью. Спиртовая группа в положении 21 позволяет получать сложные эфиры кортикостероидов. Физические свойства Препараты гормонов коры надпочечников и их синтетических аналогов представляют собой белые кристаллические вещества, имеющие желтоватый или кремовый оттенок без запаха. Они практически нерастворимы в воде, трудно или мало растворимы в большинстве органических растворителей. Препараты кортикостероидов и их аналоги являются правовращающими оптическими изомерами. Они поглощают в УФ-спектре за счет хромофора в кольце А (λmax = 238-244 нм). Химические свойства и методы анализа Стероидный цикл Вещества идентифицируются общегрупповой цветной реакцией с концентрированной кислотой серной. Реакция проводится с кристаллическими веществами, образуются окрашенные, а иногда и флуоресцирующие в УФ-свете, продукты. Например, дезоксикортикостерон дает вишневое окрашивание с зелено-коричневой флуоресценцией; кортизон – желтое окрашивание; гидрокортизон – желтое окрашивание с зеленой флуоресценцией; преднизон –зеленовато-желтое; преднизолон - красное окрашивание. α-Кетольная группа Все кортикостероиды, благодаря наличию α-кетольной (20-кето-21- гидрокси-)группы, обладают восстановительными свойствами. 298 Кортикостероиды очень легко окисляются, причем под действием разной силы окислителей образуются различные продукты. Реакции могут использоваться в определении подлинности веществ и для их количественного определения в лекарственных формах (ФЭК) Так, например, под действием слабых окислителей образуется 17- кетоальдегид. В качестве таких окислителей могут быть использованы: 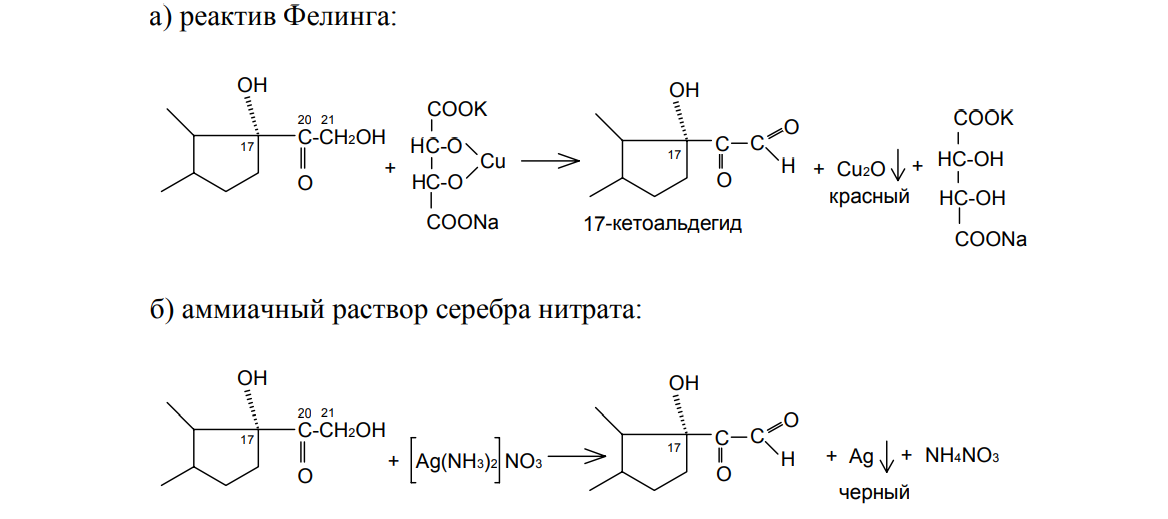 в) раствор хлорида 2,3,5-трифенилтетразолия (специфичная реакция Гёрёга). Соль тетразолия восстанавливается до красного формазана и происходит раскрытие цикла. Данную реакцию используют все зарубежные фармакопеи для количественного определения кортикостероидов (ФЭК при λmax = 590 нм): 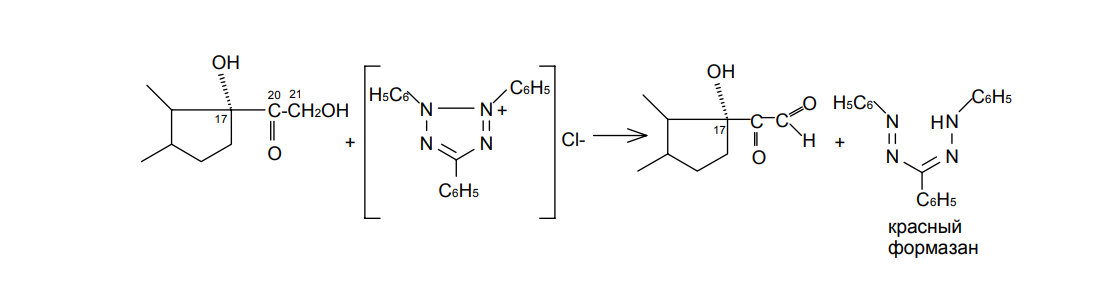 Под действием перйодата калия, хлорной кислоты или фосфорномолибденовой кислоты образуется 17-карбоновая кислота, выделяется формальдегид, который можно связывать хромотроповой кислотой (получение ауринового красителя фиолетового цвета): 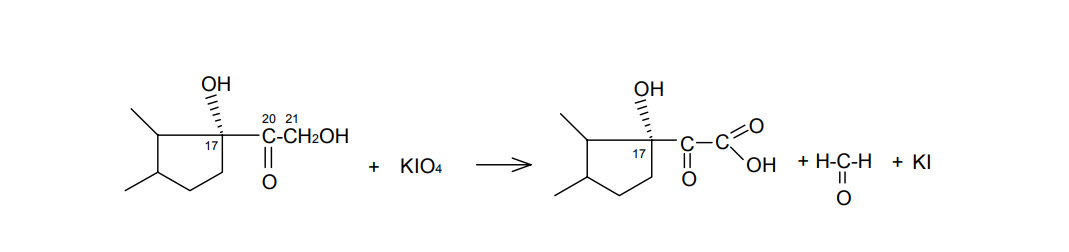 3)Карбонильная группа в 3-м положении Реакции присоединения с элиминированием воды, которые приводят к образованию окрашенных продуктов или веществ, имеющих определенную температуру плавления. Эти реакции применяются для подтверждения подлинности лекарственных веществ и их количественной оценки: 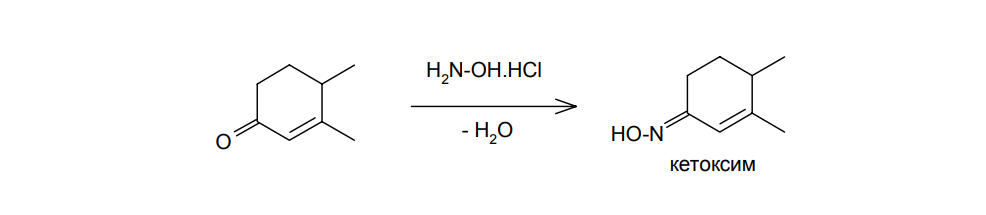 Сложно-эфирная группа Для идентификации лекарственных средств, представляющих собой сложные эфиры, используется реакция получения ацетгидроксамовой кислоты (гидролиз сложно-эфирной связи в щелочной среде и взаимодействие с NH2OH), которая затем с солями железа (III) образует соединения, окрашенные в красно-коричневый (дезоксикортикостерона ацетат) или темно-вишневый (кортизона ацетат) цвет: 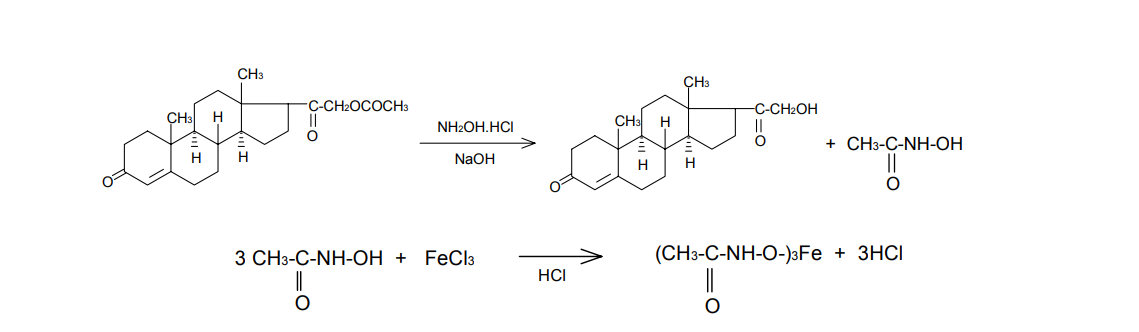 Методы количественного определения Спектрофотометрическое определение в УФ-области (кортизона ацетат, преднизон). Чистота Из примесных соединений во всех препаратах этой группы определяются посторонние стероиды. Используется ВЭЖХ или ТСХ. Хранение: Список Б. В защищенном от света месте Андрогенные гормоны Андрогенные гормоны вырабатываются мужскими половыми железами (тестикулами) в период половой зрелости. В химическом отношении эти вещества являются производными андростана: 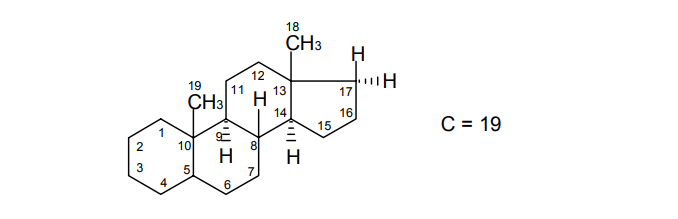 В практической медицине в качестве андрогенов широко используются эфиры тестостерона (пропионат, ципионат и энантат) и его синтетический аналог - метилтестостерон Получение Промышленный способ получения тестостерона может быть осуществлен из ацилированного дигидропрегненолона, полученного из холестерина и путем микробиологического окисления и отщепления боковой цепи у (3-ситостерина: 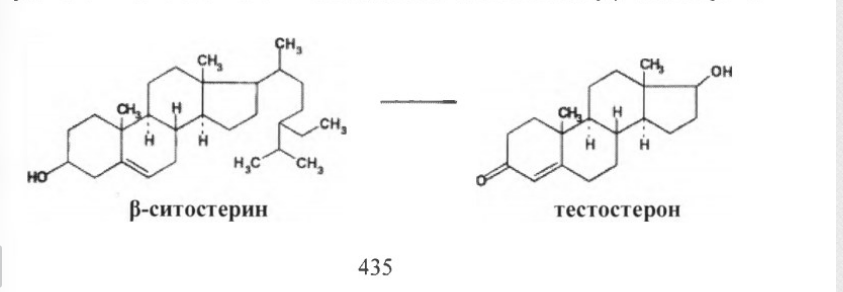 Физические свойства Белые с желтоватым оттенком мелкокристаллические порошки, нерастворимые в воде, растворимы в спирте, хлороформе и маслах. Химические свойства и методы анализа 1. Для идентификации веществ используют общегрупповую реакцию на стероидный цикл с кислотой серной концентрированной: метилтестостерон и метиландростендиол образуют желто-оранжевое окрашивание с характерной флуоресценцией, метандростенолон – красное окрашивание. 2. Для обнаружения кетогруппы в 3 положении (тестостерона пропионат, метилтестостерон, метандростенолон) проводят общие реакции образования оксимов, гидразонов, изоникотиноилгидразонов, фенилгидразонов: 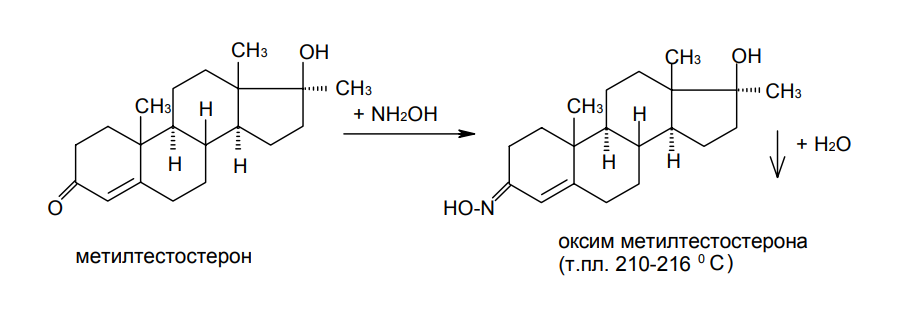 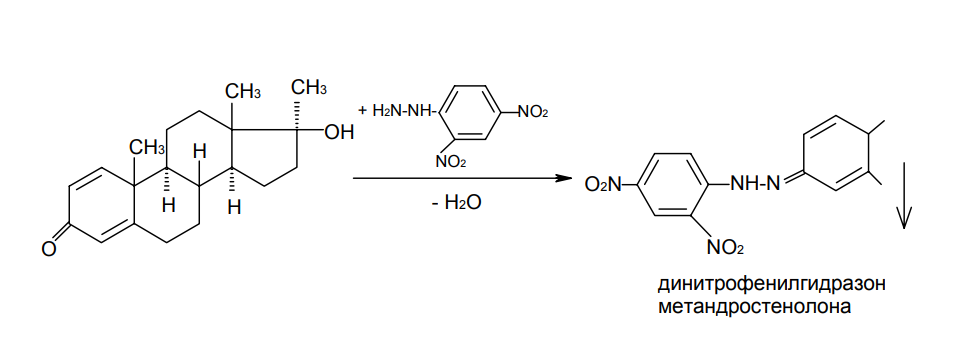 Тестостерона пропионат можно идентифицировать по сложноэфирной группировке: а) по реакции гидролиза с последующей проверкой температуры плавления выделяющегося тестостерона (Т.пл. 150-156 о С): 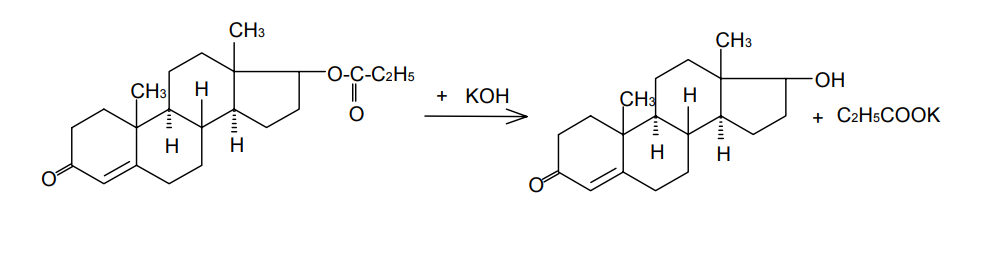 Количественное определение 1) Перечисленные реакции лежат в основе методов количественного определения (гравиметрия оксимов, гидразонов; ФЭК гидроксаматов) 2) Метод УФ-спектрофотометрии. 3) Фотоколориметрия (1% и 5 % масляные растворы тестостерона пропионата определяют по окраске изоникотиноилгидразона тестостерона пропионата). Хранение Андрогенные и анаболические стероидные препараты хранят по списку Б, в хорошо укупоренной таре, предохраняя от действия света и влаги. Эстрогенные гормоны Эстрогенные гормоны вырабатываются в фолликулах. Они являются производными эстрана (кольцо А – ароматическое): 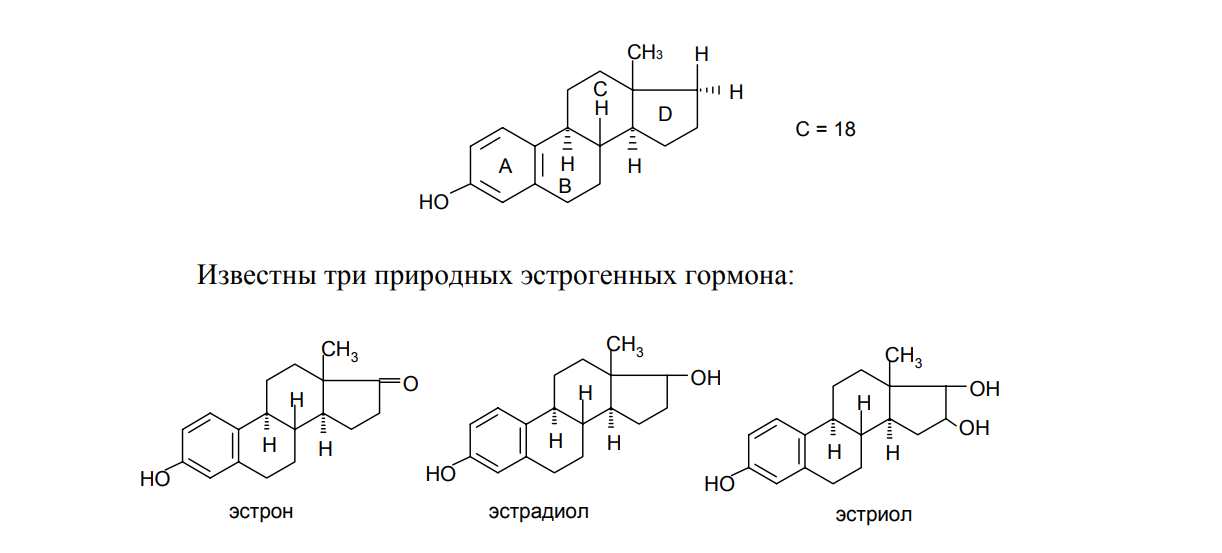 Одним из основных эстрогенов является эстрадиол. Эстрадиол имеет два гидроксила: в 3-м положении – фенольный и в 17-м положении – спиртовой. В качества лекарственного средства применяется эстрадиола ди- 304 пропионат. В этой форме вещество более устойчиво и оказывает пролонгированное действие. Наряду с этим препаратом применяется синтетический аналог с этинильной группой (не гормон, но обладает эстрогенной активностью) – этинилэстрадиол. Выпускается в таблетках по 0.00001 и 0.00005 г. Применяется при гипофункции яичников как средство заместительной терапии, а также входит в состав оральных контрацептивных средств (вместе с гестагенами). Получение Промышленный способ получения эстрона основан на использовании в качестве исходного продукта 1,4,6-андростантриен-3,17-диона, который при нагревании до 600°С ароматизируется с выбросом молекулы метана с образованием 8,9-дигидроэквиленина. Двойная связь последнего в положении Сб-С7 была восстановлена водородом над палладиевым катализатором с получением эстрона: 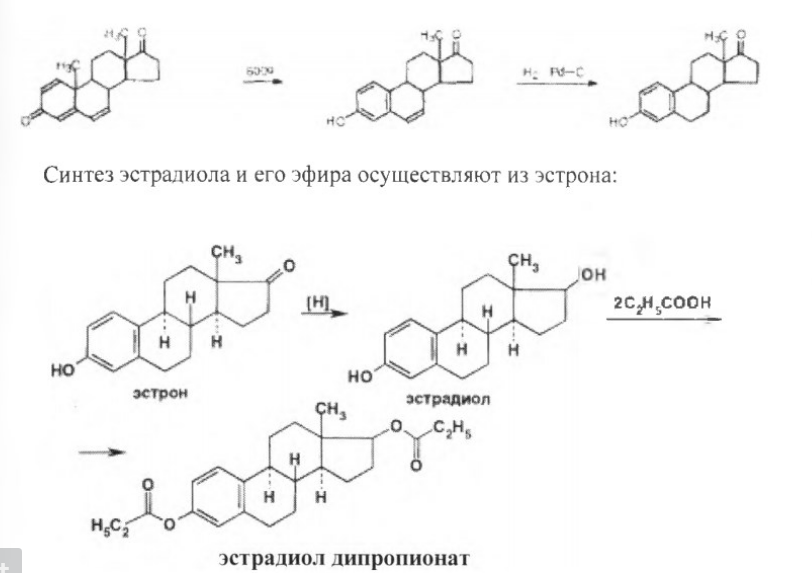 Физические свойства Белые, слегка желтоватого цвета мелкокристаллические порошки, очень мало растворимые в воде, растворимы в спирте и в щелочах, так как являются фенолами. За счет ароматического кольца А поглощают в УФобласти спектра (λmax = 280 нм). Химические свойства и методы анализа Подлинность вещества устанавливается общей цветной реакцией на стероидный цикл с конц. H2SO4: этинилэстрадиол дает оранжево-красную окраску с желтовато-зеленой флуоресценцией; местранол – кровавокрасное окрашивание с аналогичной флуоресценцией. Эстрадиола дипропионат под действием конц. H2SO4 гидролизуется с образованием пропионовой кислоты. Последующее нагревание в присутствии этанола ведет к образованию этилового эфира пропионовой кислоты, имеющего характерный запах: 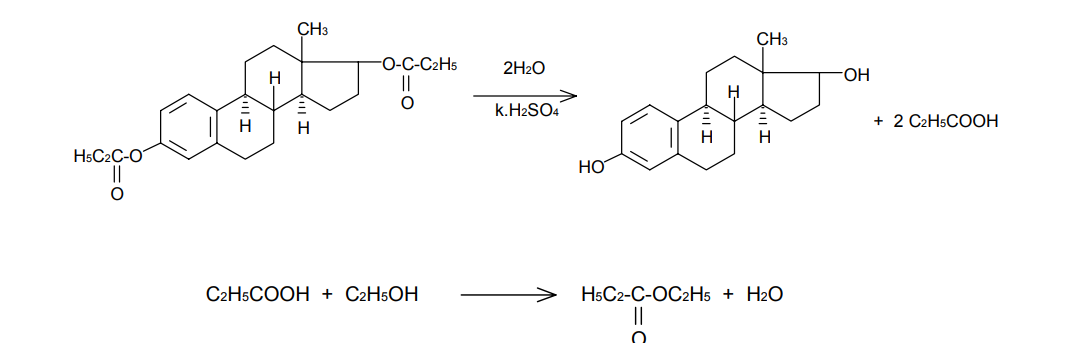 Ароматическое кольцо А в стероидном цикле имеет фенольный гидроксил и его можно идентифицировать по реакциям: а) электрофильного замещения (бромирование, нитрование, образование азокрасителя, ауринового красителя). Например, азокраситель получают путем сочетания фенола с солью диазония (получают из сульфаниловой кислоты) в щелочной среде. Образуется раствор темно-красного цвета. Эта реакция применяется для количественного определения этинилэстрадиола в таблетках: 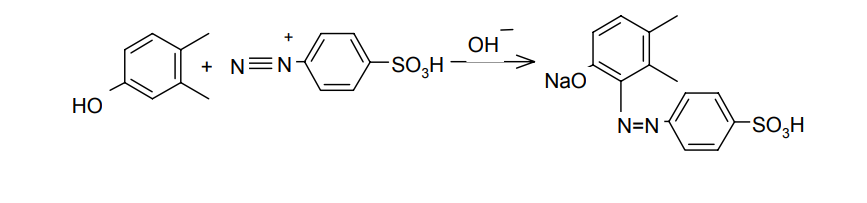 С реактивом Марки (формальдегид в конц. серной кислоте) образуется ауриновый краситель, окрашенный в малиновый или фиолетовый цвет; б) по реакции солеобразования и комплексообразования с солями тяжелых металлов, например с FeCl3; в) образования сложных эфиров, например, с бензоилхлоридом, которые имеют характерную температуру плавления: 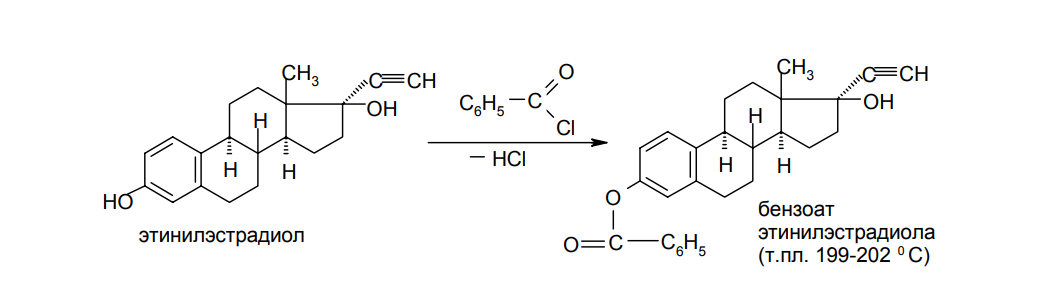 Эстрадиола дипропионат идентифицируют по образованию эстрадиола (Т.пл. 173-179 о С) после щелочного гидролиза с последующей очисткой его от примесей. Для идентификации используют ИК- и УФ-спектры лекарственных веществ стероидной природы. Для доказательства этинильной группы в структуре этинилэстрадиола применяется реакция с AgNO3. Этинилэстрадиол количественно определяют методом косвенной нейтрализации, также как прегнин. Методы количественного определения 1) ФЭК Этинилэстрадиол (таблетки) определяют по окраске азокрасителя: 2) Для количественного определения эстрадиола дипропионата используют реакцию омыления точно отмеренным количеством 0.1 М спиртового раствора гидроксида калия, избыток которого титруют 0.1 М раствором соляной кислоты (индикатор фенолфталеин): 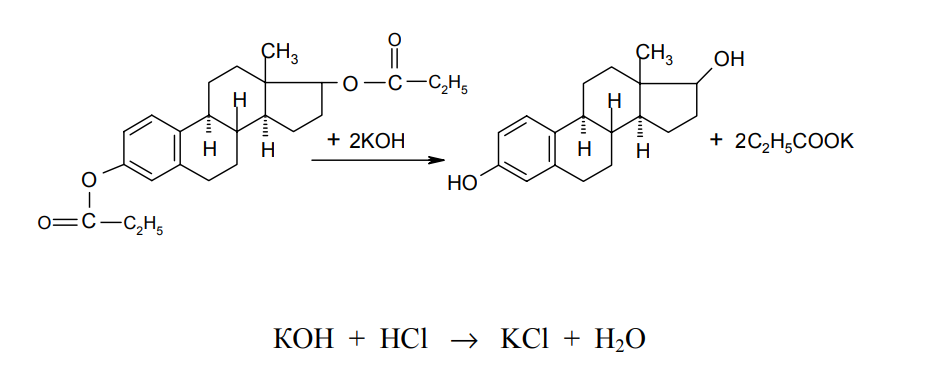 Хранение Список Б. Этинилэстрадиол хранят в хорошо укупоренных банках оранжевого стекла, а эстрадиола дипропионат в сухом, защищенном от света месте. Заключение: Стероидные гормоны — группа физиологически активных веществ (половые гормоны, кортикостероиды и др.), регулирующих процессы жизнедеятельности у животных и человека. У позвоночных синтезируются из холестерина в коре надпочечников, клетках Лейдига семенников, в фолликулах и желтом теле яичников, а также в плаценте. Ряд перечисленных химических реакций применяют для количественного определения стероидных гормонов и их аналогов титриметрическими или фотоколориметрическим методами. Испытания на подлинность и количественное определение выполняют также методом УФ-спектрофотометрии. Список литературы: 1)Учебник: Арыстанова Т.А. Фармацевтическая химия. (Том 1) стр.(494-536). 2) Учебник: А.П.Арзамасцев. Фармацевтическая химия. 3)Государственная фармакопея РеспубликиКазахстан.-Алматы: Издательский дом «Жибек жолы».-2008.-Том1 4) https://puzatik.net/raznoe/steroidnyj-gormon-steroidnyj-profil-v-slyune-vezhh.html 5) http://алхимия-красоты.рф/views/alchemy/theory/chemistry/biochemistry/steroids.php |
