Тема 4 Межклеточная передача возбуждения. Физиология синапсов
 Скачать 336.59 Kb. Скачать 336.59 Kb.
|
|
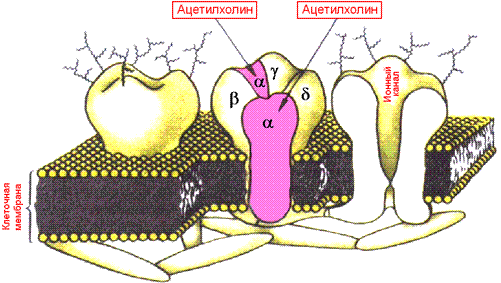
| В качестве примера ионотропного синапса приведем Н-холинергический синапс |
Рецепторы постсинаптических мембран - это белковые структуры, которые являются интегральными белками плазматической мембраны, они синтезируются в эндоплазматическом ретикулюме клетки, после чего они попадают (встраиваются) в постсинаптическую мембрану, пройдя предварительно "сортировку" в аппарате Гольджи. При нарушении белкового синтеза концентрация рецепторов может существенно снижаться и приводить к уменьшению функциональных возможностей синаптической передачи. В ряде случаев у человека могут вырабатываться антитела к собственным рецепторам постсинаптической мембраны. Это приводит к нарушению функции синапса. Синтез рецепторов - контролируемый процесс. Например, если мышца денервирована, то число рецепторов области постсинаптической мембраны снижается. Одновременно во внесинаптических областях возрастает концентрация рецепторов, это делает мышцу более чувствительной в отношении циркулирующего в крови медиатора .
Постсинаптические потенциалы
О
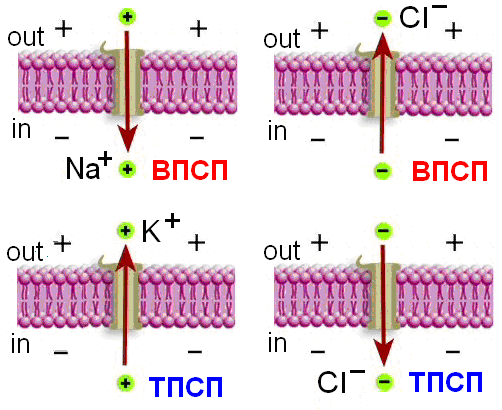 бразование постсинаптических потенциалов связано с активацией медиатором хемовозбудимых (рецепторуправляемых) ионных каналов, имеющихся в постсинаптической мембране. Так же как электровозбудимые, хемовозбудимые каналы образованы макромолекулами белка, пронизывающими липидный бислой мембраны.
бразование постсинаптических потенциалов связано с активацией медиатором хемовозбудимых (рецепторуправляемых) ионных каналов, имеющихся в постсинаптической мембране. Так же как электровозбудимые, хемовозбудимые каналы образованы макромолекулами белка, пронизывающими липидный бислой мембраны. Деполяризация постсинаптической мембраны получила название возбуждающий постсинаптический потенциал (ВПСП). ВПСП может быть обусловлена входом в клетку катиона или выходом аниона
ВПСП распространяется электротонически в околосинаптическую (например, в мионевральном синапсе) или более отдалённую (например, аксонный холмик нейрона) область плазматической мембраны.
Если значение электротона в названных областях достаточно велико и достигает критического уровня деполяризации, то генерируется потенциал действия.
Эта деполяризация постсинаптической мембраны имеет нерегенеративный характер, поскольку хемовозбудимые каналы не обладают электровозбудимостью: порция медиатора, поступившая к постсинаптической мембране, активирует определенное число хемовозбудимых каналов. Это вызывает деполяризацию мембраны, но такая деполяризация не способствует дальнейшему увеличению числа активируемых каналов. Поэтому значение постсинаптического потенциала зависит от концентрации медиатора, действующего на мембрану: чем больше эта концентрация, тем выше до определенного предела постсинаптический потенциал.
Таким образом, постсинаптический потенциал в отличие от потенциала действия градуален. То есть, возбуждение в постсинаптической мембране в форме образования постсинаптического потенциала происходит по закону силы, а не по закону «всё или ничего» как при образовании потенциала действия. В этом отношении постсинаптический потенциал сходен с локальным ответом, хотя имеет иной механизм.
В тормозных синапсах в результате взаимодействия медиатора с рецепторами происходит гиперполяризация (например за счет увеличения проницаемости мембраны для ионов калия и хлора, при этом калий выходит, а хлор входит в клетку).
Это называется тормозным постсинаптическим потенциалом (ТПСП). В гиперполяризованном состоянии клетка снижает свою возбудимость и благодаря этому прекращает отвечать на внешние раздражители, или (если она обладала свойством автоматии) уменьшает спонтанную активность.
Метаботропные синапсы.
При передаче сигнала в метаботропных синапсах используется мультимолекулярная система, состоящая из
рецептора,
ГТФ-связывающего белка (G-белка),
фермента,
второго посредника,
э
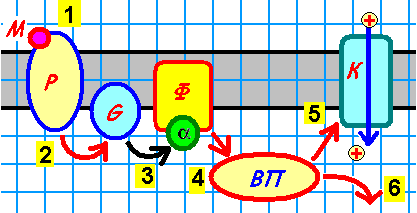 ффектора.
ффектора.Мультимолекулярная система: рецептор – G-белок - фермент - второй посредник - эффектор. 1 ‑ взаимодействие медиатора и рецептора; 2 ‑ активация рецептором G-белка; 3 ‑ активация альфа-субединицей фермента; 4 ‑ образование второго посредника; 5 ‑ влияние на ионный канал; 6 ‑ влияние на транскрипцию или трансляцию.
Как могут быть связаны (сопряжены) метаботропные рецепторы с ионным каналом?
Через G-белки (система «G-белок – ионный канал»): М‑холинорецепторы, адренорецепторы
Через изменение концентрации внутриклеточного посредника типа циклического аденозинмонофосфата (цАМФ), в результате чего меняется активность внутриклеточных протеаз - а как следствие этого - изменение функциональной активности клетки.
G
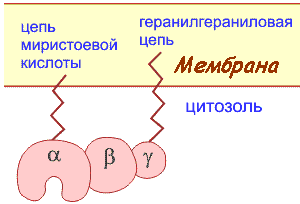 -белки — это семейство белков, относящихся к ГТФазам и функционирующих в качестве вторичных посредников во внутриклеточных сигнальных каскадах. G-белки названы так, поскольку в своём сигнальном механизме они используют замену ГДФ на ГТФ как молекулярный функциональный «выключатель» для регулировки клеточных процессов. G-белки принадлежат к большой группе ферментов ГТФаз.
-белки — это семейство белков, относящихся к ГТФазам и функционирующих в качестве вторичных посредников во внутриклеточных сигнальных каскадах. G-белки названы так, поскольку в своём сигнальном механизме они используют замену ГДФ на ГТФ как молекулярный функциональный «выключатель» для регулировки клеточных процессов. G-белки принадлежат к большой группе ферментов ГТФаз.G-белки биологических мембран имеют гетеротримерную структуру. Они состоят из большой альфа-субъединицы (около 45 килодальтон - кДа), а также меньших бета- и гамма-субъединиц.
ГТФ-азный цикла G‑ белков
В покое на постсинаптической мембране находится комплекс рецептор‑G-белок c ГДФ.
В литературе выделяют 5, 6 и более фаз.
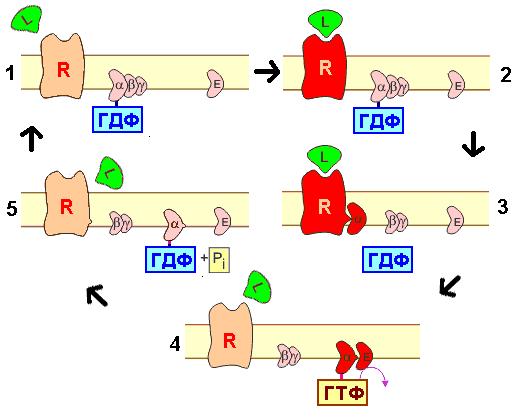
ГТФ-азный цикла G‑белков. 1- фаза покоя; 2 - оединяется медиатора (лиганда) к рецептору; 3 - диссоциация G‑белка; 4 - активация эффектора; 5 - дефосфорилирование ГТФ. Красное окрашивание рецептора на рисунке символизирует активацию; R – рецептор; Е - эффектор; L – медиатор (лиганд, агонист).
Связывание медиатора (агониста) с рецептором приводит к белок-белковому взаимодействию между рецептором и G-белком и ускоряет диссоциацию ГДФ. В результате образуется короткоживущий комплекс агонист - рецептор - G-белок, не связанный ни с каким нуклеотидом.
Связывание с этим комплексом молекулы ГТФ снижает сродство рецептора к G‑белку, что приводит к диссоциации комплекса и высвобождению рецептора.
Потенциально рецептор может активировать большое количество молекул G-белка, обеспечивая, таким образом, высокий коэффициент усиления внеклеточного сигнала на данном этапе.
Активированная альфа-субъединица G‑белка диссоциирует от бета-гамма-субъединиц и вступает во взаимодействие с соответствующим эффектором, оказывая на него активирующее или ингибирующее воздействие.
Альфа-субъдиница с присоединенным с ней ГТФ способна взаимодействовать с эффектором в мембране - ферментами, такими, как аденилатциклаза , или, возможно, ионными каналами . Фермент может активироваться или ингибироваться, а ионный канал - открываться или закрываться. Конкретные примеры будут рассмотрены ниже и в последующих лекциях.
Взаимодействие с эффектором, однако, длится до тех пор, пока альфа-субъединица, являющаяся ГТФ-азой, удерживает ГТФ.
Вскоре присоединенный ГТФ гидролизуется до ГДФ. Когда это происходит, альфа‑субъединица снова меняет свою конформацию и теряет способность активировать эффектор. После этого альфа-ГДФ взаимодействует с бета-гамма-комплексом и снова образует тримерный комплекс, завершая, таким образом, цикл.
Предполагают, что комплекс из бета-гамма-субъединиц тоже может (прямо или опосредованно) влиять на эффекторные ферменты и ионные каналы.
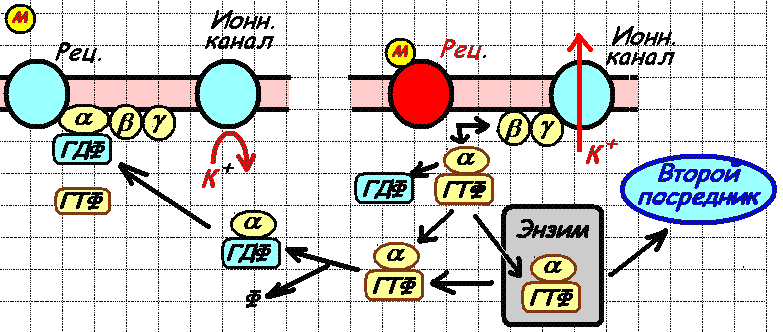
Влияние бета-гамма-субъединиц G‑белка на ионные каналы.
П
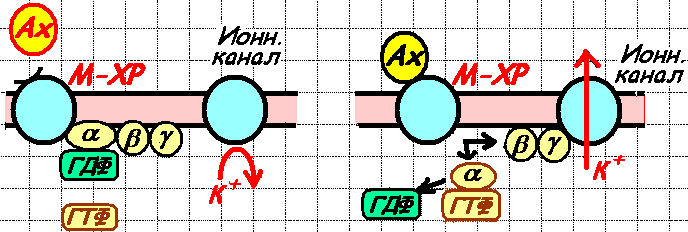 ример прямой активация калиевого канала субъединицами G-белка показан
ример прямой активация калиевого канала субъединицами G-белка показан Прямая активация калиевого канала субъединицами G-белка (вариант для воспроизведения).
Нервно-мышечный синапс скелетного мышечного волокна.
Нервно-мышечный синапс (НМС) довольно большие образования, различимые даже под лупой. Изучение этих синапсов было начато раньше других. Поэтому НМС хорошо изучены.
Следует отметить, что длительная история изучения НМС привела к возникновению многочисленных синонимов как по отношению к названию синапсу, так и его частей. Синонимы НМС – мионевральный синапс, нервно-мышечное соединение, аппарат нервно-мышечный, бляшка двигательная, бляшка моторная, синапс аксо-мышечный, синапс нейромускулярный, моторная бляшка, двигательная бляшка, двигательный концевой аппарат, концевая пластинка, двигательная концевая пластинка.
Следует отметить, что длительная история изучения НМС привела к возникновению многочисленных синонимов как по отношению к названию синапсу, так и его частей. Синонимы НМС – мионевральный синапс, нервно-мышечное соединение, аппарат нервно-мышечный, бляшка двигательная, бляшка моторная, синапс аксо-мышечный, синапс нейромускулярный, моторная бляшка, двигательная бляшка, двигательный концевой аппарат, концевая пластинка, двигательная концевая пластинка.
Но концевой пластинкой (End-Plate) чаще называют постсинаптическую мембрану, отсюда возбуждающий постсинаптический потенциал (ВПСП) чаще называют потенциалом концевой пластинки (ПКП).
Нервный отросток проходя по сарколемме мышечного волокна утрачивает миелиновую оболочку и образует сложный аппарат с цитолеммой мышечного волокна.
| НМС – типичный химический синапс. Холинергический, потому что медиатором является ацетилхолин. Н-холинергический [эн, не аш и не эйч], потому что агонистом ацетилхолина в этом синапсе является никотин. Часто такие синапсы называют никотиновыми. Н-холинергический, мышечного типа, потому что антагонистами ацетилхолина в этом синапсе являются кураре и курареподобные вещества. |
Структура нервно-мышечного синапса
М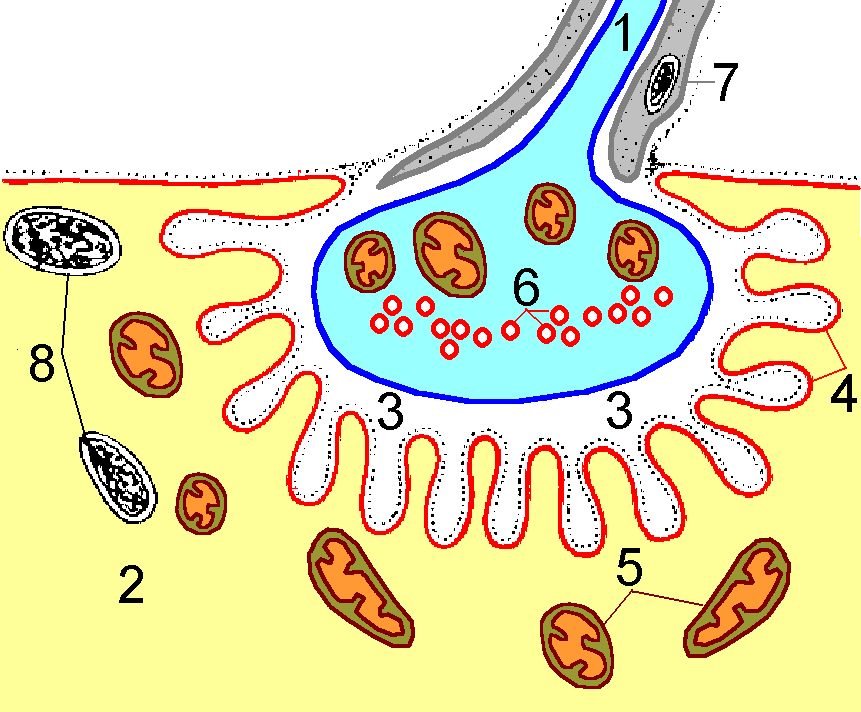 ионевральный синапс (по Е.А.Шубниковой с изменениями). 1 — аксон мотонейрона: 2 — мышечное волокно; 3 — синаптическая щель; 4 — пальцевидные инвагинации сарколеммы; 5 — митохондрии мышечного волокна; 6 — синаптические пузырьки; 7 — леммоцит; 8 — ядра мышечного волокна.
ионевральный синапс (по Е.А.Шубниковой с изменениями). 1 — аксон мотонейрона: 2 — мышечное волокно; 3 — синаптическая щель; 4 — пальцевидные инвагинации сарколеммы; 5 — митохондрии мышечного волокна; 6 — синаптические пузырьки; 7 — леммоцит; 8 — ядра мышечного волокна.
Для НМС характерно наличие большого числа изгибов на пресинаптической и, особенно, на постсинаптической мембране. Благодаря этому, вероятно, возрастает площадь контакта пресинапса с постсинапсом, что увеличивает вероятность взаимодействия.
Терминали аксонов содержат большое количество митохондрий и синаптических пузырьков с медиатором (ацетилхолином).
В основном везикулы расположены в определенных местах пресинапса - около так называемых активных зон. В норме везикулы не подходят близко к пресинаптической мембране, вероятно, из-за того, что имеют такой же заряд, как и пресинапс, хотя возможно и наличие жесткой структуры, которая удерживает везикулы в подвешенном состоянии. Каждая везикулам содержит примерно по 1000-10000 молекул ацетилхолина.
Синаптическая мембрана аксона и постсинаптическая мембрана мышечного волокна разделены синаптической щелью.
В синаптической щели расположен гликокаликс - волокна, которые выполняют опорную функцию (связь механическая). Здесь расположена ацетилхолинэстераза (АХЭ), способная расщеплять ацетилхолин со скоростью 1 мл/мс.
В области синапса мышечное волокно не имеет поперечной исчерченности, характерно скопление митохондрий и ядер.
Гребешки постсинаптической мембраны следуют с интервалом примерно в 1 мкм. На вершине гребешка концентрация холинорецепторов достигает максимальных значений (примерно 20000 рецепторов на 1 мкм кв.), а в устьях - т.е. в глубине - около 1000 рецепторов. Во внесинаптической зоне, естественно, концентрация холинорецепторов меньше - порядка 50 на 1 мкм кв.
Молекулярная масса рецепторов нервно-мышечного синапса определена с помощью методики связывания рецептора бунгаротоксином (яд полосатой крайоты - вид змеи) и равна 250.000. Молекула рецептора состоит из 5 субъединиц – 2‑х α, β, γ, δ. Узнающая субъединица - это α. Внешне рецептор похож на гриб. Внутри рецептора проходит ионный канал, пропускающий Na+.
Этапы передачи возбуждения в НМС
1. Деполяризация пресинаптической мембраны пришедшим по аксону потенциалом действия (ПД).
2. Открытие потенциалзависимых Сa++ каналов на пресинаптической мембране и поступление Сa++ в пресинапс (пассивный транспорт).
3. Выход в синаптическую щель ацетилхолина путем экзоцитоза.
4. Диффузия медиатора к постсинаптической мембране.
5. Взаимодействие ацетилхолина с Н холинорецепторами постсинаптической мембраны мышечного волокна.
6. Открытие никотиновых рецепторных каналов постсинаптических каналов, пассивный вход Na+ в мышечное волокно.
7. Образование потенциала концевой пластинки - ПКП (возбуждающего постсинаптического потенциала - ВПСП) в области постсинаптической мембраны.
8. Электротоническое распространение ПКП в околосинаптическую область.
9. Формирование ПД мышечного волокна на сарколемме околосинаптической области.
| Ацетилхолин в синаптической щели быстро разрушается ацетилхолинэстеразой (АХЭ), превращаясь в холин (он вновь захватывается для последующего синтеза) и ацетат. |
Миниатюрный потенциал концевой пластинки
Один квант ацетилхолина активирует 1,5·103 каналов. Через один активированный канал нейромышечного соединения проходит приблизительно 2·104 одновалентных ионов. Постоянная времени затухания миниатюрного потенциала концевой пластинки соответствует постоянной времени закрытия канала. Постоянная времени закрытия канала зависит от разности потенциалов на мембране (потенциалзависимый канал). Деполяризация продлевает, а гиперполяризация укорачивает время открытых каналов.
Фармакологическая модификации НМС
Как и все синапсы, нервно-мышечный синапс подвергается фармакологической модификации (см. подробно в учебнике [1] С.71).
Коротко. Можно блокировать проведение ПД по пресинаптическому элементу (новокаином), блокировать высвобождение медиатора, например, за счет удаления из среды ионов кальция или добавления ионов марганца, или при помощи ботулинического токсина, можно заблокировать синтез АХ, угнетая захват холина. Наконец, что в практическом отношении чрезвычайно важно, можно блокировать сами рецепторы и, тем самым, полностью прекратить передачу возбуждения в синапсе. Это можно сделать, используя такие вещества, которые при высоких концентрациях способны вытеснять ацетилхолин с ХР. Этим свойством обладают кураре и курареподобные вещества (д‑тубокурарин, диплацин и т.д.). Эта процедура находит широкое применение в хирургии. Существует также возможность управлять активностью ацетилхолинэстеразы (АХЭ). Если ее активность уменьшить до определенной степени, то это будет способствовать накоплению АХ в синаптической щели. Такая ситуация при определенной патологии (миастения гравис, когда количество выбрасываемого медиатора резко снижено) является благоприятной. Если инактивация АХЭ достигает значительной величины, то это сопровождается развитием стойкой деполяризации в области синапса и приводит к блокаде проведения возбуждения через мионевральный синапс. В конечном итоге это может привести к гибели организма. На этом явлении основано применение фосфороорганических соединений (ФОС) в качестве отравляющих веществ (ОВ) или в качестве инсектицидов (дихлофос, хлорофос и т.д.).
Электрические и смешанные синапсы.
В электрических синапсах ширина синаптической щели составляет всего 2 – 4 нм. Особенно важным является то, что в таких синапсах через синаптическую щель перекинуты мостики, образованные белковыми частицами (рис. ). Они представляют собой своеобразные каналы шириной 1 – 2 нм, пронизывающие пре- и постсинаптическую мембраны синапса. Благодаря существованию таких каналов, размеры которых позволяют переходить из клетки в клетку неорганическим ионам и даже небольшим молекулам, электрическое сопротивление в области такого синапса (получившего название щелевого uлu высокопроницаемого контакта) оказывается очень низким. Это позволяет пресинаптическому току распространяться на постсинаптическую клетку без угасания. Поэтому механизм работы электрического синапса сходен в общих чертах с механизмом распространения волны деполяризации по нервному или мышечному волокну.
В некоторых межнейронных синапсах электрическая и химическая передача осуществляются параллельно благодаря тому, что щель между пре- и постсинаптической мембранами имеет участки со структурой химического и электрического синапсов. Все 3 типа синапсов: электрический, химический и смешанный — схематически показаны на рис. .
Сравнение электрических и химических синапсов.
Прежде всего, из морфологических особенностей бросается в глаза разная толщина синаптической щели. В химическом синапсе она равна примерно 50 нм (т.е. в 5 раз больше толщины биомембраны), в электрическом – 2 нм (т.е. 5 раз больше тоньше биомембраны).
Где находится генератор постсинаптического тока? В химическом синапсе– на постсинаптической мембране. В электрическом синапсе – на пресинаптической мембране.
Наличие синаптической задержки? Каково быстродействие синапсов?
В химическом синапсе – до 0,5 мс. В электрическом синапсе – отсутствует. В быстродействии значительно превосходят химические синапсы.
Какова надёжность передачи возбуждения?
Значительно выше у электрических. В химическом синапсе химические и физические факторы влияющие на освобождение, действие, разрушение медиатора будут оказывать существенное воздействие на межклеточный контакт.
Направление проведения возбуждения?
В химическом синапсе – одностороннее (ортодромное). Структурная асимметрия обуславливает функциональную асимметрию.
В электрическом синапсе – двустороннее (часто между нейронами с одинаковыми функциями) и одностороннее (часто между нейронами с разными функциями, например, сенсорными и моторными).
Выраженность следовых эффектов?
В электрических синапсах следовые эффекты выражены слабо. И этот казалось бы положительный момент делает электрические синапсы непригодными для инегрирования, суммации последовательных сигналов.
Конечные эффекты?
И химические, и электрические могут быть возбуждающими и тормозными. Мнение, что электрические синапсы могут быть только возбуждающими устарело. Однако тормозные электрические синапсы встречаются редко.
Электрические синапсы имеют большую площадь контакта.
Только химическим синапсам приписывают следующие свойства:
утомляемость,
эффект облегчения (увеличение выделения квантов медиатора пропорционально частоте приходящих импульсов),
эффект тренировки (зависимость эффективности синаптической передачи от частоты использования синапса.
Смешанные синапсы.
Наряду с наличием чисто электрических или химических связей, в ЦНС млекопитающих и человека обнаружены смешанные синапсы (рис. 4.7). В смешанных синапсах одна и та же нервная терминаль имеет зону, где концентрируются везикулы и происходит секреция медиатора, и в то же время рядом (на расстоянии 10—100 нм) формирует зону щелевого контакта, где встроены коннексоны, — т.е. имеется щелевой электрический контакт. При этом как тормозные, так и возбуждающие синапсы могут образовывать смешанные синапсы. Однако наиболее типичны возбуждающие смешанные синапсы, которые обнаружены в сетчатке, верхних оливах, гиппокампе и неокортексе, где возбуждающим медиатором является глутамат.
Нексусы.
Снаружи гладкомышечную клетку покрывают базальная мембрана, которая отсутствует в области плотных контактов – нексусов. Нексус – это область плотного контакта, своеобразное соединительное устройство между двумя соседними клетками, которая обеспечивает передачу сигналов от клетки к клетке. Зрелая гладкомышечная клетка способна к делению на протяжении всей жизни организма, в отличие от скелетной мышцы, которая имеет многоядерные волокна и к делению не способна.

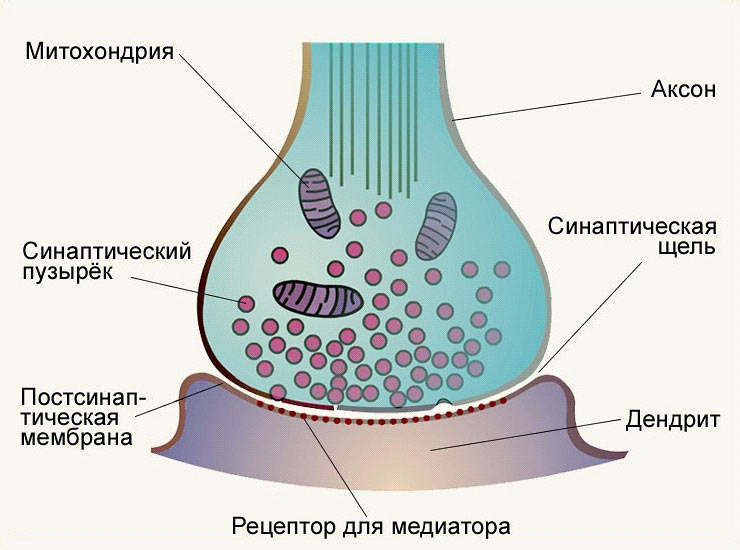 едиатор высвобождается из булавовидного расширения посредством экзоцитоза, проходит через синаптическую щель и связывается с рецепторами на постсинаптической мембране. Под постсинаптической мембраной расположена субсинаптическая активная зона, в которой после активации рецепторов постсинаптической мембраны происходят разнообразные биохимические процессы.
едиатор высвобождается из булавовидного расширения посредством экзоцитоза, проходит через синаптическую щель и связывается с рецепторами на постсинаптической мембране. Под постсинаптической мембраной расположена субсинаптическая активная зона, в которой после активации рецепторов постсинаптической мембраны происходят разнообразные биохимические процессы.