химия. Тесты Гидролиз (2). Тздар гидролизі
 Скачать 122.15 Kb. Скачать 122.15 Kb.
|
|
Тұздар гидролизі Вариант №1 1.Сулы ерітіндісінің рН > 7 тұз: A) CaCl2; B) KMnO4; C) Zn(NO3)2; D) Ca(CN)2; E) FeBr3. 2.Темір (III) хлориді ерітіндісімен натрий карбонаты ерітіндісін араластырғанда түзілетін темір (III) қосылысы: A) FeOHCl2; B) Fe(OH)2Cl; C) FeOHCO3; D) Fe2(CO3)3; E) Fe(OH)3. 3. Гидролизденгенде реакция орталығының рН-ы ең жоғары : A) Na2CO3 + H2O NaHCO3 + NaOH; K2(H2CO3) = 5,010-11; B) Na2CO3 + H2O H2CO3 + NaOH; K1(H2CO3) = 3,710-7; C) Na3PO4 + H2O NaH2PO4 + NaOH; K3(H3PO4) = 3,010-12; D) Na3PO4 + H2O Na2HPO4 + NaOH; K2(H3PO4) = 6,210-8; E) Na3PO4 + H2O Na3PO4 + NaOH; K1(H3PO4) = 7,510-3; 4. Иондану тұрақтысы HN3 (рН1) және NH4OH (рН2) ерітінділерінің бірдей. Осы ерітінділердің концентрациялары бірдей сулы ерітінділерінің рН-ы қандай? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 5. Анион бойынша гидролиз тұрақтысы қай формуламен анықтайды? A) 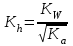 B) B) 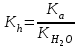 C) C) 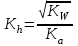 D) 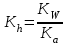 E) E) 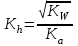 6. 0,1М калий ацетатының гидролиздену дәрежесін есепте, егер Ка(СН3СООН) = 10-5: A) 10-2; B) 10-3; C) 10-4; D) 10-5; E) 10-3. 7. 0,01 моль/л сода Na2CO3 ерітіндісінің реакция орталығының рН-ын анықтаңыз , тұздың бірінші сатылы гидролизін ескере отырып (250С Ка(Н2СО3) = 10-11): A) 10,8; B) 14,0; C) 10,0; D) 11,0; E) 12,0. Тұздар гидролизі Вариант №2 1. Гидролиз кезінде негіздік тұздар түзетін тұз; A) Cr2(SO4)3; B) Cr2S3; C) Cr2(CO3)2; D) (NH4)2S; E) Na2CO3. 2. Мырыш хлориді гидролизденгенде реакция орталығы қандай: A) рН 7; B) рН 7; C) рН > 7. 3. Қай тұзда гидролизденгенде рН- ы ең жоғары: A) NH4Cl + H2O NH4OH + HCl; K(NH4OH) = 3,710-7; B) FeCl3 + H2O FeOHCl2 + HCl; K1(Fe(OH)3) = 810-8; C) FeOHCl2 + H2O Fe(OH)2Cl + HCl; K2(Fe(OH)3) =1,8 10-11; D) Fe(OH)2Cl + H2O Fe(OH)3 + HCl; K3(Fe(OH)3) =1,35 10-12; E) ZnOHCl + H2O Zn(OH)2 + HCl; K2(Zn(OH)2) = 7,510-9; 4. Иондану константалары бірдей СН3СООН пен NH4OH ерітінділерде Егер молярлық концентрациялары бірдей болса СН3СООNa (pH1) пен NH4NO3 (pH2, онда осы ерітінділердің рН- тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 5. Катион бойынша гидролиз жүрсе, онда гидролиздену константасы қай формуламен анықталады: A) 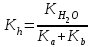 B) B) 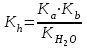 C) C) D) 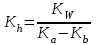 E) E) 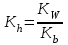 6. 0,1 М натрий карбонаты ерітіндісінің (250С Ка(Н2СО3) =1∙10-7) гидролиздену дәрежесін анықтаңыз: A) 2∙10-2; B) 10-3; C) 10-4; D) 10-5; E) 10-6. 7. Натрий дигидрофосфатының 0,01моль/л ерітіндісінің рН-ын есептеңіз, егер 250С Ка(Н3РО4) = 1∙10-8 (тек бірінші сатысын ескеріп) : A) 7; B) 8; C) 10; D) 4; E) 9. Тұздар гидролизі Вариант №3 1. Аммоний нитраты гидролизденгенде ортаның реакциясы қандай: A) күшті қышқылды ; B) күшті сілтілі ; C) бейтарап; D) әлсіз қышқылды; E) әлсіз сілтілі. 2. FeCl3 ерітіндісінің гидролизін өсіруүшін қай реагентті қосу керек : A) СН3СООН; B) HCl; C) NH4Cl; D) Na2CO3; E) ZnCl2. 3. Біріккен гидролизде қай формуламен гидролиздену константасын есептейді: A) 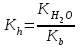 C) C) 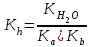 D) 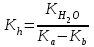 E) E) 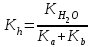 4. Қай тұзда гидролизденгенде рН- ы ең жоғары: A) Na3BO3 + H2O Na2HBO3 + NaOH; K3(Na3BO3) = 1,610-14; B) Na2HBO3 + H2O NaH2BO3+ NaOH; K2(Na3BO3) = 1,810-13; C) Na2HBO3 + H2O H3BO3 + NaOH; K3(H3BO3) = 5,810-10; D) Na2CO3 + H2O NaHCO3 + NaOH; K2(H2CO3) = 5,010-11; E) Na2CO3 + H2O H2CO3 + NaOH; K1(H2CO3) = 3,710-7; 5. Иондану константалары бірдей Н3AsO4 пен Fe(OH)3 ерітінділерде. Егер молярлық концентрациялары бірдей болса Н3AsO4 (pH1) пен Fe(OH)3 (pH2), онда осы ерітінділердің рН- тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 6. 0,1 М натрий ацетаты ерітіндісінің (250С Ка(СН3СООН) =1∙10-5) гидролиздену дәрежесін анықтаңыз: A) 10-2; B) 10-3; C) 10-4; D) 10-5; E) 10-6; 7. Аммоний хлоридының 0,01моль/л ерітіндісінің рН-ын есептеңіз, егер 250С Кв(NH4ОН) = 10-6 : A) 4 B) 5 C) 6 D) 7 E) 8 Тұздар гидролизі Вариант №4 1.Берілген схема бойынша сумен қай зат әрекеттеседі: Kn+ + HOH KOH(n-1)+ + H+ A) Na2CO3; B) K2SiO3; C) Na2SO3; D) NaCl; E) NH4Cl. 2. Калий ионы К+ неге гидролизденбейді, себебі қандай? A) күшті донор;B) әлсіз донор; C) аквакомплекс түзбейді; D) күшті акцептор; E) әлсіз акцептор. 3. Мына формуламен 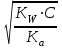 қандай шаманы анықтауға болады: қандай шаманы анықтауға болады:A) иондану константасын; B) иондану дәрежесін ; C) гидролиз дәрежесін; D) гидролиздену константасын; E) мольдік үлесін. 4. Қай тұзда гидролизденгенде рН- ы ең жоғары: A) Na3BO3 + H2O Na2HBO3 + NaOH; K3(Na3BO3) = 1,610-14; B) Na2HBO3 + H2O NaH2BO3+ NaOH; K2(Na3BO3) = 1,810-13; C) Na3PO4 + H2O NaH2PO4 + NaOH; K3(H3PO4) = 3,010-12; D) Na3PO4 + H2O Na2HPO4 + NaOH; K2(H3PO4) = 6,210-8; E) Na3PO4 + H2O Na3PO4 + NaOH; K1(H3PO4) = 7,510-3; 5. Иондану константалары бірдей КNO2 пен Fe(OH)2 ерітінділерде. Егер молярлық концентрациялары бірдей болса КNO2 (pH1) пен Fe(OH)2 (pH2), онда осы ерітінділердің рН-тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 6. Аммоний формиатының HCOONH4 иондану константасын есепте , егер 250С Kа(HCOOH) = 1,810-4 ; Kв(NH4OH) = 1,810-5 болса: A) 210-8; B) 410-7; C) 610-3; D) 810-5; E) 310-6. 7. Калий цианиді ерітіндісінің рН-ын есепте, егер молярлы концентрациясы 0,01 моль/л және 250С Kh(HСN) = 110-10 болса: A) 8; B) 10; C) 11; D) 12; E) 9. Тұздар гидролизі Вариант №5 1. Мырыш хлориді сулы ерітіндісінің ортасы қандай? A) рН = 7; B) рН = 1 - 4; C) рН = 11 – 14; D) рН = 4 - 6; E) рН = 7 - 10. 2. SO42- және NO3- иондары неге гидролизденбейді ? A) әлсіз донор; B) күшті донор; C) әлсіз акцептор; D) күшті акцептор; E) тұрақты иондар 3. Анион бойынша гидролизденетін тұздың гидролиздену константасын есептейтін формула: A) 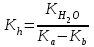 ; B) ; B) 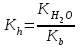 ; C) ; C) 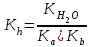 D) 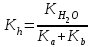 4. Қай тұзда гидролизденгенде рН- ы ең төмен: A) Na2CO3 + H2O NaHCO3 + NaOH; K1(H2CO3) = 3,710-7; B) Na2CO3 + H2O H2CO3 + NaOH; K2(H2CO3) = 5,010-11; C) Na3PO4 + H2O NaH2PO4 + NaOH; K1(H3PO4) = 7,510-3; D) Na3PO4 + H2O Na2HPO4 + NaOH; K2(H3PO4) = 6,210-8; E) Na3PO4 + H2O Na3PO4 + NaOH; K3(H3PO4) = 3,010-12; 5. Иондану константалары бірдей НBrO пен Al(OH)3 ерітінділерде. Егер молярлық концентрациялары бірдей болса NaBrO (pH1) пен Al(NO2)3 (pH2), онда осы ерітінділердің рН-тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 6. 0,1 М натрий дигидрофосфаты ерітіндісінің (250С Ка(H3PO4) =1∙10-7) гидролиздену дәрежесін анықтаңыз: A) 10-2; B) 10-6; C) 10-4; D) 10-3; E) 10-5; 7. Мыс (II) сульфаты ерітіндісінің рН-ын есепте, егер молярлы концентрациясы 0,01 моль/л және 250С Кв(Cu(OH)2) = 110-6 болса: A) 8; B) 7; C) 5; D) 2; E) 4. Тұздар гидролизі Вариант №6 1. (NH4)2S тұзының гидролизінде реакция ортасы қандай болады, егер 250С Kb(NH4OH) = 1,810-5, Ka(H2S) = 610-8 : A) күшті сілтілі; B) күшті қышқылды; C) әлсіз қышқылды D) әлсіз сілтілі E) бейтарап 2. К2S тұзының гидролизін артыру үшін қай реагенті қосу керек: A) Na2SiO3; B) CH3COONa; C) KOH; D) NH4OH; E) NH4Cl. 3. Катион бойынша гидролиз жүрсе, онда гидролиздену константасы қай формуламен анықталады: A) 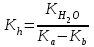 ; B) ; B) 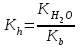 ; C) ; C)  D)  4. Қай тұзда гидролизденгенде рН- ы ең төмен: A) NH4Cl + H2O NH4OH + HCl; K(NH4OH) = 3,710-7; B) FeCl3 + H2O FeOHCl2 + HCl; K1(Fe(OH)3) = 810-9; C) FeOHCl2 + H2O Fe(OH)2Cl + HCl; K2(Fe(OH)3) =1,8 10-12; D) Fe(OH)2Cl + H2O Fe(OH)3 + HCl; K3(Fe(OH)3) = 1,3510-11; E) ZnOHCl + H2O Zn(OH)2 + HCl; K1(Zn(OH)2) = 7,510-9; 5. Иондану константалары бірдей Н3PO4 пен Fe(OH)3 ерітінділерде. Егер молярлық концентрациялары бірдей болса Na3PO4 (pH1) пен Fe(NO2)3 (pH2), онда осы ерітінділердің рН-тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 6. 0,1 М темір (III) хлориді ерітіндісінің (250С Кв(Fe(OH)3 =1∙10-7) гидролиздену дәрежесін анықтаңыз: A) 10-2; B) 10-4; C) 10-6; D) 10-1; E) 10-3; 7. Калий фосфаты ерітіндісінің рН-ын есепте, егер молярлы концентрациясы 0,1 моль/л және 250С Ка(Н3РО4) = 10-11 болса: A) 11; B) 9; C) 8; D) 12; E) 6. Тұздар гидролизі Вариант №7 1.Хром (III) сульфаты толық гидролизденгенде өнімі қандай: A) [CrOH(H2O)5]+2; B) [Cr(H2O)6]+3; C) [Cr(OH)2(H2O)4]+; D) [Cr(OH)3(H2O)3]0; E) Cr(OH)3; 2. Калий сульфиді сулы ерітіндісінің реакция орталығы (рН) қандай: A) рН = 1 – 4; B) рН = 4 – 7; C) рН = 7; D) рН = 7 – 10; E) рН = 10 -14. 3. Біріккен гидролизде қай формуламен гидролиздену константасын есептейді: A)  ; B) ; B)  ; C) ; C)  D)  4. Қай тұзда гидролизденгенде рН- ы ең төмен: A) Na3BO3 + H2O Na2HBO3 + NaOH; K3(Na3BO3) = 1,610-14; B) Na2HBO3 + H2O NaH2BO3+ NaOH; K2(Na3BO3) = 1,810-13; C) Na2HBO3 + H2O H3BO3 + NaOH; K1(H3BO3) = 5,810-10; D) Na2CO3 + H2O NaHCO3 + NaOH; K2(H2CO3) = 5,010-11; E) Na2CO3 + H2O H2CO3 + NaOH; K1(H2CO3) = 3,710-7; 5. Иондану константалары бірдей Н2SeO3 пен Pb(OH)2 ерітінділерде. Егер молярлық концентрациялары бірдей болса Na2SeO3 (pH1) пен Pb(NO2)2 (pH2), онда осы ерітінділердің рН-тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 6. 0,1 М натрий силикаты ерітіндісінің (250С Ка(H2SiO3) = 110-5) гидролиздену дәрежесін анықтаңыз: A) 10-2; B) 10-3; C) 10-4; D) 10-5; E) 10-6; 7. 0,01 М аммоний хлориді ерітіндісінде рН-ын анықта, егер гидролиздену дәрежесі 10-2 тең болса: A) 2; B) 4; C) 6; D) 8; E) 10. Тұздар гидролизі Вариант №8 Егер алюминий нитраты мен натрий сульфиты сулы ерітінділері әрекеттескенде, алюминийдің қандай қосылысы түзіледі: A) Al(OH)3; B) Al2(SO3)3; C) Al(OH)(NO3)2; D) Al(OH)2NO3; E) AlOHSO3. 2.Кобальт (II) нитраты сулы ерітіндісінің реакция орталығының (рН) қандай: A) рН = 7; B) рН = 1 – 4; C) рН = 4 – 7; D) рН = 7 – 10; E) рН = 10 -14. 3. Катион бойынша гидролиз жүрсе, онда гидролиздену константасы қай формуламен анықталады: A)  B) B)  C) C)  D)  4. Қай тұзда гидролизденгенде рН- ы ең төмен: A) Na3BO3 + H2O Na2HBO3 + NaOH; K3(Na3BO3) = 1,610-14; B) Na2HBO3 + H2O NaH2BO3+ NaOH; K2(Na3BO3) = 1,810-13; C) Na3PO4 + H2O NaH2PO4 + NaOH; K3(H3PO4) = 3,010-12; D) Na3PO4 + H2O Na2HPO4 + NaOH; K2(H3PO4) = 6,210-8; E) Na3PO4 + H2O Na3PO4 + NaOH; K1(H3PO4) = 7,510-3; 5. Иондану константалары бірдей Н2SiO3 пен Fe(OH)3 ерітінділерде. Егер молярлық концентрациялары бірдей болса Na2SіO3 (pH1) пен Fe(NO2)3 (pH2), онда осы ерітінділердің рН-тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 6. 0,1 М натрий цианиді ерітіндісінің (250С Ка(HCN) = 10-9) гидролиздену дәрежесін анықтаңыз: A) 10-2; B) 10-3; C) 10-4; D) 10-5; E) 10-6; 7. 0,01 М натрий силикаты ерітіндісінде рН-ын анықта, егер 250С Ка(Н2SiO3) = 10-8 тең болса: A) 7; B) 8; C) 9; D) 10; E) 11. Тұздар гидролизі Вариант №9 1. Төменгі схема бойынша қандай қосылыс гидролизденеді: An- + HOH HA + OH- A) CuCl2; B) ZnSO4; C) Na2CO3; D) KNO3; E) NH4Cl. 2. Аммоний карбонаты сулы ерітіндісінде реакция орталығы (рН ) қандай: A) рН = 1 – 4; B) рН = 4 – 7; C) рН = 7; D) рН = 7 – 10; E) рН = 10 -14. 3. Біріккен гидролизде қай формуламен гидролиздену константасын есептейді: A)  B) B)  D)  E) E)  4. Қай тұзда гидролизденгенде рН- ы ең төмен: A) NaNO2 + H2O HNO2 + NaOH; K3(HNO2) = 5,010-4; B) Na2HBO3 + H2O NaH2BO3+ NaOH; K2(Na3BO3) = 1,810-13; C) Na3PO4 + H2O NaH2PO4 + NaOH; K3(H3PO4) = 3,010-12; D) Na3PO4 + H2O Na2HPO4 + NaOH; K2(H3PO4) = 6,210-8; E) Na3PO4 + H2O Na3PO4 + NaOH; K1(H3PO4) = 7,510-3; 5. Иондану константалары бірдей Н3AsO4 пен Fe(OH)3 ерітінділерде. Егер молярлық концентрациялары бірдей болса Na3AsO4 (pH1) пен Fe(NO2)3 (pH2), онда осы ерітінділердің рН-тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 6. 0,1 М натрий силикаты ерітіндісінің (250С Ка(Н2SiO3) = 10-7) гидролиздену дәрежесін анықтаңыз: A) 10-2; B) 10-4; C) 10-6; D) 10-3; E) 10-5; 7. 0,01 М калий карбонаты ерітіндісінде рН-ын анықта, егер 250С Ка(Н2СО3) = 10-6 тең болса: A) 11; B) 9; C) 8; D) 12; E) 6. Тұздар гидролизі Вариант №10 1. Анионы бойынша гидролизденетін тұз : A) CuCl2; B) ZnSO4; C) Na2CO3; D) KNO3; E) NH4Cl. 2. Натрий карбонаты сулы ерітіндісінің реакция орталығы (рН) қандай: A) рН = 1 – 4; B) рН = 4 – 7; C) рН = 7; D) рН = 7 – 10; E) рН = 10 -14. 3. Қай тұздың гидролиздену константасы төменгі формуламен анықталады  : :A) Na2SiO3; B) CH3COONH4; C) KCl; D) CH3COONa; E) NH4Cl. 4. Қай тұзда гидролизденгенде рН- ы ең жоғары: A) NaNO2 + H2O HNO2 + NaOH; K3(HNO2) = 5,010-4; B) Na2HBO3 + H2O NaH2BO3+ NaOH; K2(Na3BO3) = 1,810-13; C) Na3PO4 + H2O NaH2PO4 + NaOH; K3(H3PO4) = 3,010-12; D) Na3PO4 + H2O Na2HPO4 + NaOH; K2(H3PO4) = 6,210-8; E) Na3PO4 + H2O Na3PO4 + NaOH; K1(H3PO4) = 7,510-3; 5. Иондану константалары бірдей Н3PO4 пен Fe(OH)3 ерітінділерде. Егер молярлық концентрациялары бірдей болса Na3PO4 (pH1) пен Fe(NO2)3 (pH2), онда осы ерітінділердің рН-тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 6. 0,01 М натрий силикаты ерітіндісінің (250С Ка(Н2SiO3) = 10-7) гидролиздену дәрежесін анықтаңыз: A) 3210-2; B) 0,3210-2; C) 3,210-2; D) 10-2; E) 210-2; 7. 0,1 М калий карбонаты ерітіндісінде рН-ын анықта, егер 250С Ка(Н2СО3) = 10-7 тең болса: A) 11; B) 9; C) 8; D) 12; E) 7. Тұздар гидролизі Вариант №11 1. Катионы бойынша гидролизденетін тұз : A) CuCl2; B) K2SO3; C) Na2CO3; D) KNO3; E) Na3PO4. 2. Калий карбонаты сулы ерітіндісінің реакция орталығы (рН) қандай: A) рН = 1 – 4; B) рН = 4 – 7; C) рН = 7; D) рН = 7 – 10; E) рН = 10 -14. 3. Қай тұздың гидролиздену константасы төменгі формуламен анықталады  : :A) Al2(SO4)3; B) CH3COONH4; C) KCl; D) CH3COONa; E) NH4Cl. 4. Қай тұзда гидролизденгенде рН- ы ең жоғары: A) NaNO2 + H2O HNO2 + NaOH; K3(HNO2) = 5,010-4; B) Na2S + H2O NaHS + NaOH; K2(H2S) = 1,210-15; C) NaHS + H2O H2S + NaOH; K1(H2S) = 5,710-8; D) Na3PO4 + H2O Na2HPO4 + NaOH; K2(H3PO4) = 6,210-8; E) Na3PO4 + H2O Na3PO4 + NaOH; K1(H3PO4) = 7,510-3; 5. Иондану константалары бірдей СН3СООН пен NH4OH ерітінділерде. Егер молярлық концентрациялары бірдей болса СН3СООNa (pH1) пен NH4NO3 (pH2), онда осы ерітінділердің рН-тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 6. 1 М натрий силикаты ерітіндісінің (250С Ка(Н2SiO3) = 10-7) гидролиздену дәрежесін анықтаңыз: A) 3210-4; B) 0,3210-4; C) 3,210-4; D) 10-4; E) 210-4; 7. 0,001 М калий карбонаты ерітіндісінде рН-ын анықта, егер 250С Ка(Н2СО3) = 10-7 тең болса: A) 11; B) 9; C) 8; D) 12; E) 7. Тұздар гидролизі Вариант №12 1.Қай тұз жартылай гидролизденгенде негіздік түздар түзеді: A) Cr2(SO4)3; B) Cr2S3; C) Cr2(CO3)2; D) (NH4)2S; E) Na2CO3. 2. Мырыш хлориді гидролизденгенде реакция орталығы қандай: A) рН 7; B) рН 7; C) рН > 7. 3. Қай тұзда гидролизденгенде рН- ы ең жоғары: A) NH4Cl + H2O NH4OH + HCl; K(NH4OH) = 3,710-7; B) FeCl3 + H2O FeOHCl2 + HCl; K1(Fe(OH)3) = 810-8; C) FeOHCl2 + H2O Fe(OH)2Cl + HCl; K2(Fe(OH)3) =1,8 10-11; D) Fe(OH)2Cl + H2O Fe(OH)3 + HCl; K3(Fe(OH)3) =1,35 10-12; E) ZnOHCl + H2O Zn(OH)2 + HCl; K2(Zn(OH)2) = 7,510-9; 4. Иондану константалары бірдей СН3СООН пен NH4OH ерітінділерде. Егер молярлық концентрациялары бірдей болса СН3СООNa (pH1) пен NH4NO3 (pH2), онда осы ерітінділердің рН-тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 5. Катион бойынша гидролиз жүрсе, онда гидролиздену константасы қай формуламен анықталады: A) 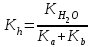 B) B) 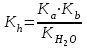 C) C) D) 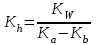 E) E) 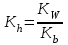 6. 0,1 М натрий карбонаты ерітіндісінің (250С Ка(Н2СО3) = 10-7) гидролиздену дәрежесін анықтаңыз: A) 2∙10-2; B) 10-3; C) 10-4; D) 10-5; E) 10-6. 7. 0,01 М натрий дигидрофосфаты ерітіндісінде рН-ын анықта, егер 250С Ка(Н3РО4) = 1∙10-8 тең болса: A) 7; B) 8; C) 10; D) 4; E) 9. Тұздар гидролизі Вариант №13 1.Берілген схема бойынша сумен қай зат әрекеттеседі: Kn+ + HOH KOH(n-1)+ + H+ A) Na2CO3; B) K2SiO3; C) Na2SO3; D) NaCl; E) NH4Cl. 2. Калий ионы К+ неге гидролизденбейді, себебі қандай? A) күшті донор;B) әлсіз донор; C) аквакомплекс түзбейді; D) күшті акцептор; E) әлсіз акцептор. 3. Мына формуламен  қандай шаманы анықтауға болады: қандай шаманы анықтауға болады:A) иондану константасын; B) иондану дәрежесін ; C) гидролиз дәрежесін; D) гидролиздену константасын; E) мольдік үлесін. 4. Қай тұзда гидролизденгенде рН- ы ең жоғары: A) Na3BO3 + H2O Na2HBO3 + NaOH; K3(Na3BO3) = 1,610-14; B) Na2HBO3 + H2O NaH2BO3+ NaOH; K2(Na3BO3) = 1,810-13; C) Na3PO4 + H2O NaH2PO4 + NaOH; K3(H3PO4) = 3,010-12; D) Na3PO4 + H2O Na2HPO4 + NaOH; K2(H3PO4) = 6,210-8; E) Na3PO4 + H2O Na3PO4 + NaOH; K1(H3PO4) = 7,510-3; 5. Иондану константалары бірдей КNO2 пен Fe(OH)2 ерітінділерде. Егер молярлық концентрациялары бірдей болса КNO2 (pH1) пен Fe(OH)2 (pH2), онда осы ерітінділердің рН-тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 6. Аммоний формиатының HCOONH4 иондану константасын есепте , егер 250С Kа(HCOOH) = 1,810-4 ; Kв(NH4OH) = 1,810-5 болса: A) 210-8; B) 410-7; C) 610-3; D) 810-5; E) 310-6. 7. Калий цианиді ерітіндісінің рН-ын есепте, егер молярлы концентрациясы 0,01 моль/л және 250С Kh(HСN) = 110-10 болса: A) 8; B) 10; C) 11; D) 12; E) 9. Тұздар гидролизі Вариант №14 1. (NH4)2S тұзының гидролизінде реакция ортасы қандай болады, егер 250С Kb(NH4OH) = 1,810-5, Ka(H2S) = 610-8 : A) күшті сілтілі; B) күшті қышқылды; C) әлсіз қышқылды D) әлсіз сілтілі E) бейтарап 2. К2S тұзының гидролизін артыру үшін қай реагенті қосу керек: A) Na2SiO3; B) CH3COONa; C) KOH; D) NH4OH; E) NH4Cl. 3. Катион бойынша гидролиз жүрсе, онда гидролиздену константасы қай формуламен анықталады: A)  ; B) ; B)  ; C) ; C)  D)  4. Қай тұзда гидролизденгенде рН- ы ең төмен: A) NH4Cl + H2O NH4OH + HCl; K(NH4OH) = 3,710-7; B) FeCl3 + H2O FeOHCl2 + HCl; K1(Fe(OH)3) = 810-9; C) FeOHCl2 + H2O Fe(OH)2Cl + HCl; K2(Fe(OH)3) =1,8 10-12; D) Fe(OH)2Cl + H2O Fe(OH)3 + HCl; K3(Fe(OH)3) = 1,3510-11; E) ZnOHCl + H2O Zn(OH)2 + HCl; K1(Zn(OH)2) = 7,510-9; 5. Иондану константалары бірдей Н3PO4 пен Fe(OH)3 ерітінділерде. Егер молярлық концентрациялары бірдей болса Na3PO4 (pH1) пен Fe(NO2)3 (pH2), онда осы ерітінділердің рН-тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 6. 0,1 М темір (III) хлориді ерітіндісінің (250С Кв(Fe(OH)3 =1∙10-7) гидролиздену дәрежесін анықтаңыз: A) 10-2; B) 10-4; C) 10-6; D) 10-1; E) 10-3; 7. Калий фосфаты ерітіндісінің рН-ын есепте, егер молярлы концентрациясы 0,1 моль/л және 250С Ка(Н3РО4) = 10-11 болса: A) 11; B) 9; C) 8; D) 12; E) 6. Тұздар гидролизі Вариант №15 Егер алюминий нитраты мен натрий сульфиты сулы ерітінділері әрекеттескенде, алюминийдің қандай қосылысы түзіледі: A) Al(OH)3; B) Al2(SO3)3; C) Al(OH)(NO3)2; D) Al(OH)2NO3; E) AlOHSO3. 2.Кобальт (II) нитраты сулы ерітіндісінің реакция орталығының (рН) қандай: A) рН = 7; B) рН = 1 – 4; C) рН = 4 – 7; D) рН = 7 – 10; E) рН = 10 -14. 3. Катион бойынша гидролиз жүрсе, онда гидролиздену константасы қай формуламен анықталады: A)  B) B)  C) C)  D) 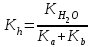 4. Қай тұзда гидролизденгенде рН- ы ең төмен: A) Na3BO3 + H2O Na2HBO3 + NaOH; K3(Na3BO3) = 1,610-14; B) Na2HBO3 + H2O NaH2BO3+ NaOH; K2(Na3BO3) = 1,810-13; C) Na3PO4 + H2O NaH2PO4 + NaOH; K3(H3PO4) = 3,010-12; D) Na3PO4 + H2O Na2HPO4 + NaOH; K2(H3PO4) = 6,210-8; E) Na3PO4 + H2O Na3PO4 + NaOH; K1(H3PO4) = 7,510-3; 5. Иондану константалары бірдей Н2SiO3 пен Fe(OH)3 ерітінділерде. Егер молярлық концентрациялары бірдей болса Na2SіO3 (pH1) пен Fe(NO2)3 (pH2), онда осы ерітінділердің рН-тары қандай болады ? A) рН1 > рН2; B) рН1 рН2; C) рН1 < рН2; 6. 0,1 М натрий цианиді ерітіндісінің (250С Ка(HCN) = 10-9) гидролиздену дәрежесін анықтаңыз: A) 10-2; B) 10-3; C) 10-4; D) 10-5; E) 10-6; 7. 0,01 М натрий силикаты ерітіндісінде рН-ын анықта, егер 250С Ка(Н2SiO3) = 10-8 тең болса: A) 7; B) 8; C) 9; D) 10; E) 11. |
