№ п/п
|
Разделы дисциплины
|
Лекции
|
Семинары
|
Лаборатор-ные работы
|
|
Модуль 1
|
|
|
|
1
|
Первый закон термодинамики
|
+
|
+
|
+
|
2
|
Второй закон термодинамики
|
+
|
+
|
+
|
3
|
Термодинамика растворов
|
+
|
+
|
+
|
4
|
Фазовые равновесия
|
+
|
+
|
+
|
5
|
Химическое равновесие
|
+
|
+
|
+
|
6
|
Адсорбционное равновесие
|
+
|
-
|
+
|
|
Модуль 2
|
|
|
|
7
|
Статистическая термодинамика идеальных газов
|
+
|
+
|
-
|
8
|
Статистическая термодинамика реальных систем
|
+
|
-
|
-
|
|
Модуль3
|
|
|
|
9
|
Формальная кинетика
|
+
|
+
|
+
|
10
|
Теории химической кинетики
|
+
|
+
|
-
|
11
|
Катализ
|
+
|
+
|
+
|
| Модуль 4 |
|
|
|
12
|
Равновесные и неравновесные явления в растворах электролитов
|
+
|
+
|
+
|
13
|
Термодинамика электрохимических цепей.
|
+
|
+
|
+
|
14
|
Строение заряженных границ раздела.
|
+
|
-
|
-
|
15
|
Электрохимическая кинетика.
|
+
|
-
|
+
|
№ п/п
|
№ раздела дисциплины
|
Наименование лабораторных работ
|
1.
|
1
|
Определение энергии сгорания органического вещества и расчет его энтальпии образования.
|
2.
|
1
|
Определение энтальпии растворения соли в воде в открытом калориметре.
|
3.
|
1
|
Измерение теплоемкости металлов и сплавов.
|
4
|
2,3
|
Определение энтальпии испарения и нормальной температуры кипения индивидуальных жидкостей методом тензиметрии.
|
5
|
4
|
Изучение фазовых диаграмм двухкомпонентных систем. Фазовые диаграммы двухкомпонентных эвтектических систем.
|
6
|
4
|
Изучение фазовых диаграмм двухкомпонентных систем. Равновесие жидкость-пар в двухкомпонентной системе.
|
7
|
4
|
Изучение фазовых диаграмм трехкомпонентных систем с ограниченной взаимной растворимостью.
|
8
|
5
|
Определение констант равновесия и термодинамических характеристик реакций спектральным методом.
|
9
|
6
|
Определение изотермы адсорбции сорбата на силикагеле хромато графическим методом.
|
10
|
6
|
Расчет теплоты сорбции хроматографическим методом.
|
11
|
9
|
Гидролиз сложных эфиров в присутствии кислоты.
|
12
|
9
|
Изучение кинетических закономерностей реакции иодирования ацетона.
|
13
|
9
|
.Кинетика фотохимического распада перекиси водорода
|
14
|
9, 11
|
Каталитическое разложение перекиси водорода на платиновых катализаторах.
|
15
|
9, 11
|
Изучение кинетики гидролиза n-нитрофенилфосфата щелочной фосфатазой методом спектрофотометрии.
|
16
|
9, 11
|
.Изучение кинетики каталитического разложения перекиси водорода
|
17
|
9, 11
|
Изучение кинетики гетерогеннокаталитических реакций импульсным газохроматографическим методом.
|
18
|
12
|
Определение константы диссоциации органической кислоты.
|
19
|
12
|
Кондуктометрическое титрование.
|
20
|
13
|
Химические цепи с электродами первого и второго рода.
|
21
|
13
|
Концентрационные цепи с электродами второго рода.
|
22
|
13
|
Применение метода ЭДС для определения термодинамических параметров ( ∆ H, ∆ G, ∆ S) химических реакций.
|
23
|
15
|
Коррозия. Изучение процессов анодного растворения и пассевации металлов электрохимическими методами.
|
24
|
15
|
Гальваника. Изучение процессов катодного выделения металлов и начальных стадий электрокристаллизации.
|
№ п/п
|
№ раздела дисциплины
|
Наименование семинарских занятий
|
1.
|
1
|
I закон термодинамики. Внутренняя энергия, работа различных процессов
|
2.
|
1
|
Энтальпия, теплоемкость
|
3.
|
1
|
Термохимия. Закон Гесса, уравнение Кирхгофа.
|
4
|
2
|
II закон термодинамики. Энтропия. Вычисление абсолютных энтропий.
|
5
|
2
|
Фундаментальное уравнение Гиббса, термодинамические потенциалы (идеальные газы, химические реакции
|
6
|
2
|
Фундаментальное уравнение Гиббса, термодинамические потенциалы (реальные газы, конденсированное состояние)
|
7
|
3
|
Растворы. Равновесие жидкость-пар в идеальных и реальных системах. Закон Рауля
|
8
|
3
|
Криоскопия и эбулиоскопия.
|
9
|
4
|
Правило фаз. Уравнение Клапейрона-Клаузиуса. Однокомпонентные системы.
|
10
|
4
|
Правило фаз. Уравнение Шредера. Двухкомпонентные системы.
|
11
|
5
|
Химическое равновесие. Расчет выходов продуктов реакций в идеальных и реальных газовых системах.
|
12
|
5
|
Изотерма химической реакции. Стандартная энергия Гиббса. Зависимость константы равновесия от температуры.
|
13
|
5
|
Сложные равновесия
|
14
|
7
|
Статистическая термодинамика Суммы по состояниям. Расчет для Н и Н2 при 298.15 и 1000 К
|
15
|
7
|
Статистическая термодинамика Расчет 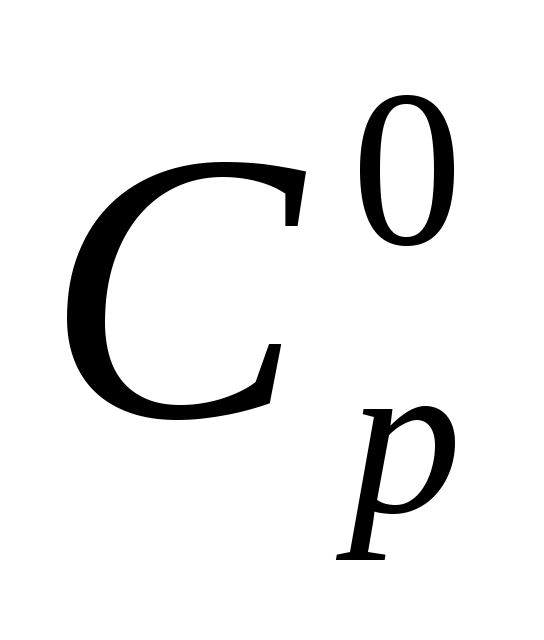 , , 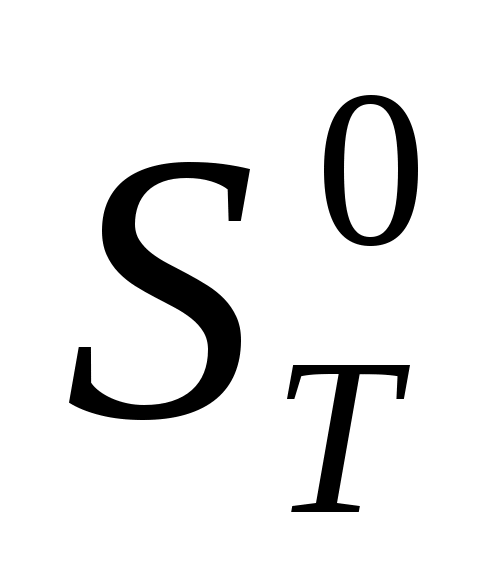 и и 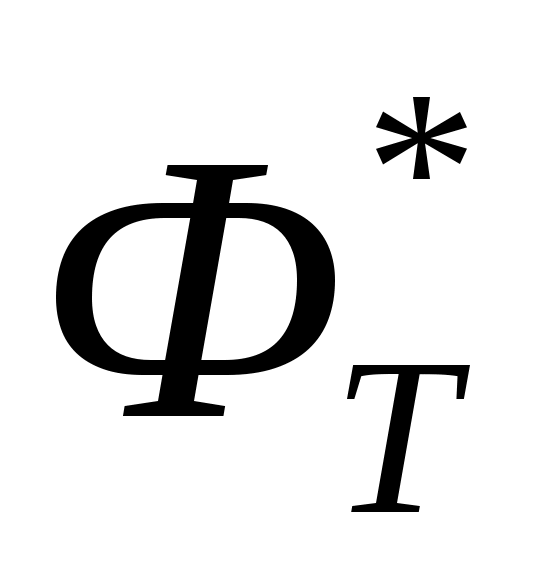 для H и H2 при 298.15 и 1000 и К. для H и H2 при 298.15 и 1000 и К.
|
15
|
7
|
Статистическая термодинамика Расчет Кр реакций.
|
16
|
9
|
Кинетика необратимых реакций. Методы определения порядков реакций.
|
17
|
9
|
Кинетика обратимых и параллельных реакций
|
18
|
9
|
Кинетика последовательных реакций. Метод стационарных концентраций Боденштейна.
|
19
|
9
|
Температурная зависимость скоростей химических реакций. Уравнение Аррениуса.
|
20
|
10
|
Теория столкновений. Бимолекулярные реакции
|
21
|
10
|
Теория столкновений. Мономолекулярные реакции
|
22
|
10
|
Теория активированного комплекса. Статистический аспект.
|
23
|
10
|
Теория активированного комплекса. Термодинамический аспект.
|
24
|
10
|
Кинетика цепных реакций (теоретический семинар).
|
25
|
11
|
Кинетика ферментативных каталитических реакций.
|
26
|
12
|
Коэффициенты активности сильных и слабых электролитов.
|
27
|
12
|
Удельная и эквивалентная электропроводности сильных и слабых электролитов. Числа переноса ионов.
|
28
|
13
|
ЭДС. Расчет ЭДС химических цепей с электродами различного типа.
|
29
|
13
|
Расчет ЭДС концентрационных цепей.
|
30
|
13
|
Термодинамика гальванического элемента. Расчет энтальпии, энтропии и энергии Гиббса реакции.
|
 Скачать 0.51 Mb.
Скачать 0.51 Mb.