Учебное пособие по курсу Ядерная безопасность для студентов, обучающихся по направлению Ядерная энергетика и теплофизика
 Скачать 5.76 Mb. Скачать 5.76 Mb.
|
1.2. Модель атома Резерфорда.Прежде, чем заняться собственно радиацией, необходимо вспомнить некоторые основные понятия. Прежде всего, все состоит из атомов. В конце 19–го века Дж. Дж. Томсоном был открыт электрон. Было понято, что это составная часть атома. Томсоном предложена модель атома - «пудинг с изюмом». Э. Резерфорд изучал рассеяние альфа-частиц на атомах и установил, что некоторые из частиц рассеиваются на большие углы. Это показало неприемлемость модели атома Томсона. Резерфорд предложил планетарную модель атома. Размер атома 10-10м, размер ядра 10-14м. Чтобы представить себе относительные размеры ядра к атому можно сказать, что это монета (ядро) на Красной площади. 1.3. Постулаты Бора.Было непонятно, как атомы могут существовать. Электрон движется с ускорением вокруг ядра. Согласно выводам электродинамики, любая заряженная частица, двигаясь с ускорением, должна излучать электромагнитное излучение (причем переменной частоты), терять при этом энергию, и электрон должен довольно быстро упасть на ядро. Тем не менее, атомы существуют и излучают свет определенных фиксированных для каждого типа атомов частот. Н. Бором были сформулированы следующие утверждения, называемые постулатами. Электроны могут двигаться только по разрешенным орбитам, не испуская излучение. Атомы излучают, когда электрон переходит из одного стационарного состояния (орбиты) в другое. При этом частота испускаемого излучения () связана с энергиями стационарных состояний соотношением 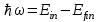 , где , где 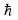 = 1.054 10-27 эрг с – постоянная Планка, = 1.054 10-27 эрг с – постоянная Планка,Еin и Еfin – начальная и конечная энергии атома. 3)Разрешенные орбиты определяются на основании квантования момента количества движения M = n 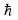 , где n=1,2,…- номер орбиты. , где n=1,2,…- номер орбиты.1.4 Возбуждение и ионизация атомовНа основе этих постулатов впервые возникла идея квантования энергии атома, дискретных энергетических уровней. Эти уровни принято обозначать буквами латинского алфавита K,L,M,N…, где K соответствует n=1, L – n=2, и т.д. Взаимодействие электромагнитного излучения, в частности света, с атомами теперь могло быть обрисовано следующим образом (рис.1.1).  Рисунок 1.1 - Боровская модель атома 1.5 Видимый свет. Энергия фотоновВидимый свет имеет энергию фотонов 1.8-3.0 эВ. Минимальная энергия, требуемая для ионизации, составляет 3.9 эВ для цезия. Отсюда ясно, что видимый свет не может быть ионизирующим излучением. 1.6 Рентгеновское излучение. Схема получения. Характеристическое и тормозное излучение. Синхротронное излучение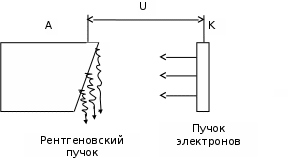 U – напряжение, К – нагреваемый катод, А – анод. Рисунок 1.2 - Схема получения рентгеновского излучения В 1895г. Вильям Рентген, немецкий физик, изучая так называемые катодные лучи (поток электронов, испускаемый нагретым катодом), открыл излучение, которое он назвал Х-лучи, и которое теперь называют рентгеновским излучением (рис.1.2). Рентгеновское излучение состоит из фотонов с энергией квантов до 70 кэВ и обладает чрезвычайно высокой проникающей способностью. В 1901 г. Рентген удостоен Нобелевской премии по физике. Он был первым Нобелевским лауреатом. Спектр рентгеновского излучения имеет непрерывную часть - тормозное излучение, и дискретную часть, состоящую из отдельных энергетических линий, называемую характеристическим излучением. Характеристическое излучение возникает в многоэлектронных атомах при выбивании одного из внутренних электронов. При этом электроны с верхних уровней начинают переходить на освободившееся место, излучая фотоны. В спектре образуется серия отдельных энергетических полос, причем их расположение по оси энергии характерно для каждого элемента - отсюда и название. Эти линии в спектре также обозначают K, L, M, N и т.д. С начала 20 века и по настоящее время рентгеновские аппараты широко используются в медицине и промышленности. В последние десятилетия используются также относительно более новые и более мощные источники излучения - синхротроны - ускорители электронов. Электроны в них движутся по круговым орбитам, т. е. с ускорением, и излучают жесткое гамма-излучение (синхротронное). |
