Углеродные нановолокна синтез, характеристика и электрохимически. Углеродные нановолокна синтез, характеристика и электрохимические свойства
 Скачать 356.47 Kb. Скачать 356.47 Kb.
|
|
Углеродные нановолокна: синтез, характеристика и электрохимические свойства Абстрактный Углеродные нановолокна (УНФ) были синтезированы методом раскисления со-катализатора реакцией между порошком C2H5OC2H5, Zn и Fe при температуре 650 ° С в течение 10 ч. Эти нановолокна имеют диаметр 80 нм и длину от нескольких микрометров до десятков микрометров. Рентгеновская дифракция, рамановская спектроскопия и просвечивающая электронная микроскопия высокого разрешения показывают, что в готовом виде УНФ обладают низкой графитовой кристалличностью. Полученный CNFs в качестве электрода показывает емкость 220 мАч/г и высокую обратимость с небольшой гистерезис в реакциях вставки/деинтеркаляции литий-иона. Кроме того, обсуждается возможный рост CNFs. 2005 Elsevier Ltd. Все права защищены. 1. Введение Возрастающие требования к электротехнике привели к увеличению потребности в электродных материалах аккумуляторов, электрохимических емкостях, вольтамперометрии и т. д. [1]. Как известно, литий-ионные аккумуляторы в настоящее время используются в самых разнообразных портативных электронных устройствах из-за их высокой плотности энергии. Однако по-прежнему существует необходимость в улучшении хороших характеристик литий-ионных аккумуляторов (для использования) в гибридных электромобилях [2,3]. Быстрые реакции заряда и разряда требуются, когда литий-ионные аккумуляторы используются для применения на большой мощности. Таким образом, литий-ионный процесс переноса должен быть очень быстрым в таких батареях. Как правило, процесс переноса литий-ионов в батареях состоит из трех этапов: (1) перенос литий-ионов через электролит; (2) перенос литий-ионов через границы раздела между электролитом и активными электродными материалами; (3) диффузия лития через активные электродные материалы на каждом электроде. Среди этих стадий хорошо известно, что диффузия литий-иона через активные электродные материалы протекает медленно [4]. Соответственно, либо поиск электродных материалов с быстрой диффузией, либо сокращение диффузионного пути является перспективная ориентация в дальнейшем развитии литий-ионных аккумуляторов. В то время как углеродистые материалы использовались в качестве электродов для литий-ионных аккумуляторов [5-7]. Высококристаллический графит получил широкое промышленное применение благодаря своей высокой емкости и плоскому потенциалу по сравнению с металлическим литием в процессах заряда/разряда [2]. Поскольку наноразмерные углеродные материалы обладают большой площадью поверхности и представляют собой относительно большое количество литий-ионных вставок на их поверхности, сопротивления переноса заряда на границе раздела между электролитом и активными электродными материалами являются ожидалось, что он будет маленьким. Кроме того, углеродные наноматериалы позволяют сократить пути диффузии лития-Иона внутри них, что приводит к кажущейся быстрой диффузии литий-иона. В последнее время появились углеродные наноматериалы с различной морфологией (углеродные нанотрубки, нановолокна, нанопроволоки, и наноматериалы) интенсивно изучались в качестве отрицательных электродных материалов в литий-ионных аккумуляторах [8-10]. Сообщалось, что некоторые углеродистые наноматериалы обладают хорошими электрохимическими свойствами [11,12]. Как правило, CNFs можно синтезировать с помощью химического осаждения вапора (CVD), горячего распыления с помощью нитей накала, шаблонные методы и т. д. [13-15]. Например, метод CVD плазмы высокой плотности [16], используемый для выращивания CNFs; вертикально выровненные углеродные нановолокна были изготовлены с помощью композиции Cu–Ni [17]; аморфные УНФ были синтезированы методом ионно-лучевого облучения [18]; здесь мы предлагаем способ получения УНФ с помощью процесса раскисления со-катализатора. Кроме того, были исследованы зарядно-разрядные свойства готовых УНФ 2. Экспериментальный раздел В типичном процессе синтеза CNFs, C2H5OC2H5 (7,5 мл) и смесь из 1000 г порошка Zn и 0,500 г порошка Fe помещали в 20-мл автоклав из нержавеющей стали. Автоклав герметизировали и выдерживали при температуре 650 ° С в течение 10 ч, затем давали остыть до комнатной температуры. Продукты собирали, промывали разбавленным раствором HCl, дистиллированной водой и этанолом последовательно, а затем сушили в вакууме при температуре 50 ° С в течение 4 ч. Конечный продукт после этого был охарактеризован используя стандартную методику. Рентгеновские дифракционные картины (РРД) регистрировались на Rigaku D с длиной волны излучения Cu ka1 k = 1,54178 а . Спектр комбинационного рассеяния света исследовали на французском конфокальном лазерном микро-Рамановском спектрометре Labram-HR, использовали аргон-ионный лазер с длиной волны 514,5 Нм. Изображения просвечивающей электронной микроскопии (Тэм) и диаграммы направленности электронов выбранной области (САЭД) были получены с помощью прибора Hitachi Модель просвечивающего электронного микроскопа H-800. Полевая эмиссионная сканирующая электронная микроскопия (FESEM, JEOL JSM-6700F) был использован для наблюдения за морфологией продуктов. Электронная микроскопия высокого разрешения (HRTEM) снимки были сделаны на просвечивающем электронном микроскопе JEOL-2010 . Электрохимические характеристики УНФ в качестве электрода измерялись с помощью двухэлектродных монетных ячеек (CR2032) Lij1M LiPF6 (EC:DEC = 1:1)jCNFs. Электродный ламинат CNFs готовили в виде гранул диаметром 14 мм путем заливки суспензии, состоящей из 85 мас.% активного оксида, 15 мас.% связующего Поли(винилиденфторида) (ПВДФ), на медную фольгу. В качестве сепаратора использовалась микропористая полипропиленовая мембрана Celgard 2400. Эти клетки были гальваностатически циклируется между 0 и 3 В при комнатной температуре на многоканальной тестовой системе аккумуляторных батарей (NEWARE БТС-610) для анализа электрохимического отклика. Плотность тока составляет 0,1 ма/см2 . Все электрохимические эксперименты проводились при температуре окружающей среды в бардачке, заполненном аргоном (99,999%). 3. Результат и обсуждение Типичная рентгеновская картина продуктов ( промытых разбавленным раствором HCl для удаления оксидов металлов и избытков металлов) показана на рис. 1А. Высокие и низкие пики при 26,0 и 43,5 могут быть проиндексированы на (0 0 2) и (1 0) дифракционных плоскостях гексагонального графита (картотеки JCPDS, № 41-1487) соответственно. Тот факт, что дифракционные пики 002 имеют относительно низкую интенсивность и широкую форму, говорит о том, что полученные углеродные нановолокна обладают низкой графитизацией и кристаллизацией. Кроме того, расширение наличие графитовых пиков указывает на существование некоторых неупорядоченных структур в изделиях. Никаких примесей в рентгенограмме не наблюдается. Представитель рамановский спектр (Рис. 1Б) показывает, что пик в 1607 см1 и относительно слабый широкий пик 1345 см1 , которые приписывают роман-активный E2g в самолет, режима вибрации и Роман-не активен A1g в плоскости дыхания вибрации режим, названный г (графит)- и D (расстройство)-полосы, соответственно [19]. Более конкретно, эти два пика демонстрируют режим графита E2g, связанный с вибрацией sp2 - связанные атомы углерода в двумерной гексагональной решетке (например, в графеновом слое) и режиме A1g графита связаны с особенностями беспорядка из-за эффекта конечного размера частиц или искажения решетки кристаллов графита. Когда степень графитизации уменьшается, положение G-полосы смещается в сторону более высокого волнового числа. Таким образом, по сравнению с 1582 см1 [20,21], пиковое положение полосы G образца высокоориентированного пиролитического графита (ХОПГ), полученные нами данные выше, что свидетельствует о том, что УНФ проявляют относительно низкую степень графитизации. Результаты идентичны приведенному выше рентгеновскому дисплею. 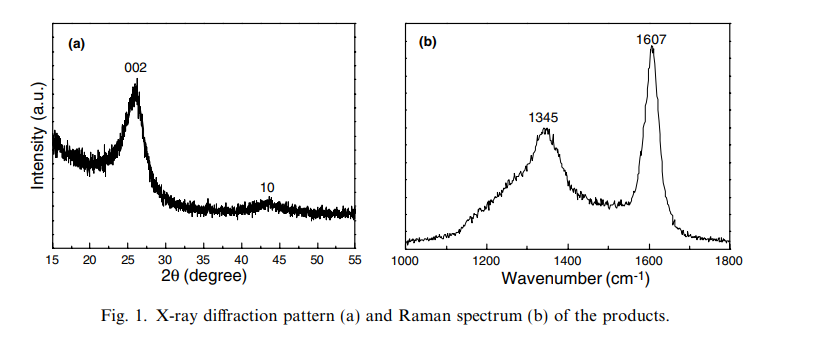  Можно легко обнаружить, что CNFs составляют большую часть получаемого продукта, и наблюдается небольшое количество примесей. Эти нановолокна имеют диаметр от 60 до 100 нм и длину от нескольких микрометров до десятков микрометров. Вставка на рис. 2b - это изображение конца CNFs с большим увеличением, показывающее твердую, а не полую структуру. Это означает, что полученные продукты являются твердыми нановолокнами, а не обычными нанотрубками. Более близкие наблюдения показывают, что большинство УНФ с гладкой и круглой поверхностью гнутся и несколько вьются. Структурная характеристика CNFs подробно исследована с помощью микроскопии SAED и HRTEM. Показано на рис. 3 - это изображение TEM продуктов. Шаблон SAED (вставка рис. 3а) показывает кольцо, соответствующее плоскостям (0 0 2) гексагонального углерода. Между тем несколько пар дуг в кольце указывают на некоторую ориентацию плоскостей 0 0 2 в CNFs. на рис. 3С показано ТЭМ-изображение отдельного углеродного нановолокна диаметром 100 Нм, а также обнаружен рисунок SAED и соответствующее изображение HRTEM (рис. 3d) его конца здесь. HRTEM показывает, что межслойное расстояние углеродного нановолокна составляет 0,342 Нм, что согласуется с параметром плоской решетки (0 0 2) графитированного углерода. SAED (вставка на рис. 3d) демонстрирует сильные дуги для 0 0 2 дифракций, подразумевая ориентацию плоскостей 0 0 2 в отдельном углеродном нановолокне, в соответствии с обсуждением SAED выше. Основываясь на анализе HRTEM и SAED, стек графеновых слоев почти перпендикулярен оси нановолокна ([0 0 2] обозначен стрелкой на рис. 3d). Этот феномен аналогичен описанному в литературе [22–24]. Профиль напряжения ячейки CNF/Li на разрядных кривых (Рис. 4) показывает электрохимическое поведение заряда–разряда при напряжении 0-3 В. Когда Li+ вставляется в CNFs в первом разряде можно различить два наклонных диапазона потенциалов (1,2–0,4 В и 0,4–0 в по сравнению с Li+/Li). Первый наклон следует отнести к разложению электролита и образованию межфазного слоя твердого электролита (SEI) на поверхности УНФ [25,26]. Большой потенциальный наклон в 0,4–0 В может быть связано с введением лития в CNFs. Первая разрядная емкость CNFs получается при 430 мАч/г, а во втором цикле она имеет разрядную емкость 260 мАч/г, что показывает сохранение емкости на уровне 60,5%. Необратимая емкость связана с введенным литием, расходуемым на формирование слоя SEI в первом процессе разряда. На рис. 4 также показана обратимая емкость 220 мА * ч/г до 30 циклов, что говорит о том, что введение/извлечение литий-иона приводит к высокой обратимости и малому гистерезису. Хотя точный процесс роста CNFs не очень ясен, мы можем предварительно использовать для его описания процесс, аналогичный модели гамали и Эббезенса [27]. Согласно этой модели, скорость распределения атомов углерода на поверхности катализаторов в основном влияет на образование углеродных наностержней. В нашем эксперименте катализаторы играют важную роль в росте нановолокон. Когда катализаторы (порошки Zn и Fe) отсутствуют в реакционной системе, получаются только углеродные твердые сферы. Если в качестве катализатора реакции выступает только металл Zn, то получаемые продукты в основном состоят из углеродных нанотрубок. В то время как, если только металл Fe по отдельности служит катализатором, полученные продукты состоят из некоторых углеродных сфер, нанотрубок и нескольких углеродных фрагментов. Только при одновременном добавлении порошка Zn и Fe в реакционную систему можно получить CNFs. Таким образом, мы предполагаем, что процесс включает в себя синергетический эффект совместного катализатора Zn и Fe. Феномен синергетического эффекта катализаторов также можно найти в некоторых сообщениях [28,29]. Мы предполагаем, что эффективность смешанный катализатор Zn/Fe связан с подвижностью атомов углерода на поверхности частиц катализатора. Более конкретно, сначала C2H5OC2H5 раскисляется Zn и Fe с образованием большого количества атомов углерода с повышением температуры реакции, а затем атомы углерода образуют однородную систему при содействии катализаторов. Вслед за этим некоторые атомы углерода присоединяются к поверхности катализаторов, образуя графитовые слои в виде колпачка, которые считаются затравочными структурами для роста УНФ. По мере того как реакция продолжается, CNFs может вырасти вдоль произведенной структуры семени. Наконец, нановолокна созревают только тогда, когда атомы углерода непрерывно поступают с надлежащей скоростью с поверхности катализаторов. Если скорость атомов углерода на поверхности катализатора медленная, то графитовые слои образуют углеродные нанотрубки. Напротив, графитовые слои производят углеродные сферы, то есть большинство получаемых продуктов являются углеродными сферами. Обсуждение идентично описанным выше экспериментам на катализаторах. Аналогичные реакционные процессы упоминаются и в литературе [23,30]. Кроме того, полученные нановолокна приобретать диаметром 60-100 Нм. Вариабельность диаметров может быть связана с разнообразием размеров катализаторов. Это явление аналогично предыдущему докладу [31]. Конечно, из -за сложности экспериментального процесса точный механизм образования CNFs все еще нуждается в дальнейших исследованиях. 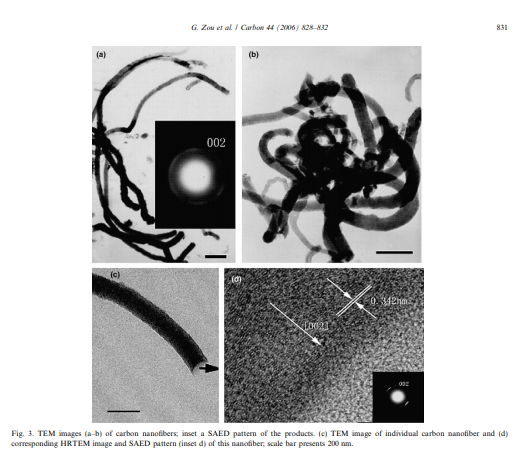 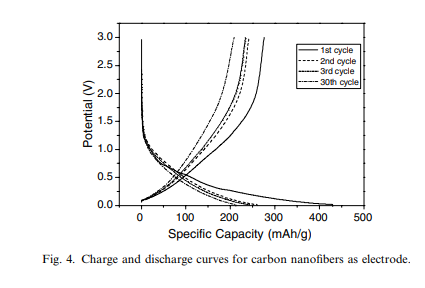 4. Заключение Впервые мы синтезировали CNFs с использованием C2H5OC2H5 в качестве исходного материала при синергетической роли порошков Zn и Fe. Эти нановолокна имеют диаметр 80 Нм, длину от нескольких микрометров до десятков микрометров и низкую графитовую кристалличность. Экспериментальные результаты показывают, что УНТ в качестве электрода обладают высокой обратимостью при малом гистерезисе вставки/ реакции экстракции литий-иона. Кроме того, комбинирование влияние порошков Fe и Zn является ключевым для образования CNFs. Синергетический эффект со-катализатора в реакционном процессе ценен для синтеза и изучения других углеродистых материалов. |
