Приложение 1. Урок httpsresh edu rusubjectlesson2053main
 Скачать 288 Kb. Скачать 288 Kb.
|
|
Смотреть видео-урок https://resh.edu.ru/subject/lesson/2053/main/ п. 49-51 1. Как классифицируют вещества? 2. Что такое естественные семейства? Выписать в рабочую тетрадь названия групп сходных по свойствам элементов (стр. 168 – 169 учебника) и перечислить элементы, которые входят в состав этих групп. 3. Сформулируйте периодический закон Д.И. Менделеева. 4. Опишите структуру Периодической системы: 1) Период – это 2) Малый период – это 3) Большой период – это Сколько периодов имеется в периодической системе элементов? 4) Группа – это 5) Главная подгруппа – это 6) Побочная подгруппа – это Сколько групп имеется в периодической системе элементов? 5. Распределите на группы следующие химические элементы: натрий, никель, кальций, марганец, сера, цирконий, бром, железо, магний, медь, цинк, алюминий, селен, свинец, серебро.
6. Найдите элементы по его положению в периодической системе и запишите его символ: а) элемент 3 –го периода, VI группы; б) элемент 5–го периода, II группы побочной подгруппы; 7. Укажите максимальную валентность для следующих элементов: а) Na б) C в) Mg г) N Памятка Закономерности изменений свойств химических элементов в группах и периодах Слева направо по периоду (см. таблицу Менделеева): металлические свойства простых веществ уменьшаются неметаллические свойства увеличиваются радиус атома уменьшается электроотрицательность элементов возрастает восстановительные свойства уменьшаются окислительные свойства увеличиваются основные свойства оксидов и гидроксидов уменьшаются Кислотные свойства оксидов и гидроксидов усиливаются идет увеличение числа электронов на внешнем уровне увеличивается максимальная валентность элементов Сверху вниз по группе (см. таблицу Менделеева) (для главной подгруппы): металлические свойства простых веществ увеличиваются неметаллические свойства уменьшаются радиус атома увеличивается электроотрицательность элементов уменьшается основные свойства оксидов и гидроксидов усиливаются кислотные свойства оксидов и гидроксидов убывают Число электронов на внешнем уровне не меняется К основным оксидам относятся оксиды металлов с валентностью I и II . К кислотным оксидам относятся оксиды неметаллов и оксиды металлов валентностью V, VI и VII. К амфотерным оксидам относятся Al2O3, BeO, ZnO, Cr2O3 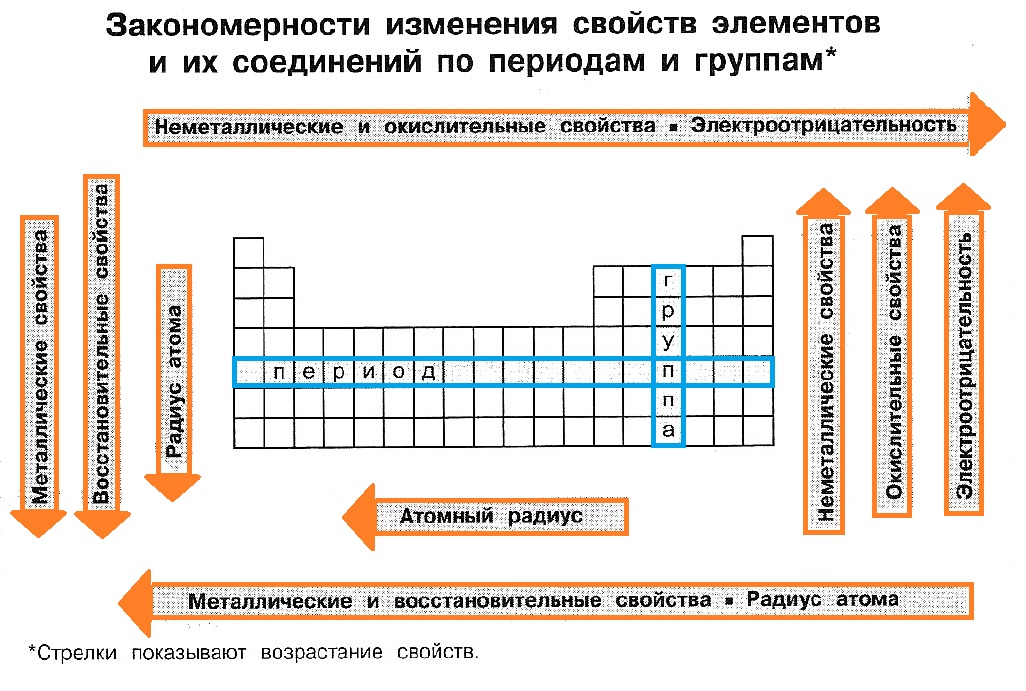 |
