2.1 Реакция Лебедева Началом для исследования способов получения диеновых непредельных углеводородов, которые до сир пор активно применяются для того, чтобы получать синтетический каучук, стала реакция С.В.Лебедева (Рисунок 1). Данное открытие позволило синтезировать искусственную резину, используя при этом более дешёвые материалы. 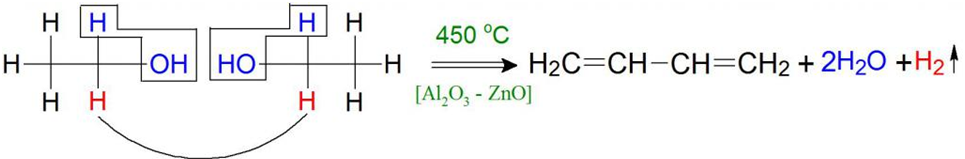 Рисунок 1 – Реакция Лебедева Эту реакция относят к каталитическом пиролизу, который протекает в присутствии алюмо-цинковых оксидных катализаторов и при температуре около 450°С. Реакция Лебедева интересна тем, что сама она проходит с одну стадию, но в нутрии неё происходят сразу несколько изменений – отщепление воды, отщепление водорода и присоединение алкильных остатков между собой. Когда С.В.Лебедев только начал свои исследования, он применял для создания бутадиена нефть. Впоследствии он стал получать диены из этилового спирта, который он получал реакцией брожения картофеля, но для того чтобы получить резину для одной автомобильной шины, надо переработать до 500 кг картофеля, что являлось очень затратным. Поэтому позже реакция Лебедева для получения бутадиена из этилового спирта была усовершенствована и это привело к тому, что выход диена оставлял 22%. Так, в конечном варианте синтеза, основными продуктами являются бутадиен – 1,3 CH2=CH‒CH=CH2, вода H2O и водород H2 ( могут образовываться и некоторые дополнительные органические вещества, например, ароматические соединения, высшие спирты, этилен, пропилен, бутилены и ацетальдегид, но, как правило, они не указываются в основном уравнении реакции Лебедева). Так как бутадиен является газообразным веществом, нерастворимым в воде, то от других газообразных углеводородов его отделяют конденсацией, абсорбцией спирта, отмывкой H2O или ректификацией. Механизм данной реакции происходит при разложении 2 молекул этанола, которое осуществляется благодаря катализаторам, отщепляющим 1 молекулу водород и 2 молекулы воду. Дальше, согласно механизму Лебедева, происходит присоединение алкильных остатков друг к другу, после чего образуются две непредельные сопряжённые связи в 1,3 –положениях.
2.2 Реакция Коновалова
Реакция Коновалова или нитрование – это реакция, при которой в алифатических и алициклических соединениях происходит замещение атома водорода на нитрогруппу, при нитровании разбавленной азотной кислотой:
RH+HNO3 = RNO2+Н2О Реакция Коновалова может протекать при повышенном или нормальном давлении. Скорость реакции зависит от температуры, концентрации азотной кислоты HNO3 и строения исходного соединения. Обычно для этой реакции используется азотная кислота, которая имеет концентрацию от 7 до 70%. Оптимальная температура для данной реакции 110-140°С. Наиболее легко замещаются атомы водорода у третичного атома углерода, сложнее у вторичного и наиболее трудно у первичного. При нитровании алкана, который содержит третичный атом углерода, образуется большое количество динитро- и тринитросоединений. При нитровании алициклических углеводородов, имеющие третичный атом углерода, используют 9 - 10% - ную азотную кислоту. Нитрование жирно -ароматических углеводородов проходит в а – положение боковой цепи, при этом образуются мононитросоединения. Легче чем соответствующие углероды, нитрируются алхилгалониды. Алхигалогениды, имеющие первичные и вторичные атомы углероды, образуют нитросоединения, которые будут содержать галоген, третичные отщепляют галогеноводород и при этом образуются непредельные углеводороды, которые могут, в свою очередь, подвергаться нитрованию. Спирты в условиях реакции окисляются до кислот, из альдегидов могут образовываться гемдинитросоединения. При нитровании кетонов образуются динитрокетоны или карбоновые кислоты и динитроалканы (Рисунок 2). |
 Скачать 180.18 Kb.
Скачать 180.18 Kb.
