Воздействие ионизирующего излучения на сердце. Воздействие ионизирующего излучения на сердце
 Скачать 79.52 Kb. Скачать 79.52 Kb.
|
|
Воздействие ионизирующего излучения на сердце Сердце считается радиорезистентным органом, так как регенерация кардиомиоцитов взрослой сердечной мышцы незначительна, поэтому ее эффективность замещать повреждения невелика. При фракционном облучении 60% и более объема сердца риск поражения составляет 5%. Фракционированная доза в 40 Гр может вызывать дегенерацию миокарда. При облучении всего сердца в дозе 60 Гр может наступить смерть организма в связи с кровоизлиянием в перикард или от констриктивного перикардита. При ограниченном облучении в той же дозе возникает очаговый фиброз миокарда. Наиболее опасным считается облучение в дозе более 50 Гр, поражающее до 30% ткани миокарда и более. При радиационном облучении повреждение сердца проявляется в период от нескольких месяцев до нескольких лет. При хроническом длительном облучении формируется перикардит с миокардиальным и эндокардиальным фиброзом и плевральным или перикардиальным выпотом. Тяжелым поздним осложнением является панкардит или «панцирное сердце» с возможным формированием приобретенных пороков сердца. Хронический перикардит - один из наиболее частых осложнений, который регистрируется у 96% пациентов. Наиболее часто повреждается пристеночный слой перикарда с его фиброзированием и утолщением, что клинически проявляется одышкой, болями в грудной клетке, расширением вен. Результатом повреждения перикарда является в последующем развитие жировой и амилоидной дегенерации. Клинические проявления поражения сердца при терапевтической радиотерапии могут характеризоваться стенокардией, ухудшением коронарного кровотока, снижением сократительной способности миокарда; развиваются инфаркты, сердечная недостаточность. Чаще описанные проявления регистрируются у лиц молодого возраста (25-40 лет) При дозах более 30 Гр пролиферация и в дальнейшем фиброзирование эндотелия коронарных артерий с появлением очагов некроза выявляются практически в 100% случаев. Однако причиной поражения сердца является не только изменение сосудов, как считалось ранее, но и непосредственное прямое воздействие на кардиомиоциты. Ускорение фиброза коронарных артерий и атеросклероз после лучевого воздействия могут вызвать коронарную болезнь сердца. В патологический процесс вовлекаются крупные и мелкие кровеносные и лимфатические сосуды. У больных, умерших через 1-12 лет после облучения, при вскрытии обнаруживалась картина обширного инфаркта с 75% поражением коронарных артерий. Признаки фиброзно-мышечной гиперплазии стенок обнаруживаются в артериях и венах различного калибра. Однако в отдаленном периоде после облучения, морфологические исследования коронарных артерий свидетельствуют о том, что наиболее тяжелые изменения (дегенерация и фиброз) обнаруживаются в средней мышечной оболочке сосудов. В интиме сосудов обнаруживаются бляшки, однако без липидных отложений, что отличает их от атеросклеротических. Тем не менее в экспериментах определены прямые количественные соотношения между дозой облучения, уровнем сывороточных липидов и развитием поражения коронарных артерий. В качестве раннего физиологического эффекта облучения сердца регистрируется удлинение интервала Q-T, которое отмечено спустя 1 мес после окончания облучения, с последующим купированием и вновь проявлением указанных изменений через 6-12 мес в результате формирующегося фиброза миокарда. Эти изменения обнаруживаются у 88% пациентов. Кроме того, регистрируется укорочение интервала Р-Q. С увеличением суммарной поглощенной дозы уменьшается сосудистый и соединительнотканный компонент. При действии низких доз ионизирующего излучения отмечаются фибробластическая пролиферация и продукция коллагена, в то время как при более высоких дозах в большей степени выражена гибель клеток. После перенесенной острой, подострой и хронической лучевой болезни длительное время фиксируется снижение функциональных способностей сердца. Прямое действие ионизирующей радиации на кардиомиоциты, строму сердца, кровеносные сосуды приводит к развитию миокардиодистрофии и миокардиосклерозу, чему способствуют нейротрофические, нейроциркуляторные, а также эндокринные факторы. Важная роль в повреждении миокарда принадлежит катехоламинам и нарушению баланса электролитов в сердечной мышце. В этой ситуации в отдаленные сроки после радиационного воздействия сердечно-сосудистые нарушения регистрируются при предъявлении функциональных нагрузок. Экспериментальные исследования, проведенные З.И. Калмыковой и соавт. (1984), свидетельствуют о наличии ЭКГ-изменений у животных, подвергшихся радиационному воздействию: снижении вольтажа желудочкового комплекса и лабильности ритма сердца, которые подвержены фазным изменениям. Так, в начальном периоде радиационного воздействия зарегистрировано снижение вольтажа желудочкового комплекса и брадикардия с последующей тахикардией. Низковольтажная ЭКГ обнаруживается у животных с 3-го месяца и до конца жизни. При хронической форме облучения в период с 1,5 до 3 лет регистрируется перегрузка правых отделов сердца. У 80% животных регистрируется легочное сердце, хотя на ЭКГ признаки перегрузки правого сердца отмечены лишь у 30% животных, что может быть связано с левожелудочковой гипертрофией, которая носит компенсаторный характер и нивелирует на ЭКГ признаки повышенной нагрузки на правое сердце. Регистрация системного АД свидетельствует о наличии артериальной гипертензии через 2-4 нед в случае хронического облучения, с последующим переходом к лабильности АД спустя 2-5 лет. Через 1-2 мес после радиационного воздействия развивается венозная гипотония, которая при хроническом радиационном воздействии прогрессирует в связи со снижением тонических свойств венозных сосудов. Радиационное поражение сердца Поражение сердца под влиянием ионизирующей радиации происходит при лучевой терапии рака легкого, молочной железы, пищевода, лимфогранулематоза лимфоузлов средостения. Под влиянием лучевой терапии могут развиваться изменения во всех структурах сердца, включая перикард, миокард, коронарные артерии, эндокард. Механизм развития радиационно-индуцированной кардиомиопатии Как указывают Weichselbaum и соавт. (1997), радиационное воздействие на сердце осуществляется через следующие основные механизмы: образование свободных электронов; образование свободных гидроксильных радикалов кислорода, возникающих при гидролизе воды, составляющей 80% объема клеток; значительное повышение активности такихцитокинов, как фактор некроза опухоли, фактор роста фибробластов; активация апоптоза (запрограммированной клеточной смерти) — см. раздел, посвященный патогенезу дилатационной кардиомиопатии; микроваскулярная деструкция. Под влиянием указанных факторов повреждается ДНК клеток миокарда, развиваются кардиоцитотоксический эффект, гибель кардиомиоцитов, фиброз миокарда. Клинические особенности Одной из характерных клинических особенностей воздействия радиации на сердце является поражение перикарда в виде фибринозного или экссудативного перикардита. Острый (фибринозный) перикардит развивается во время лучевой терапии приблизительно у 1.5-2% больных. Его клиническая картина такая же, как при острых перикардитах другой этиологии. Больные жалуются на острые боли в области сердца, усиливающиеся при дыхании, повышение температуры тела. При аускультации сердца определяется шум трения перикарда у левого края грудины (в зоне абсолютной тупости сердца). Следует обратить внимание на то, что у некоторых больных симптомы острого перикардита могут появиться через 3-6 месяцев после лучевой терапии и нередко проходят самостоятельно. После лучевой терапии может развиться экссудативный и кон-стриктивный перикардит, клиническая картина их типична и описана в гл. «Перикардиты». Лучевой констриктивный перикардит развивается после облучения большого объема ткани сердца в дозе более 40-50 Гр. Нередко бывает так, что выпот полости перикарда не дает клинических проявлений и обнаруживается только при эхокардиографии. В отдаленном периоде после лучевой терапии (через 9-12 мес. — несколько лет) возможно развитие кардиомиопатии с вовлечением эндокарда. Под влиянием радиации развиваются процессы интенсивного фиброзообразования в миокарде, эндокарде, преимущественно правого желудочка. Радиационная кардиомиопатия клинически проявляется застойной сердечной недостаточностью преимущественно по правожелудочковому типу, митральной недостаточностью (за счет фиброза митрального клапана), нарушениями сердечного ритма и проводимости. Как правило, при радиационной кардиомиопатии границы сердца остаются нормальными, дилатации левого желудочка нет, развивается преимущественно рестриктивная кардиомиопатия с нарушением диастолической функции левого желудочка. Реже радиационная кардиомиопатия сопровождается нарушением систолической функции левого желудочка или комбинированной систоло-диастолической дисфункцией. Тяжелым осложнением лучевой терапии может быть панкардит с развитием фиброза всех трех оболочек сердца (перикарда, миокарда, эндокарда), что проявляется симптоматикой резко выраженной застойной сердечной недостаточности (одышка, набухание шейных вен, периферические отеки, увеличенная болезненная печень, часто асцит, плевральный выпот, парадоксальный пульс). Через несколько лет после лучевой терапии может наблюдаться ускоренное развитие ИБС, причем поражение коронарных артерий характеризуется преимущественно интенсивным фиброзным процессом. Клиника ишемической болезни сердца типичная. Формирование клапанных пороков наблюдается редко. Инструментальные исследования Электрокардиография. Как правило, наблюдаются неспецифические изменения конечной части желудочкового комплекса в виде снижения интервала ST книзу от изолинии (по неишемическому типу) и уменьшение амплитуды зубца Т преимущественно в грудных отведениях. При развитии экссудативного перикардита наблюдается снижение вольтажа всех зубцов ЭКГ. Чрезвычайно характерны нарушения сердечного ритма разнообразного характера и атриовентрикулярные и внутрижелудочковые блокады. При развитии стенокардии или инфаркта миокарда появляется соответствующая ЭКГ-картина (см. гл. «Инфаркт миокарда»). Эхокардиография. Определяется увеличение толщины стенки левого и правого желудочков, митральная регургитация, нарушение диастолической функции левого желудочка. Может обнаруживаться выпот в полости перикарда. Структура радиационно-индуцированной болезни сердца Радиация может затронуть все структуры сердца, поэтому диапазон постлучевых сердечно-сосудистых проблем довольно широк. В структуре радиационно-индуцированной болезни описаны перикардит, кардиомиопатия, коронарная и клапанная патология, нарушения ритма сердца и проводимости (см. таблицу) [29, 8, 27, 2, 23]. Эти различные клинические проявления радиационно-индуцированной болезни сердца имеют разную зависимость от полученной дозы, но обычно формируются спустя 10-15 лет после лучевой терапии. Таблица. Радиационно-индуцированная болезнь сердца
Механизм развития постлучевых повреждений Механизм развития постлучевых повреждений полностью не изучен. Предполагается, что лучевая терапия вызывает эндотелиальное повреждение и периваскулярный фиброз с пролиферацией гладкомышечных клеток [30, 35, 37]. Радиация также оказывает протромбический эффект, влияя на фактор Виллебранда, что было замечено после облучения эндотелиальных клеток in vitro [30]. Структурные изменения в коронарных артериях, которые формируются вследствие лучевой терапии, подобны атеросклерозу, но имеют отличия [23, 29]: высокая частота проксимального стеноза и устьевой локализации; высокая частота безболевой ишемии (из-за автономной дисфункции вегетативной нервной системы с уменьшенным восприятием ангинозной боли). высокая частота поражения левой главной коронарной артерии, левой передней нисходящей артерией и правой коронарной артерией. Это происходит из-за включения их в область радиационного воздействия во время лучевой терапии при медиастинальных лимфомах или раке молочной железы [31]. Интересно, что цитолитический эффект ионизирующего излучения пытаются применять для предотвращения рестенозов коронарных и других артерий после реконструктивных операций, используя внутрипросветное облучение [32] или неинвазивное дистанционное облучение на зоны реконструкции артерий [34]. В сообщениях говорится о хороших результатах, но это всего лишь сиюминутный успех. Долговременные результаты таких вмешательств не изучались. Методы снижения постлучевой патологии На частоту развития и характер лучевых повреждений оказывают влияние условия проведения лучевой терапии: величина суммарной очаговой дозы, поля воздействия, погрешности планирования, объём здоровых тканей, подвергшихся облучению и т.д. [29, 8, 2]. Техническое усовершенствование радиотерапевтической аппаратуры, развитие клинической дозиметрии, разработка предлучевой топометрии с использованием компьютерной техники служат основой повышения эффективности лучевой терапии при лечении опухолей. Наличие в предлучевой топометрии рентгеносимулятора, компьютерного томографа, возможность использования магнитно-резонансного и позитронного эмиссионного томографа позволяют весьма точно определить границы мишени, подлежащей облучению. Даже такая мелочь, как синхронизация лучевой терапии с дыханием, позволяет уменьшить дозу ионизирующего излучения в органах риска (сердце и лёгкие) и, тем самым, снизить вероятность развития лучевых осложнений. Кроме того, ведутся эксперименты по применению цитопротекторов, например, амифостина Радиационное излучение может причинить ущерб любым тканям и органам, в том числе перикарду, миокарду, клапанам, проводящей системе сердца и венечным артериям. Большая часть знаний о ССЗ, вызванных лучевой терапией, основана на результатах наблюдения за пациентами с болезнью Ходжкина. Радиационное облучение грудной клетки также используют для лечения рака молочной железы, легких и семиномы. Клиническое течение ССЗ, вызванных воздействием радиационного излучения, будет более изученным после того, как улучшатся показатели долгосрочного выживания больных с онкологическими заболеваниями. Поражение миокарда Существует, по крайней мере, два механизма, лежащих в основе повреждения миокарда облучением: микроциркуляторные нарушения и свободно-радикальное повреждение. В экспериментах на животных показано, что процесс повреждения можно разделить на три этапа. Острая фаза наступает вскоре после воздействия радиации и характеризуется острым воспалением артерий малого и среднего диаметра. Далее следует фаза латентного повреждения, в ходе которой повреждается эндотелий капилляров, происходит тромботическая окклюзия и развивается ишемия. Со временем наступает гибель кардиомиоцитов и развивается фиброз. К счастью, у большинства пациентов после лучевой терапии поражение миокарда протекает достаточно мягко и чаще всего не сопровождается клиническими симптомами. Клинически выраженная КМП встречается достаточно редко и чаще всего протекает по рестриктивному типу. ДКМП-подобная КМП развивается у пациентов, получавших лечение антрациклиновыми антибиотиками, так как кардиотоксичность производных антрациклина в ходе лучевой терапии повышается. Перикардит Перикардиты также могут возникать после перенесенного облучения. Для них характерно отсроченное начало. Развитие острого раннего перикардита обычно ассоциировано с индуцированным радиацией некрозом больших опухолей, расположенных рядом с сердцем. Развитие отсроченных осложнений после лучевой терапии - достаточно редкое явление. Отсроченное поражение перикарда может развиться спустя месяцы и годы после лучевой терапии и манифестировать в двух частично сочетающихся вариантах: острый перикардит, у 20% пациентов трансформирующийся в хронический констриктивный перикардит; хронический выпотной перикардит, который может развиться спонтанно спустя годы. Пациентам, имеющим симптомы и (или) риск возникновения гемодинамических нарушений, можно рекомендовать тотальную париетальную перикардэктомию, которая ассоциирована с более благоприятным прогнозом, нежели выполнение перикардиоцентеза. Поражение проводящей системы (нарушения ритма) Распространенность и частота возникновения поражения проводящей системы сердца после лучевой терапии неизвестны. Его позднее возникновение затрудняет установление причинно-следственной связи с перенесенной лучевой терапией, но описаны случаи развития после облучения синдрома слабости синусового узла и АВ-блокады разной степени. Чаще последние возникают не на инфранодальном уровне, а на уровне непосредственно АВ-узла. Также регистрируют наджелудочковые и желудочковые аритмии. Поражение клапанов Среди 294 больных с ходжкинской лимфомой, получавших лучевую терапию и не имевших нарушений сердечной деятельности, у 29% было обнаружено поражение клапанов сердца, которое потребовало назначения антибактериальной терапии. Поражение АК встречалось чаще, чем митрального и трикуспидального, вероятно, вследствие его наиболее близкого расположения к источнику излучения. Есть сообщения как о развитии клапанных стенозов, так и о возникновении СН без указания частоты распространенности указанных нарушений. Частота обнаружения дисфункции клапанов увеличивается со временем, прошедшим после лучевой терапии. Ишемическая болезнь сердца У пациентов, получавших лучевую терапию на область средостения, отмечен повышенный риск возникновения ИБС. Левая передняя нисходящая и правая венечные артерии находятся в зоне типичного лучевого покрытия и поражаются наиболее часто. Чаще всего обнаруживают проксимальные стенозы с захватом устья венечных артерий. ИБС, как правило, развивается у пациентов, имеющих, по крайней мере, один из установленных факторов риска до начала лучевой терапии. Клиническая картина У пациентов с ССЗ, возникшими вследствие облучения, присутствуют характерные симптомы. Острый перикардит сопровождается болями в грудной клетке и лихорадкой, в то время как поражение миокарда может дебютировать нарастающей одышкой. Большинство больных, прошедших лучевую терапию, симптомов не имеют. Субклиническая дисфункция миокарда, перикардиальный выпот и клапанная дисфункция более распространены, чем клинически выраженная патология. Вследствие повреждения излучением нервных окончаний сердца бессимптомный ИМ регистрируют в этой группе чаще, чем в общей популяции населения. Пациентам, получающим лучевую терапию, для диагностики скрытых аномалий необходимо периодически проводить обследование сердечно-сосудистой системы. Неинвазивное обследование должно включать 12-канальную ЭКГ, пробу с физической нагрузкой, ХМ ЭКГ и оценку липидного профиля. По показаниям можно выполнять МРТ. Таким пациентам необходимы постоянный мониторинг и своевременное обнаружение факторов риска развития ИБС, а также первичная профилактика при их возникновении. Больным с изменениями клапанов следует проводить профилактику инфекционного эндокардита. Наступление беременности ассоциировано с повышенной нагрузкой на сердечно-сосудистую систему, поэтому пациентки нуждаются в тщательном обследовании и оценке состояния сердечно-сосудистой системы до родов. Современная техника проведения лучевой терапии подразумевает применение низких доз общего облучения, а также использование специальных экранов для уменьшения облучения сердца и снижения риска развития заболеваний. Антиоксиданты и дексразоксан защищают от кардиотоксического действия антрациклинов, а амифостин уменьшает токсичный эффект радиации. По возможности следует избегать сочетанного проведения кардиотоксичной химио- и лучевой терапии. Лечение артериальной гипертензии и гиперлипидемии также может уменьшить вероятность развития ИБС в будущем. Otto M. Hess, William McKenna и Heinz-Peter Schultheiss Болезни миокарда Сердечно-сосудистая система при острой лучевой болезни. Сердце после радиационного поражения Функциональные и морфологические изменения сердечнососудистой системы занимают значительное место в патогенезе острой лучевой болезни и, как показали наблюдения последних лет, в развитии поздних и отдаленных последствии заболевания. Указания на те или иные проявления расстройства кровообращения и структурные нарушения в сердце и кровеносных сосудах можно найти почти во всех работах, касающихся биологического действия ионизирующих излучений на животный организм. Однако специальные морфологические исследования сердца и сосудов относительно немногочисленны, причем большая часть их относится к местному действию ионизирующих излучений. Только в немногих работах имеются достаточно полные сведения о морфологических изменениях в этих органах при острой лучевой болезни, вызванной общим облучением. Вместе с тем литературные данные, касающиеся физиологии и патологии кровообращения в условиях лучевого поражения свидетельствуют о значительных расстройствах гемоциркуляции при острой лучевой болезни [Лебединский А. В., 1956; Горизонтов П. Д., 1962; Куршаков Н. А., 1963; Гуськова А. К., Байсоголов Г. Д., 1971]. После облучения стойко понижается артериальное и венозное давление, уменьшается скорость кровотока и объема циркулирующей крови, изменяется частота и ритм сердечных сокращений. Одновременно появляются признаки кровоточивости сосудов вследствие изменения реологических свойств крови и прочности сосудистых стенок, которые всегда наблюдаются при патологоаватомическом исследовании в разгар типичной формы острой лучевой болезни, вызванной однократным внешним облучением в минимальной смертельной дозе [Краевский Н. А., 1957]. 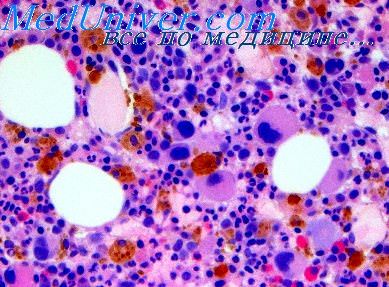 Сведения о патоморфологических изменениях в сердце при лучевых поражениях до сих пор в основном относятся к случаям изолированного облучения области сердца у людей, подвергшихся лучевой терапии при заболеваниях органов грудной клетки. В свое время было отмечено, что изолированное облучение в небольших дозах не вызывает существенных морфологических изменеиий и только воздействие в массивных дозах приводит к выраженным нарушениям в миокарде и других структурах сердца. В частности, И. М. Жданов (1941) не смог выявить каких-либо заметных морфологических изменений в мышцах и нервном аппарате сердца у кроликов после локального облучения фильтрованными рентгеновскими лучами даже в дозе 1500 Р. В некоторых работах последних лет тоже не отмечено существенных изменений в мышечных волокнах и эндотелии сосудов сердца после локального облучения рентгеновскими и у-лучами [Mollmann H. ct al., 1971]. В то же время в других исследованиях с помощью светового и электронного микроскопов отчетливо прослежено, что локальное внешнее облучение области сердца, например, в дозах 500—2400 рад, вызывает отчетливые изменения миокардиальных клеток и кровеносных сосудов сердца в виде расширения и переполнения кровью их просветов, плазматического пропитывания стенок, набухания и вакуолизации эндотелия (Morgenroth J. К. et al., 1967; Fajardd L. et al., 1970; Huff H. et al., 1972; Лебкова Н. П., 1967]. Однако Л. А. Яковлева (1975) считает, что эти изменения прежде всего зависят от нарушения нервной и гуморальной регуляции, а не от непосредственного действия радиации на сердце. Морфология сердца при острой лучевой болезни. Патология сердца после радиационного поражения Анализ литературных материалов показывает, что морфологические изменения в сердце после местного облучения рентгеновскими лучами в пределах эритемной дозы (600 Р) ограничиваются лишь явлениями острого венозного застоя, а после воздействия в дозах, превышающих 1000 рад, наступает нарушение кровообращения вследствие набухания эндотелия капилляров и нарушения целостности их стенок, отека периваскулярной и интерстициальной ткани, кровоизлияния и очаговых дистрофических изменений в сердечной мышце, вплоть до гибели отдельных мышечных волокон, с последующим уменьшением капиллярной сети и развитием интерстициального склероза [Лебкова Н. П., 1976]. Наиболее тяжелые изменения описаны после многократных облучений области сердца. В этих случаях обнаруживается переполнение кровью мелких кровеносных сосудов и капилляров, плазматическое пропитывание сосудистых стенок и наличие отечной жидкости в периваскулярной и межуточной ткани, кровоизлияния, признаки белковой и жировой дистрофии, исчезновение поперечной исчерченности, некроз мышечных волокон, а в отдаленные сроки — большое количество липофусцина н атрофия мышечных волокон. Одновременно происходит разрастание периваскулярной межуточной ткани, склеротическое утолщение эпикарда, дистрофические изменения в нервных образованиях [Фунштейн Л. В. и др., 1976; Fajardo L. et al., 1970, 1971; Bourain Y. et al., 1977]. Отмеченные закономерности свидетельствуют об определенной зависимости характера патологоанатомических изменений в сердце от количества энергии, поглощенной тканью органов, что подтверждается и наблюдениями в условиях общего облучения организма. Поэтому вполне очевидно, что некоторые исследователи, применявшие в своих экспериментах мягкие рентгеновские лучи, не обнаружили в сердце заметных изменений, кроме признаков застойного полнокровия капилляров и мелких кровеносных сосудов. Как известно, при острой лучевой болезни, обусловленной внешним облучением, развиваются тяжелые функциональные нарушения сердечной деятельности [Куршаков Н. А., 1954; Горизонтов П. Д., 1962]. Тем не менее даже в монографических трудах, посвященных патологической анатомии экспериментальной лучевой болезни [Яковлева Л. А,, 1966], состоянию миокарда уделяется мало внимания. Отмечается только, что в сердце облученного организма наблюдаются дистрофические изменения. Существует даже мнение о достаточной устойчивости сердца к лучистой энергии [Herapelmann L. et ai., 1952; Jones A. et al., 1960]. Однако большинство исследователей относят его к радиочувствительным органам [Саркисов Д. С, 1955; Краевский Н. А„ 1957, 1962; Фунштейн Л. В., 1961; Иванов А. Е., 1962], поражение которого занимает существенное место в патогенезе острой лучевой болезни. В случаях данного поражения людей, описанных ранее в зарубежной литературе [Shipman Т., 1962; Feindger J. et al., 1967], имелось расстройство кровообращения главным образом по типу правосторонней сердечной недостаточности, сопровождавшееся массивным отеком тканей. Источник: https://meduniver.com/Medical/gistologia/792.html MedUniver Макроскопические изменения сердца после радиации. Вегетативная нервная система после острой лучевой болезни Для макроскопической картины поражения сердца при типичной форме острой лучевой болезни характерно наличие кровоизлияний и, как проявление общего истощения, значительное уменьшение жира под эпикардом. Кровоизлияния обнаруживаются главным образом ни высоте заболевания в клетчатке, окружающей перикард, под эпикардом и эндокардом и реже в сердечной мышце. Образование кровоизлияний в стенках предсердий и в перегородке желудочков вблизи нервных узлов и проводящих путей сердца, по-видимому, может быть причиной нарушения сердечной деятельности, а в некоторых случаях и смертельных исходов [Краевский Н. А., 1957; Ахмедов Н. К., Ушакова Э. Я., 1974; Tullis J., Warren Sh., 1947; Liebow A. et al., 1949; Hempelmann L. et al., 1952]. В области ушка сердца кровоизлияния могут достигать очень больших размеров, нередко пропитывают стенку предсердия, распространяются на крупные сосуды и перикард. Весьма часты кровоизлияния по ходу венечных сосудов. Другие макроскопические изменения со стороны серозных оболочек и мышцы сердца обычно не выявляются. Только в тяжелых случаях, на высоте болезни или в отдаленные сроки хронического поражения, можно видеть некоторую тусклость поверхности разреза и дряблость сердечной мышцы с умеренными признаками белковой и жировой дистрофии [Краевский Н. Л., 1957]. Однако следует отметить, что описанное относится к типичной форме нсосложненной экспериментальной острой лучевой болезни, вызванной равномерным облучением организма в минимальной смертельной дозе. В литературе имеются данные о возможности развития «фибринозного перикардита» у людей, погибших после однократного у-нейтронного облучения в суммарной дозе 750 рад [Hempelmann L. et al., 1952]. Как полагают авторы, наличие фибринозно-геморрагического выпота в полость перикарда связано с непосредственным действием излучения на сердце. О развитии перикардита после облучения области сердца сообщают и другие исследователи [Parstens L., Allen J., 1968; Lawson P., 1972]. Насколько можно судить по описанию соответствующих микроскопических изменений, в этих случаях имело место резкое нарушение проницаемости кровеносных сосудов и капилляров вследствие массивного локального облучения сердца. При микроскопическом исследовании, как правило, обнаруживаются более существенные изменения всех структур сердца. В начале болезни, даже через несколько часов после облучения [Беспалова Л. А., 1969], отмечаются полнокровие венозной сети, умеренное набухание стенок артериол и мелких вен, отек и метахромазия интерстициальной ткани, набухание коллагеновых « расплавление аргирофильных волокон, незначительное набухание мышечных волокон, появление оксифильных мышечных волокон с сохраненной поперечной исчерченностью и обычной формой ядер, уменьшение во всех мышечных волокнах содержания ДНК и РНК [Степанов Р. П., 1977]. Одновременно отмечается отек и гомогенизация волокон проводящей системы, мукоидное набухание ткани клапанов сердца. Однако эти изменения выявляются лишь на высоте острой лучевой болезни. Ни в начале заболевания, ни в латентном периоде существенных изменений отметить не удается. Лишь в разгар болезни в интрамуральных ганглиях сердца обнаруживается вакуолизация и сморщивание отдельных нервных клеток, пикноз ядер, интенсивная импрегнация этих клеток серебром. В толстых пучках безмиединовых нервных волокон появляется значительное количество волоконец, интенсивно воспринимающих серебро и имеющих крупные варикозные вздутия. Аналогичные изменения нервных волокон встречаются и в нервных пучках, расположенных в стенках сосудов. Особенно значительные изменения в нервных волокнах наблюдаются в очагах кровоизлияний [Зайратьянц В. Б., 1957; Ахмедов Н. К., Ушакова Э. Я., 1974]. Источник: https://meduniver.com/Medical/gistologia/793.html MedUniver Дегенерация сердца после лучевого поражения. Радиационное поражение мышц сердца С течением времени указанные изменения нарастают и к концу латентного периода (конец 1-й недели) начинают улавливаться признаки более грубых структурных нарушений. К этому времени становится очевидной белковая дистрофия мышечных волокон и изменения проводящей системы, явления «фуксинофильной дегенерации» и пикноз ядер. Данные гистохимических исследований указывают на существенные изменения активности окислительно-восстановительных ферментов, уменьшение содержания гликогена, фосфолипидов и нейтральных жиров в мышечных волокнах и в проводящей системе сердца, начиная с первых часов после облучения [Иванов А. Е., Куршакова Н. Н., 1959; Schmdt К. et aj,, 1968]. Электронно-микроскопически при этом в саркоплазме определяются оптически пустые перинуклеарные вакуоли, отек цитоплазматических структур, вакуолизация митохондрий, разъединение вставочных дисков, очаговые расплавления и дегенерация миофибрнлл [Беспалова Л. А., 1969, 1973; Allen J. et at., 1968]. Кроме того, можно видеть большое количество мышечных волокон, ядра которых увеличнны, имеют вытянутую форму и фестончатую границу, что, как известно, свойственно для гипоксических состояний. В сердечных сосудах обычно наблюдаются признаки стаза, возросшей проницаемости и плазматического пропитывания стенок артериол и мелких вен. При этом клетки эндотелия выглядят набухшими, выступают в просвет сосуда, ядра их сморщиваются и интенсивно окрашиваются основными красками. В ннтерстициальной ткани отмечается значительное количество жидкости, дающей метахроматическую реакцию, и мелкие периваскуляриые кровоизлияния диаисдсзиого характера. Все это свидетельствует о нарастании тканевой гипоксии и понижения окислительно-восстановительных процессов в клетках. Вместе с тем известно, что при очень массивном облучении области сердца в дозах 3000, 8000, 12 000 рад, приводящем к гибели люден в течение первых 2 сут. в миокарде был только интенсивный отек межуточной ткани. Наиболее выраженные морфологические изменения в сердце совпадают по срокам с периодом наиболее отчетливых проявлений лучевой болезни. В это время дистрофические изменения наблюдаются во всех структурных элементах сердечной стенки. Имеет место набухание мышечных волокон с частичной или полной потерей поперечной исчерченности, выраженными явлениями миоцитолиза. Ядра мышечных волокон сморщиваются или бывают увеличенными, с неровными краями. Появляется большое количество мышечных волокон с гомогенизированной цитоплазмой, обладающей неспецифической птронинофилией и свойством метохроматтчески окрашиваться фуксином. В некоторых мышечных волокнах, особенно в сосочковых мышцах и в стенках правой половины сердца, при окраске шарлахом и Суданом выявляются мелкие капли жира, образующиеся, судя по гистохимическим исследованиям, вследствие глубоких нарушений жирового обмена на высоте болезни. На это указывает значительное уменьшение фосфолипидов и одновременное накопление нейтрального жира, свидетельствующее о нарушении процессов расщепления ляпидов в мышечных волокнах сердца. Такие изменения сочетаются с глубокими сдвигами в энергетическом обмене. В мышечных волокнах резко снижается содержание гликогена, активность щелочной фосфатазы, окислительно-восстановительных ферментов. В отдельных случаях изменения мышечных волокон могут достигать большей степени, вплоть до их гибели. При этом клеточная воспалительная реакция вокруг некротизированных участков, как правило, отсутствует. Однако наблюдения показывают, что на месте погибших мышечных волокон асе же появляются клетки фибробластического ряда, число которых по мере удлинения продолжительности жизни облученного, организма нарастает [Беспалова Л. А., 1969; Yang V. et al., 1976]. Кроме того, в зоне деструкции обычно различаются мышечные волокна с амитотически делящимися ядрами. Имеет место также значительное набухание и вакуолизация волокон проводящей системы. Источник: https://meduniver.com/Medical/gistologia/794.html MedUniver |
