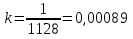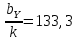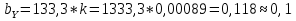Министерство науки и высшего образования Российской Федерации
Федеральное государственное образовательное учреждение Высшего образования
Российский Химико-Технологический Университет им. Д. И. Менделеева
Факультет нефтегазохимии и полимерных материалов
Кафедра химической технологии углеродных материалов
Задача
Теория гетерогенных процессов
Выполнил: студент группы П-46 Будник М.Ю.
Проверил: д.х.н., проф.Бухаркина Т.В..
Москва, 2019
Условие задачи
Дана реакция:A + Y→ B + Z
Периодический реактор, измеряется концентрация вещества А.
Пределы варьирования концентраций веществ:
A от 0,2 моль/л до 1 моль/л
Y от 5 моль/л до 10 моль/л
Предполагаем кинетическую модель следующего вида:
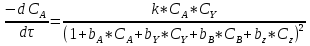
Предварительные опыты
Обратимость реакции
СA = 0,5 моль/л; CY = 5 моль/л; Св = 0 моль/л; Сz = 0 моль/л
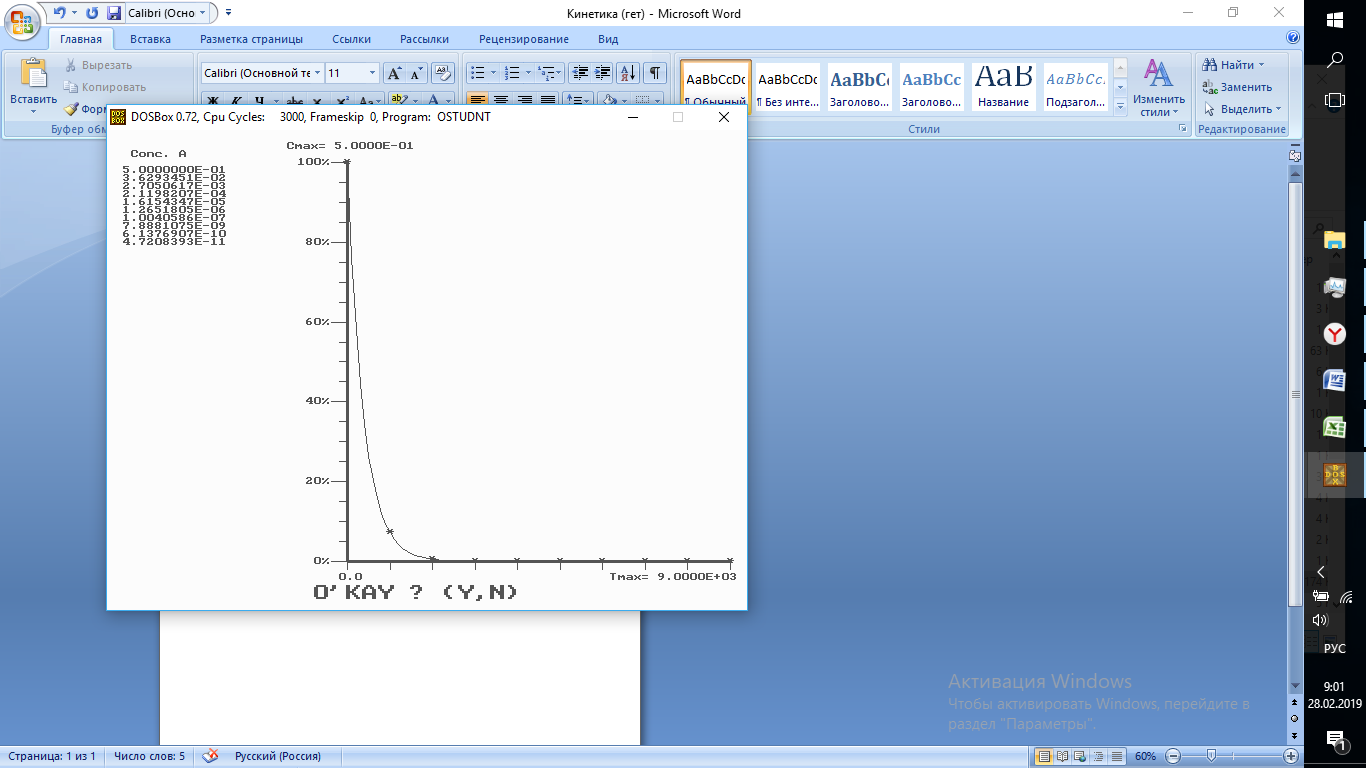
При τ→ ∞ степень превращения вещества А стремится к нулю
Вывод: реакция не обратима
Влияние продуктов на скорость реакции
СA = 0,5 моль/л; CY = 5 моль/л; Св = 0 моль/л; Сz = 0 моль/л;
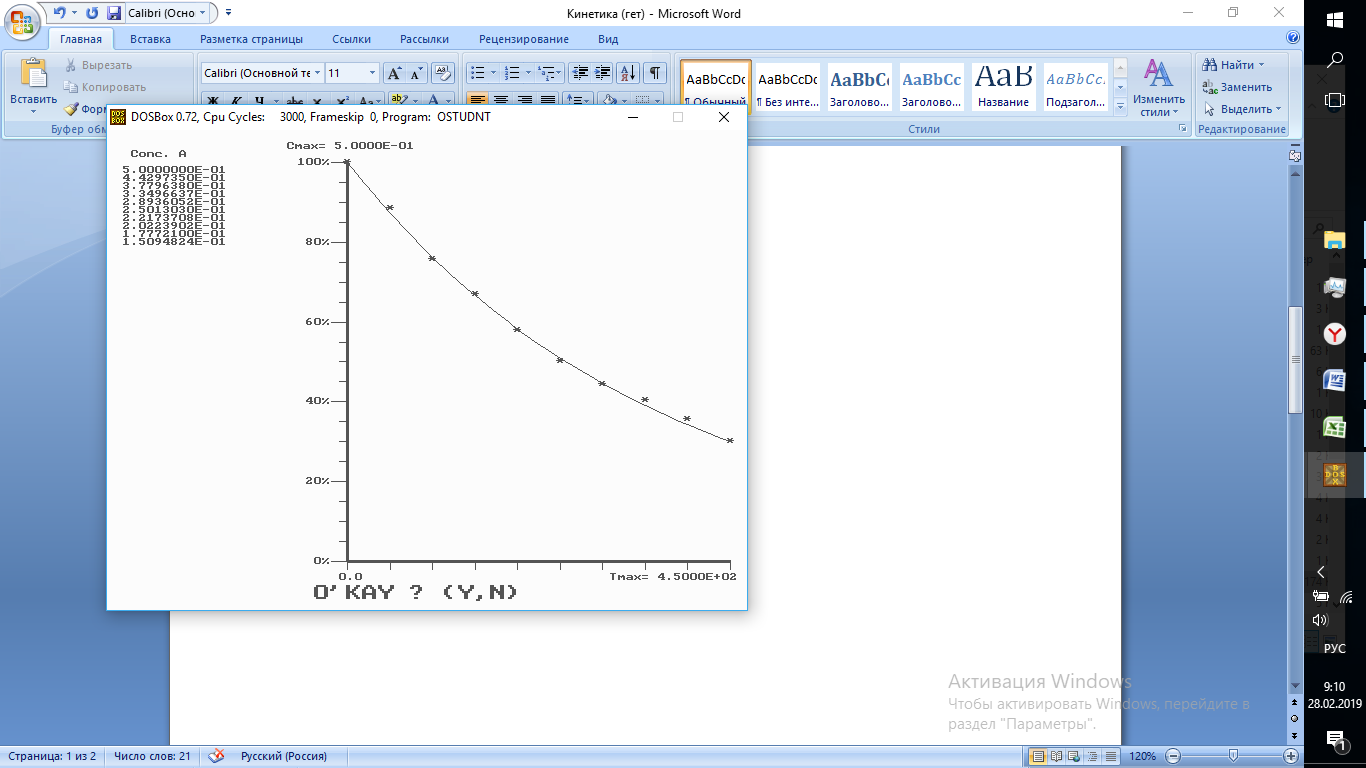
СA = 0,5 моль/л; CY = 5 моль/л; Св = 0,2 моль/л; Сz = 0 моль/л;
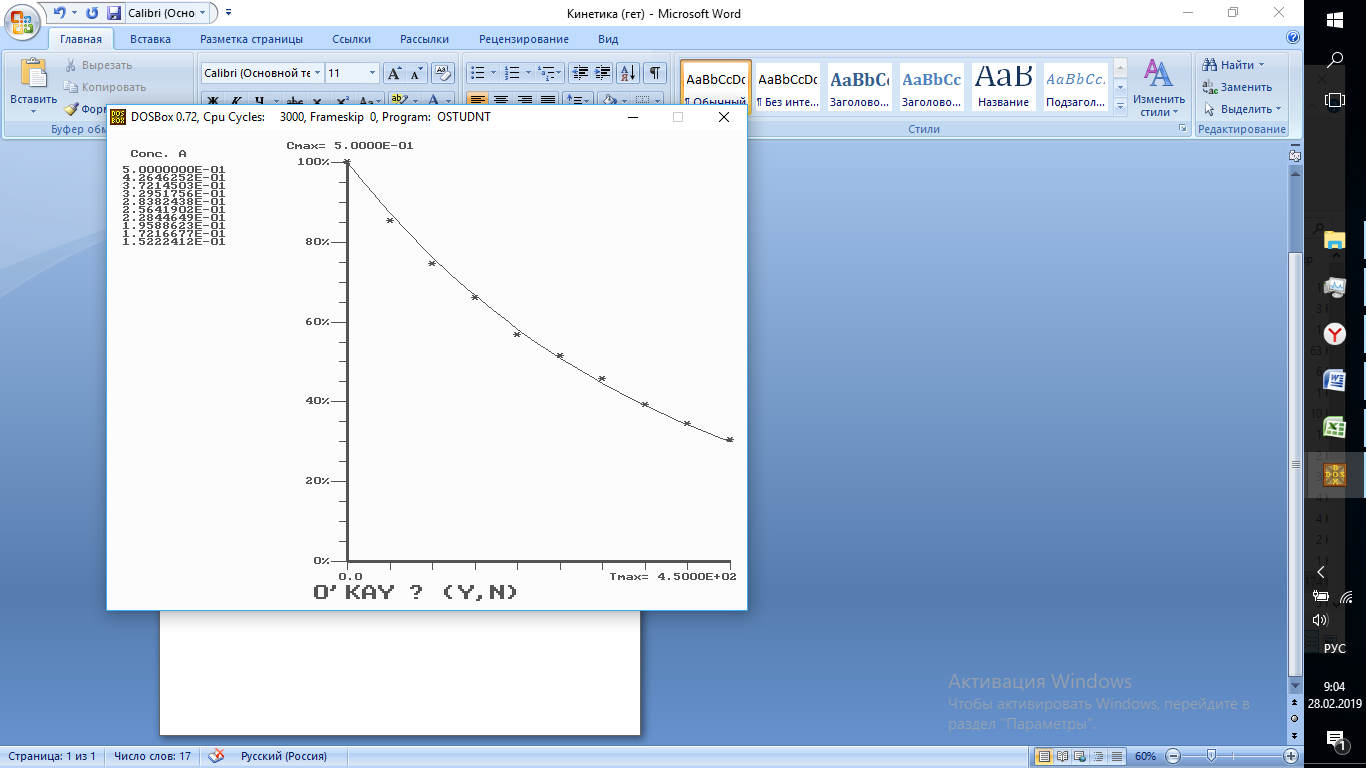
Са = 0,5 моль/л; CY = 5 моль/л; Св = 0 моль/л; Сz = 0,2 моль/л;
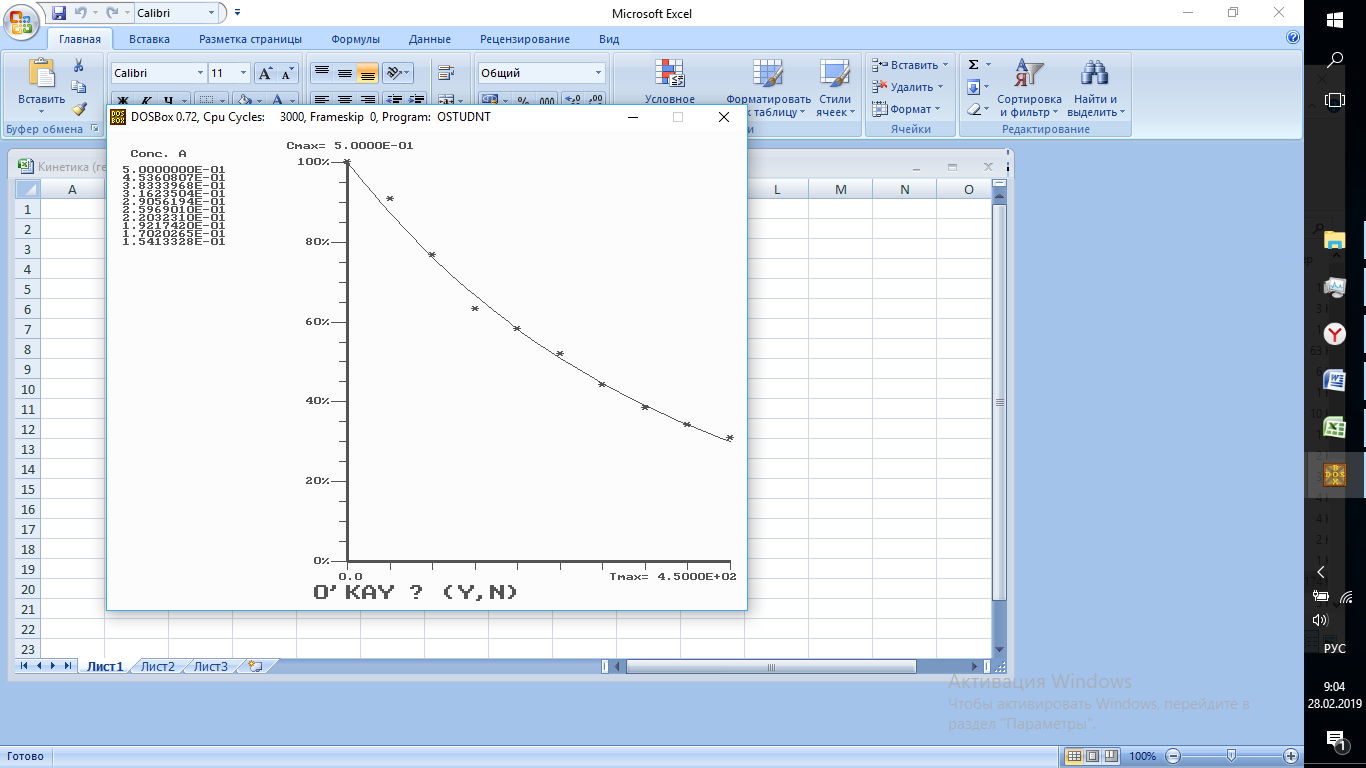
|
СВ = 0 моль/л;
СZ = 0 моль/л
|
СВ = 0,2 моль/л; СZ = 0 моль/л
|
СВ = 0 моль/л;
СZ = 0 ,2 моль/л
|
τ
|
СА, моль/л
|
СА, моль/л
|
СА, моль/л
|
0
|
0,5
|
0,5
|
0,5
|
50
|
0,426
|
0,454
|
0,443
|
100
|
0,372
|
0,383
|
0,378
|
150
|
0,33
|
0,316
|
0,335
|
200
|
0,284
|
0,291
|
0,289
|
250
|
0,256
|
0,26
|
0,25
|
300
|
0,228
|
0,22
|
0,222
|
350
|
0,196
|
0,192
|
0,202
|
400
|
0,172
|
0,17
|
0,178
|
450
|
0,152
|
0,154
|
0,151
|
Внесение продуктов в исходную реакционную массу не оказывает влияние на скорость протекания процесса
Вывод: продукты не влияют на скорость реакции (не занимают активные центры катализатора)
Предполагаемая кинетическая модель имеет вид:
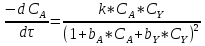
Определение порядка по веществу А
τ
|
СА, моль/л
|
lnСА
|
СА, моль/л
|
lnСА
|
СА, моль/л
|
lnСА
|
СА, моль/л
|
lnСА
|
0
|
0,2
|
-1,60944
|
0,4
|
-0,91629
|
0,7
|
-0,35667
|
0,9
|
-0,10536
|
40
|
0,176
|
-1,73727
|
0,336
|
-1,09064
|
0,593
|
-0,52256
|
0,759
|
-0,27575
|
80
|
0,151
|
-1,89048
|
0,293
|
-1,22758
|
0,504
|
-0,68518
|
0,65
|
-0,43078
|
120
|
0,128
|
-2,05573
|
0,245
|
-1,4065
|
0,441
|
-0,81871
|
0,576
|
-0,55165
|
160
|
0,102
|
-2,28278
|
0,211
|
-1,5559
|
0,364
|
-1,0106
|
0,473
|
-0,74866
|
200
|
0,0864
|
-2,44877
|
0,173
|
-1,75446
|
0,32
|
-1,13943
|
0,4
|
-0,91629
|
240
|
0,0763
|
-2,57308
|
0,151
|
-1,89048
|
0,277
|
-1,28374
|
0,335
|
-1,09362
|
280
|
0,0629
|
-2,76621
|
0,123
|
-2,09557
|
0,221
|
-1,50959
|
0,288
|
-1,24479
|
320
|
0,0545
|
-2,90955
|
0,111
|
-2,19823
|
0,194
|
-1,6399
|
0,236
|
-1,44392
|
360
|
0,045
|
-3,10109
|
0,092
|
-2,38597
|
0,159
|
-1,83885
|
0,209
|
-1,56542
|
Кинетические кривые линиализовались в координатах lnCa – t
Вывод: порядок по веществу А первый (вещество А не занимает активные центры катализатора)
Предполагаемая кинетическая модель имеет вид:
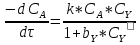
Определение порядка по веществу Y
|
CY0 = 5 моль/л
|
CY0 = 6 моль/л
|
|
CY0 = 8 моль/л
|
CY0 = 9 моль/л
|
τ
|
СА, моль/л
|
lnСA
|
СА, моль/л
|
lnСA
|
τ
|
СА, моль/л
|
lnСA
|
СА, моль/л
|
lnСA
|
0
|
0,2
|
-1,6094379
|
0,2
|
-1,6094379
|
0
|
0,2
|
-1,6094379
|
0,2
|
-1,6094379
|
50
|
0,182
|
-1,7037485
|
0,17
|
-1,7719568
|
40
|
0,172
|
-1,760260
|
0,169
|
-1,7778565
|
100
|
0,154
|
-1,8708026
|
0,147
|
-1,9173226
|
80
|
0,146
|
-1,9241486
|
0,146
|
-1,9241486
|
150
|
0,136
|
-1,9951003
|
0,126
|
-2,0714733
|
120
|
0,13
|
-2,0402208
|
0,126
|
-2,0714733
|
200
|
0,115
|
-2,1628231
|
0,109
|
-2,216407
|
160
|
0,11
|
-2,2072749
|
0,107
|
-2,2349264
|
250
|
0,1001
|
-2,3015855
|
0,0928
|
-2,3773086
|
200
|
0,0969
|
-2,3340757
|
0,0906
|
-2,4013010
|
300
|
0,0849
|
-2,4662811
|
0,0816
|
-2,5059260
|
240
|
0,0802
|
-2,5232317
|
0,076
|
-2,5770219
|
350
|
0,0769
|
-2,565249
|
0,0668
|
-2,706052
|
280
|
0,0698
|
-2,6621212
|
0,0673
|
-2,6985950
|
400
|
0,0693
|
-2,6693103
|
0,0564
|
-2,8752861
|
320
|
0,0633
|
-2,7598699
|
0,0588
|
-2,8336134
|
450
|
0,0583
|
-2,8421531
|
0,0484
|
-3,028255
|
360
|
0,0542
|
-2,9150743
|
0,0499
|
-2,9977342
|
kэф
|
CY0, моль/л
|
0
|
0
|
0,00277
|
5
|
0,00314
|
6
|
0,00364
|
8
|
0,00385
|
9
|
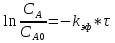
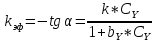
График зависимости kэф – Сy имеет нелинейный характер
Вывод: порядок по веществу У – дробно-линейный
Определение констант кинетической модели
1/kэф
|
1/CY0, л/моль
|
361,0108
|
0,2
|
318,4713
|
0,16666667
|
274,7253
|
0,125
|
259,7403
|
0,11111111
|
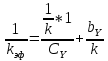
Точки легли на прямую
Вывод: кинетическая модель имеет вид:
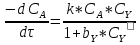
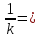 1128 1128
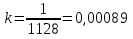
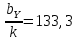
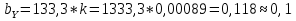 |
 Скачать 0.51 Mb.
Скачать 0.51 Mb.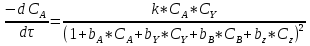




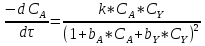
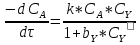
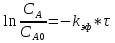
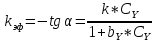
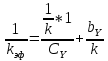
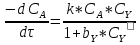
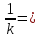 1128
1128