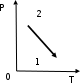Задание 2.. Задание 2 Ответить на вопросы
 Скачать 35.29 Kb. Скачать 35.29 Kb.
|
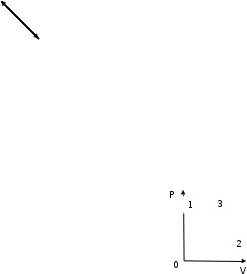
Задание 2Ответить на вопросыПереход некоторой массы газа из состояния 1 в состояние 3 состоит из двух процессов – адиабатического и изотермического (рис. 1). Какому из указанных процессов соответствует процесс 2 – 3 на диаграмме P – V.
Процесс 2 -- 3 является адиабатическим. В каком процессе тепло к системе подводится, температура системы не меняется? Ответ: Температура системы не изменяется в изотермических системах. При этом ΔT=0. Запишем первое начало термодинамики: Q = ΔU + A Но ΔU=0 (так как температура не изменяется), то подведенное тепло Q тратится на совершение системой работы А. Может ли теплоемкость газа быть отрицательной? Ответ: Теплоёмкостью тела С называется количество теплоты Q, необходимое для повышения температуры тела на 1К. По определению С=Q/ΔТ. Очевидно, что теплоёмкость газа может быть отрицательной, если работа, совершаемая газом, больше подводимого к газу тепла. В ходе такого процесса газ будет охлаждаться. Как с помощью молекулярно-кинетической теории объяснить тот факт, что жидкость имеет определенный объем? Ответ: Одним из характерных свойств жидкости является то, что она имеет определённый объём. Жидкость чрезвычайно трудно сжать механически, поскольку, в отличие от газа, между молекулами очень мало свободного пространства. Давление, производимое на жидкость, заключённую в сосуд, передаётся без изменения в каждую точку объёма этой жидкости Как зависит средняя длина свободного пробега молекул газа от давления при постоянной температуре? Ответ: В действительности все молекулы движутся, вследствие чего число соударений определяется средней скоростью движения молекул по отношению друг к другу, а не средней скоростью 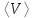 молекул относительно стенок сосуда: молекул относительно стенок сосуда: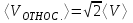 (1) (1)Поэтому среднее число соударений должно быть увеличено в 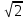 раз: раз: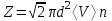 (2) (2) Из соотношений (1) и (2) получим для средней длины свободного пробега следующую формулу:  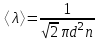 (3) (3)Из уравнения состояния идеального газа 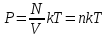 следует, что концентрация молекул газа равна 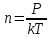 Тогда формулу (3) можно записать 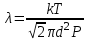 (4) (4)где k – постоянная Больцмана, Т – термодинамическая температура, Р – давление, d – эффективный диаметр молекул газа. Из формулы (4) видно, что при постоянной температуре с увеличением давления Р средняя длина свободного пробега молекул газа уменьшается. Что такое эффективный диаметр молекул. Чем оно определяется? Ответ: Эффективный диаметр молекулы — минимальное расстояние, на которое сближаются центры двух молекул при столкновении. Эффективный диаметр молекулы определяется ее размерами и углом между направлением ее движения и осью вращения. При наложении магнитного поля на парамагнитный газ его молекулы стремятся ориентироваться своими магнитными моментами по направлению поля; при этом возникает прецессия. Что означает выражение «внутренняя энергия системы является однозначной функцией ее состояния»? Ответ: Это означает, что изменение внутренней энергии при переходе из одного состояния в другое не зависит от пути перехода. Для некоторой массы газа m получена зависимость давления от абсолютной температуры (рис. 2). Сжимался или расширялся газ во время нагревания?
Ответ: Основной газовый закон PV=νRT перепишем в виде V=νRTP Из анализа графика следует, что отношение температуры к давлению остается постоянным. Имеем дело с изохорическим процессом, объем газа остаётся постоянным. |