Практическая работа Определение хлорида натрия методом аргентометрии. определение хлорида натрия методом аргентометрии. Занятие 32. Определение хлорида натрия в поваренной соли методом аргентометрии
 Скачать 39.48 Kb. Скачать 39.48 Kb.
|
|
Практическое занятие №32. Определение хлорида натрия в поваренной соли методом аргентометрии. Учебная цель: закрепить теоретические знания по теме «Титриметрический анализ». Образовательные результаты: Студент должен Уметь: - пользоваться лабораторным оборудованием; - выполнять задания согласно плану; - анализировать результаты проведенной работы, проводить вычисления и делать выводы; - фиксировать результаты выполненной работы согласно требованиям к ее оформлению. Знать: - особенности анализа веществ методом аргентометрии. Задачи практической работы: 1. Выполнить практическую работу; 2.Оформить отчёт по практической работе. Обеспеченность занятия (средства обучения): Ручка. Карандаш простой. Оборудование для проведения анализа: - натуральные образцы поваренной соли. - аналитические и технические весы. - электроплита, водяные бани. - колбы мерные (500 см3) и конические (100 см3). - химические стаканы, емкостью 200, 400, 500 см3. - лупа. - пипетки - стеклянные палочки. - фильтры. - сушильный шкаф (t=140-150оС) - фарфоровые ступки, тигель - держатель тигеля - воронки. - раствор фенолфталеина - серебро азотнокислое (0.1 н раствор). - калий хромовокислый (10%-ный раствор). Вопросы для закрепления теоретического материала к практической работе: На каком принципе основан аргентометрический метод анализа? Какие химические реактивы используются в анализе? Какова методика определения хлорида натрия в поваренной соли методом аргентометрии? Инструкция по выполнению практической работы: Внимательно изучить краткий теоретический материал. Изучить порядок выполнения задания. Методика анализа результатов, полученных в ходе практической работы: контролем является защита отчета по практическому занятию. Краткие теоретические и учебно-методические материалы по теме: Методы, применяемые для определения хлористого натрия, основаны на титровании иона хлора азотнокислым серебром (аргентометрический метод) либо нитратом закисной ртути (меркурометрический метод). Хлористый натрий извлекают водой, чаще непосредственно из навески испытуемого вещества или из обугленной навески продукта, если экстракт, получаемый первым способом, имеет темную окраску. Аргентометрический метод основан на следующем принципе: к нейтральному раствору хлорида прибавляют в качестве индикатора несколько капель хромовокислого калия и титруют раствором азотнокислого серебра. При этом образуется красный осадок хромовокислого серебра Этот осадок исчезает при взбалтывании, так как между хромовокислым серебром и хлористым натрием происходит обменное разложение и образуется нерастворимый осадок хлористого серебра 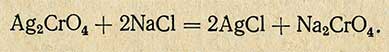 В момент превращения всего хлора в хлористое серебро жидкость, над осадком приобретает неисчезающую красноватую окраску, что указывает на конец реакции. Методика определения. Образец соли растирают в порошок в фарфоровой ступке. Навеску измельченного продукта 10г соли взвешивают на аналитических весах. Затем ее переносят через воронку в химический стакан емкостью 400 см3 , смывая частицы продукта дистиллированной водой, приливают 200 см3 дистиллированной воды, тщательно взбалтывают и ставят на кипящую водяную баню на 20 мин (случае анализа продуктов растительного происхождения). При анализе веществ, богатых крахмалом или белками, содержимое колбы выдерживают при 30° С в течение 30 мин при частом взбалтывании. Затем стакан охлаждают 10 минут и фильтруют раствор в мерную колбу емкостью 500 см3 через бумажный фильтр. 10 см3 фильтрата переносят в коническую колбу. Раствор разбавляют до 50 см3 дистиллированной водой, нейтрализуют 0,1 н. раствором щелочи в присутствии фенолфталеина. Туда же добавляют 2-3 капли 10%-ного раствора хромовокислого калия. Полученный раствор титруют раствором азотнокислого серебра при энергичном взбалтывании до момента перехода желто-белого цвета осадка в слабый красновато-бурый цвет, не исчезающий при дальнейшем перемешивании. Если водная вытяжка вещества интенсивно окрашена, то навеску исследуемого продукта берут в фарфоровый тигель и осторожно обугливают до тех пор, пока содержимое тигля не будет легко распадаться от надавливания стеклянной палочкой. Обугленное вещество охлаждают, количественно переносят через воронку в мерную колбу емкостью 250 мл, смывая тигель несколько раз дистиллированной водой. Колбу доливают до 3/4 объема горячей дистиллированной водой и выдерживают 15 мин в кипящей водяной бане при периодическом взбалтывании. После охлаждения содержимое колбы доводят дистиллированной водой до метки, перемешивают и фильтруют через складчатый фильтр в сухую колбу. 50 мл фильтрата переносят в коническую колбу, нейтрализуют и титруют так же, как указано выше. Содержание поваренной соли (в %) в обоих случаях рассчитывают по следующей формуле: 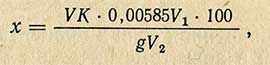 где V - количество мл 0,1 н. раствора азотнокислого серебра, пошедшего на титрование; К - коэффициент поправки к титру раствора азотнокислого серебра; 0,00585 - титр азотнокислого серебра, выраженный по хлористому натрию; V1 - объем вытяжки, приготовленной из навески, мл; g - навеска вещества, г; V2 - объем вытяжки, взятой для титрования, мл. Задания практической работы: Выполнить работу Оформить результаты в тетради. |
