бх гликолиз гликогеногенез. Анаэробном процессе
 Скачать 0.62 Mb. Скачать 0.62 Mb.
|
|
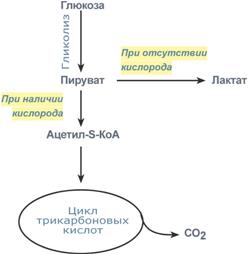
1. Характеристика процесса гликолиза (молочнокислое брожение) Бескислородное окисление глюкозы включает два этапа В анаэробном процессе пировиноградная кислота восстанавливается до молочной кислоты (лактата), поэтому в микробиологии анаэробный гликолиз называют молочнокислым брожением. Лактат далее ни во что не превращается, единственная возможность утилизовать лактат – это окислить его обратно в пируват. Многие клетки организма способны к анаэробному окислению глюкозы. Для эритроцитов он является единственным источником энергии. Клетки скелетной мускулатуры за счет бескислородного расщепления глюкозы способны выполнять мощную, быструю, интенсивную работу, как, например, бег на короткие дистанции, напряжение в силовых видах спорта. Вне физических нагрузок бескислородное окисление глюкозы в клетках усиливается при гипоксии – при различного рода анемиях, при нарушении кровообращения в тканях независимо от причины. Гликолиз Анаэробное превращение глюкозы локализуется в цитозоле и включает два этапа из 11 ферментативных реакций. Первый этап гликолиза  Первый этап гликолиза – подготовительный, здесь происходит затрата энергии АТФ, активация глюкозы и образование из нее триозофосфатов. Первая реакция гликолиза сводится к превращению глюкозы в реакционно-способное соединение за счет фосфорилирования 6-го, не включенного в кольцо, атома углерода. Эта реакция является первой в любом превращении глюкозы, катализируется гексокиназой. Вторая реакция необходима для выведения еще одного атома углерода из кольца для его последующего фосфорилирования (фермент глюкозофосфат-изомераза). В результате образуется фруктозо-6-фосфат. Третья реакция – фермент фосфофруктокиназа фосфорилирует фруктозо-6-фосфат с образованием почти симметричной молекулы фруктозо-1,6-дифосфата. Эта реакция является главной в регуляции скорости гликолиза. В четвертой реакции фруктозо-1,6-дифосфат разрезается пополам фруктозо-1,6-дифосфат-альдолазой с образованием двух фосфорилированных триоз-изомеров – альдозы глицеральдегида (ГАФ) и кетозы диоксиацетона (ДАФ). Пятая реакция подготовительного этапа – переход глицеральдегидфосфата и диоксиацетонфосфата друг в друга при участии триозофосфатизомеразы. Равновесие реакции сдвинуто в пользу диоксиацетонфосфата, его доля составляет 97%, доля глицеральдегидфосфата – 3%. Эта реакция, при всей ее простоте, определяет дальнейшую судьбу глюкозы: при нехватке энергии в клетке и активации окисления глюкозы диоксиацетонфосфат превращается в глицеральдегидфосфат, который далее окисляется на втором этапе гликолиза, при достаточном количестве АТФ, наоборот, глицеральдегидфосфат изомеризуется в диоксиацетонфосфат, и последний отправляется на синтез жиров. Второй этап гликолиза  Второй этап гликолиза – это освобождение энергии, содержащейся в глицеральдегидфосфате, и запасание ее в форме АТФ. Шестая реакция гликолиза (фермент глицеральдегидфосфат-дегидрогеназа) – окисление глицеральдегидфосфата и присоединение к нему фосфорной кислоты приводит к образованию макроэргического соединения 1,3-дифосфоглицериновой кислоты и НАДН. В седьмой реакции (фермент фосфоглицераткиназа) энергия фосфоэфирной связи, заключенная в 1,3-дифосфоглицерате тратится на образование АТФ. Реакция получила дополнительное название – реакция субстратного фосфорилирования, что уточняет источник энергии для получения макроэргической связи в АТФ (от субстрата реакции) в отличие от окислительного фосфорилирования (использование энергии электрохимического градиента ионов водорода на мембране митохондрий). Восьмая реакция – синтезированный в предыдущей реакции 3-фосфоглицерат под влиянием фосфоглицератмутазы изомеризуется в 2-фосфоглицерат. Девятая реакция – фермент енолазаотрывает молекулу воды от 2-фосфоглицериновой кислоты и приводит к образованию макроэргической фосфоэфирной связи в составе фосфоенолпирувата. Десятая реакция гликолиза – еще одна реакция субстратного фосфорилирования – заключается в переносе пируваткиназой макроэргического фосфата с фосфоенолпирувата на АДФ и образовании пировиноградной кислоты. Последняя реакция бескислородного окисления глюкозы, одиннадцатая – образование молочной кислоты из пирувата под действием лактатдегидрогеназы. Важно то, что эта реакция осуществляется только в анаэробных условиях. Эта реакция необходима клетке, так как НАДН, образующийся в 6-й реакции, в отсутствие кислорода не может окисляться в митохондриях. При наличии кислорода пировиноградная кислота переходит в митохондрию и превращается в ацетил-S-КоА. Анаэробный гликолиз - самодостаточный процессДля стабильного протекания гликолиза в бескислородных условиях необходимы ряд простых условий: поступление глюкозы, наличие минимальных количеств АТФ для активации процесса на первом этапе и АДФ как акцептора для фосфатов на втором этапе, пополнение запасов окисленного НАД для шестой реакции. Если первые два условия подразумеваются сами собой, то для решения третьего условия существует специальное решение: в анаэробных условиях образуемый в шестой, глицеральдегидфосфат-дегидрогеназной реакции, НАДН используется в одиннадцатой реакции для восстановления пирувата до лактата. Образуемый таким образом НАД опять возвращается в шестую реакцию. Следовательно, клетке не нужны дополнительные источники НАД и дополнительные способы уборки НАДН! Процесс поддерживается самостоятельно. Процесс циклического восстановления и окисления НАД в реакциях анаэробного окисления глюкозы получил название гликолитическая оксидоредукция. 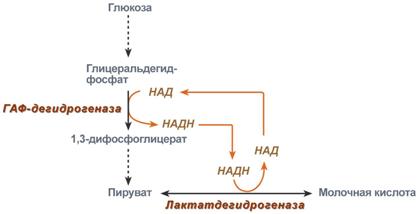 Схема гликолитической оксидоредукции НАД-НАДНВ аэробных условиях гликолитической оксидоредукции не происходит, НАДН отдает свои атомы водорода на челночные системы для их передачи в дыхательную цепь митохондрий. 2. Анаэробное окисление глюкозы. Судьба продуктов гликолиза в анаэробных условиях. Энергетический эффект окисления глюкозы и гликогена в анаэробных условиях. Для расчета количества АТФ, образованной при окислении глюкозы необходимо учитывать: Реакции, идущие с затратой или образованием АТФ и ГТФ, Реакции, продуцирующие НАДН и ФАДН2 и использующие их, Так как глюкоза образует две триозы, то все соединения, образующиеся ниже ГАФ-дегидрогеназной реакции, образуются в двойном (относительно глюкозы) количестве. Расчет АТФ при анаэробном окисленииНа подготовительном этапе на активацию глюкозы затрачивается 2 молекулы АТФ, фосфат каждой из которых оказывается на триозе – глицеральдегидфосфате и диоксиацетонфосфате. В следующий второй этап входят две молекулы глицеральдегидфосфата, каждая из которых окисляется до пирувата с образованием 2-х молекул АТФ в седьмой и десятой реакциях – реакциях субстратного фосфорилирования. Таким образом, суммируя, получаем, что на пути от глюкозы до пирувата в чистом виде образуется 2 молекулы АТФ. Однако надо иметь в виду и шестую, глицеральдегидфосфат-дегидрогеназную, реакцию, из которой выходит НАДН. Если условия анаэробные, то он используется в лактатдегидрогеназной реакции, где окисляется для образования лактата и в получении АТФ не участвует. 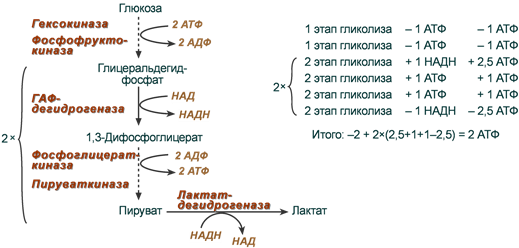 Расчет энергетического эффекта анаэробного окисления глюкозыАэробное окислениеЕсли в клетке имеется кислород, то НАДН из гликолиза направляется в митохондрию (челночные системы), на процессы окислительного фосфорилирования, и там его окисление приносит дивиденды в виде 2,5 молей АТФ. Образовавшийся в гликолизе пируват в аэробных условиях превращается в ПВК-дегидрогеназном комплексе в ацетил-S-КоА, при этом образуется 1 молекула НАДН. Ацетил-SКоА вовлекается в ЦТК и, окисляясь, дает 3 молекулы НАДН, 1 молекулу ФАДН2, 1 молекулу ГТФ. Молекулы НАДН и ФАДН2 движутся в дыхательную цепь, где при их окислении в сумме образуется 9 молекул АТФ. В целом при сгорании одной ацетогруппы в ЦТК образуется 10 молекул АТФ. 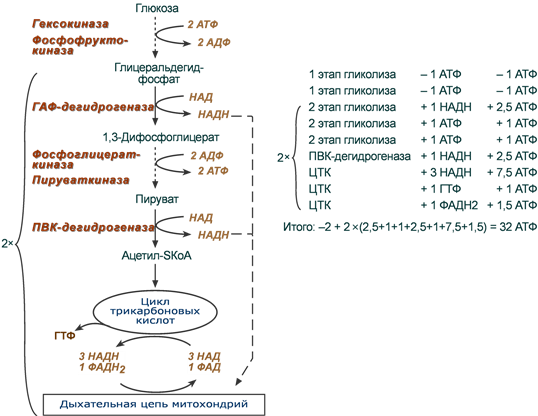 Расчет энергетического эффекта аэробного окисления глюкозыСуммируя результаты окисления "гликолитического" и "пируватдегидрогеназного" НАДН, "гликолитический" АТФ, энергетический выход ЦТК и умножая все на 2, получаем 32 молекулы АТФ. 3. Судьба продуктов гликолиза в аэробных условиях. Глицеролфосфатная и малат-аспартатная челночные системы. Энергетический выход аэробного окисления глюкозы. НАДН гликолиза могут доставляться в митохондрииМолекулы НАДН, образованные в шестой реакции гликолиза, в зависимости от наличия кислорода имеют, как минимум, два пути своего дальнейшего превращения: либо остаться в цитозоле и вступить в одиннадцатую реакцию гликолиза (анаэробные условия), либо проникнуть в митохондрию и окислиться в дыхательной цепи (аэробные условия). Челночные системыТак как сама молекула НАДН через мембрану не проходит, то существуют специальные системы, принимающие атомы водорода от НАДН в цитоплазме и отдающие их в матриксе митохондрий. Эти системы получили название челночные системы. Определены две основные челночные системы – глицеролфосфатная и малат-аспартатная. На основании наличия алкогольдегидрогеназы во многих тканях, в том числе и в нервной, дискутируется вопрос о существовании этанол-ацетальдегидной челночной системы, однако однозначных экспериментальных доказательств пока не получено. Глицеролфосфатный челночный механизмКлючевыми ферментами глицеролфосфатного челнока являются изоферменты глицерол-3-фосфат-дегидрогеназы – цитоплазматический и митохондриальный. Они отличаются своими коферментами: у цитоплазматической формы – НАД, у митохондриальной – ФАД. В цитозоле метаболиты гликолиза – диоксиацетонфосфат и НАДН образуют глицерол-3-фосфат, поступающий в митохондрии. Там он окисляется с образованием ФАДН2. Далее ФАДН2 направляется в дыхательную цепь и используется для получения энергии. Таким образом, в результате действий челнока цитозольный НАДН+H+как бы "превращается" в митохондриальный ФАДН2. В действительности цитозольный глицерол-3-фосфат не проникает в матрикс, так как митохондриальная глицерол-3-фосфат-дегидрогеназа  расположена на внешней стороне внутренней митохондриальной мембраны. Она обеспечивает перенос атомов водорода от глицерол-3-фосфата на ФАДН2 и дальнейшую передачу их на коэнзим Q дыхательной цепи. расположена на внешней стороне внутренней митохондриальной мембраны. Она обеспечивает перенос атомов водорода от глицерол-3-фосфата на ФАДН2 и дальнейшую передачу их на коэнзим Q дыхательной цепи. Схема работы глицерол-фосфатной челночной системыЭтот челнок активен в печени, в белых скелетных мышцах и в бурой жировой ткани. Однако в гепатоците в состоянии покоя и после еды часть глицерол-3 фосфата в митохондрию не пойдет, а будет использоваться в цитозоле для синтеза фосфолипидов и триацилглицеролов. Малат-аспартатный челночный механизмКлючевыми ферментами этого челнока являются изоферменты малатдегидрогеназы – цитоплазматический и митохондриальный. Он является распространенным по всем тканям. Этот механизм более сложен: постоянно идущие в цитоплазме при участии фермента аспартатаминотрансферазы (АСТ) реакции трансаминирования аспарагиновой кислоты с α-кетоглутаратом поставляют оксалоацетат, который под действием цитозольного пула малатдегидрогеназы и за счет "гликолитического" НАДН восстанавливается до яблочной кислоты (малата). Последняя антипортом с α-кетоглутаратом проникает в митохондрии и, являясь метаболитом ЦТК, окисляется в оксалоацетат с образованием НАДН. Так как мембрана митохондрий непроницаема для оксалоацетата, то он при помощи аспартатаминотрансферазы трансаминируется до аспарагиновой кислоты, которая в обмен на глутамат выходит в цитозоль. Таким образом, атомы водорода от цитозольного НАДН перемещаются в состав митохондриального НАДН. 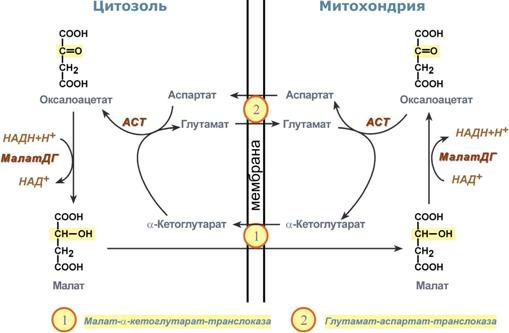 Схема работы малат-аспартатной челночной системыАэробное окислениеЕсли в клетке имеется кислород, то НАДН из гликолиза направляется в митохондрию (челночные системы), на процессы окислительного фосфорилирования, и там его окисление приносит дивиденды в виде 2,5 молей АТФ. Образовавшийся в гликолизе пируват в аэробных условиях превращается в ПВК-дегидрогеназном комплексе в ацетил-S-КоА, при этом образуется 1 молекула НАДН. Ацетил-SКоА вовлекается в ЦТК и, окисляясь, дает 3 молекулы НАДН, 1 молекулу ФАДН2, 1 молекулу ГТФ. Молекулы НАДН и ФАДН2 движутся в дыхательную цепь, где при их окислении в сумме образуется 9 молекул АТФ. В целом при сгорании одной ацетогруппы в ЦТК образуется 10 молекул АТФ. 4. Этапы аэробного окисления глюкозы. Суммарное уравнение аэробного распада глюкозы. Какие преимущества дает клетке ее аэробное окисление? В чем заключается эффект Пастера и каков его биохимический механизм? Глюкоза – это субстрат для получения энергииЭнергетика любой клетки нашего организма основана на окислении глюкозы. Окисление глюкозы происходит по двум направлениям:
Окисление с образованием пентоз: рибозы, рибулозы, ксилулозы. Этот путь называется пентозофосфатный шунт и не связан с получением энергии Окисление с получением энергии. Второй путь, т.е. тот по которому глюкоза окисляется для получения энергии, называется гликолиз (греч. glykos — сладкий и греч. lysis — растворение). Конечным продуктом гликолиза является пировиноградная кислота (пируват). В зависимости от дальнейшей судьбы пирувата различают аэробное и анаэробное окисление глюкозы. Целью обоих типов окисления является получение АТФ. В аэробном процессе пировиноградная кислота превращается в ацетил-SКоА (реакции ПВК-дегидрогеназы) и далее сгорает в реакциях цикла трикарбоновых кислот до СО2 (реакции ЦТК). Общее уравнение аэробного окисления глюкозы: C6H12O6 + 6 O2 + 32 АДФ + 32 Фнеорг → 6 CO2 + 44 H2О + 32 АТФ В анаэробном процессе пировиноградная кислота восстанавливается до молочной кислоты (лактата). Лактат является метаболическим тупиком и далее ни во что не превращается, единственная возможность утилизовать лактат – это окислить его обратно в пируват. В микробиологии анаэробный гликолиз называют молочнокислым брожением. Суммарное уравнение анаэробного гликолиза имеет вид: C6H12O6 + 2 АДФ + 2 Фнеорг → 2 Лактат + 2 H2O + 2 АТФ Глюкоза – это источник оксалоацетатаПосле того как пируват синтезировался, он необязательно превращается в ацетил-SКоА или молочную кислоту. Существенное значение имеет его способность карбоксилироваться в оксалоацетат, особенно эта реакция активна в печени. Наличие избытка оксалоацетата "подталкивает" реакции цикла трикарбоновых кислот (доступность субстрата), ускоряет связывание ацетильной группы, ее окисление и производство энергии. При голодании отсутствие глюкозы в клетках и активация глюконеогенеза в гепатоцитах, ухудшение окисления глюкозы до пирувата при сахарном диабете влечет за собой недостаточное количество оксалоацетата. Это сопровождается гипоэнергетическим состоянием клетки и активацией синтеза кетоновых тел в печени. Аэробное окисление глюкозы включает реакции гликолиза и последующее окисление пирувата в цикле Кребса и дыхательной цепи до СО2 и Н2О. При аэробных условиях пируват проникает в митохондрии, где полностью окисляется до СО2 и Н2О. Если содержание кислороданедостаточно, как это может иметь место в активно сокращающейся мышце, пируват превращается в лактат. В процессе гликолиза образуется АТФ. Суммарное уравнение гликолиза можно представить следующим образом: Эффект Пастера  Эффект Пастера - это снижение потребления глюкозы и прекращение продукции молочной кислоты клеткой в присутствии кислорода. Биохимическая основа эффекта заключается в конкуренции за субстрат между пируватдегидрогеназой, превращающей пируват в ацетил-S-КоА, и лактатдегидрогеназой, превращающей пируват в лактат. У пируватдегидрогеназы сродство гораздо выше и в обычных аэробных условиях она окисляет большую часть пировиноградной кислоты. Как только поступление кислорода уменьшается (анемии, нарушение кровообращения, спазм сосудов, тромбозы и т.п.) происходит следующее: внутримитохондриальные процессы дыхания не идут и НАДН в дыхательной цепи не окисляется, моментально накапливающийся в митохондриях НАДН тормозит цикл трикарбоновых кислот, ацетил-S-КоА не входит в ЦТК и вместе с НАДН ингибирует ПВК-дегидрогеназу. В этой ситуации пировиноградной кислоте не остается ничего иного как превращаться в молочную. При наличии кислорода ингибирование ПВК-дегидрогеназы прекращается и она, обладая большим сродством к пирувату, выигрывает конкуренцию. Отличной иллюстрацией к сказанному служит чувствительность миокарда и нейронов к недостатку кислорода: Роль лактатдегидрогеназы в клетке В норме работу клеток нервной системы и миокарда при аэробных условиях обеспечивает большое количество митохондрий и поступление из крови субстратов для окисления – глюкозы, кетоновых тел, жирных кислот (только для миокарда), лактата, превращегося в пируват. 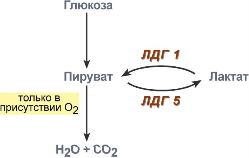 В основе высокой чувствительности этих органов к отсутствию кислорода лежит отличие изоферментов лактатдегидрогеназы друг от друга. Рассмотрим это на прмиере ЛДГ-1 и ЛДГ-5. В основе высокой чувствительности этих органов к отсутствию кислорода лежит отличие изоферментов лактатдегидрогеназы друг от друга. Рассмотрим это на прмиере ЛДГ-1 и ЛДГ-5.Сердечный изофермент ЛДГ-1, обладая высоким сродством к молочной кислоте, переводит ее в пировиноградную, "стремясь" поднять концентрацию пирувата с целью его включения в цикл трикарбоновых кислот (только в аэробных условиях) и получения энергии для сокращения миокардиоцита. Поэтому миокард не образует лактат, но зато может использовать его для получения энергии, захватывая из крови, но только в аэробных условиях. Аналогично лактат используется нервной системой. При нехватке кислорода свойства изофермента ЛДГ-1 не изменятся, он по-прежнему будет сдвигать реакцию в сторону продукции пировиноградной кислоты (на схеме "справа-налево"). Однако без кислорода "сгореть" в ЦТК пируват не может и выйти из клетки тоже не может, т.к. клеточные мембраны непроницаемы для него. Являясь кислотой, он закисляет цитозоль, изменяя активность ферментов и, возможно, как-то еще проявляет токсичность. Таким образом, происходят необратимые повреждения кардиомиоцита и нейрона – развивается инфаркт миокарда. или ишемический инсульт. В тоже время изофермент скелетной мышцы ЛДГ-5 обладает высоким сродством к пирувату, при отсутствии кислорода в клетке быстро и эффективно превращает его в молочную кислоту, обратная же реакция практически не идет. Закисление саркоплазмы снижает работоспособность миоцита. Мышца, хоть и не в состоянии работать в таких условиях, все-таки сохраняет жизнеспособность. Но в клетке молочная кислота не накапливается – она легко проходит через клеточные мембраны и быстро удаляется из мышцы. После "отключки" скелетная мышца вновь становится работоспособной через несколько минут. Таким образом, в анаэробных условиях сильнее всего будут страдать сердечная мышца и нервная система, что, собственно говоря, и наблюдается в медицинской практике. 5. Характеристика процесса глюконеогенеза Глюконеогенез – это синтез глюкозы из неуглеводных компонентов: лактата, пирувата, глицерола, кетокислот цикла Кребса и других кетокислот, из аминокислот. Все аминокислоты, кроме кетогенных лейцина и лизина, способны участвовать в синтезе глюкозы. Углеродные атомы некоторых из них (глюкогенных) полностью включаются в молекулу глюкозы, некоторых (смешанных) частично. Кроме получения глюкозы, глюконеогенез обеспечивает и уборку лактата, постоянно образуемого в эритроцитах или при мышечной работе, и глицерола, являющегося продуктом липолиза в жировой ткани. Как известно, в гликолизе существуют три необратимые реакции: пируваткиназная (десятая), фосфофруктокиназная (третья) и гексокиназная (первая). В этих реакциях происходит высвобождение энергии для синтеза АТФ. Поэтому в обратном процессе возникают энергетические барьеры, которые клетка обходит с помощью дополнительных реакций. Глюконеогенез включает все обратимые реакции гликолиза, и особые обходные пути, т.е. он не полностью повторяет реакции окисления глюкозы. Его реакции способны идти во всех тканях, кроме последней глюкозо-6-фосфатазной реакции, которая идет только в печени и почках. Поэтому, строго говоря, глюконеогенез идет только в этих двух органах. Обход десятой реакции гликолизаНа этом этапе глюконеогенеза работают два ключевых фермента – в митохондриях пируваткарбоксилаза и в цитозоле фосфоенолпируват-карбоксикиназа, при этом в реакциях тратятся два макроэрга - АТФ и ГТФ. В химическом плане обходной путь десятой реакции выглядит достаточно просто:  Упрощенный вариант написания обхода десятой реакции гликолизаОднако дело в том, что пируваткарбоксилаза находится в митохондрии, а фосфоенолпируват-карбоксикиназа – в цитозоле. Дополняет проблему непроницаемость митохондриальной мембраны для оксалоацетата. Зато через мембрану может пройти малат, предшественник оксалоацетата по ЦТК. Поэтому в реальности все выглядит более сложно: 1. В цитозоле пировиноградная кислота может появиться при окислении молочной кислоты и в реакции трансаминированияаланина. После этого пируват симпортом с ионами Н+, движущимися по протонному градиенту, проникает в митохондрии. В митохондриях пируваткарбоксилаза превращает пировиноградную кислоту в оксалоацетат. Пируваткарбоксилазная реакция идет в клетке постоянно, так как оксалоацетат является главным регулятором скорости ЦТК. Реакция называется анаплеротической (пополняющей) реакцией ЦТК. 2. Далее оксалоацетат мог бы превратиться в фосфоенолпируват, но для этого сначала он должен попасть в цитозоль. Поэтому происходит реакция восстановления оксалоацетата в малат при участии малатдегидрогеназы. В результате малат накапливается, выходит в цитозоль и здесь превращается обратно в оксалоацетат. Повернуть малатдегидрогеназную реакцию ЦТК вспять позволяет избыток НАДН в митохондриях. НАДН поступает из β-окисления жирных кислот, активируемого в гепатоците при голодании. 3. В цитоплазме фосфоенолпируват-карбоксикиназа осуществляет превращение оксалоацетата в фосфоенолпируват, для реакции требуется энергия ГТФ. От молекулы отщепляется тот же углерод, что и присоединяется. 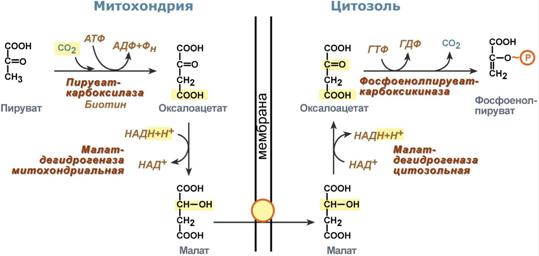 Обход десятой реакции гликолизаОбход третьей реакции гликолизаВторое препятствие на пути синтеза глюкозы – фосфофруктокиназная реакция – преодолевается с помощью фермента фруктозо-1,6-дифосфатазы. Этот фермент есть в почках, печени, поперечно-полосатых мышцах. Таким образом, эти ткани способны синтезировать фруктозо-6-фосфат и глюкозо-6-фосфат.  Обход третьей реакции гликолизаОбход первой реакции гликолизаПоследняя реакция катализируется глюкозо-6-фосфатазой. Она имеется только в печени и почках, следовательно, только эти ткани могут продуцировать свободную глюкозу.  Обход первой реакции гликолиза Обход первой реакции гликолизаКак вещества включаются в глюконеогенез?Синтез глюкозы из молочной кислотыПри физической нагрузке в мышцах продуцируется большое количество молочной кислоты, особенно если нагрузка интенсивная, максимальной мощности.Также молочная кислота непрерывно образуется эритроцитами, независимо от состояния организма. С током крови она поступает в гепатоцит и здесь превращается в пируват. Далее реакции идут по классической схеме. Суммарная реакция глюконеогенеза из молочной кислоты: Лактат + 4АТФ + 2ГТФ + 2H2O → Глюкоза + 4АДФ + 2ГДФ + 6Фн Синтез глюкозы из аминокислотРяд аминокислот являются глюкогенными, то есть их углеродные скелеты в той или иной степени способны включаться в состав глюкозы. Такими является большинство аминокислот, кроме лейцина и лизина, атомы углерода которых никогда не участвуют в синтезе углеводов. В качестве примера синтеза глюкозы из аминокислот рассмотрим участие в этом процессе глутамата, аспартата, серина и аланина. Аспарагиновая кислота (после реакции трансаминирования) и глутаминовая кислота (после дезаминирования) превращаются в метаболиты ЦТК, соответственно, в оксалоацетат и α-кетоглутарат. Аланин, трансаминируясь, образует пировиноградную кислоту, которая способна карбоксилироваться до оксалоацетата. Оксалоацетат, являясь первым элементом в процессе глюконеогенеза, далее включается в синтез глюкозы. Серин в трехступенчатой реакции под воздействием сериндегидратазы теряет аминогруппу и превращается в пируват, который вступает в глюконеогенез. 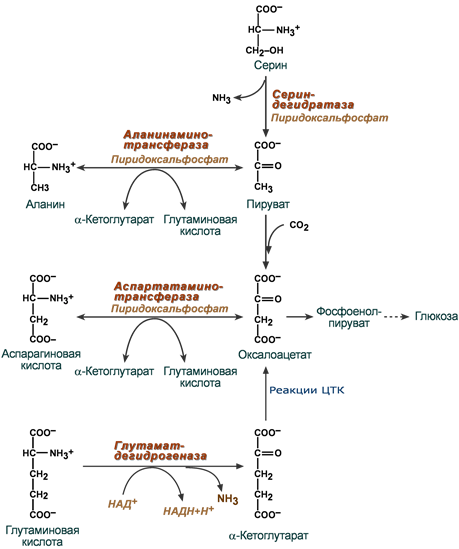 Включение аминокислот в синтез глюкозыСинтез глюкозы из глицеринаПри физической нагрузке под влиянием адреналина или при голодании под влиянием глюкагона и кортизола в адипоцитах активно происходит распад триацилглицеролов (липолиз). Одним из продуктов этого процесса является спирт глицерин, который поступает в печень. Здесь он фосфорилируется, окисляется до диоксиацетонфосфата и вовлекается в реакции глюконеогенеза. 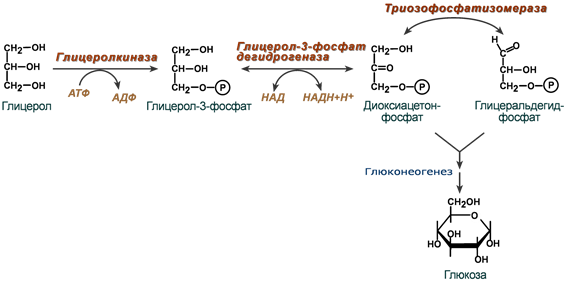 Включение глицерина в синтез глюкозыЭнергетический баланс глюконеогенезаВреакциях глюконеогенеза разрывается 6 макроэргических фосфатных связей связей в 4 молекулах АТФ и 2 молекулах ГТФ. Для синтеза 1 молекулы глюкозы необходимы 2 молекулы пирувата. Запишем суммарное уравнение глюконеогенеза: 2 Пируват + 2NADH + 4H+ + 4АТФ + 2ГТФ + 6H2O → Глюкоза + 2NAD+ + 4АДФ + 2ГДФ + 6Фн На карбоксилирование 2 молекул пирувата затрачивается 2 молекулы АТФ. Далее 2 молекулы ГТФ требуются для образования фосфоенолпирувата из оксалоацетата. И ещё 2 молекулы АТФ необходимы для фосфорилирования 2 молекул 3-фосфо- глицерата до 1,3-бисфосфоглицерата. Энергия восстановительных эквивалентов (NADH) нужна для образования глицеральдегид-3-фосфата. При голодании глюконеогенез обеспечивается энергией с помощью β-окисле- ния жирных кислот. Если привести все энергоносители к одному знаменателю (АТФ), то мы получим, что в ходе глюконеогенеза затрачивается: 1.4 молекулы АТФ и 2 молекулы ГТФ (эквивалентны 2 молекулам АТФ); 2.2 молекулы NADH (эквивалентны 6 молекулам АТФ). Суммируем все затраты и получаем: 4 АТФ + 2 АТФ + 6 АТФ = 12 АТФ Итак, в ходе глюконеогенеза затрачивается 12 молекул АТФ. 6. Роль гликолиза и глюконеогенеза в метаболизме плода и новорожденных. Гликолиз и глюконеогенез дополняют друг другаТак как синтез и окисление глюкозы являются крайне важными для существования клетки (гликолиз) и всего организма (глюконеогенез), то регуляция этих процессов отвечает запросам органов и тканей при различных условиях. Поскольку гликолитическое окисление глюкозы является способом получения энергии в аэробных и анаэробных условиях, то оно непрерывно происходит во всех клетках и, конечно, должно и будет активировано при усилении работы клетки, например, сокращение миоцита, движение нейтрофилов; служит источником глицерола и ацетил-SКоА, используемых для синтеза жиров в гепатоцитах и адипоцитах, то такое окисление активируется при избытке глюкозы в этих клетках. Глюконеогенез, как образование глюкозы в печени из неуглеводных источников, необходим: при гипогликемии во время мышечной нагрузки – синтез глюкозы из молочной кислоты, поступающей из работающих мышц, и из глицерола, образующегося при мобилизации жиров; при гипогликемии при кратком голодании (до 24 часов) – синтез преимущественно из молочной кислоты, непрерывно поступающей в печень из эритроцитов, при гипогликемии при длительном голодании – в основном синтез из аминокислот, образующихся при катаболизме белков, и также из молочной кислоты и глицерина. Таким образом, глюконеогенез, идущий в печени, обеспечивает глюкозой все остальные клетки и органы (эритроциты, нервная ткань, мышцы и др.), в которых активны процессы, требующие глюкозу. Поступление глюкозы в эти клетки также необходимо, чтобы поддержать концентрацию оксалоацетата и обеспечить сгорание в ЦТК ацетил-SКоА, получаемого из жирных кислот или кетоновых тел. В целом можно выделить два способа регуляции гликолиза и глюконеогенеза: гормональная при участии гормонов и метаболическая, т.е. при помощи промежуточных или конечных продуктов обмена глюкозы. Существуют три основных участка, на которых происходит регуляция этих процессов: первая реакция гликолиза, третья реакция гликолиза и обратимая ей, десятая реакция гликолиза и обратимые ей. Регуляция глюконеогенезаГормональная активация глюконеогенеза осуществляется глюкокортикоидами, которые увеличивают синтез пируваткарбоксилазы, фосфоенолпируват-карбоксикиназы, фруктозо-1,6-дифосфатазы. Глюкагон стимулирует те же самые ферменты через аденилатциклазный механизм путем фосфорилирования. Энергия для глюконеогенеза поступает от β-окисления жирных кислот. Конечный продукт этого окисления, ацетил-SКоА аллостерически стимулирует активность первого фермента глюконеогенеза – пируваткарбоксилазы. Кроме этого, фруктозо-1,6-дифосфатаза стимулируется при участии АТФ. 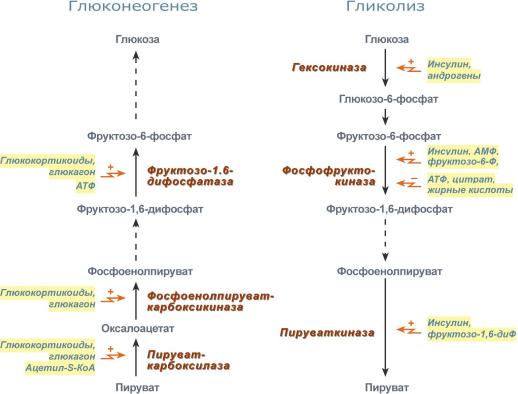 Гормональные и метаболические факторы, регулирующие гликолиз и глюконеогенезРегуляция гликолизаГормональная регуляцияВ печени гликолиз стимулируется инсулином, повышающим количество ключевых ферментов гликолиза (гексокиназы, фосфофруктокиназы, пируваткиназы). В печени активность глюкокиназы, кроме инсулина, регулируется другими гормонами: активацию вызывает андрогены, подавляют ее активность глюкокортикоиды и эстрогены. В других тканях активность гексокиназ повышается тиреоидными гормонами, снижается – глюкокортикоидами и соматотропином. Метаболическая регуляцияГексокиназа непеченочных клеток ингибируется продуктом собственной реакции – глюкозо-6-фосфатом. Фосфофруктокиназа: активируется АМФ и собственным субстратом (фруктозо-6-фосфат), ингибируется – АТФ, лимонной кислотой, жирными кислотами. Пируваткиназа активируется фруктозо-1,6-дифосфатом (прямая положительная регуляция). Молекулы АМФ, стимулирующие гликолиз, образуются в аденилаткиназной реакции, активируемой при появлении избытка АДФ. Особенно ярко значение такой регуляции проявляется при мышечной работе: АДФ + АДФ ↔ АТФ + АМФ 7. Реципрокная регуляция гликолиза и глюконеогенеза: Регуляция гликолизаГормональная регуляцияВ печени гликолиз стимулируется инсулином, повышающим количество ключевых ферментов гликолиза (гексокиназы, фосфофруктокиназы, пируваткиназы). В печени активность глюкокиназы, кроме инсулина, регулируется другими гормонами: активацию вызывает андрогены, подавляют ее активность глюкокортикоиды и эстрогены. В других тканях активность гексокиназ повышается тиреоидными гормонами, снижается – глюкокортикоидами и соматотропином. Метаболическая регуляцияГексокиназа непеченочных клеток ингибируется продуктом собственной реакции – глюкозо-6-фосфатом. Фосфофруктокиназа: активируется АМФ и собственным субстратом (фруктозо-6-фосфат), ингибируется – АТФ, лимонной кислотой, жирными кислотами. Пируваткиназа активируется фруктозо-1,6-дифосфатом (прямая положительная регуляция). Молекулы АМФ, стимулирующие гликолиз, образуются в аденилаткиназной реакции, активируемой при появлении избытка АДФ. Особенно ярко значение такой регуляции проявляется при мышечной работе: АДФ + АДФ ↔ АТФ + АМФ РЕГУЛЯЦИЯ ГЛИКОЛИЗА И ГЛЮКОНЕОГЕНЕЗАВцелом можно выделить два способа регуляции гликолиза и глюконеогенеза: гормональная и метаболическая, т.е. при помощи промежуточных или конечных продуктов обмена глюкозы. Существуют три основных участка, на которых происходит регуляция: o первая реакция гликолиза, o третья реакция гликолиза и обратимая ей, o десятая реакция гликолиза и обратимые ей. Регуляция глюконеогенезаГормональная активация глюконеогенеза осуществляется глюкокортикоидами, кото- рые увеличивают синтез пируват-карбоксилазы, фосфоенолпируваткарбоксикиназы, фруктозо-1,6-дифосфатазы. Глюкагон стимулирует те же самые ферменты через аденилатциклазный механизм путем фосфорилирования. Кроме гормонов, имеются метаболическая регуляция, при которой аллостерически активируется пируваткарбоксилаза при помощи ацетил-S-КоА, фруктозо-1,6-дифосфатаза при участии АТФ. Регуляция гликолизаГликолиз стимулируется инсулином, повышающим количество молекул гексокиназы, фосфофруктокиназы, пируваткиназы. В печени активность глюкокиназы регулируется гормонами: активацию вызывает инсулин и андрогены, подавляют ее активность глюкокортикоиды и эстрогены. К метаболической регуляции наиболее чувствительна фосфофруктокиназа. Она активируется АМФ и собственным субстратом, ингибируется – АТФ, лимонной кислотой, жирными кислотами. Пируваткиназа активируется фруктозо-1,6-дифосфатом. Гексокиназа клеток (кроме гепатоцитов) ингибируется продуктом собственной реакции – глюкозо-6- фосфатом. 8. Глюкозо-лактатный цикл (цикл Кори), его значение при физической работе. Источники молочной кислоты в организме. люкозо-лактатный цикл (цикл Кори)Глюкозо-лактатный цикл – это циклический процесс, объединяющий реакции глюконеогенеза и реакции анаэробного гликолиза. Глюконеогенез происходит в печени, субстратом для синтеза глюкозы является лактат, поступающий в основном из эритроцитов или мышечной ткани. В эритроцитах молочная кислота образуется непрерывно, так как для них анаэробный гликолиз является единственным способом образования энергии. В скелетных мышцах высокое накопление молочной кислоты (лактата) является следствием гликолиза при очень интенсивной, субмаксимальной мощности, работе, при этом внутриклеточный рН снижается до 6,3-6,5. Но даже при работе низкой и средней интенсивности в скелетной мышце всегда образуется некоторое количество лактата. Убрать молочную кислоту можно только одним способом – превратить ее в пировиноградную кислоту. Однако сама мышечная клетка ни при работе, ни во время отдыха не способна превратить лактат в пируват из-за особенностей изофермента лактатдегидрогеназы-5. Зато клеточная мембрана высоко проницаема для лактата и он движется по градиенту концентрации наружу. Поэтому во время и после нагрузки (при восстановлении) лактат легко удаляется из мышцы. Это происходит довольно быстро, всего через 0,5-1,5 часа в мышце лактата уже нет. Малая часть молочной кислоты выводится с мочой. Большая часть лактата крови захватывается гепатоцитами, окисляется в пировиноградную кислоту и вступает на путь глюконеогенеза. Глюкоза, образованная в печени, используется самим гепатоцитом или возвращается обратно в мышцы, восстанавливая во время отдыха запасы гликогена. Также она может распределиться по другим органам.  Глюкозо-лактатный (выделен желтым) и глюкозо-аланиновый циклы9. Глюкозо-аланиновый цикл, его значение при физической работе и голодании. Глюкозо-аланиновый циклЦелью глюкозо-аланинового цикла также является уборка пирувата, но кроме этого решается еще одна немаловажная задача – доставкааминного азота из мышцы в печень. При мышечной работе и в покое в миоците распадаются белки и образуемые аминокислоты трансаминируются с α-кетоглутаратом и полученный глутамат взаимодействует с пируватом. Образующийся аланин является транспортной формой аминного (аминокислотного) азота и пирувата из мышцы в печень. В гепатоците идет обратная реакция трансаминирования, аминогруппа через глутамат передается на синтез мочевины, пируват используется для синтеза глюкозы. Кроме мышечной работы, глюкозо-аланиновый цикл активируется во время голодания, когда белки мышц и других тканей распадаются и многие аминокислоты используются в качестве источника энергии, а их азот необходимо доставить в печень. 10. Особенности метаболизма глюкозы в печени, мозге, скелетных мышцах, жировой ткани, эритроцитах. Метаболизм глюкозы в эритроцитах. Эритроциты лишены митохондрий, поэтому в качестве энергетического материала они могут использовать только глюкозу. В эритроцитах катаболизм глюкозы обеспечивает сохранение структуры и функции гемоглобина, целостность мембран и образование энергии для работы ионных насосов. Глюкоза поступает в эритроциты путём облегчённой диффузии с помощью ГЛЮТ-2. Около 90% поступающей глюкозы используется в анаэробном гликолизе, а остальные 10% - в пентозофосфатном пути. Конечный продукт анаэробного гликолиза лактат выходит в плазму крови и используется в других клетках, прежде всего гепатоцитах. АТФ, образующийся в анаэробном гликолизе, обеспечивает работу Nа+, К+-АТФ-азы и поддержание самого гликолиза, требующего затраты АТФ в гексокиназной и фосфофруктокиназной реакциях. Важная особенность анаэробного гликолиза в эритроцитах по сравнению с другими клетками - присутствие в них фермента бисфосфоглицератмутазы. Бисфосфоглицератмутаза катализирует образование 2,3-бисфосфоглицерата из 1,3-бисфосфоглицерата. Образующийся только в эритроцитах 2,3-бисфосфоглицерат служит важным аллостерическим регулятором связывания кислорода гемоглобином. Глюкоза в эритроцитах используется и в пентозофосфатном пути, окислительный этап которого обеспечивает образование кофермента NADPH, необходимого для восстановления глу-татиона. Метаболизм глюкозы в печени. Основная роль печени в углеводном обмене заключается в обеспечении постоянства концентрации глюкозы в крови. Это достигается регуляцией между синтезом и распадом гликогена, депонируемого в печени. В печени синтез гликогена и его регуляция в основном аналогичны тем процессам, которые протекают в других органах и тканях, в частности в мышечной ткани. Синтез гликогена из глюкозы обеспечивает в норме временный резерв углеводов, необходимый для поддержания концентрации глюкозы в крови в тех случаях, если ее содержание значительно уменьшается (например, у человека это происходит при недостаточном поступлении углеводов с пищей или в период ночного «голодания»). Необходимо подчеркнуть важную роль фермента глюкокиназы в процессе утилизации глюкозы печенью. Глюкокиназа, подобногексокиназе, катализирует фосфорилирование глюкозы с образованием глюкозо-6-фосфата, при этом активность глюкокиназы в печенипочти в 10 раз превышает активность гексокиназы. Важное различие между этими двумя ферментами заключается в том, что глюкокиназа в противоположность гексокиназе имеет высокое значение КМ для глюкозы и не ингибируется глюкозо-6-фосфатом. Считают, что основная роль печени – расщепление глюкозы – сводится прежде всего к запасанию метаболитов-предшественников, необходимых для биосинтеза жирных кислот и глицерина, и в меньшей степени к окислению ее до СО2 и Н2О. Синтезированные впечени триглицериды в норме выделяются в кровь в составе липопротеинов и транспортируются в жировую ткань для более «постоянного» хранения. В реакциях пентозофосфатного пути в печени образуется НАДФН, используемый для восстановительных реакций в процессах синтезажирных кислот, холестерина и других стероидов. Кроме того, при этом образуются пентозофосфаты, необходимые для синтезануклеиновых кислот. Наряду с утилизацией глюкозы в печени происходит и ее образование. Непосредственным источником глюкозы в печени служитгликоген. Распад гликогена в печени происходит в основном фосфоролитическим путем. В регуляции скорости гликогенолиза в печенибольшое значение имеет система циклических нуклеотидов. Кроме того, глюкоза в печени образуется также в процессе глюконеогенеза. Метаболизм глюкозы в мозгу. Основным субстратом дыхания мозговой ткани является глюкоза. В 1 мин 100 г ткани мозга потребляют в среднем 5 мг глюкозы. Подсчитано, что более 90% утилизируемой глюкозы в ткани мозга окисляется до СО2 и Н2О при участии цикла трикарбоновых кислот. В физиологических условиях роль пентозофосфатного пути окисления глюкозы в мозговой ткани невелика, однако этот путь окисленияглюкозы присущ всем клеткам головного мозга. Образующаяся в процессе пентозофосфатного цикла восстановленная форма НАДФ (НАДФН) используется для синтеза жирных кислот и стероидов. Между глюкозой и гликогеном мозговой ткани имеется тесная связь, выражающаяся в том, что при недостаточном поступлении глюкозыиз крови гликоген головного мозга является источником глюкозы, а глюкоза при ее избытке – исходным материалом для синтеза гликогена. Распад гликогена в мозговой ткани происходит путем фосфоролиза с участием системы цАМФ. Однако в целом использование гликогена в мозге по сравнению с глюкозой не играет существенной роли в энергетическом отношении, так как содержание гликогена в головном мозге невелико. Наряду с аэробным метаболизмом углеводов мозговая ткань способна к довольно интенсивному анаэробному гликолизу. Значение этого явления пока недостаточно ясно, ибо гликолиз как источник энергии ни в коей мере не может сравниться по эффективности с тканевым дыханием в головном мозге. Метаболизм глюкозы в мышцах. При работе умеренной интенсивности мышца может покрывать свои энергетические затраты за счет аэробного метаболизма. Однако при больших нагрузках, когда возможность снабжения кислородом отстает от потребности в нем, мышца вынуждена использовать гликолитический путь снабжения энергией. При интенсивной мышечной работе скорость расщепления гликогена или глюкозы с образованием молочной кислоты увеличивается в сотни раз. Соответственно содержание молочной кислоты в мышечной ткани может повышаться до 1,0–1,2 г/кг и более. С током крови значительное количество молочной кислоты поступает в печень, где ресинтезируется в глюкозу и гликоген (глюконеогенез) за счет энергии окислительных процессов. Метаболизм глюкозы в жировой ткани. В адипоцитах для обеспечения реакций синтеза жира распад глюкозы идёт по двум путям: гликолиз, обеспечивающий образование глицерол-3-фосфата и ацетил-КоА, и пентозофосфатный путь, окислительные реакции которого обеспечивают образование NADPH, служащего донором водорода в реакциях синтеза жирных кислот. |