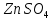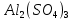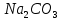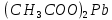Гидролиз. Гидролиз,Ортикова. Исследование гидролиза солей
 Скачать 40.07 Kb. Скачать 40.07 Kb.
|
|
ПЕРВОЕ ВЫСШЕЕ ТЕХНИЧЕСКОЕ УЧЕБНОЕ ЗАВЕДЕНИЕ РОССИИ  МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ федеральное государственное бюджетное образовательное учреждение высшего образования «САНКТ-ПЕТЕРБУРГСКИЙ ГОРНЫЙ УНИВЕРСИТЕТ» Кафедра общей химии Лабораторная работа №5 По дисциплине Химия Тема: Исследование гидролиза солей Автор: студент гр. РГИ-21 / Ортикова Т.В. / (подпись) (Ф.И.О.) Проверил _________ / / (должность) (подпись) (Ф.И.О.) Оценка: Дата: Санкт-Петербург 2021 Цель работы - ознакомиться с процессом гидролиза солей и его следствиями, научиться составлять уравнения гидролиза. Содержание протокола: Опыт 1.
2ZnSO4 + 2H2O = [ZnOH]2SO4 + H2SO4 2Zn2+ + 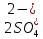 + 2HOH = 2ZnOH+ + + 2HOH = 2ZnOH+ + 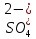 + 2H+ + + 2H+ + 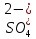 Zn2+ + HOH = ZnOH+ + H+ В растворе образуются катионы водорода, значит, среда кислая Al2(SO4)3 + 2H2O = 2AlOHSO4 + H2SO4 2Al3+ + 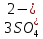 + 2HOH = 2AlOH2+ + 2 + 2HOH = 2AlOH2+ + 2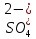 + 2H+ + + 2H+ + 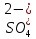 Al3++HOH = AlOH2++H+ В растворе образуются катионы водорода, значит, среда кислая Na2CO3+H2O = NaHCO3+NaOH 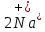 + + 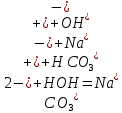 CO32-+HOH = HCO3-+OH- В растворе образуются анионы гидроксила, значит, среда щелочная 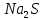 + +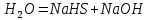 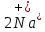 + + 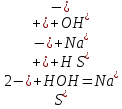 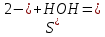 H H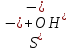 В растворе образуются анионы гидроксила, значит, среда щелочная (CH3COO)2Pb+H2O + PbOHCH3COO+CH3COOH Pb2++ CH3COO- + HOH = PbOH++CH3COOH Среда раствора слабокислая, так как константа диссоциации уксусной кислоты больше константы диссоциации катиона гидроксосвинца. Опыт 3(В). Первая ступень гидролиза: SbCl3 + H2O = SbOHCl2 + HCl Sb3+ + HOH = SbOH2+ + H+ Вторая ступень гидролиза: SbOHCl2 + HOH = Sb(OH)2Cl + HCl SbOH2+ + HOH = Sb(OH)2+ + H+ На второй ступени также образуется хлорид стибила (III) : Sb(OH)2Cl = SbOCl + H2O Опыт 4. 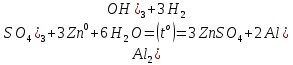 Небольшой треск Опыт 5. А) 2FeCl3 + 3Na2CO3 + 3H2O = 2Fe(OH)3+ 6NaCl + 3CO2 2Fe3+ +6 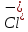 + 6N + 6N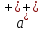 3CO32- + 3HOH = 2Fe(OH)3+ 6N 3CO32- + 3HOH = 2Fe(OH)3+ 6N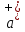 + 6C + 6C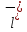 + 3CO2 + 3CO22Fe3+ + 3CO32- + 3HOH = 2Fe(OH)3+ 3CO2 Образование красно-коричневого осадка и выделение газа Б) 2CuSO4 + 2Na2CO3 + H2O = [CuOH]2CO3 + 2 Na2SO4 + CO2 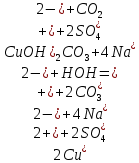 2Cu2+ + 2CO32- + HOH = [CuOH]2CO3 + CO2 Образование голубого осадка и выделение газа Вывод: Ознакомились с процессом гидролиза солей и его следствиями, научились составлять уравнения гидролиза по слабому катиону, слабому аниону, и когда обе части соли слабые. |