ИЗОФЛАВОНОИДЫ лек2. Изофлавоноиды
 Скачать 58 Kb. Скачать 58 Kb.
|
|
ИЗОФЛАВОНОИДЫ Изофлавоноиды в растения встречаются как производные изофлавона. Генистеин - 5,7, 4 -триокси-изофлавон и даидзеин - 5,7,3 ,4 - тетраокси-изофлавон содержатся в створках фасоли и др. растений сем. Бобовых. Формононетин - 7, 4 - метоксиизофлавон и его 7-глюкозид -ононин содержатся в корнях стальника. 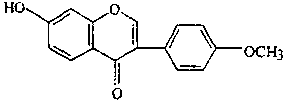 формононетин формононетинДРУГИЕ КЛАССЫ ФЛАВОНОИДОВ 1. Ксантоны. Алпизарин и его 6-С-гаикозид - мангиферин содержатся в траве золототысячника и копеечника альпийского. 2. Флаволигнаны - силибин, силимарин содержатся в плодах расторопши пятнистой (остро-пестро). ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА ФЛАВОНОИДОВ Физические свойства Катехины, лейкоантоцианидины, флаванонолы, изофлавоны - бесцветные; флаваноны, флавоны, флавонолы - желтые; халконы и ауроны - оранжевые; антоцианидины в зависимости от реакции среды красные, синие или фиолетовые аморфные или кристаллические вещества, без запаха, горького вкуса, с определенной температурой плавления ( гликозиды - 100-180 С, агликоны до 300° С). Растворимость. Гликозиды, катехины и лейкоантоцианидины хорошо растворимы в воде, этаноле и метаноле различной концентрации, не растворимы в органических растворителях ( диэтиловом эфире, хлороформе, ацетоне). Свободные агликоны, за исключением катехинов и лейкоантоцианидинов не растворимы в воле, но хорошо растворимы в этаноле, метаноле и других органических растворителях (диэтиловом эфире, хлороформе, ацетоне). Все флавоноиды хорошо растворимы в пиридине, диметилформамиде и щелочах. Все флавониды оптически активны, способны флюоресцировать в УФ-свете, имеют характерные УФ, характеризующиеся наличие 2-х максимумов поглощения и ИК-спектры. Химические свойства Химические свойства обусловлены особенностью строения флавоноидов: наличием арматического и пиронового колец, функциональных групп. 1. Гликозиды подвергаются ферментативному и кислотному гидролизу до агликонов и cахаров. O-гликозиды гидролизуются легко, С-гликозиды только в жестких условиях смесью Килиани (смесь концентрированных хлористоводородной и уксусной кислот). 2. Благодаря кольцам А и В флавоноиды способны: образовывать комплексные соединения с солями металлов (железа, алюминия, циркония). С солями железа в зависимости от количества гидроксильных групп соли от зеленой, сине до коричневой окраски, с солями алюминия - желтой, с желто-зеленой флюоресценцией; вступать в реакцию азосочетания с солями диазония с образованием азокрасителя. 3. Флавоноиды, содержащие пироновый цикл (флавоны и флавонолы): способны восстанавливаться атомарньм (свободным) водородом в кислой среде, полученным по реакции взимодействия кислоты с металлическим магнием или цинком до антоцинидинов (проба Синода или цинидиновая проба); растворяться в щелочах с образованием растворимых в воде фенолятов 4. Флавоноиды, содержащие пирановый цикл (катехины, лейкоантоцианидины) способны легко окисляться до производных флавона и флавонола. 5. Флавоноиды при сплавлении в жестких условиях со щелочью распадаются на составные части, что используется для установления структуры. Физические и химические свойства используются в анализе сырья на подлинность и доброкачественность. АНАЛИЗ ЛЕКАРСТВЕННОГО РАСТИТЕЛЬНОГО СЫРЬЯ, СОДЕРЖАЩЕГО ФЛАВОНОИДЫ Учитывая растворимость агликонов и гликозидов флавоноидов в спире, проводят экстракцию флавоноидов из сырья метанолом или этанолом. Спиртовое извлечение упаривают и разбавляют водой, после охлаждения неполярные вещества (белки, жирные масла, стерины, хлорофилл) выпадают в осадок, который отделяют. Часто для удаления сопутствующих веществ сырье сначала обрабатывают хлороформом, т.е. "обезжиривают", а затем уже экстрагируют спиртом различной концентрации. Спиртовое извлечение исследуют. Проводят качественный и количественный анализ. Качественный анализ Для установления подлинности используют в анализе качественные реакции и хроматографическое исследование. Качественные реакции 1. Проба Синода (цианидиновая проба). Реакция основана на способности окисленных форм флавоноидов восстанавливаться водородом в момент выделения до антоцианидинов. В кислой среде образуются оксониевые соли, окраска которых зависит от структуры флавоноида. Флавоны дают оранжево-красные, флавонолы от розовой до малиновой окраски соли. 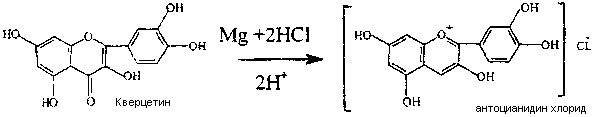 Антоцианидины, халконы и ауроны в кислой среде сразу дают окрашенные оксониевые соли. Эта реакция приводится в ГФХ1 изд. для установления подлинности цветков бессмертника песчаного. 2. Проба Брианта. Проводится в случае положительной цианидиновой пробы. Эта реакция дает возможность сделать заключение о присутствии в сырье гликозидов и агликонов. В пробирку, где проводилась проба Синода добавляют октанол и встряхивают, если: окраска перешла в октанол, то в сырье содержатся только агликоны, которые растворимы в октаноле; окраска осталась в водной фазе - в сырье только гликозиды; окрасились оба слоя - в сырье присутствуют флавоноиды как в виде гликозидов, так и в виде агликонов. 3. Реакция с солями железа (хлоридом окисного железа), образуются комплексные соединения окрашенные в черно-синий цвет, если флавоноиды - триоксипроизводные и в зеленый, если диоксироизводные. 4.Реакция с 2-5%-ным спиртовым раствором алюминия хлорида. Образуются хелатные комплексы за счет водородных связей, возникающих между карбонильной и оксигруппой, желтого цвета с желто-зеленой флюоресценцией. Эта реакция приведена в ГФХ1 изд. для подтверждения подлинности сырья зверобоя, горца перечного и птичьего. Аналогично образуются комплексы с солями циркония. 5. Реакция с 1%-ным раствором основного ацетата свинца. Антоиианидины дают синий аморфный осадок. Флавоны, халконы и ауроны - осадки ярко-желтого цвета. 6. Реакция с 10%-ным спиртовым раствором щелочи с образованием фенолятов желтого цвета на флавоны и флавонолы. Антоцианидины образуют со щелочами соли от синего до оливково-зеленого цвета. 7. Реакция азосочетания с диазосоединениями. Образуется азокраситель оранжевого, красного или вишнево-красного цвета. 8. Борно-лимонная реакция с реактивом Вильсона (по 0,5 г борной и лимонной кислот в метаноле). Реакция отличия флавоноидов от фуранохромонов. Флавоноиды дают комплексы с борной кислотой желтой окраски с ярко-желтой флюоресценцией, которые не разрушаются лимонной кислотой. Хроматографическое исследование Для идентификации и разделения флавоеноидов используют метод бумажной, колоночной хроматографии и хроматографии в тонком слое сорбента. Используют различные системы растворителей: БХ чаще всего БУВ (бутанол - уксусная кислота - вода) 4:1:5; 4:1:2 ТСХ- хлороформ-метанол 8:3; 8:2 Идентифицируют флавоноиды по характерному свечению на хроматограммах в УФ-свете и после проявления хромогенными реактивами. Катехины и лейкоантоцианидины не флюоресцируют. Гликозиды флавонов и изофлавонов флюоресцируют голубым или синим светом, флавонолов - темно-коричневым или черным, агликоны флавонов - коричневым, флавонолов - желтым, халконы и ауроны имеют желтую или оранжевую флюоресценцию. Для проявления флавоноидов на хроматограммах используют: 1.Пары аммиака 25%-ного. Происходит усиление окраски пятен в УФ-свете или изменение окраски до желтой. 2. 2-5%-ный спиртовый раствор алюминия хлорида - желто-зеленая флюоресценция в УФ-свете, в видимом свете - желтое окрашивание. 3. Катехины проявляют 1°/о-ным раствором ванилина в концентрированной хлороводородной кислоте, в видимом свете наблюдается красное окрашивание. Реже используют реактив Вильсона, 2%-ный метанольный раствор хлорокиси циркония, раствор пятихлористой сурьмы в хлороформе, диазореактив. В ГФХ1 изд. приводится исследование методом бумажной хроматографии халконов и ауронов в траве череды, изофлавонов в корнях стальника; хроматографии в тонком слое сорбента на "Силуфле" - флавоноидов в цветках и плодах боярышника, флавон-5-гликозидов в траве хвоща полевого. Количественное определение Для количественного определения флавоноидов в лекарственном растительном сырье используют физико-химические методы анализа. Преимущественно фотоэлектроколориметрические и спектрофотометрические методы. Фотоэлектроколориметрический метод (ФЭК). ФЭК основан на измерении оптической плотности окрашенных растворов, полученных по реакции флавоноидов с солями металлов и азосочетания с солями диазония. ГФХ1 изд. дает ФЭК-метод для определения содержания суммы флавоноидов в листья вахты трехлистной. Предварительно сырье очищают от хлорофилла хлороформом, получают спиртовое извлечение флавоноидов, затем проводят реакцию образования азокрасителя с диазотированным стрептоцидом и измеряют оптическую плотность окрашенного раствора с помощью ФЭК. Содержание суммы флавоноидов расчитывают по калибровочному графику, построенному по стандартному образцу рутина. Спектрофотометрический метод (СФМ). СФМ основан на способности флавоноидов или их окрашенных комплесов поглощать монохроматический свет при определенной длине волны. 1. Получают спиртовое извлечение и измеряют собственное поглощение в: цветках бессмертника песчаного при длине волны 315 нм, рассчитывают содержание флавоноидов на изсалипурпозид с использованием оптической плотности ГСО изосалипурпозида. корнях стальника при длине волны 260 нм; расчитывают на ононин с учетом оптической плотности ГСО ононина. цветках пижмы измеряют оптическую плотность флавоноидов и фенол-карбоновых кислот в буферном растворе и пересчитывают на лютеолин с учетом оптической плотности ГСО лютеолина. 2. Получают спиртовое извлечение, затем проводят реакцию образования комплекса с 2%-ным спиртовым раствором алюминия хлорида и измеряют оптическую плотность в: траве зверобоя в пересчете на рутин с учетом оптической плотности ГСО рутина; траве горца перечного в пересчете на кверцетин с учетом удельного показателя поглощения комплекса кверцетина с алюминия хлоридом; траве горца птичьего в пересчете на авикуларин с учетом удельного показателя поглощения комплекса авикулярина с алюминия хлоридом. 3. Получают извлечение антоцианов 1%-ным раствором хлороводородной кислоты из цветков василька синего, при этом образуются окрашенные оксониевые соли, у которых измеряют оптическую плотность и пересчитывают на 3,5 дигликозид цианидина (цианин) с учетом удельного показателя поглощения цианина в 1%-ном растворе хлороводородной кислоты. Хроматоспектрофотометирический метод 1. Предварительное разделение флавоноидов в тонком слое сорбента (цветки боярышника). Стадии определения получение спиртового извлечения очистка извлечения хроматографическое разделение флавоноидов на пластинке "Силуфол" в системе растворителей хлороформ-метанол 8:2 вместе со свидетелем ГСО гиперозида идентификация гиперозида и свидетеля на пластинках в УФ-свете элюирование гиперозида и ГСО смесью диоксана и воды 1:1 измерение оптической плотности испытуемого раствора и ГСО при длине волны 365 нм расчет содержания гиперозида 2. Предварительное разделение на колонке с полиамидом (плоды боярышника) Стадии определения получают спиртовое извлечение отгоняют спирт и обрабатывают остаток 10%-ным раствором натрия хлорида полученный раствор наносят на колонку с полиамидом элюируют флавоноиды с колонки 95%-ным этанолом, собирают окрашенный в желтый цвет элюат в мерную колбу на 25 мл измеряют оптическую плотность элюата при длине волны 365 нм параллельно измеряют оптическую плотность элюата ГСО гиперозида, полученного аналогично элюату флавоноидов пересчитывают на гиперозид с учетом оптической плотности элюата ГСО гиперозида. 3. В траве сушеницы топяной выделяют следующие стадии количественного определения: получют спиртовое извлечение отгоняют спирт и остаток обрабатывают 10%-ным раствором натрия хлорида полученный раствор переносят на колонку с полиамидом элюируют флавоноиды с колонки 95%-ным этанолом и собирают окрашенный темно-желтый цвет элюат в мерную колбу на 50 мл измеряют оптическую плотность элюата при длине волны 338 нм параллельно определяют оптическую плотность раствора стандартного образца вещества сравнения (СОВС) калия бихромата пересчитывают на гнафалозид А с учетом оптической плотности СОВС и коэффициента пересчета калия бихромата на гнафалозид А и поправочного коэффициента на неполное элюирование гнафалозида А с полиамидного сорбента. 4. Количественное содержание ксантонов в траве золототысячника: получают извлечение подкисленным 60%-ным этанолом 2 мл извлечения наносят на колонку с полиамидным сорбентом элюируют ксантоны 95%-нм этанолом и собирают окрашенный в желтый цвет элюат в мерную колбу на 50 мл получают окрашенный комплекс с алюминия хлоридом измеряют оптическую плотность окрашенного комплекса параллельно измеряют оптическую плотность окрашенного комплекса ГСО алпизарина с алюминия хлоридом пересчитывают на алпизарин с учетом оптической плотности комплекса ГСО алпизарина с алюминия хлоридом. |
