годовая контрольная работа 8класс. 8 ГКР. Контрольная работа 8 класс i вариант Часть а четыре энергетических уровня содержит электронная оболочка атома
 Скачать 25.78 Kb. Скачать 25.78 Kb.
|
|
Годовая контрольная работа 8 класс I вариант Часть А А1. Четыре энергетических уровня содержит электронная оболочка атома: а) калия б) бериллия в) кремния г) гелия А2. Шесть электронов находятся на внешнем энергетическом уровне атома: а) золота б) углерода в) хром г) кислорода А3. Выберите соединение с ковалентной полярной связью: а) H2 б) H2S в) NaI г) N2 а) SO2 б) SO3 в) MgS г) SF6 А5. Выберите формулу оксида железа (III): а) FeO б) FeCl3 в) Fe2O3 г) ОF2 А6. Выберите ряд формул, в котором все вещества являются основаниями: а) Fe2O3, ZnO, Cu(OH)2 б) Ba(NO3)2, Ba(OН)2, Н2SО4 в) КОН, Fe(OH)3, NaОН г) Zn(OН)2, НCl, H2O А7. Оксид кальция СаО реагирует с: а) HNO3 б) Li2O в)Cu г)MgSO4 а) водопроводная вода б) углекислый газ в) кислород г) медь А9. Уравнение реакции замещения: а) Zn + 2HCl = ZnCl2 + H2 б) ZnO + H2SO4 = ZnSO4 + H2O в) Cu(OH)2 = CuO + H2O г) Fe + S = FeS А10. Процессу окисления соответствует схема изменения степени окисления: а)  б)  в)  г)  Часть В В1. Ядро атома 15N содержит 7 протонов и … нейтронов. В2. Установите соответствие между формулой вещества и его принадлежностью к определенному классу неорганических соединений. Класс веществ:Формула вещества: оксиды а) HNO2 основания б) P2O5 кислоты в)Fe(OH)3 соли г) Mg(NO3)2 В3. Установите соответствие между реагентами и названием продуктов реакции Реагенты Продукты реакции 1) BaCl2 + Na2SO4 = а) = хлорид бария + вода 2) BaO + HCl = б) = нитрат бария + вода 3) Ba + H2O = в) = гидроксид бария + водород 4) Ba(OH)2 + HNO3 = г) = сульфат бария + вода д) = сульфат бария + хлорид натрия В4. Массовая доля кислорода в серной кислоте H2SO4 равна …% Часть С С1. Осуществите цепочку следующих превращений. Укажите типы химических реакций. Fe→Fe2O3→FeCl3→Fe(OH)3 → Fe2O3 С2. Вычислите массу оксида меди, вступившей в реакцию с 250 г серной кислоты. Годовая контрольная работа 8 класс 2 вариант Часть А А1. Элемент третьего периода главной подгруппы II группы Периодической системы химических элементов Д. И. Менделеева: а) алюминий б) бериллий в) магний г) натрий А2. Число электронов, протонов и нейтронов в атоме фтора F: а) p+—9, n0—10, e—19 б) p+—10, n0—9, e- —10 в) p+—10, n0—9, e- —9 г) p+—9, n0—10, e- —9 А3. При помощи ионной химической связи образовано вещество: а) кислород б) поваренная соль в) медь г) вода А4. Вещество, в котором сера проявляет степень окисления +4, имеет формулу: а) H2S б) SO2 в) SO3 г) Na 2S А5. Вещество, имеющее формулу NaNO3, называется: а) карбонат натрия б) нитрит натрия в) хлорид натрия г) нитрат натрия А6. Ряд формул, в котором все вещества являются оксидами: а) ZnO, ZnCl2 , HCl б) SO3 , MgO, CuO в) KOH, K 2O, MgO г) HNO3 , P2O5 , NaCl А7. Процессу восстановления соответствует схема изменения степени окисления: а) 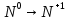 б) 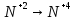 в) 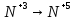 г) 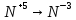 А8. Укажите правильную последовательность действий при разделении смеси поваренной соли и речного песка: а) выпаривание, фильтрование, растворение в воде б) фильтрование, выпаривание, растворение в воде в) растворение в воде, выпаривание, фильтрование г) растворение в воде, фильтрование, выпаривание А9. Уравнение реакции обмена: а) CaO+SiO2= CaSiO3 б) FeS+ 2HCl= FeCl2+H2 S в) 2 KClO3 = 2KCl+ 3O2 г) Mg+ 2HCl= MgCl2+ H2 А10. С раствором гидроксида натрия NaOH взаимодействует вещество, формула которого: а) HCl б) MgO в) KOH г) Mg Часть В В1. Схема распределения электронов по слоям атома химического элемента – 2,8,7. Химическая формула высшего оксида этого элемента … В2. Установите соответствие между формулой вещества и его принадлежностью к определенному классу неорганических соединений. Класс веществ:Формула вещества: 1) оксиды а) NaOH г) NaNO3 2) основания б)HCl д)H2 3) кислоты в)CaO 4) соли В3. Установите соответствие между формулой вещества и реагентами, с которыми это вещество может взаимодействовать: ФОРМУЛА ВЕЩЕСТВА РЕАГЕНТЫ а) N2 1) Zn, BaCl2 б) CuSO4 2) Li, O2 в) KOH 3) FeCl3, HCl 4) HCl, Mg В4. Массовая доля кислорода в азотной кислоте HNO3 равна …% Часть С С1. Осуществите цепочку следующих превращений. Укажите тип реакции. Fe→Fe2O3→FeCl3→Fe(OH)3 → Fe2O3 С2. Определите массу карбоната кальция CaCO3, используя уравнение химической реакции: СаСО3 = СаО + СО2, если при его термическом разложении выделяется 45 литров углекислого газа СО2. |
