Бешенство, Пономарева А.Н. Курсовая работа Лист 16 Реферат Тема Бешенство студентка 4 курса 3 группы Факультета ветеринарной медицины Пономарёва Анна Николаевна
 Скачать 3.1 Mb. Скачать 3.1 Mb.
|
Реферат Тема: «Бешенство» Выполнила: студентка 4 курса 3 группы Факультета ветеринарной медицины Пономарёва Анна Николаевна Москва 2021 г. ОглавлениеЭтиология вируса бешенства и заболевания. 3 Экология и морфология вируса бешенства. 4 Строение генома вируса. 5 Антигенные свойства вируса. 6 Этапы репродукции вируса. 8 Этапы органного патогенеза. 9 Диагностика бешенства. 9 Специфическая профилактика. 16 Этиология вируса бешенства и заболевания.Бешенство – острая особо опасная вирусная болезнь теплокровных животных и человека, характеризующаяся поражением нервной системы и заканчивающаяся летальностью. Заболевание распространено повсеместно, за исключением некоторых островных государств (Англия, Япония, Австралия и т.д.) Ранее считалось, что птица не восприимчива к ВБ. В последние годы мнение изменилось. Некоторые исследователи утверждают, что домашние птицы, особенно куры, чувствительны к вирусу бешенства. Больная птица пуглива, беспокойна, агрессивна, бегает, прыгает, кричит. Нападает на других птиц, людей, животных. Наносит удары когтями и клювом людям в лицо, животным в голову. На второй день наступает паралич и смерть. Бешенство в 100 % заканчивается гибелью. Однако, описано 6 случаев полного или частичного выздоровления человека. Пятеро получили определённое количество инъекций антирабической вакцины до появления симптомов. Только 15-ти летняя девочка в США, укушенная летучей мышью, выздоровела без предварительной специфической терапии. Девочку искусственно перевели в состояние комы и лечили неспецифическими противовирусными препаратами. В других случаях эта методика показала себя не эффективной. Таксономия вируса: Царство Viraе Порядок Mononegavirales Семейство Rhabdoviridae Род Lyssavirus Вид вирус бешенства Лиссавирусы - это единственный род, поражающий только млекопитающих. Генотипы. Различают 7 генотипов и 4 неклассифицированных вируса 1 генотип (вирусы классического бешенства) включает штаммы уличного (дикого) бешенства (в т.ч. вирус дикования или арктического бешенства), выделенные от наземных млекопитающих, насекомоядных, плотоядных и кровососущих летучих мышей, а также фиксированные (вакцинные) вирусы бешенства. Распространён практически по всему миру. 2 генотип (Лагос-Бат) включает вирусы, изолированные от плотоядных летучих мышей, собак и кошек Центральной и Южной Африки. Нет информации о патогенности для человека. 3 генотип (Мокола) выделен от землероек, человека, собак и кошек в Центральной и Южной Африке. 4 генотип (Дувенхаге) выделен от человека, укушенного летучей мышью, и от летучих мышей в Южной Африке и Зимбабве. 5 генотип (лиссавирус европейских летучих мышей 1-го типа) циркулирует в Европе, в т.ч. в России. Вирус был изолирован от 11-ти летней девочки, укушенной в губу летучей мышью. 6 генотип (лиссавирус европейских летучих мышей 2-го типа) циркулирует в Европе. Выделен от человека в Шотландии и Финляндии. 7 генотип (лиссавирус австралийских летучих мышей) выделен также от людей. Все лиссавирусы, кроме Лагос-Бат (2 генотип) вызывают у людей летальные энцефалиты. Экология и морфология вируса бешенства.Из 7 генотипов рода Lyssavirus экология шести генотипов вируса связана с летучими мышами. У вируса Мокола (3-ий генотип) основной хозяин не известен. Экология вируса бешенства 1-го генотипа связана как с плотоядными наземными животными, так и с летучими мышами. Нет информации о возможности происхождения вариантов вируса бешенства наземных хищников от вирусов летучих мышей и наоборот. Однако, описаны случаи интродукции вируса летучих мышей в популяции наземных животных в регионах, свободных от бешенства. Морфология вируса. Рабдовирусы позвоночных имеют пулевидную форму (от др.-греч. рабдос – палка). Длина вириона от 100 до 430 нм, диаметр примерно 75 нм. Вирион имеет суперкапсидную оболочку (пеплос) с отростками –пепломерами. Спиральный тип симметрии. Электронная фотография.  Строение генома вируса.Геном представлен линейной односпиральной молекулой РНК негативной полярности, кодирует 5 структурных белков. РНК не обладает инфекционностью. Инфекционностью и транскриптазной активностью обладает нуклеокапсид, состоящий из РНК в комплексе с тремя внутренними белками N, L, P. 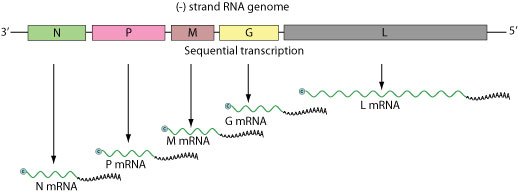 Белки вириона. L – РНК-зависимая РНК- полимераза, принимает участие в транскрипции и репликации. N – нуклеопротеин, является главным белковым компонентом рибонуклеопротеидного комплекса (РНП), основной функцией которого является транскрипция и репликация генома, индуцирует развитие клеточно-опосредованного иммунного ответа и АТ P – фосфопротеин, компонент вирусной полимеразы, участвует в транскрипции M – мембранный белок тесно связан с РНП , способствует процессу почкования вириона, ингибирует транскрипцию клеточной ДНК. G –гликопротеин в составе бислойной липопротеиновой оболочки представлен в виде пепломеров (шипов) и играет главную роль в развитии инфекционного процесса, индукции факторов протективного иммунитета, проявляет ГА активность. 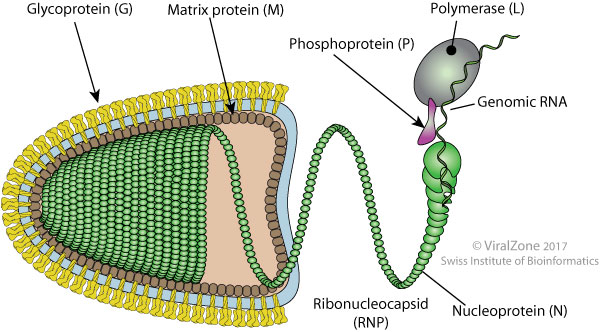 Поверхностный гликопротеин G отвечает за адсорбцию, слияние мембран, участвует в проникновении вируса в клетку путём эндоцитоза. На финальной стадии сборки и почкования нуклеокапсиды одевают вирусную оболочку, представленную G-белком, который интегрирован в клеточную мембрану. Отвечает за нейровирулентность, нейроинвазивность и исход вирусной инфекции. Антигенные свойства вируса.Антигенной вариабельностью вирус бешенства не обладает (все штаммы родственны в иммунобиологическом отношении). Современные вакцины в антигенном отношении полностью «покрывают» всё разнообразие вариантов вируса бешенства, циркулирующих на 5 континентах, а также эффективны по отношению к вирусам 4-7-го генотипов. Не эффективны только для лиссавирусов 2-го и 3-го генотипов, т.к. гомология аминокислот G-белка этих вирусов к ВБ менее 62%. Различают 5 групп по вирулентности: 1 гр. – усиленные штаммы, характеризуются высокой вирулентностью, коротким инкубационным периодом и постоянным образованием телец Бабеша-Негри 2 гр. – а) вирус, выделенный от собак (встречается в странах Африки), характеризуется внезапным изменением поведения и развитием параличей; - б) от КРС с клиникой чумы и развитием параличей (передаётся летучими мышами); - в) от людей на острове Троица в 1929 г., одновременно болели КРС и непарнокопытные. Установлено, что этот вирус передавался летучими мышами-вампирами. 3 гр. – штаммы, выделенные от песцов и собак при диковании (Россия и Канада); никогда не болеет человек 4 гр. – вирус выделен из мозга умершей в США девочки Флури в 1940 г. , болеют животные с параличами; в клетках головного мозга данный штамм не образует телец Бабеша-Негри. 5 гр. – вирусы бешенства, выделенные от людей.  Этапы репродукции вируса.1. Адсорбция вируса на клетках-мишенях (нейроциты) (белок G) и Проникновение вируса в клетку по типу эндоцитоза; 2. Депротеинизация в вакуоли клетки за счёт лизосомной актив- ности и выход нуклеокапсида (РНК+N,L,P)-матрица для Транскр и Р 4. Транскрипция - 2 типа: синтез пяти иРНК для трансляции вир. белков, антигеномные полные плюс-РНК для репликации генома; 5. Трансляция (синтез структурных белков вириона и ферментов для репликации генома); 6-7. Репликация вирусного генома (минус-РНК); 8 Сборка вириона: (обр-е РНП: РНК+N,Р, L) 9. Выход вируса по типу почкования. 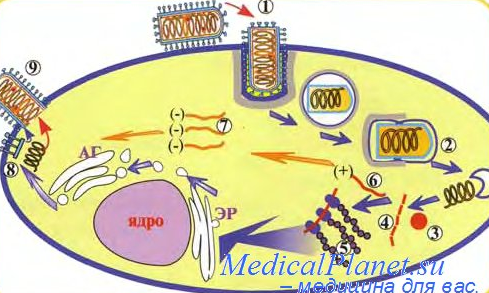 Этапы органного патогенеза.1 ст. - проникновение вируса контактным путём при укусе или ослюнении (инфицировании)только раневой поверхности; 2 ст. – первичная репродукция и накопление при укусе - в воротах инфекции (в мышечных клетках: на G-белке ВБ расположен сайт, имеющий сродство к рецепторам, находящимся на поверхности нейронов и мышечных клеток); при ослюнении – вирионы захватываются двигательными или чувствительными нервными окончаниями и сразу транспортируются в ЦНС; 3 ст. – первичная дессиминация по центростремительным нейронам в ЦНС (нейропробазия) (скорость 50-100 мм/сутки); 4 ст. – вторичная репродукция и накопление в клетках головного мозга; 5 ст. – вторичная дессиминация по центробежным нейронам к периферическим органам (септиневрия); 6 ст. – выделение вируса со слюной и другими секретами и экскретами (слёзная жидкость, кровь, моча, фекалии и др.) Диагностика бешенства.Диагноз на бешенство устанавливают комплексно на основании: 1. эпизоотологических данных; 2. клинических признаков; 3. лабораторных исследований патологического материала. Трупы, подозрительные в заражении бешенством, вскрывать запрещено. Лабораторная диагностика патматериала. 1. Отбор патологического материала проводят с соблюдением правил личной безопасности! от крупных животных - голова; от мелких животных - труп целиком или голова 2. Отобранный патматериал упаковывают во влагонепроницаемую тару и в металлический контейнер. (транспортировка материала, исключающая распространение вируса в окружающую среду) 3. Материал доставляют в лабораторию, имеющую разрешение на работу с возбудителями особо опасных болезней. Лабораторные исследования проводят сразу же при получении патматериала. 4. Не допускаются для исследования!!! пробы в стадии гнилостного разложения пробы, консервированные глицерином, фиксированные метиловым спиртом, формалином или др., способствующим возникновению неспецифической флуоресценции 5. Лабораторную диагностику бешенства животных проводят в соответствии с Межгосударственным стандартом ГОСТ 26075-2013 от 01.01.2015 г. «Методы лабораторной диагностики бешенства». Подготовка патматериала к исследованию: вскрытие черепной коробки; извлечение головного мозга; приготовление мазков-отпечатков и суспензии из нескольких отделов головного мозга (кора больших полушарий, продолговатый мозг, аммоновы рога, мозжечок). Методы лабораторной диагностики. Метод флуоресцирующих антител – МФА (РИФ, прямой вариант). Метод биопробы в культуре клеток. Метод биопробы на белых мышах . Метод иммуноферментного анализа – ИФА (твёрдофазный, сэндвич вариант). Реакция диффузионной преципитации – РДП. Для МФА готовят мазки: кусочек ткани из каждого отдела мозга растирают в ступке до гомогенной массы, из которой делают мазки на предметных стёклах или мазки-отпечатки (по общепринятой методике) Для контроля делают мазки или отпечатки из мозга здоровых, не болевших бешенством и не вакцинированных против бешенства, белых мышей. 1 этап – индикация вируса методом флуоресцирующих антител (МФА). АГ (мазок) + АТ (специфический конъюгат: флуоресцирующий антирабический иммуноглобулин) = комплекс АГ- АТ Результат МФА - свечение в виде зеленоватых гранул в люминесцентном микроскопе Положительный результат 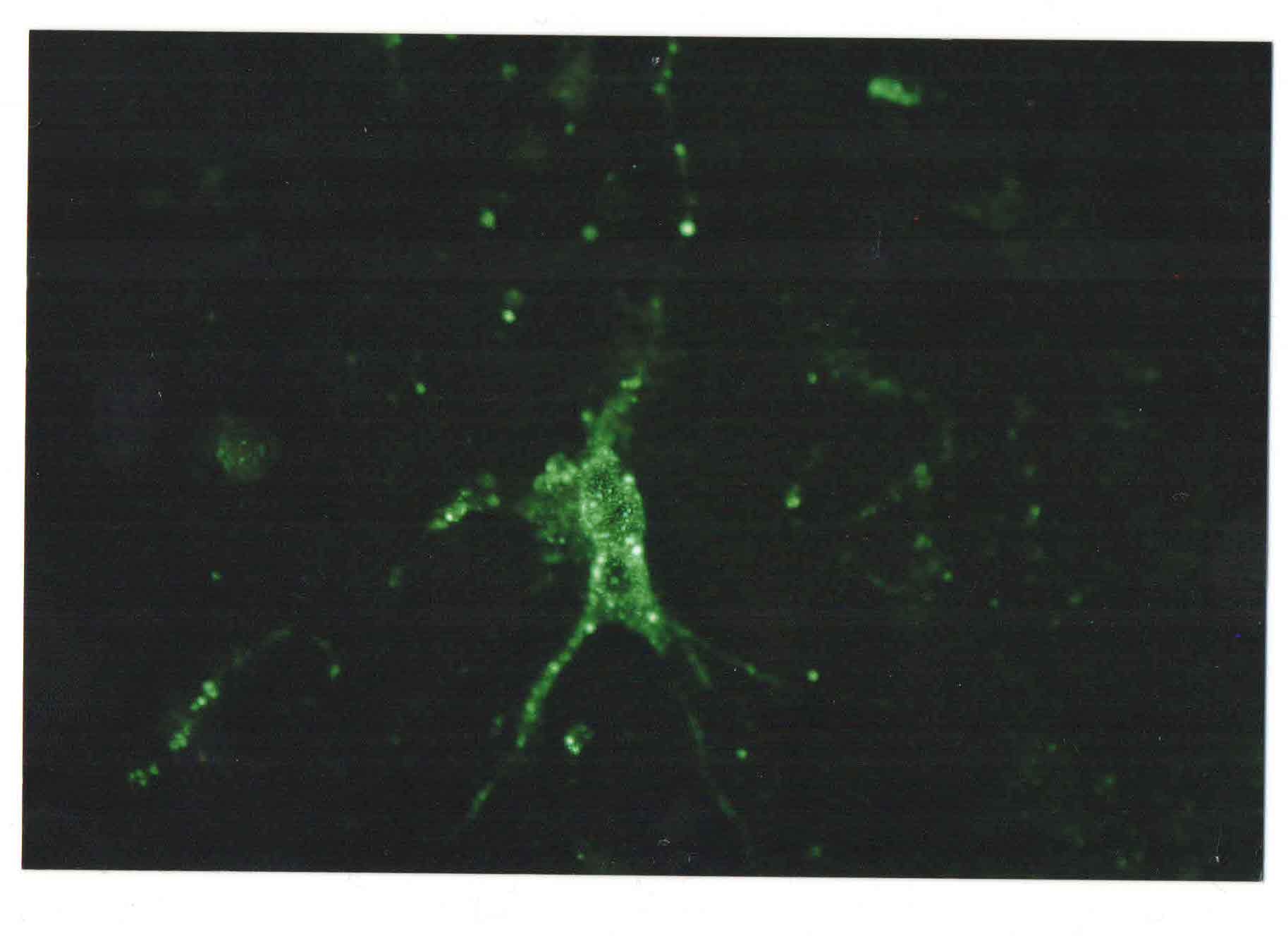 Отрицательный результат  1. Диагноз БЕШЕНСТВО считается установленным, если в нескольких полях зрения микроскопа в исследуемом препарате обнаруживают типичное свечение в виде зеленоватых гранул! При этом в контрольных препаратах подобного свечения не обнаруживается. 2. В случае отрицательного результата (свечение не обнаружено) продолжают проводить исследования методами биопробы на белых мышах или культуре клеток. 2 этап – изоляция вируса. Биологическая проба на белых мышах или выделение вируса бешенства в культуре клеток мышиной нейробластомы (CCL-131 или НГУК-1) Методы являются альтернативными (т.е. взаимозаменяемыми) Изоляция вируса методом биопробы на белых мышах. 1. 5-6 белых мышат заражают интрацеребрально. Срок наблюдения – 30 суток Признаки положительной биопробы: взъерошенность шерсти, тремор, нарушение координации движения, прострация, парезы и параличи, гибель. Гибель мышей в первые двое суток после заражения не учитывают (неспецифическая). Идентификация вируса, выделенного от положительной биопробы. От павших мышей, начиная с третьих суток после заражения (положительная биопроба), отбирают головной мозг для идентификации вируса методом флуоресцирующих антител (МФА). Положительный диагноз на бешенство считают установленным при обнаружении свечения в виде зеленоватых гранул в люминесцентном микроскопе. Положительный результат 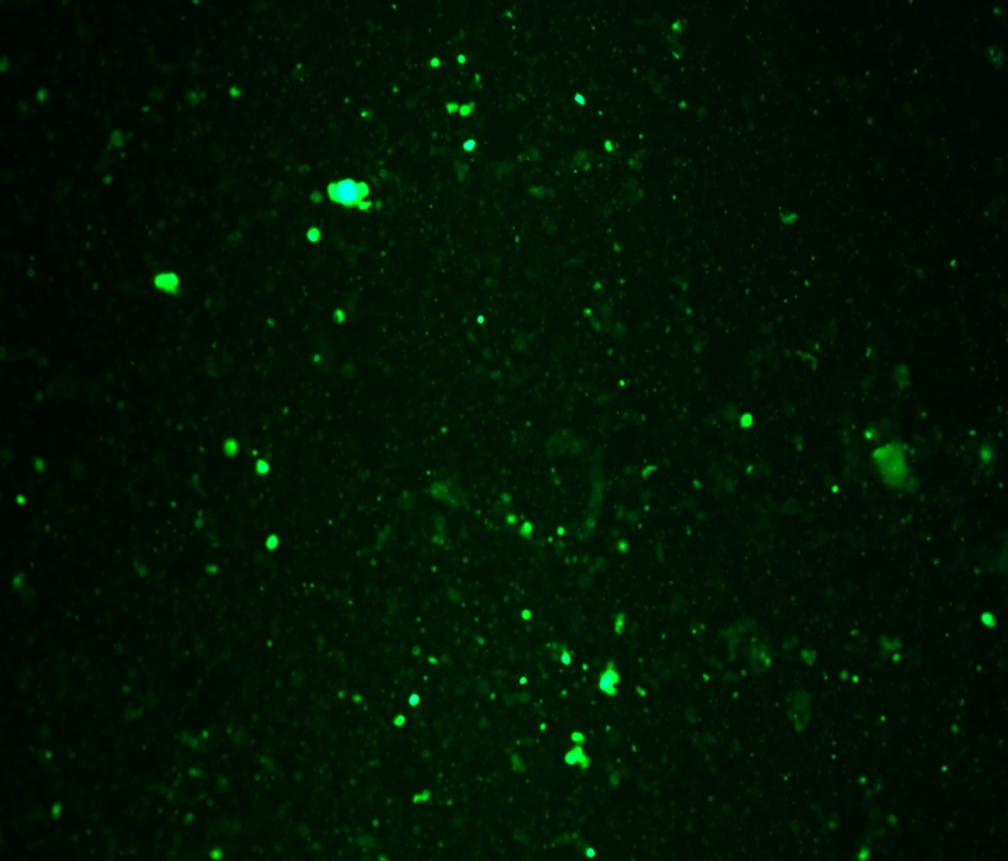 Отрицательный результат  Отрицательный диагноз на бешенство может быть дан по истечении 30 суток наблюдения при условии, что все заражённые животные останутся живыми и здоровыми. Результаты биопробы являются окончательными и дальнейшие исследования не проводят! Изоляция вируса методом биопробы в культуре клеток. Матрасы с культурой клеток мышиной нейробластомы заражают суспензией из головного мозга. Срок инкубации – 42-48 час. В качестве положительного контроля используют суспензию мозга мыши, заражённой в.бешенства (шт.CVS), отрицательного контроля – суспензию мозга здоровой мыши. Через 48 часов проводят идентификацию вируса бешенства методом флуоресцирующих антител (МФА). Отрицательный диагноз ставят, если в культуре клеток методом флуоресцирующих антител (МФА) вирус бешенства не выявлен. Результаты выделения вируса бешенства в культуре клеток окончательные, дальнейшие исследования не проводят! Положительный диагноз на бешенство считают установленным при обнаружении свечения в виде зеленоватых гранул в люминесцентном микроскопе. Иммуноферментный анализ (ИФА, сэндвич-вариант). АТспецифические (в лунке планшета) + АГ (суспензия отдела головного мозга ) + АТ (специфический конъюгат: ферментативный антирабический иммуноглобулин) + субстрат = комплекс Результат ИФА – окрашивание продукта реакции в лунке планшета. Положительный диагноз на бешенство считают установленным, если при визуальном учёте результата ИФА хотя бы в одном разведении исследуемого материала (одной лунке) наблюдается специфическое окрашивание. Отрицательный результат ИФА должен быть подтверждён следующими методами: МФА, биопробой на белых мышах или культуре клеток. Реакция диффузионной преципитации (РДП). АГ (10% суспензия из гол.мозга) + АТ (специфическая антирабическая сыворотка) = комплекс АГ- АТ в агаровом геле (линия преципитации). Учёт проводят через 6-24-48 ч. Реакцию считают положительной при наличии даже одной линии преципитации между лунками, содержащими исследуемый материал (АГ) и антирабической сывороткой (АТ). 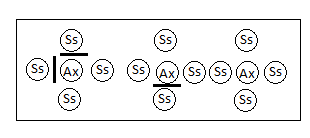 Отрицательный результат РДП должен быть подтверждён следующими методами: МФА, биопробой на белых мышах или культуре клеток Положительный диагноз на бешенство считают установленным при выявлении даже одной линии преципитации. Световая микроскопия внутриклеточных телец Бабеша-Негри. 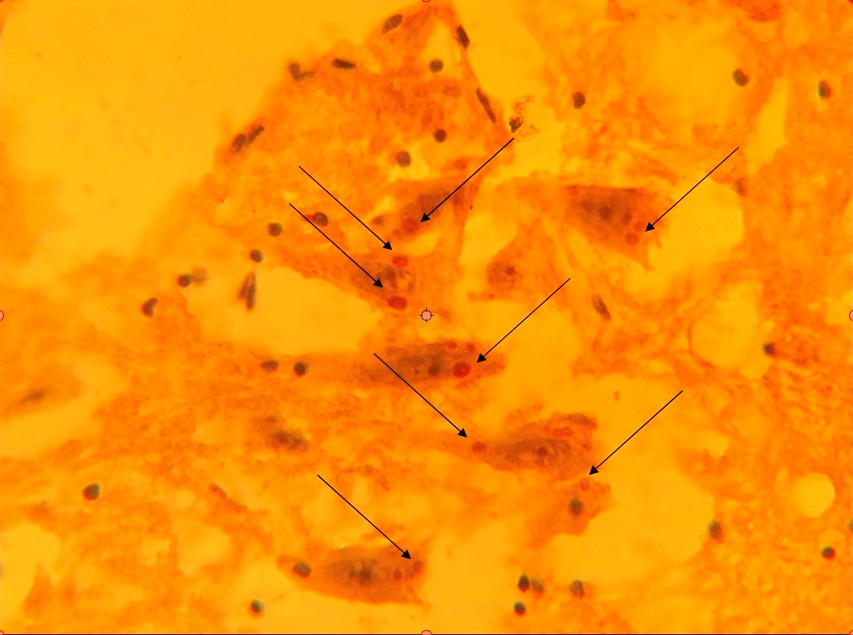 Специфическая профилактика.В 1885 году Л. Пастер впервые применил антирабическую вакцину для иммунизации людей. При пассировании ВБ, выделенного из головного мозга бешеной собаки, от кролика кролику наблюдалось постепенное сокращение инкубационного периода. На 133-ем пассаже инкубационный период составил 7 дней и при дальнейших пассажах не менялся. Вирус был назван фиксированным (virus Fix). Этот вирус частично или полностью утратил способность выделяться через слюнные железы и проникать в ЦНС при подкожном введении Вирус полностью утратил вирулентность, но сохранил антигенные и иммуногенные свойства. Частично аттенуированный штамм вируса бешенства Пастера используют для производства вакцин до сих пор. Вакцины I поколения цельновирионные: живые (для КРС и диких животных) инактивированные (для человека и мелких домашних животных); Вакцины III поколения (ДНК-вакцины) применяют для оральной иммунизации диких животных. Вакцины II поколения (субъедничные) - экспериментальные серии.   |

