Суммативное оценивание за раздел 10.2С «Химическое равновесие»
Задания
Химическое равновесие имеет динамический характер. Объясните, как вы это понимаете на примере реакции
Н2 (г) + I2 (г) 2HI (г)
Изменение температуры, давления, концентрации веществ, приводит к смещению химического равновесия.
На примере реакции 2HBr (г) H2 (г) + Br2 (ж) - Q, объясните, в какую сторону (вправо/ влево) будет смещено равновесие при:
увеличении давления
Обоснуйте ответ.
уменьшении температуры
Обоснуйте ответ
уменьшении концентрации продуктов реакции
Обоснуйте ответ
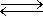 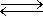 Напишите выражение константы равновесия Ксдля следующих реакций : 2NO (г) + O2 (г) 2NO2 (г) CO2 (г) C(графит) 2CO (г) Напишите выражение константы равновесия Ксдля следующих реакций : 2NO (г) + O2 (г) 2NO2 (г) CO2 (г) C(графит) 2CO (г)
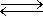 При некоторой температуре равновесные концентрации в системе 2CO (г) + O2 (г) 2CO2(г) составляли: При некоторой температуре равновесные концентрации в системе 2CO (г) + O2 (г) 2CO2(г) составляли:
[CO] = 0,2 моль/л, [O2] = 0,32 моль/л, [CO2] = 0,16 моль/л. Определить константу равновесия при этой температуре.
|
|
 Скачать 20.4 Kb.
Скачать 20.4 Kb.