|
|
практическая работа №2. Практическая работа 1 Осуществление цепочки химических превращений Цель
Дата________ ФИ______________________
Практическая работа № 1
Осуществление цепочки химических превращений
Цель: Осуществить реакции, соответствующие указанным цепочкам превращений. Систематизировать знания о соединениях металлов.
Оборудование: пробирки, штатив для пробирок,
Реактивы: растворы гидроксида натрия (NaOH), соляной кислоты (HCl), хлорида цинка (ZnCl2), железный гвоздик (железо Fe)
С правилами техники безопасности ознакомлен (а).
Ход работы
Что делали
|
Что наблюдали, выводы.
|
Уравнение реакции
|
Сu ← CuSO4 → Cu(OH)2 → CuCl2
1 2 3
|
1 ↓ _____
CuSO4
|
_____________________
_____________________
_____________________
_____________________
|
|
2. ↓ ________

CuSO4
|
_____________________
_____________________
_____________________
_____________________
|
|
3. ↓ ________

Cu(OH)2
|
_____________________
_____________________
_____________________
_____________________
|
|
ZnCl2 → Zn(OH)2 → ZnCl2
1 2
|
1. ↓ ________

ZnCl2
|
_____________________
_____________________
_____________________
_____________________
|
|
2. ↓ ________

Zn(OH)2
|
_____________________
_____________________
_____________________
_____________________
|
|
П.р.
Оценка ___________
Дата________ ФИ______________________
Практическая работа № 2
Решение экспериментальных задач на распознавание и получение соединений металлов
Цель: применить знания, полученные при изучении темы «Металлы», в экспериментальном решении задач; закрепить навыки проведения химического эксперимента.
Оборудование: пробирки, штатив для пробирок
Реактивы: растворы гидроксида натрия (NaOH), хлорида бария (ВаCl2) серной кислоты (Н2SO4), карбоната натрия ( Na2CO3). железный гвоздик (железо Fe)
С правилами техники безопасности ознакомлен (а).
Ход работы
Что делали
|
Что наблюдали, выводы.
|
Уравнение реакции
|
В пробирках находятся растворы гидроксида натрия, хлорида бария, карбоната натрия, опытным путем определить в какой пробирке находится каждое вещество
|
Н2SO4
↓ ↓ ↓
  
1 2 3
|
1.____________________
_____________________
_____________________
_____________________
_____________________
2.____________________
_____________________
_______________________________________________________________3.____________________
____________________________________________________________________________________
|
1._____________________________________
_______________________________________
2._____________________________________
_______________________________________
3._____________________________________
_______________________________________
|
Получить сульфат железа (II) из железа, доказать опытным путем наличие ионов железа (II) в растворе.
|
а). Получение сульфата железа (II)
↓_________

__________
|
____________________
_____________________
_____________________
_____________________
_____________________
|
|
б). Определение ионов железа (II)
↓_________

__________
|
____________________
_____________________
_____________________
_____________________
_____________________
|
|
Оценка _________
Дата________ ФИ______________________
Практическая работа № 3
Решение экспериментальных задач по теме «Подгруппа галогенов»
Цель: применить знания, полученные при изучении темы «Неметаллы подгруппы галогенов», в экспериментальном решении задач. Продолжить формировать умения и навыки работать с лабораторным оборудованием, реактивами, соблюдая технику безопасности
Оборудование: пробирки, штатив для пробирок
Реактивы: растворы соляной кислоты (HCl), карбоната натрия (Na2 CO3) гидроксида натрия (NaOH), нитрата серебра (AgNO3), хлорида натрия (NaCl), бромида натрия(NaBr),
иодида натрия (NaI), гранулы цинка(Zn), медная проволока (Cu). Оксид меди (II) (CuO). индикатор фенолфталеин
С правилами техники безопасности ознакомлен (а).
Ход работы
Что делали
|
Что наблюдали, выводы.
|
Уравнение реакции
|
Задача 1. Изучение свойств соляной кислоты
|
А) взаимодействие с металлами
↓ HCl ↓
 
2
Zn Cu
|
1.____________________
_____________________
_____________________
_____________________
_____________________
_____________________
2.____________________
_____________________
___________________________________________________________________________________
|
1._______________________________________
_______________________________________
2.________________________________________
__________________________________________
|
Б) взаимодействие с основными оксидами
HCl
↓
CuO
Пробирку закрепить в пробиркодержателе и нагреть (правила нагревания!)
|
____________________
_____________________
_____________________
_____________________
_____________________
_____________________
_______________________________________________________________
|
_______________________________________
__________________________________________
|
В) взаимодействие с солями
HCl
↓

Na2 CO3
|
____________________
_____________________
_____________________
_____________________
_____________________
_____________________
|
_______________________________________
__________________________________________
|
2. Задача 2. Качественные реакции на анионы галогенов. Определите с помощью характерных реакций каждое из выданных вам веществ: хлорид натрия, бромид натрия, иодид натрия
|
AgNO3
↓ ↓ ↓
  
1 2 3
|
1.___________________
_____________________
_____________________
_____________________
_____________________
2.___________________________________________________________________________________3.__________________________________________________________________________________________________________________________
|
1.
__________________________________________
__________________________________________
2.
__________________________________________
__________________________________________
3. __________________________________________
__________________________________________
|
Оценка _________
Дата________ ФИ______________________
Практическая работа № 3
Решение экспериментальных задач по теме «Подгруппа кислорода»
Цель: применить знания, полученные при изучении темы «Неметаллы подгруппы кислорода», в экспериментальном решении задач. Продолжить формировать умения и навыки работать с лабораторным оборудованием, реактивами, соблюдая технику безопасности
Оборудование: пробирки, штатив для пробирок
Реактивы: растворы поваренной соли (хлорида натрия -NaCl), хлорида бария (ВаCl2) серной кислоты (Н2SO4), гранулы цинка(Zn), индикатор лакмус
С правилами техники безопасности ознакомлен (а).
Ход работы
Что делали
|
Что наблюдали, выводы.
|
Уравнение реакции
|
Задача 1. Провести реакции, подтверждающие качественный состав серной кислоты. Написать уравнения реакции.
|
Индикатор BaCl2
↓ ↓
 
2
H2SO4
|
1.____________________
_____________________
_____________________
_____________________
_____________________
_____________________
2.____________________
_____________________
___________________________________________________________________________________
|
1._______________________________________
_______________________________________
2.________________________________________
__________________________________________
|
Задача 2. В пробирку положите 1-2 гранулы цинка. Прилейте в неё 2-3 мл серной кислоты. Что наблюдаете? Составьте уравнение методом электронного баланса, укажите окислитель и восстановитель.
|
↓ H2SO4

Zn
|
____________________
_____________________
_____________________
_____________________
_____________________
|
__________________________________________
__________________________________________
|
Задача 5. Определить, содержит ли поваренная соль примесь сульфатов ( сульфата натрия)
Написать уравнения реакций в молекулярном и ионном виде
|
BaCl2
↓

Раствор поваренной соли .
|
____________________
_____________________
_____________________
_____________________
_____________________
|
__________________________________________
__________________________________________
|
Оценка _________
Дата________ ФИ_______________
Практическая работа № 5
Получение и собирание газов
Цель: изучить лабораторные способы получения, собирания и распознавания газов. Продолжить формировать умения и навыки работать с лабораторным оборудованием, реактивами, соблюдая технику безопасности
Оборудование: пробирки, штатив для пробирок, лучина, хим. стаканы, вата,
Реактивы: перманганат калия (KMnO4), гидроксид кальция (Ca(OH)2). Хлорид аммония(NH4Cl), карбонат кальция (СаСО3), соляная кислота (HCl), индикатор универсальный
С правилами техники безопасности ознакомлен (а).
Ход работы
Что делали
|
Что наблюдали, выводы.
|
Уравнение реакции
|
|
1) Получение
Собрать прибор
KMnO4
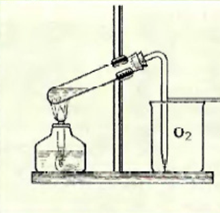
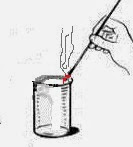
2) Распознавание:
|
1.____________________
_____________________
_____________________
_____________________
_____________________
_____________________
2.____________________
_____________________
___________________________________________________________________________________
|
1._______________________________________
_______________________________________
2.________________________________________
__________________________________________
|
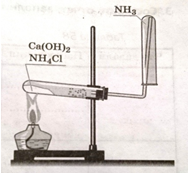
Получение, собирание и распознавание аммиака
|
1) Получение: Собрать прибор
|
1___________________
_____________________
_____________________
_____________________
_____________________
_______________________________________________________________
|
1_________________________________________
__________________________________________
|
2) Распознавание:
поднести к пробирке с аммиаком влажный универсальный индикатор
|
2.____________________
_____________________
_____________________
_____________________
_____________________
|
2._____________________________________
__________________________________________
|
Получение собирание и распознавание углекислого газа
|
1.. Получение
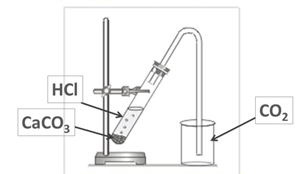
2. Распознавание
В стакан с углекислым газом долить известковую воду (гидроксид кальция)
|
1.___________________
_____________________
_____________________
_____________________
_____________________
________________________________________
2.____________________
_____________________
___________________________________________________________________________________
|
1._________________________________________
_______________________________________
2.________________________________________
__________________________________________
|
Оценка_________ |
|
|
 Скачать 189.35 Kb.
Скачать 189.35 Kb.




