03 вар_2 кр(эл). Задание к контрольной работе Провести анализ лекарственного средства по требованиям фармакопейной статьи Ацетилсалициловая кислота
 Скачать 492.5 Kb. Скачать 492.5 Kb.
|
|
Контрольная работа 2, вариант 3 Задание к контрольной работе № 2. Провести анализ лекарственного средства по требованиям фармакопейной статьи «Ацетилсалициловая кислота» (ГФ XII). Привести последовательность определения по каждому параметру ФС, дать краткую характеристику метода определения, если необходимо – привести уравнения химических реакций и расчетные формулы. Ацетилсалициловая кислота ФС.2.1.0006.15 Аспирин Взамен ГФ XII, ч. 1, ФС 42-0220-07; Acidum acetylsalicylicum взамен ФС 42-0040-00 2-(Ацетилокси)бензойная кислота  С9Н8O4 М. м. 180,16 Cодержит не менее 99,5 % ацетилсалициловой кислоты С9Н8O4 в пересчете на сухое и свободное от остаточных органических растворителей вещество. ОписаниеБелый или почти белый кристаллический порошок или бесцветные кристаллы без запаха или со слабым запахом. Цвет следует характеризовать названиями: белый, синий, зеленый, желтый, оранжевый, красный и т. п. При оттеночных цветах на первом месте указывают тот цвет, который содержится в меньшей доле, а затем через дефис - преобладающий цвет (например, красно-коричневый). Слабоокрашенные образцы имеют оттенок цвета, название которого характеризуют суффиксом «-оват» (например, «желтоватый») или указывают «светло-» (например, «светло-желтый»). Цвет твердых веществ следует определять на матово-белом фоне (белая плотная или фильтровальная бумага) при рассеянном дневном свете в условиях минимального проявления тени. Небольшое количество вещества помещают на белую бумагу и без нажима равномерно распределяют по поверхности бумаги (осторожно разравнивают шпателем или другим приспособлением) так, чтобы поверхность оставалась плоской. Запах. Запах следует характеризовать терминами: «без запаха», «с характерным запахом», «со слабым характерным запахом». Испытание проводят сразу после вскрытия упаковки. 0,5 – 2,0 г препарата равномерно распределяют на часовом стекле диаметром 6 - 8 см; через 15 мин определяют запах на расстоянии 4 - 6 см или делают вывод о его отсутствии. В случае легко летучих жидкостей наносят 0,5 мл на фильтровальную бумагу и запах определяют сразу же после нанесения, если нет других указаний в частной фармакопейной статье. РастворимостьЛегко растворим в спирте 96 %, растворим в хлороформе, мало растворим в воде. Растворимость - свойство вещества растворяться в разных растворителях. Субстанция растворима в хлороформе, легко растворима 96% спирте, мало в воде. При оценке растворимости в спирте берут 1 г субстанции и вносят в отмеренное количество растворителя (1 мл 96% спирта) и непрерывно встряхивают в течение 10 минут при 20 ± 2°С. препарат считают растворившимся (легко растворим), если в растворе при наблюдении в проходящем свете не обнаруживаются частицы вещества. Если препарат не растворяется, то следует добавлять растворитель до 10 мл. При оценке растворимости в хлороформе берут 1 г субстанции и вносят в отмеренное количество растворителя (10 мл хлороформа) и непрерывно встряхивают в течение 10 минут при 20 ± 2°С. препарат считают растворившимся (растворим), если в растворе при наблюдении в проходящем свете не обнаруживаются частицы вещества. Если препарат не растворяется, то следует добавлять растворитель до 30 мл. При оценке растворимости в воде берут 10 мг субстанции и вносят в отмеренное количество растворителя (1 мл воды) и непрерывно встряхивают в течение 10 минут при 20 ± 2°С. препарат считают растворившимся (мало растворим), если в растворе при наблюдении в проходящем свете не обнаруживаются частицы вещества. Если препарат не растворяется, то следует добавлять растворитель до 10 мл. Подлинность
ИК –спектр химического соединения является одной из его наиболее важных характеристик. ИК область спектра занимает диапазон длин волн от границы видимой до микроволновой области (0,75 до 200 мк). Однако, обычно под ИК областью подразумевают более узкий интервал от 2,5 до 16 мк. (Более коротковолновый и длинноволновый участки спектры называют соответственно ближней и дальней ИК областями. Для характеристики ИК излучения более часто используют волновые числа (величины обратные длинам волн – обратные сантиметры, см -1). При облучении образца ИК светом с непрерывно меняющейся частотой определенные участки спектра излучения поглощаются молекулой, а луч проходящий через вещество ослабляется в области поглощения. Регистрируя интенсивность прошедшего излучения в зависимости от длин волн (или волновых чисел), получают кривую, на которой видны полосы поглощения. Это и есть ИК-спектр. В наблюдаемом спектре не должно обнаруживаться различия со спектром стандартного образца. 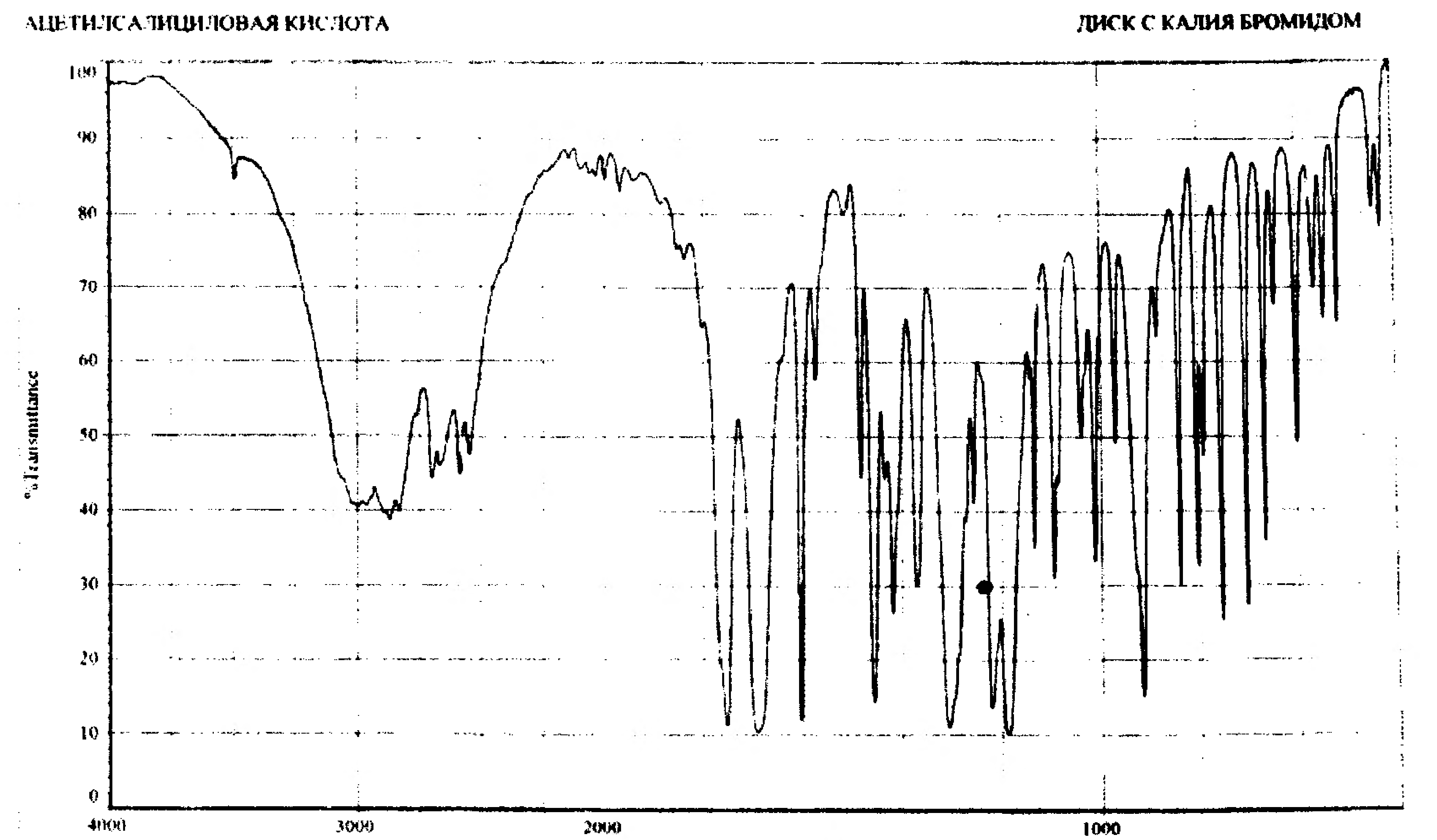
Спектр поглощения в УФ–области выражают в виде графической зависимости оптической плотности (D) или молярного коэффициента поглощения ( В наблюдаемых спектрах не должно обнаруживаться различия со спектром стандартного образца и должны присутствовать указанные минимумы и максимумы поглощения
При кипячении с раствором гидроксида натрия происходит гидролиз 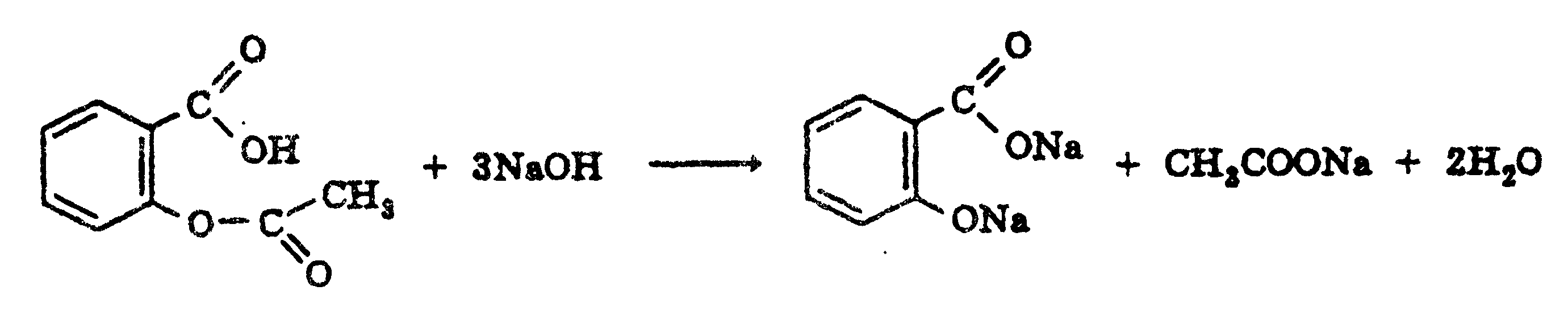 Подкисление серной кислотой дает нерастворимый осадок салициловой кислоты: 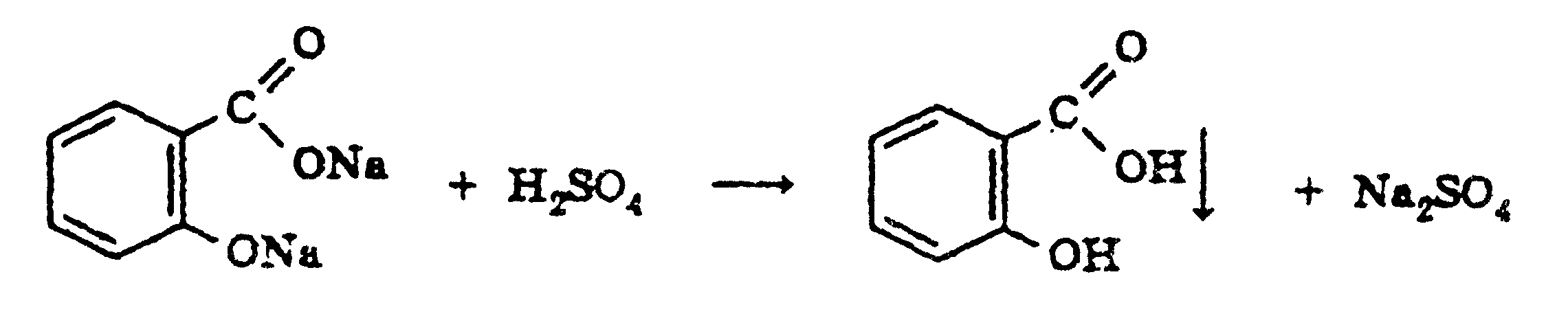 Салициловая кислота дает комплекс с железом (фиолетовое окрашивание): 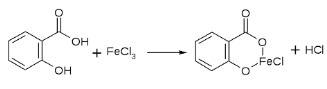
При добавлении серной кислоты протекает кислотный гидролиз с образованием салициловой кислоты и уксусной кислоты:  Прибавляют 0,1 мл формалина; появляется розовое окрашивание: 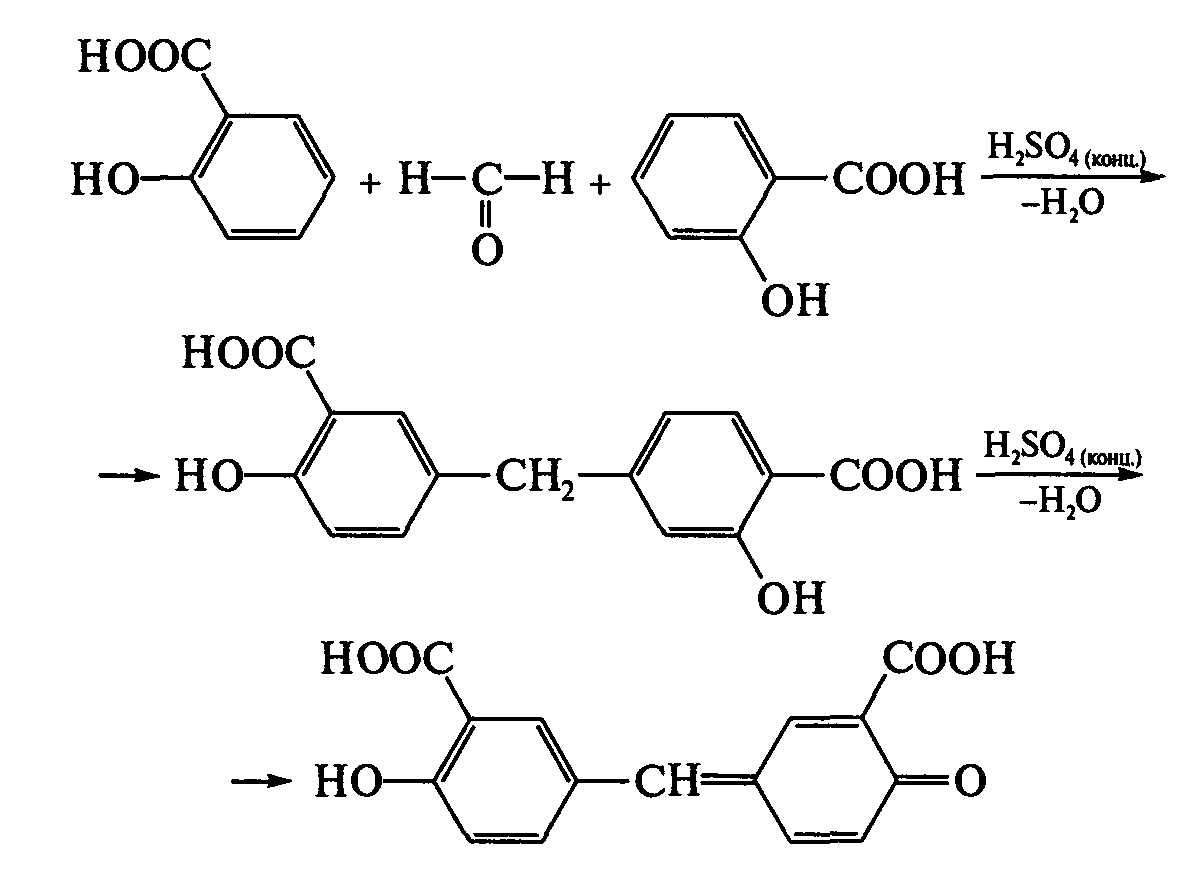 Формалин взаимодействует с салициловой кислотой с образованием арилметанового красителя. Прозрачность раствораРаствор 2 г субстанции в 20 мл спирта 96 % должен быть прозрачным (ОФС «Прозрачность и степень мутности жидкостей»). Прозрачность раствора ацетилсалициловой кислоты определяют путем сравнения испытуемого раствора с эталоном визуально. Испытание проводят в пробирках с притертой пробкой из прозрачного бесцветного стекла с внутренним диаметром около 15 мм при освещении электрической лампой матового стекла мощностью 40 Вт, расположенной над образцом. Раствор считают прозрачным, если он по прозрачности не отличается эталона I Цветность раствораРаствор, полученный в испытании на «Прозрачность раствора», должен быть бесцветным (ОФС «Степень окраски жидкостей»). Испытания проводят в одинаковых пробирках из бесцветного, прозрачного, нейтрального стекла с внутренним диаметром от 15 до 25 мм, используя равные слои высотой 40 мм испытуемой жидкости и эталона сравнения В9, описанного в статье. Сравнивают окраску в дневном отраженном свете сверху вдоль вертикальной оси пробирок на матово-белом фоне. Вещества, нерастворимые в растворе натрия карбоната0,5 г субстанции растворяют в 10 мл теплого 10 % раствора натрия карбоната. Полученный раствор должен быть прозрачным. Таким образом оценивают возможные нерастворимые примеси. Кислота ацетилсалициловая растворяется в растворе карбоната натрия с образованием натриевой растворимой соли. Если присутствуют примеси то они остаются в виде нарастворимого осадка. Сравнивают с эталоном I. Родственные примесиОпределение проводят методом ВЭЖХ. Испытуемый раствор. Около 0,1 г субстанции (точная навеска) помещают в мерную колбу вместимостью 10 мл, растворяют в ацетонитриле и доводят объем раствора ацетонитрилом до метки. Раствор сравнения. Около 0,05 г стандартного образца салициловой кислоты (точная навеска) помещают в мерную колбу вместимостью 50 мл, растворяют в подвижной фазе (ПФ) и доводят объем раствора ПФ до метки. 1 мл полученного раствора помещают в мерную колбу вместимостью 100 мл и доводят объем раствора ПФ до метки. Раствор для проверки пригодности хроматографической системы. 0,01 г стандартного образца салициловой кислоты растворяют в 10 мл ПФ. 1,0 мл полученного раствора помещают в мерную колбу вместимостью 100 мл, прибавляют 0,2 мл испытуемого раствора и доводят объем раствора ПФ до метки. Используют свежеприготовленные растворы. Хроматографические условия
Хроматографируют раствор для проверки пригодности хроматографической системы. Разрешение (R) между пиками ацетилсалициловой кислоты и салициловой кислоты должно быть не менее 6. Хроматографируют испытуемый раствор и раствор сравнения. Время регистрации хроматограммы испытуемого раствора должно не менее чем в 7 раз превышать время удерживания ацетилсалициловой кислоты. На хроматограмме испытуемого раствора площадь пика любой примеси должна быть не более площади пика на хроматограмме раствора сравнения (не более 0,1 %); суммарная площадь пиков примесей должна не более чем в 2,5 раза превышать площадь пика на хроматограмме раствора сравнения (не более 0,25 %). ВЭЖХ – серийный метод определения органических соединений многих классов; его широко используют при анализе различных лекарственных средств с целью установления их подлинности, чистоты и количественного содержания. Высокоэффективная жидкостная хроматография выполняется под повышенным давлением жидкости до 666,5 кПа (500 атм.). Разделение смеси происходит в колонке, заполненной сорбентом с очень малым размером зерен (3-5 мк), и это является основной особенностью ВЭЖХ, поскольку обеспечивает быстрый перенос при высокой эффективности разделения. Важной особенностью ВЭЖХ является возможность проведения процесса при комнатной температуре, что ценно при исследовании неустойчивых соединений. Разделение смеси достигается за счет различия в сродстве компонентов смеси к неподвижной и подвижной фазам. 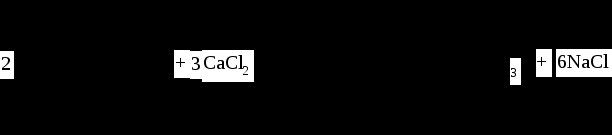 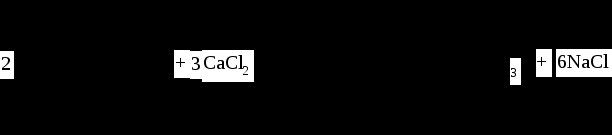 ХлоридыНе более 0,004 % (ОФС «Хлориды»). 1,5 г субстанции взбалтывают в течение 2 мин с 30 мл воды и фильтруют, отбирают для анализа 10 мл фильтрата. Допустимая примесь. Испытания основаны способности ионов серебра образовывать с хлоридами, в зависимости от их содержания, белый творожистый осадок, белую муть или опалесценцию, не исчезающие от прибавления азотной кислоты. Поэтому определение проводят в азотнокислой среде: Ag+ + Cl- → AgCl↓ Для приготовления эталонного раствора хлорид-ионов, навеску прокаленного хлорида натрия массой 0,0660 г растворяют водой в мерной колбе на 100 мл и доводят раствор до метки (раствор А). 0,5 мл раствора А разбавляют водой до 100 мл (раствор Б). Этот раствор является эталонным и содержит 2 мкг иона С1- в 1 мл. Готовят серию стандартных растворов хлорид-ионов добавляют нитрат серебра в растворы сравнения и в испытуемый раствор. Сравнивают с эталоном и делают вывод о содержании хлорид ионов. СульфатыНе более 0,02 % (ОФС «Сульфаты»). Для анализа отбирают 10 мл фильтрата, полученного в испытании на «Хлориды». Допустимая примесь. Растворы сульфатов в зависимости от их концентрации образуют с растворами солей бария белый осадок или муть, не исчезающие от прибавления разведенной хлористоводородной кислоты. Предельная чувствительность реакции 0,003 мг (3 мкг) сульфат-иона в 1 мл раствора. 0,01 мг (10 мкг) сульфат-иона в 1 мл раствора дает при этой реакции через 10 мин заметную муть. Определение проводят следующим образом: к 10 мл раствора испытуемого препарата, приготовленного, как указано в соответствующей частной статье, прибавляют 0,5 мл разведенной хлористоводородной кислоты и 1 мл раствора хлорида бария, перемешивают и через 10 мин сравнивают с эталоном, состоящим из 10 мл эталонного раствора Б и такого же количества реактивов, какое прибавлено к испытуемому раствору. Муть, появившаяся в испытуемом растворе, не должна превышать эталон. Эталонный раствор сульфат-иона. 1,814 г сульфата калия, высушенного при температуре от 100 до 105°С до постоянной массы, растворяют в воде в мерной колбе вместимостью 1 л и доводят объем раствора водой до метки (раствор А). 10 мл раствора А помещают в мерную колбу вместимостью 1 л и доводят объем раствора водой до метки (раствор Б). Этот раствор содержит 0,01 мг (10 мкг) сульфат-иона в 1 мл. Потеря в массе при высушиванииНе более 0,5 % (ОФС «Потеря в массе при высушивании», способ 1, температура от 80 до 85 ºС). Для определения используют около 1,0 г (точная навеска) субстанции. Проведем моделирование. Подготовить бюкс: помыть, высушить, довести до постоянной массы. Доведенным до постоянной массы считают в том случае, если последующее взвешивание отличается от предыдущего не более чем на 0,0005 г. mбюкса 19,4567 г. 2. На весах отвечать необходимое количество исследуемого вещества. m вещества+бюкса = 20,4598 г. 3. Сушат до постоянной массы (условия высушивания, температура и навеска приводятся в соответствующих частных статьях). По истечении времени бюкс достать и поместить в эксикатор для охлаждения. Взвесить. m вещества+бюкса = 20,4579 г. 4. Рассчитать массу препарата до высушивания: m вещества= m вещества+бюкса - mбюкса = 20,4598-19,4567 = 1,0031 5. Рассчитать массу препарата после высушивания: m вещества= m вещества+бюкса - mбюкса = 20,4579-19,4567 = 1,0012 6. Рассчитать процентное содержание воды: где m – масса лекарственного препарата до высушивания, m1 – масса после высушивания, ω – массовая доля воды в препарате, %. Соответствует требованиям. Сульфатная золаНе более 0,1 % (ОФС «Сульфатная зола»). Для определения используют около 0,5 г (точная навеска) субстанции. Сульфатная зола характеризует наличие минеральных примесей. Фарфоровый, кварцевый или платиновый тигель прокаливают при температуре 550-650 ºС в течение 30 мин, охлаждают в эксикаторе над силикагелем или другим подходящим осушителем и точно взвешивают по окончании каждого прокаливания. Точную навеску испытуемого вещества помещают в предварительно прокаленный тигель, смачивают 1 мл серной кислоты концентрированной и осторожно (избегая сильного вспенивания вещества) нагревают на пламени, песчаной бане или электрической плитке с закрытым нагревательным элементом и терморегулятором до обугливания. После охлаждения смачивают остаток 1 мл серной кислоты концентрированной и осторожно нагревают до удаления паров серной кислоты. Затем тигель помещают в муфельную печь и прокаливают при температуре 550-650 ºС до тех пор, пока остаток полностью не превратится в пепел. При этом следует избегать появления пламени, сплавления золы и спекания ее со стенками тигля. По окончании прокаливания тигель охлаждают в эксикаторе, взвешивают и рассчитывают процентное содержание остатка. В случае получения результата, превышающего допустимый предел, указанный в фармакопейной статье, остаток вновь смачивают серной кислотой концентрированной, сжигают в течение 30 мин, прокаливают до постоянной массы или до тех пор, пока два последовательных результата взвешивания не будут отличаться не более чем на 0,5 мг или содержание остатка не будет удовлетворять указанному пределу. Проведем математическое моделирование mтигля 31,9658 г. 1. На весах отвешать необходимое количество исследуемого вещества. m вещества+тигля = 32,4312 г. 2. По завершении процедуры тигль помещают в эксикатор для охлаждения. Взвесить. m зола+тигель = 31,4660 г. 3. Рассчитать массу препарата до обработки: m вещества= m вещества+тигля - mтигля = 32,4312-31,9658 = 0,4654 г 4. Рассчитать массу золы после прокаливания: m золы= m зола+тигля - mтигля = 31,9660-31,9658 = 0,0002 г 5. Рассчитать процентное содержание золы: Соответствует требованиям. Тяжелые металлыНе более 0,002 %. Определение проводят в соответствии с требованиями ОФС «Тяжёлые металлы» в зольном остатке, полученном после сжигания 0,5 г субстанции (ОФС «Сульфатная зола»). Устанавливаемые пределы содержания тяжелых металлов в фармацевтических субстанциях определяются максимальной суточной дозой препарата, произведенного из данной субстанции, и длительностью его возможного применения (согласно Инструкции по медицинскому применению). Испытуемый раствор. Зольный остаток, полученный после сжигания 0,5 г испытуемого образца в присутствии серной кислоты концентрированной, обрабатывают при нагревании на сетке 2 мл насыщенного раствора аммония ацетата, нейтрализованного раствором натрия гидроксида, прибавляют 3 мл воды и фильтруют в пробирку через беззольный фильтр, предварительно промытый 1 % раствором уксусной кислоты, а затем горячей водой. Тигель и фильтр промывают 5 мл воды, пропуская её через тот же фильтр в ту же пробирку. Эталонный раствор. В тигель помещают серную кислоту концентрированную в количестве, взятом для сжигания испытуемого образца и далее поступают как с испытуемым образцом, но промывание тигля и фильтра производят лишь 3 мл воды, после чего к фильтрату прибавляют 2 мл стандартного раствора свинец-иона (5 мкг/мл). Контрольный раствор. Готовят так же, как и испытуемый раствор, но без испытуемого образца. Далее используют метод 1 или метод 2. Метод 1. К полученным растворам прибавляют по 1 мл уксусной кислоты разведенной 30%, 2 капли 2% раствора натрия сульфида, перемешивают и через 1 мин сравнивают окраску растворов. В сравниваемых растворах допустима слабая опалесценция от выделившейся серы. Метод 2. К полученным растворам прибавляют по 2 мл ацетатного буферного раствора рН 3,5, перемешивают, прибавляют по 1 мл тиоацетамидного реактива, перемешивают и через 2 мин сравнивают окраску растворов. Стандартные растворы свинец-иона Стандартный раствор 100 мкг/мл свинец-иона 0,0799 г свинца нитрата помещают в мерную колбу вместимостью 500,0 мл и растворяют в 50 мл воды с добавлением 0,5 мл азотной кислоты концентрированной, доводят объем раствора водой до метки и перемешивают. Стандартный раствор 5 мкг/мл свинец-иона 5,0 мл стандартного раствора свинец-иона (100 мкг/мл свинец-иона) помещают в мерную колбу вместимостью 100 мл, доводят объем раствора водой до метки и перемешивают. Срок хранения – 1 сут. Остаточные органические растворителиВ соответствии с требованиями ОФС «Остаточные органические растворители». Оценивают методом газовой хроматографии. Остаточные органические растворители – это растворители, которые используются на любой стадии производства лекарственного средства и полностью не удаляются после завершения технологического процесса. Оценка содержания остаточных растворителей в ГX осуществляется по параметрам удерживания, к которым относятся: время удерживания (τr, приведенное время удерживание (τя), относительное удерживание (τотн) и некоторые другие характеристики, например, индексы Ковача, индивидульные для каждого отдельно взятого растворителя. Для расшифровки хроматограмм с целью идентификации составляющих ее пиков чаще пользуются методом эталонных веществ или их смесей. Один вариантов этого метода состоит в последовательном хроматографировании анализируемой и эталонной смеси в одинаковых условиях. Равенство времени удерживания пиков соответствующих компонентов обеих смесей может служить основанием для идентификации. Другой вариант заключается в том, что в исследуемую смесь вводят эталонный компонент, наличие которого в этой смеси предполагают. Увеличение высоты соответствующего пика /без его расширения/ по сравнению с высотой этого пика на хроматограмме, полученной до введения эталона, может свидетельствовать о присутствии искомого соединения в анализируемой смеси. Количественную оценку проводят по: высоте пика; ширине пика или площади пика. Микробиологическая чистотаВ соответствии с требованиями ОФС «Микробиологическая чистота». В нестерильных лекарственных средствах допускается наличие лимитированного количества микроорганизмов, при отсутствии определенных видов бактерий, представляющих опасность для здоровья человека. Используют один из вариантов чашечного агарового метода (глубинный, двухслойный, поверхностный, модифицированный глубинный), метод мембранной фильтрации или пробирочный метод наиболее вероятных чисел (НВЧ). Чашечный агаровый метод Для культивирования микроорганизмов используют агаризованные питательные среды: соево-казеиновый агар или среду № 1, сухую, для контроля микробной загрязненности - для выращивания бактерий, агар Сабуро или среду № 2, сухую, для контроля микробной загрязненности - для выращивания грибов. Для выращивания бактерий инкубируют при температуре (32,5 ± 2,5) °С, а на среде для грибов - при температуре (22,5 ± 2,5) °С. Для каждого разведения образца используют не менее 2-х чашек Петри с определенной средой. После расплавления среды охлаждают до температуры (45 ± 5) °С и вносят в чашки Петри в необходимом количестве. Глубинный метод Образец, приготовленный для анализа, в количестве 1 мл вносят в стерильную чашку Петри диаметром 90 мм. Добавляют 15-20 мл агаризованной питательной среды и быстро перемешивают вращательными движениями. После застывания агара чашки переворачивают и инкубируют посевы. Подсчет колоний производят через 48-72 ч (предварительные результаты) и через 5 сут (окончательные результаты). Отбирают чашки, где число колоний бактерий на фильтрах не превышает 100, а грибов - 50, и рассчитывают число микроорганизмов на 1,0 г, или на 1,0 мл образца, или на 1 пластырь. 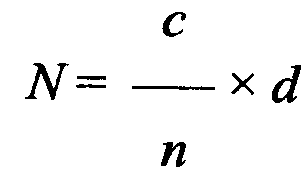 Количественное определениеОколо 0,5 г субстанции (точная навеска) растворяют в 10 мл нейтрализованного по фенолфталеину и охлажденного до температуры 8 – 10 ºС спирта 96 % и титруют 0,1 М раствором натрия гидроксида до появления розового окрашивания (индикатор – 0,1 мл 1 % раствора фенолфталеина). Параллельно проводят контрольный опыт. 1 мл 0,1 М раствора натрия гидроксида соответствует 18,02 мг ацетилсалициловой кислоты С9Н8O4. Титрование протекает по схеме:  Содержание кислоты ацетилсалициловой в процентах (Х) в препарате вычисляется по формуле: Где V – объем 0,1 н раствора щелочи, К – поправочный коэффициент, Т – 0,018 г/мл, а – масса навески . f =1,  ХранениеВ плотно укупоренной упаковке. Список литературы 1. Фармацевтическая химия: учеб. пособие для вузов/ ред. А. П. Арзамасцев. М.: «ГЭОТАР-Медиа»,2005. – 635 с. 2. Беликов В.Г. Фармацевтическая химия в 2 - х частях / Учеб. для фарм. инст. и фарм. факул. мед. инст. - Ч. 1. - М.: Высшая школа, 1993. - 432 с. Ч. 2. - Пятигорск, 1996. - 608 с. 3. Руководство к лабораторным занятиям по фармацевтической химии: Учеб. Пособие. ред. А.П. Арзамасцев. М:.:Медицина, 2004. 4. Кулешова М.И., Гусева Л.Н., Сивицкая О.К. Анализ лекарственных форм, изготовляемых в аптеках. / Изд. 2-е перераб. и доп. - М.: Медицина, 1989. - 288 с. 5. Лабораторные работы по фармацевтической химии: Учеб. пособие для фарм. инст. и фарм. факул. мед. инст. / Беликов В.Г., Вергейчик Е.Н., Годяцкий В.Е. и др. - М.: Высшая школа, 1989. - 375 с. 6. Фармацевтическая химия: руководство к практическим занятиям для студентов, обучающихся по специальности 060108 фармация / Е.С. Гагарина, А.В. Озерская, Н.В. Кувачева и др. – Красноярск: типография КрасГМУ, 2009. – 176 с. 7. Дудко В.В., Тихонова Л.А. Анализ лекарственных веществ по функциональным группам. – Томск, 2004. – 137 с. |
