тема 1-4 раздаточный материал. 14 темы Определения
 Скачать 302.85 Kb. Скачать 302.85 Kb.
|
|
Основные средства измерения: Спектофотометры - cравнение светового потока, прошедшего через исследуемое вещество со световым потоком контрольного раствора; Колориметры фотоэлектрические концентрационные - cравнение светового потока, прошедшего через исследуемое вещество со световым потоком контрольного раствора; Иономеры- потенциометрическое измерение водородного показателя (рН); рН-метры - потенциометрическое измерение водородного показателя (рН); Анализатор жидкости кондуктометр. лаборат. «МАРК-603/1» - измерение УЭП или условной концентрации растворённых веществ в пересчёте на NaCl; Кондуктометр электронный автоматический «ЭКА-2» - измерение УЭП или условной концентрации растворённых веществ в пересчёте на NaCl; Анализатор ПАИС-02рNa- анализатор для оперативного контроля активности ионов натрия (рNa) в технологических жидкостях; Анализатор жидкости «Флюорат-02-3М»- измерение массовой концентрации неорганических и органических примесей в воде; Весы лабораторные- определение массы вещества; Барометр-измерение атмосферного давления; Прибор комбинированный - измерение относительной влажности, температуры воздуха; Газоанализаторы - измерение содержания кислорода, метана, водорода и суммы углеводородов; Психрометр аспирационный - определение влажности газообразных сред; Анализатор растворенного кислорода- определение растворенных газов в жидких средах; Анализатор кислорода портативный многофункциональный АКПМ-02-ГМ- измерение концентрации кислорода в газообразных средах; Термометр- измерение температуры образца; Секундомер механический СОС пр.- измерение времени. Основное испытательное оборудование: Электропечь SNOL 58/350- тепловая обработка материалов; Центрифуга лабораторная «LMC-3000»-центрифугирование проб; Холодильник компрессионный двухкамерный «ATLANТ» - хранение реактивов, рабочих растворов и стандартных образцов. Основное вспомогательное оборудование: Аквадистиллятор; Деионизатор мембранный; Плита нагревательная; Колбонагреватель; Перемешивающее устройство; Пробоотборник переносной; Ведро эмалированное; Устройство для сушки лабораторной посуды; Баня лабораторная. Каждая единица оборудования вносится в ученные карточки. В ПАО «ТГК-1» для обеспечения контроля СИ введена в эксплуатацию «Автоматизированная система обработки метрологической информации» (далее «АСОМИ»). Ответственным за ведением является менеджер по качеству. Данное оборудование находится на балансе ХЛ ХЦ. При вводе нового оборудования менеджер по качеству проводит обучение персонала и вносит информацию в тетрадь. Требования охраны труда при работе с вредными веществами и веществами 1 класса опасности. Все работы, связанные с применением, выделением или образованием едких, ядовитых, огне- или взрывоопасных веществ, должны проводиться в вытяжном шкафу при включенной местной вытяжной вентиляции. Применение естественной вентиляции и рециркуляции воздуха не допускается.. В помещении лаборатории должно находиться не менее двух работников. В случае отсутствия в вытяжном шкафу отверстий, предназначенных для рук, створки вытяжного шкафа во время работы можно поднимать на 20-30 см (так, чтобы в шкафу находились только руки). Сыпучие вредные вещества необходимо взвешивать в специально предназначенных для этих целей сосудах, а агрессивные и ядовитые вещества — в сосудах с притертыми пробками. Кислоты, щелочи и другие едкие и ядовитые вещества, а также пробы анализируемой воды должны набираться в пипетку при помощи резиновой груши или отбираться автоматической пипеткой или шприцем. Перед взбалтыванием растворов в колбах или пробирках необходимо закрывать их притертыми пробками. Запрещается наклоняться над сосудом, в котором происходит нагревание жидких едких и ядовитых химических веществ. Переливание едких жидкостей из бутыли в сосуд необходимо производить с помощью стеклянного сифонного устройства в вытяжном шкафу при включенной вентиляции. Раствор серной кислоты следует приготавливать, вливая ее в воду тонкой струйкой мелкими порциями при непрерывном помешивании. Запрещается наливать воду в серную кислоту во избежание возможного вскипания и выброса жидкости из сосуда. При кипячении емкости с растворами следует наполнять не более чем на ¾ их объема. Вещества 1 класса опасности следует хранить в вентилируемых закрытых и опечатанных шкафах (сейфах) в соответствии со специальными инструкциями. Ключ от шкафов должен храниться у начальника лаборатории. Пролитые на пол (стол) химические растворы и растворители следует немедленно нейтрализовать и убрать при помощи опилок или сухого песка, а пол (стол, стеллаж) протереть ветошью, смоченной соответствующим растворителем, после чего облитое место тщательно вымыть водой с моющим средством или 10% раствором соды. Эти работы следует проводить с использованием СИЗ (противогазов, респираторов, хлорвиниловых или резиновых перчаток). Пролитое или просыпанное на пол (стол) вещество 1 класса опасности необходимо засыпать опилками или песком, осторожно собрать и нейтрализовать. Участки пола или стола после этого следует обработать хлорной известью и тщательно промыть водой. При нейтрализации пролитой азотной кислоты следует применять фильтрующий противогаз. Фильтры, бумагу, использованные при работе с веществами 1 класса опасности, необходимо складывать в плотно закрывающиеся емкости для их дальнейшей утилизации. Запрещается сливать и сбрасывать в канализацию отходы химических реактивов и органических растворителей. Отходы следует собирать в специальные емкости, а также нейтрализовать их кислотой или щелочью и утилизировать. В случае попадания попадания хромовых растворов следует промыть в течение 10-15 минут быстротекущей струей воды, а затем обработать 5% гипосульфита натрия (при попадания в глаза- 1% раствором) Закон эквивалентов. Расчеты при титровании. «Массы элементов, реагирующих друг с другом, пропорциональны их эквивалентам»: число моль эквивалентов для всех веществ, участвующих в реакции, одинаково. Главное уравнение для расчетов при титровании: Сн1 х V1 = Сн2 х V2 ( Э1=Э2) т.е. произведение нормальной концентрации растворенного вещества, умноженное на объем его раствора равно произведению нормальной концентрации титранта, умноженное на объем, пошедший на титрование. Для кислотно-щелочного титрования Сн к х Vк = Сн щ х Vщ Для комплексонометрического титрования Сн ж х Vж = Сн тр х Vтр Для пересчета нормальной концентрации в г/дм3 нужно нормальную концентрацию в г-экв/дм3 ( мг-экв/дм3) умножить на моль-эквивалент вещества. Для соляной кислоты 1 моль-экв HCl = 36,5г , для серной кислоты 1 моль-экв H2SO4 = 49г. Для грубого пересчета в %-ную концентрацию разделим количество г/дм3 на 10. Титрование, титрованные растворы. Титры и поправочные коэффициенты. Титриметрический метод анализа основан на введении в точно измеренный объем раствора анализируемого вещества точно отмеренного объема раствора известной концентрации - титранта. Титрант вводится до тех пор, когда анализируемое вещество полностью прореагирует с ним. Основными титриметрическими методами на ТЭЦ являются кислотно-основное и комплексонометрическое титрование. Титр - число граммов растворённого вещества в 1 см3 раствора Т= m в-ва / V р-ра в см3 Способы выражения концентрации растворов. Молярные и нормальные растворы. Моль вещества – количество вещества, содержащее столько же молекул, сколько атомов содержится в 12 г углерода с массовым числом 12. По закону Авогадро моль любого вещества содержит 6,02х10 23 молекул. Следствие из закона Авогадро: при нормальных условиях (н.у.) один моль любого газа занимает объем, равный 22,4 л.
 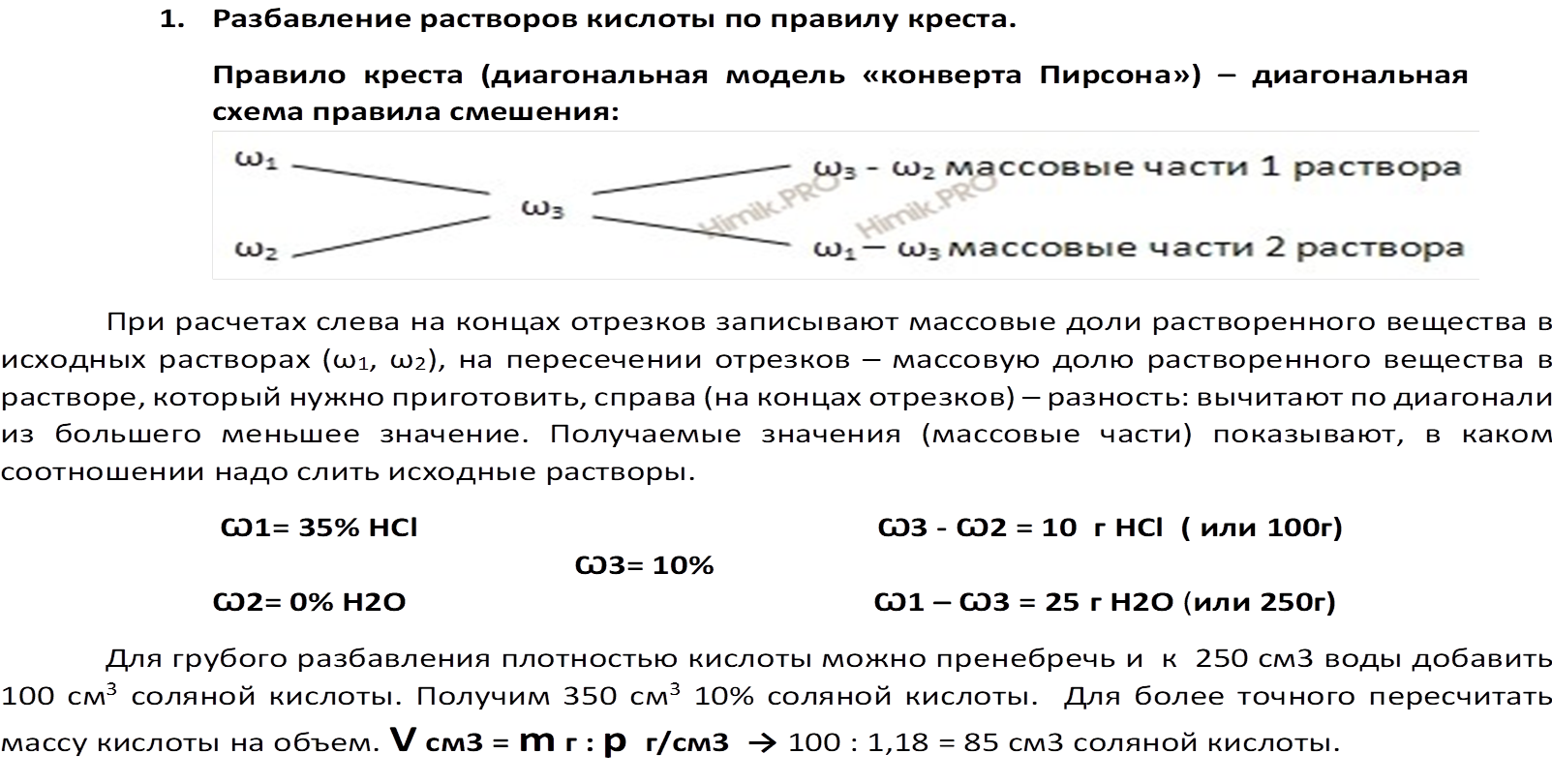 |
