Химия металлов вопросы к экзамену. 1. Элементы подгр. 1А. Строение атомов, сравнение свойств атомов, распространение в природе. Получение простых веществ и их свойства
 Скачать 274.84 Kb. Скачать 274.84 Kb.
|
|
23. Кадмий и его соединения. Кадмий (Cd) — переходный металл 2 группы таблицы Менделеева. Электронная конфигурация [Kr] 4d10 5s2 Получение Основные источники кадмия — промежуточные продукты цинкового производства, пыль свинцовых и медеплавильных заводов. Сырье обрабатывают концентрированной серной кислотой и получают CdSO4 в растворе. Из раствора Cd выделяют, используя цинковую пыль: CdSO4+Zn→Cd+ZnSO4CdSO4+Zn→Cd+ZnSO4 Полученный металл очищают переплавкой под слоем щелочи для удаления примесей цинка и свинца. Кадмий высокой чистоты получают электрохимическим рафинированием с промежуточным очисткой электролита. Физические свойства Кадмий — это мягкий, тягучий, гибкий, серебристо-белый двухвалентный металл, который можно легко разрезать. Во многом он похож на цинк, но он способен образовывать сложные соединения.  Применение Благодаря своим физическим свойствам, кадмий нашел широкое применение в технике и промышленности (особенно, начиная с 50-х годов XX века). Основные сферы применения его использования: для антикоррозийного покрытия (так называемого кадмирование) черных металлов, особенно в тех случаях, когда они контактируют с морской водой, а также для производства никель-кадмиевых электрических аккумуляторов и батарей. Кадмий входит в состав многих сплавов, как легкоплавких, применяемых в качестве припоев (например, сплав Вуда (Wood’s metal) — 50 % Bi, 25 % Pb, 12,5 % Sn, 12,5 % Cd), так и тугоплавких износостойких (например, с никелем). Кадмий используется в стержнях-замедлителях атомных реакторов, некоторые соединения кадмия имеют полупроводниковые свойства и тому подобное. Довольно долго кадмий использовался для производства красителей (пигментов) и в качестве стабилизатора в производстве пластмасс, однако сейчас, из-за токсичности, в этих целях он практически не используется. Опасность для здоровья Кадмий — один из немногих элементов, не выполняющий конструктивных функций в человеческом организме. Этот элемент и его соединения являются чрезвычайно токсичными даже в незначительных концентрациях. Имеет свойство накапливаться в организмах и экосистемах.Вдыхание кадмиевой пыли быстро приводит к заболеваниям, часто смертельным, дыхательных путей и почек (чаще всего — почечная недостаточность). Поглощение любой значительного количества кадмия вызывает немедленное поражение печени и почек. Соединения, содержащие кадмий также канцерогенными. Данные о канцерогенности кадмия ограничены. В опытах на животных не было зафиксировано роста числа опухолей из употребления кадмия. Такая тенденция наблюдалась только с вдыханием частиц пыли, содержащий неорганические соединения кадмия.Отравление кадмием является причиной болезни, которая впервые была описана в Японии в 50-х годах XX века и получила название «Итай-итай» (что дословно означает «больно-больно»). СОЕДИНЕНИЯ   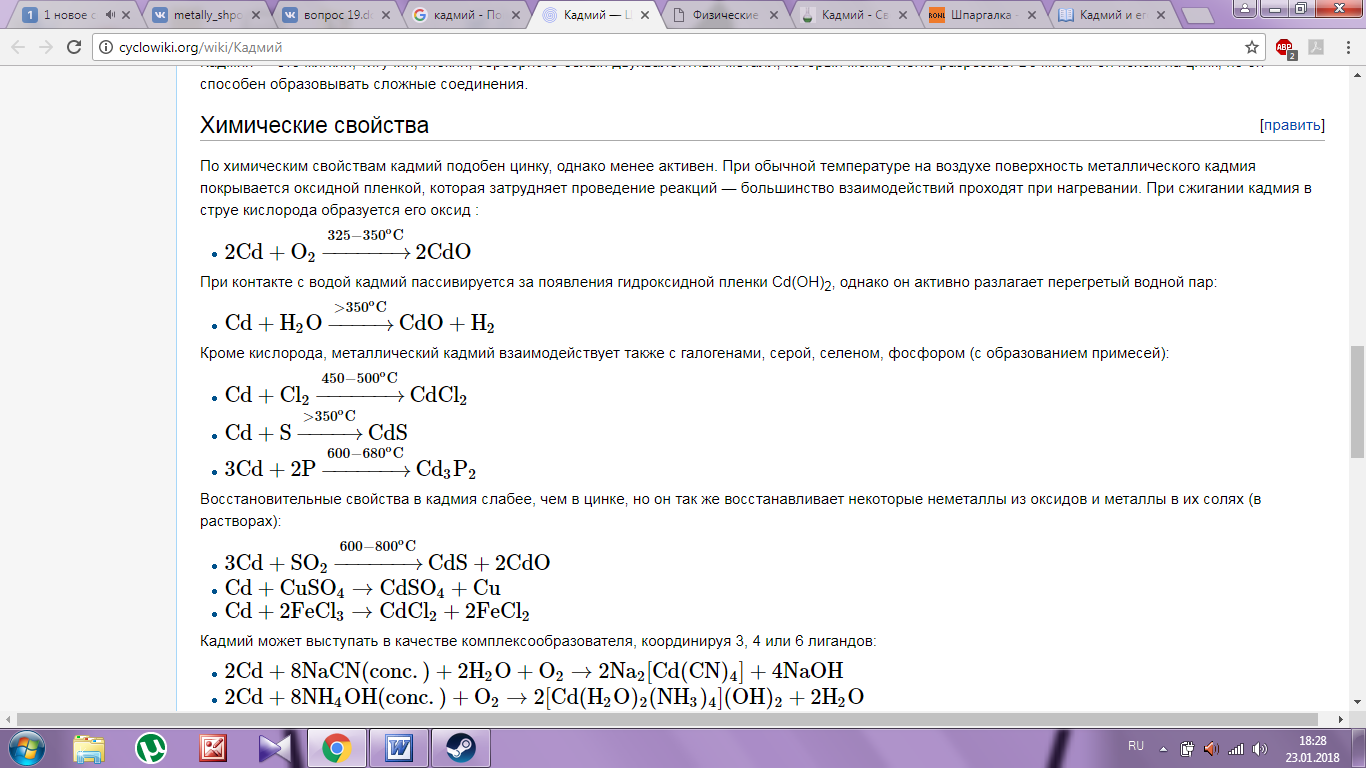 Гидроксид кадмия Гидроокись кадмияпредставляет собой мелкокристаллическое вещество. Ее мелкокристаллическоестроение является результатом очень большой скорости зарождения центровкристаллизации и очень малой скорости роста кристаллов. Едкие щелочи осаждают израстворов солей кадмия мелкокристалический студенистый, белый осадокгидроксида, не растворимый в избытке реагента. Гидроокись хорошо растворяется вкислотах, аммиаке и в растворах цианидов щелочных металлов: Cd(OH)2+4NH3(OH)=[Cd(NH3)4](OH)2+4H2O Гидроксид кадмия относится к числутруднорастворимых соединений. Оксид кадмия (II) При нагревании на воздухе кадмий загорается, образуя оксидкадмия CdO (молекулярный вес 128,41). Окисьможно получить также прокаливанием азотнокислой или углекислой солей кадмия.Этим путем оксид получается в виде бурого порошка, имеющего две модификации:аморфную и кристаллическую. Оксид кадмиявосстанавливается водородом, углеродом и окисью углерода. Водород начинаетвосстанавливать CdO при 250-260°по обратимой реакции: CdO+H2 Cd+H2O, Которая быстро заканчивается при 300°. Оксид кадмия хорошорастворяется в кислотах и в растворе сульфата цинка по обратимой реакции: CdO + H2O+ZnSO4 CdSO4+Zn(OH)2. Сульфид кадмия Сульфид (CdS, молекулярный вес 144,7) является одним из важных соединений кадмия. Он растворяется в концентрированных растворах соляной и азотной кислот, в кипящей разбавленной серной кислоте и врастворах трехвалентного железа; на холоду в кислотах растворяется плохо а вразбавленной серной кислоте нерастворим. Присплавлении металлического кадмия с серой развитие реакции сульфидообразованиятормозится предохранительными пленками CdS. Реакция 2CdO+3S=2CdS+SO2 начинается при 283° и при 424° проходитс большой скоростью. Известны три модификации CdS: аморфный (желтый) и две кристаллических(красный и желтый).Красная разновидность кристаллического сульфида тяжелее(уд. вес 4,5) желтой (уд. вес 3). Аморфный CdS при нагревании до 450° переходит в кристаллический. Сульфид кадмия принагревании в окислительной атмосфере окисляется до сульфата или окиси взависимости от температуры обжига. Сульфат кадмия Сульфат кадмия (CdSO4, молекулярный вес 208,47) представляет собой белый кристаллический порошок, кристаллизующийся в ромбической системе. Он легко растворим в воде, нонерастворим в спирте. Сульфат кристаллизуется из водного раствора в моноклиннойсистеме с 8/3 молекулами воды (CdSO4·8/3H2O), устойчив до 74°, но при более высокой температуре переходитв одноводный сульфат (CdSO4·H2O).С повышением температуры растворимость сульфата нескольковозрастает, но при дальнейшем повышении температуры снижается Было установленосуществование трех модификаций сульфата: α, β и γ. После выделенияпоследней молекулы воды при 200° из кристаллогидрата 3CdSO4·8H2O образуется α-модификация, устойчивая до 500°; придальнейшем повышении температуры возникает β-модификация, которая притемпературе выше 735° переходит в γ-модификацию. Высокотемпературныемодификации (β и γ) при охлаждении переходят в α-модификацию. |
