Физика 9 класс. 1. Физика. Методы познания природы. Физические явления
 Скачать 5.42 Mb. Скачать 5.42 Mb.
|
27. Модель строения твердых тел. Аморфные вещества и кристаллы.Всякое вещество состоит из большого числа мельчайших частичек — молекул. Каждая молекула, в свою очередь, состоит из сравнительно небольшого числа атомов. По взаимному расположению атомов или молекул твердые тела подразделяют на кристаллические и аморфные. Кристаллическими называются тела, в которых атомы и молекулы расположены в правильном геометрическом порядке, а аморфными (стеклообразными) — тела, в которых атомы и молекулы расположены беспорядочно. При переходе вещества из жидкого состояния в твердое (например, при застывании расплава металла) или при выпадении твердого вещества в осадок из насыщенного раствора (например, при твердении гипсового вяжущего) атомы и молекулы вещества стремятся занять такое положение относительно друг друга, чтобы силы их взаимодействия оказались максимально уравновешены. Поэтому их положение относительно друг друга оказывается вполне определенным, фиксированным. Такой геометрически правильный и повторяющийся в пространстве порядок расположения атомов (молекул) называют кристаллической решеткой (рис. 1). 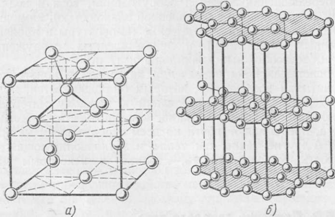 Процесс кристаллизации не совершается мгновенно, а требует определенного времени. В некоторых случаях, например при быстром охлаждении расплавленного кварца, может произойти затвердевание без кристаллизации с сохранением хаотического расположения атомов. Так образуется аморфное вещество — в нашем случае кварцевое стекло. Рис. 1. Схематическое изображение кристаллических решеток алмаза (а) и графита (б) Различие в строении кристаллических и аморфных веществ определяет и различие в их свойствах. Так, аморфные вещества, обладая нерастраченной внутренней энергией кристаллизации, химически более активны, чем кристаллические такого же состава. Например, расплав доменного шлака, используемый для получения шлаковых цементов, охлаждают по специальному ускоренному режиму для получения гранулированного шлака стеклообразного строения, обладающего повышенной химической активностью. Аморфное (стеклообразное) строение имеют также горные породы, применяемые в качестве активных минеральных добавок к цементам (туфы, пемзы, диатомиты, трепелы). Другое существенное различие между аморфными и кристаллическими веществами состоит в в том, что кристаллические вещества при нагревании до определенной температуры (температуры плавления) плавятся, а аморфные размягчаются и постепенно переходят в жидкое состояние. Прочность аморфных веществ, как правило, ниже прочности кристаллических, поэтому для получения материалов повышенной прочности специально проводят кристаллизацию стекол, например, при получении ситаллов и шлакоси- таллов — новых стеклокристаллических материалов. Различные свойства могут наблюдаться у кристаллических материалов одного и того же состава, если они кристаллизуются в разных кристаллических формах. Иллюстрацией этому служат две кристаллические формы углерода: алмаз и графит. Резкое отличие в их свойствах связано с различным строением кристаллов: атомы алмаза имеют плотнейшую тетраэдрическую решетку (рис. 1, а), а атомы графита расположены как бы слоями, причем расстояние между слоями больше, чем между соседними атомами в слоях (рис. 1,6). Такое строение графита придает ему мягкость и способность расслаиваться. Изменением свойств материала путем изменения его кристаллической решетки пользуются при термической обработке металлов (закалке или отпуске). Не меньшее влияние на свойства материала оказывают его микро- и макроструктура. Микроструктура — строение материала, видимое под микроскопом, макроструктура — строение материала, видимое невооруженным глазом или при небольшом увеличении. Большинство материалов в своем составе, кроме твердого вещества, имеют воздушные включения — поры размером от долей миллиметра до сантиметра. Количество, размер и характер пор во многом определяют свойства материала. Например, пористое стекло (пеностекло) в отличие от обычного непрозрачное и очень легкое. Форма и размер частиц твердого вещества, из которого состоит материал, также влияют на свойства материала. Так, если обычное стекло расплавить и из расплава вытянуть тонкие волокна, то получится легкая и мягкая стеклянная вата. В зависимости от формы и размера частиц и их строения различают зернистые, волокнистые и слоистые материалы. Зернистые материалы бывают рыхлыми, состоящими из отдельных не связанных одно с другим зерен (песок, гравий), или конгломератного строения (зерна прочно соединены между собой). Пример природного материала конгломератного строения — гранит, который состоит из зерен различных минералов, прочно сросшихся друг с другом. Искусственный материал конгломератного строения — строительный раствор, в котором зерна песка прочно соединены цементным камнем. Волокнистые и слоистые материалы, у которых волокна (слои) расположены параллельно одно другому, обладают различными свойствами в различных направлениях. Это явление называется анизотропией, а материалы, обладающие такими свойствами,— анизотропными. Пример анизотропного материала волокнистого строения — древесина. Она набухает поперек волокон в 10…15 раз больше, чем вдоль, а прочность древесины по разным направлениям совершенно различна. |
