Реферат хроматография. 1. Хроматография и основные особенности хроматографических методов 2
 Скачать 62.58 Kb. Скачать 62.58 Kb.
|
Содержание1.Хроматография и основные особенности хроматографических методов 2 1.1Классификация хроматографических методов 3 2.Газовая хроматография 5 3.1 Газовый хроматограф. Принципиальная схема 6 3.2 Варианты метода 7 3.2.1 Газо-адсорбционная хроматография 7 3.2.2 Газо-жидкостная хроматография 9 3.2.3 Капиллярная газовая хроматография 10 3.2.4 Реакционная газовая хроматография 12 3.2.5 Хромато-масс-спектрометрия 13 3.Аналитическое применение хроматографии 14 Список литературы 17 Хроматография и основные особенности хроматографических методовХроматография – это обширная область физико-химических методов анализа, которая занимается разработкой методов разделения сложных по составу многокомпонентных смесей. Характерными особенностями любых являются следующие: • Высокая разрешающая способность процесса разделения, обусловленная высокой эффективностью процесса, дающая возможность разделения даже близких по природе, структуре и свойствам веществ. Этим, во многом, объясняется широкое распространение хроматографии в различных областях научных исследований, в лабораторной практике, промышленности. Те разделения, которые до применения хроматографических методов не могли быть осуществлены, стали легко осуществимы после их появления. Сюда относятся, например, разделение смесей аминокислот на индивидуальные компоненты, разделение смесей углеводородов на индивидуальные вещества, разделение смесей редкоземельных элементов на отдельные элементы, выделение ферментов в чистом виде и многие другие разделения. • Мягкие условия разделения. Можно сравнить процесс хроматографического разделения смесей с процессом разделения сложных смесей методом перегонки, но если обычная перегонка осуществляется, как правило, в достаточно жестких условиях (высокая температура, глубокое вакуумирование), то хроматографические разделения осуществляются, как правило, в очень мягких условиях (при атмосферном давлении, при обычных температурах). Перечислим основные задачи, которые могут быть решены с помощью хроматографических методов: • Разделение многокомпонентных по составу смесей на индивидуальные компоненты, т.е. по существу это качественный и количественный анализ сложных смесей веществ. • Концентрирование веществ из их очень разбавленных растворов. Цели здесь могут быть самые разные: хроматографические методы позволяют сконцентрировать уран, содержащийся в природных рудах в десятых, а то и сотых долях процента; сконцентрировать радий, содержащийся в природных водах в концентрациях 10-5−10-6 г-атом/л. Может стоять задача извлечения ценных металлов (серебра, золота, платины) из разбавленных технологических растворов (гидрометаллургия) или производственных сточных вод (вопросы экологии). • Очистка технических продуктов, доведение этих продуктов до заданной степени химической чистоты, получение чистых химических реактивов. • Проверка вещества на однородность, на чистоту, т.е. идентификация вещества, доказательство того, что оно соответствует данной химической формуле. • Контроль различных производств методами хроматографии. Классификация хроматографических методовВ основу классификаций хроматографических методов положены принципы, учитывающие следующие различные особенности процесса разделения: • различия в агрегатном состоянии фаз используемой хроматографической системы; • различия в характере взаимодействий разделяемых веществ с неподвижной фазой; • экспериментальные различия в способах проведения процесса хроматографического разделения. В таблицах 1−3 приведены основные варианты классификации известных хроматографических методов. Таблица 1. Варианты хроматографии, различающиеся по агрегатному состоянию фаз
Поскольку характер взаимодействий разделяемых соединений с фазами различных хроматографических систем может сильно различаться, то почти не существует объектов, для разделения которых не удалось бы найти подходящей неподвижной фазы (твердой или жидкой) и систем подвижных растворителей. Таблица 2. Варианты хроматографии, различающиеся по характеру взаимодействий разделяемых соединений с неподвижной фазой
Таблица 3. Варианты хроматографии, различающиеся по способу проведения
Газовая хроматографияНесмотря на то, что метод газовой хроматографии был открыт только в 1952 году, теория процесса разделения смесей веществ этим методом на настоящее время разработана гораздо глубже, чем для других методов. Это объясняется прежде всего тем, что методы газовой хроматографии использовались в практике гораздо интенсивнее других. Отличительной особенностью газовой хроматографии от других методов хроматографических разделений является то, что используемая подвижная фаза должна обязательно находится в газообразном состоянии и выполнять роль газа-носителя, перемещающего разделяемые соединения по колонке. В качестве газов-носителей могут быть использованы индивидуальные газы, газообразные соединения или смеси газов и газообразных соединений. Характерными особенностями газовой хроматографии являются: • Высокая разделительная способность: по своим возможностям анализа многокомпонентных смесей газовая хроматография не имеет конкурентов. Ни один другой метод не позволяет анализировать фракции нефти, состоящие из сотен компонентов, в течение одного часа. • Универсальность: разделение и анализ самых различных смесей – от низкокипящих газов до смесей жидких и твердых веществ с температурой кипения до 500оС и выше – характеризует универсальность метода. В нефтехимической и газовой промышленности 90−100 % всех анализов можно выполнять методом газовой хроматографии. • Высокая чувствительность: высокая чувствительность метода обусловлена тем, что применяемые детектирующие системы позволяют надежно определять концентрации 10-8 – 10-9 мг/мл. Используя методы концентрирования и селективные детекторы, можно определять микропримеси с концентрациями до 10-10%. • Экспрессность: экспрессность газовой хроматографии подчеркивается тем, что продолжительность разделения в большинстве случаев составляет 10−15 минут, иногда при разделении многокомпонентных смесей 1−1.5 часа. Однако за это время анализируется несколько десятков или сотен компонентов. В некоторых специальных случаях время разделения может быть меньше одной минуты. • Легкость аппаратурного оформления: газовые хроматографы относительно дешевы, достаточно надежны, имеется возможность полной автоматизации процесса анализа. • Малый размер пробы: газовая хроматография по существу метод микроанализа, поскольку для анализа достаточно пробы в десятые доли мг. • Высокая точность анализа: погрешность измерений ± 5 % относительных легко достигается практически на любой газохроматографической аппаратуре. В специальных условиях достигается погрешность ±0.001−0.002% относительных. Следует отметить и существующие ограничения метода газовой хроматографии: • невозможность разделения и анализа смесей нелетучих соединений; • осложнения при разделении и анализе термически нестабильных соединений; • невозможность разделения и анализа соединений, способных к диссоциации в анализируемых растворах (разделение ионов). 3.1 Газовый хроматограф. Принципиальная схемаЛюбая газохроматографическая установка обязательно должна содержать следующий перечень узлов: • источник газа-носителя; • вентиль тонкой регулировки скорости потока газа-носителя; • устройство для ввода пробы; • хроматографическая колонка; • детектор; • термостат колонки и термостат детектора; • регистратор; • измеритель скорости потока газа-носителя. Рассмотрим назначение и устройство основных узлов газохроматографической установки. 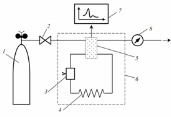 Рис. 1. Принципиальная схема газового хроматографа (1 − источник газа-носителя; 2 − вентиль тонкой регулировки скорости потока газа-носителя; 3 − устройство для ввода пробы; 4 − хроматографическая колонка; 5 − детектор; 6 – термостат колонки и термостат детектора; 7 − регистратор; 8 − измеритель скорости потока газа-носителя) 3.2 Варианты методаПри классификации вариантов методов газовой хроматографии предполагается, что подвижная фаза (газ-носитель) абсолютно инертна к неподвижной фазе и разделяемым соединениям. Таким образом, классификация вариантов основывается только на особенностях неподвижной фазы. В качестве неподвижной фазы в газовой хроматографии используется или твердый адсорбент, или жидкость, нанесенная в виде тонкой пленки на адсорбционно-инертный твердый носитель. В соответствии с типом используемых неподвижных фаз газохроматографические методы подразделяются на газо-адсорбционный и газо-жидкостный. Разделение компонентов анализируемой смеси в газо-адсорбционном варианте основано на различии разделяемых веществ в величинах адсорбции на поверхности адсорбента, а в случае газожидкостной хроматографии на различии в растворимости компонентов анализируемой смеси в неподвижной жидкой фазе. В том случае, если используемый твердый носитель неподвижной жидкой фазы проявляет адсорбционные свойства, реализуется промежуточный вариант газовой хроматографии – газо-жидко-твердофаная хроматография. Каждый из вариантов характеризуется своими положительными чертами и недостатками, которые обязательно следует учитывать при выборе оптимального метода разделения каждой конкретной смеси. 3.2.1 Газо-адсорбционная хроматографияГазо-адсорбционная хроматография представляет собой метод анализа смесей газов и легколетучих веществ. Разделение основано на различии в адсорбции на поверхности твердого носителя (адсорбента). Адсорбция может быть обусловлена неспецифическими (ориентационными, индукционными и дисперсионными) и специфическими взаимодействиями (комплексообразованием, либо образованием водородной связи) и зависит от природы адсорбента и сорбата. В качестве адсорбентов используют пористые носители, которые обладают химической, физической и термической стабильностью; однородной поверхностью, равномерным распределением по размеру пор и известной адсорбционной активностью. Адсорбционная активность зависит от удельной поверхности (определяется геометрической структурой носителя) и удельной поверхностной энергии (определяется химической структурой поверхности). Достоинствами адсорбентов в качестве неподвижных фаз являются способность выдерживать высокие температуры, отсутствие фонового сигнала при работе с ионизационными детекторами и высокая селективность. Адсорбенты делятся на неорганические, полимерные (органические) и модифицированные. Среди неорганических адсорбентов особо важны сорбенты на основе углеродных материалов. Это неполярные сорбенты, для них особую роль в процессе разделения играют геометрические параметры поверхности. Наиболее интересная особенность данных материалов – возможность разделения структурных изомеров. Широко используются полярные неорганические сорбенты на основе двуокиси кремния. Особый интерес для газо-адсорбционной хроматографии представляет использование цеолитовых молекулярных сит (M2/nO•Al2O3•xSiO2•yH2O), которые успешно позволяют разделять различные газовые смеси. Применение адсорбентов на основе Al2O3 ограничено из-за его гетерополярной поверхности, гигроскопичности и асимметрии пиков разделяемых соединений. Сорбенты используют для разделения легких углеводородов. Наиболее многообразны полимерные сорбенты на основе пористых полимеров стирола и дивинилбензола. Их удается синтезировать с заданными свойствами и очень чистой поверхностью. Это гидрофобные сорбенты, слабо удерживающие полярные молекулы, содержащие гидрокси-амино-группы. Основная область применения полимерных сорбентов – разделение полярных и реакционно-способных газов и высоко полярных органических соединений; определение воды в органических растворителях и летучих органических примесей в воде. Метод газо-адсорбционной хроматографии обычно используют для оценки содержания в атмосферном воздухе кислорода, водорода, метана, углекислого газа, окиси углерода, окислов азота, хлора, диоксида серы, сероводорода и сероуглерода. Положительным для газо-адсорбционного метода анализа является: только в этом случае проявляется высокая разделительная способность при анализе смесей газов и паров низкокипящих веществ; нелетучесть твердого адсорбента; термическая стабильность адсорбента в широком интервале изменения температуры хроматографической колонки; более высокая скорость массообмена, чем в варианте газо-жидкостной хроматографии, что приводит к быстрому разделению смесей веществ; возможность модифицирования поверхности адсорбента; достаточная механическая прочность адсорбентов; доступность адсорбентов. К недостаткам метода следует отнести: недостаточную геометрическую однородность поверхности адсорбентов; недостаточное постоянство химического состава поверхности адсорбентов из-за наличия примесей; повышенную адсорбционную активность адсорбентов; повышенную каталитическую активность адсорбентов; нелинейность изотермы адсорбции; недостаточно широкий выбор адсорбентов. 3.2.2 Газо-жидкостная хроматографияНа практике чаще используют газо-жидкостную хроматографию, благодаря многообразию неподвижных фаз. В газо-жидкостной хроматографии разделение компонентов пробы достигается за счет многократного повторения процессов распределения между движущейся газовой и неподвижной жидкой фазами. Скорость миграции компонентов зависит от их летучести и способности растворяться в стационарной жидкой фазе. Компоненты с низкой растворимостью в жидкой фазе и наибольшей летучестью при данной температуре продвигаются по колонке быстрее, и, наоборот, компоненты с низкой летучестью и высокой растворимостью в стационарной фазе обладают малой подвижностью. Чем больше подвижность, тем меньше время удерживания. В качестве носителя неподвижной фазы используют адсорбенты с поверхностью 0,5-3,0 м2/г и с размером пор (0,5-1,5)10-3 мм. Наиболее часто используют диатомитовые носители, стеклянные шарики, силикагель и политетрафторэтилен. Неподвижные фазы должны быть химически и термически стабильны, смачивать носитель и наноситься на его поверхность равномерной пленкой. Известно более тысячи неподвижных жидких фаз, достаточно часто используется около 100. По химическому составу неподвижные фазы делят на следующие классы: Углеводороды (предельные углеводороды, смеси предельных и непредельных углеводородов, ароматические углеводороды) Примеры: сквалан, парафиновое масло, апиезоновые смазки, алкилнафталины, полифениловый эфир Силоксаны с радикалами различной полярности (неполярными, среднеполярными и полярными) Примеры: метилсилоксан, метилфенилсилоксан, нитрилсилоксан, полиэфирсиликоны, эфиры простые и сложные, полиэфиры , полигликоли, фталаты и фосфаты. Выбор неподвижной фазы зависит от полярности разделяемых соединений и от их способности образовывать водородные связи. Для разделения полярных сорбатов необходимы полярные неподвижные фазы, неполярных – неполярные. Понятие полярности объединяет свойства, обуславливающие селективность за счет физического взаимодействия молекул с функциональными группами. Учитывается сумма неразрывно связанных взаимодействий, например, взаимная ориентация диполей, индуктивные и дисперсионные силы, образование водородных мостиков. В газо-жидкостной хроматографии разница в удерживании определяется и неспецифическими, и специфическими взаимодействиями. Неполярные соединения обычно разделяются в соответствии с температурами их кипения. В случае неполярной неподвижной фазы полярные соединения удерживаются существенно меньше, чем неполярные, кипящие при той же температуре. Удерживание полярных соединений увеличивается по мере роста полярности неподвижной фазы, и, наоборот, время удерживания соединений возрастает с уменьшением полярности неподвижной фазы. 3.2.3 Капиллярная газовая хроматографияШирокое многообразие используемых жидких неподвижных фаз определяет успех разделения большого количества соединений различной природы. Однако одно лишь изменение природы неподвижной фазы и связанное с этим изменение ее растворяющей способности не может обеспечить успех разделения во всех случаях. При разделении сложных смесей компонентов с близкими химическими и физическими свойствами и смесей, состоящих из большого числа разнообразных веществ, на первый план выдвигаются повышенные требования к качеству работы хроматографической колонки. Этим требованиям отвечают капиллярные колонки без носителя, когда пленка неподвижной фазы наносится на внутреннюю поверхность капилляра. Этот тип колонок, предложенный Голеем в 1957 году, обеспечивает значительно большую эффективность разделения по сравнению с обычными насадочными колонками. Математическое описание процесса миграции конечной по протяженности зоны вещества в бесконечно длинной трубке базируется на следующих положениях: реализуется ламинарное течение газа-носителя; неподвижная фаза фиксирована на внутренней стенке капилляра в виде гомогенной жидкой пленки; распределение скоростей в потоке вязкой среды в трубке круглого сечения имеет параболический характер; у оси потока скорость максимальна, а непосредственно вблизи стенок скорость перемещения среды равна нулю. Движение газа-носителя в колонках без наполнителя сопровождается значительно меньшими энергетическими потерями, чем в заполненных пористым материалом трубках с той же величиной свободного сечения. Отсутствие заполнения позволяет улучшить на два и более порядка эффективность колонки. Для приготовления капиллярных колонок используют стеклянные, кварцевые или металлические трубки, которые должны удовлетворять следующим требованиям: капилляр должен иметь нужную длину и постоянный диаметр по всей длине, причем эти параметры не должны изменяться под действием температуры и давления; внутренняя поверхность капилляра должна быть химически однородной, на ней не должно быть больших трещин и пор; поверхность должна адсорбировать сорбаты, жидкие неподвижные фазы и газ-носитель в минимальной степени; поверхность должна прочно и равномерно смачиваться неподвижной фазой, т.е. на поверхности должен быть гомогенный разделяющий слой неподвижной фазы; капилляры должны обладать необходимой механической прочностью. Приготовление колонки состоит из ряда этапов: изготовления капилляра; подготовки внутренней поверхности капилляра – травлением или дезактивацией; нанесения неподвижной фазы; кондиционирования и испытания капиллярной колонки. Для того чтобы достичь высокой разделяющей способности колонок, на внутренние стенки капиллярной трубки должна быть нанесена однородная равномерная пленка жидкости. В настоящее время используют два основных способа: динамический и статический. В случае первого внутренняя поверхность капилляра смачивается при пропускании через капилляр определенного объема раствора жидкой фазы в подходящем растворителе под действием повышенного давления какого-либо газа. Движущаяся по капилляру пробка раствора оставляет позади себя жидкую пленку, затем через капилляр пропускают инертный газ, в результате чего испаряется растворитель, и получается тонкая пленка неподвижной фазы. Статический способ заключается в том, что капилляр заполняется раствором неподвижной фазы и растворитель испаряется в условиях повышенной температуры или пониженного давления. Толщину разделяющего слоя следует выбирать исходя из того, что между подвижной газовой фазой и разделяющим слоем должен происходить интенсивный массообмен с тем, чтобы равновесие между ними устанавливалось достаточно быстро, и чтобы емкость колонки (она определяется количеством неподвижной жидкой фазы) была не слишком мала. Для увеличения емкости предложено фиксировать неподвижную фазу в тонком слое носителя, нанесенном на стенку капилляра. Существует несколько типов капиллярных колонок: 1. Капиллярные колонки с пленкой жидкой неподвижной фазой (WCOT) тонкая пленка неподвижной фазы нанесена непосредственно на внутреннюю поверхность колонки толщина пленки 0,01-1 мкм; внутренний диаметр и толщина стенок - n.10-n.100 мкм 2. Капиллярные колонки с пористым слоем, пропитанным жидкой фазой, (PLOT) на внутренних стенках расположен слой носителя, несущего неподвижную фазу толщина пленки 1 - 5 мкм 3. Капиллярные колонки с твердым носителем (ПКК-ТН или PLOT) на внутренних стенках напылен слой твердого носителя толщина пленки 10 мкм 4. Капиллярные колонки с химически привитой неподвижной фазой Отличия капиллярных колонок по своим характеристикам от насадочных определяют специфические особенности газохроматографической аппаратуры для работы с ними. Такими особенностями являются малые объемы вводимых проб, невысокие значения расхода газа-носителя и высокие скорости изменения концентрации при элюировании передних и задних фронтов хроматографических пиков. Это обусловливает тот факт, что все соединения капиллярных колонок с другими элементами прибора должны быть выполнены так, чтобы объем возникающих при этом полостей был минимальным. Особенности капиллярной хроматографии предъявляют весьма жесткие требования к детекторам. Они должны обладать высокой чувствительностью и скоростью регистрации сигнала и иметь небольшой объем измерительной камеры. В наибольшей степени удовлетворяет всем требованиям пламенно-ионизационный детектор. 3.2.4 Реакционная газовая хроматографияВ реакционной газовой хроматографии (РГХ) используются направленные химические превращения нелетучих соединений в летучие, а также неустойчивых в устойчивые. Используется несколько вариантов РГХ: химическое образование производных; пиролитическая РГХ (исследуемые вещества разлагаются при высоких температурах и затем хроматографически определяются образовавшиеся продукты); метод "вычитания" (мешающие компоненты поглощаются специфическими реагентами и не влияют на определение определяемых компонентов). К положительным особенностям РГХ относятся: расширение области применения газовой хроматографии; улучшение разделения анализируемых соединений, т.к. индивидуальные свойства соединений более заметно проявляются в образующихся производных, чем в исходных соединениях; существенное улучшение количественных характеристик аналитических определений; увеличение чувствительности детектирования; лучшая сохранность хроматографической колонки. Недостатками РГХ являются: усложнение анализа, ухудшение эффективности разделения, увеличение времени анализа. Наиболее широко применяется получение производных. Основные способы получения производных перечислены ниже: 1. Получение силильных производных. 2. Алкилирование 3. Получение сложных эфиров На практике используют: диазометановый метод, где реакция дериватизации проходит по уравнению RCOOH + CH2N2 → RCOOCH3 + N2, метанольный метод ─RCOOH + CH3OH → RCOOCH3 пиролитический метод ─ RCOOH + (CH3)4NOH → RCOOCH3 + H2O + (CH3)3N. 4. Получение простых эфиров Дериватизация соединений проходит по уравнению: ROH + CH3I →ROCH3 + HI 5. Получение ацильных производных. Наиболее распространенные ацилирующие реагенты - ангидриды соответствующих кислот. 6. Образование оксимов и гидразинов 7. Образование производных неорганических соединений (летучих хелатов металлов, алкилпроизводных ртути, гидридов, хлоридов). 3.2.5 Хромато-масс-спектрометрияСочетание ГХ и масс-спектрометрии – один из наиболее эффективных методов анализа сложных смесей в объектах окружающей среды. Аналитические возможности ГХ и масс-спектрометрии идеально дополняют друг друга, и сочетание методов позволяет получать большой объем информации. На рис. приведена схема компьютеризированной хромато-масс-спектрометрической установки, которая позволяет провести все стадии анализа самых сложных смесей органических веществ. ГХ и МС присущи общие особенности – в обоих методах: – анализ вещества проводится в газовой фазе; – количество вещества, необходимое для одного анализа, составляет 10-6г; – скорости выполнения анализов в обоих методах могут быть согласованы таким образом, что в процессе элюирования одного хроматографического пика можно измерить несколько полных масс- спектров. Различие состоит в том, что в ионном источнике масс-спектрометра поддерживается высокий вакуум (10-5-10-6 Па), тогда как давление в хроматографической колонке 105 Па. Для понижения давления используют молекулярный сепаратор, который одним концом соединен с хроматографической колонкой, а другим с ионным источником масс- спектрометра. Сепаратор удаляет из газового потока, выходящего из колонки, основную часть газа-носителя, а органическое вещество пропускает в масс-спектрометр. Давление при этом понижается до рабочего давления масс-спектрометра. Для этого используют следующие процессы массопереноса: – эффузию через узкие поры и щели; – диффузию в расширяющейся газовой струе; – диффузию через полупроницаемые мембраны. Эти процессы используются в эффузионном, струйном и мембранном молекулярных сепараторах, соответственно. Для ионизации используют ионный удар, но более интересен другой способ ионизации – химическая ионизация. При этом способе источник ионов заполняется газом-реактантом, который ионизируется электронным ударом, а молекулы определяемых органических соединений превращаются в ионы за счет взаимодействия с ионами газа-реактанта или "медленными" электронами. Такая ионизация является "мягкой", то есть образовавшиеся ионы не разваливаются на мелкие фрагменты, а остаются в виде "молекулярного иона". Для ионизации лабильных органических соединений (в том числе биологически активных) разработаны специальные методы ионизации: ионизация в электроспрее (ESI) и ее подвид – химическая ионизация при атмосферном давлении (MALDI). Развитию хромато-масс-спекторметрии способствовало также создание "быстрых" квадрупольных масс-анализаторов. Аналитическое применение хроматографииХроматография - это один из методов пробоподготовки. При анализе сложных смесей для уверенного определения количества интересующего компонента практически всегда необходима подготовка пробы к анализу: экстракция, кристаллизация, выпаривание, соосаждение и т.д. Один из методов такой подготовки пробы является процесс хроматографирования, т.е. разделения сложной смеси на составляющие компоненты. Накопленный опыт позволяет утверждать, что при анализе сложных объектов нельзя пренебрегать практически ни одним из компонентов: при экологических исследованиях установлено, что токсичное действие малых концентраций тяжелых металлов значительно выше, чем действие значительных концентраций NO2, SO2 и т.д.; при биологических исследованиях выясняют мощное влияние малых концентраций витаминов, антибиотиков, других лекарственных препаратов; при анализе пищевых продуктов на фоне большого содержания белков, жиров, углеводов весьма важно определение токсинов, минеральных веществ; качество выпускаемой продукции в значительной степени определяется наличием или, наоборот, отсутствием различных добавок, находящихся в малых концентрациях. Эти примеры можно умножить. Из сказанного можно сделать вполне определенный вывод: в настоящее время требуется детальный химический анализ разнообразных смесей и биологических объектов. Решение этой задачи невозможно без применения достаточно эффективных методов разделения сложных смесей. Среди таких методов доминирует хроматография. Бурно развиваясь в последнее десятилетие, этот метод открыл возможность разделения смесей, содержащих десятки и сотни компонентов, их количественный и качественный анализ, препаративное выделение индивидуальных веществ. Принципы хроматографии весьма универсальны, благодаря чему она оказалась пригодной для изучения объектов самой разной природы, от нефти и газов атмосферы до белков и даже вирусов. Период, наступивший в аналитической химии органических соединений с начала 60-х годов без преувеличения может быть назван эпохой хроматографии. Один из вариантов этого метода - колоночная жидкостная хроматография, был создан русским ботаником Цветом М.С. (откуда название хроматографов "Цвет") в 1903г. На протяжении последующих сорока лет хроматография не находила широкого практического применения. Лишь после 1950г. приходит время признания хроматографии. В 1952г. были выполнены первые работы по жидкостной хроматографии, а вскоре освоен выпуск газовых хроматографов, и в течение последующих 20 лет газохроматографический анализ стал основным методом исследования летучих термически устойчивых соединений. Но большинство органических соединений не обладает необходимой для газовой хроматографии летучестью и термостойкостью, и хроматографировать их можно только в более мягких условиях, характерных для жидкостной колоночной хроматографии. Скорость же и эффективность разделения, а также чувствительность анализа по этому методу долго оставались неудовлетворительными. И лишь в 1965-75 гг. были в принципе решены основные научные и технологические проблемы, сдерживавшие развитие метода. Последовавший затем прогресс был столь поразителен, что современная инструментальная разновидность метода получила самостоятельное наименование - высокоэффективная жидкостная хроматография. Важнейшим катализатором развития хроматографической науки и практики были потребности разных химических и естественных наук, начиная от медицины и кончая криминалистикой , не говоря уже о науках химических и биологических. Внедрение хроматографических методов в эти области радикальным образом изменило тактику и методику исследований, обеспечило новые возможности контроля производства (до 200 хроматографов на 1 предприятии). Хроматографическое оборудование сейчас можно увидеть и в химической лаборатории, и в цехе, и в больнице, и в кабине корабля. Можно утверждать, что внедрение хроматографии прививает современному химику новый взгляд на вещества и смеси, которые он исследует. Оказывается, ни одно вещество не такое чистое, каким кажется, и не одна смесь не такая простая, какой кажется, пока досконально не изучены хроматографическими методами. В справедливости этого исследовательского тезиса убежден, наверное, каждый в чью работу хроматография вошла прочно. Но пессимизм здесь только в форме, а не в содержании, так как обнаружение в смеси с помощью хроматографии новых компонентов или примесей может обернуться ценным научным результатом или, по меньшей мере, предотвратить ошибочные решения и выводы. Итак, хроматография - это: а) ряд теоретических представлений, посвященных законам сорбции и массопередачи; б) материальный фундамент - приборы и сорбенты; в) методологические и прикладные исследования, приводящие к созданию конкретных методик. Список литературыШаповалова Е.Н., Пирогов А.В., "Хроматографические методы анализа" Методическое пособие для специального курса, Москва, 2007 В. А. Винарский, "Хроматография" Курс лекций в двух частях Часть 1. Газовая хроматография, МИНСК Научно-методический центр "Электронная книга БГУ" 2003 Орлов В.И. Аратсков А.А, "Жидкостная хроматография". | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
