ИДЗ по физике. ИДЗ2. 1. На диаграмме v T
 Скачать 402.5 Kb. Скачать 402.5 Kb.
|
|
1. На диаграмме V – T изображен процесс, который произошел с идеальным газом при постоянном давлении и постоянном объеме. Как при этом изменилась масса газа? (Во сколько раз увеличилась или уменьшилась?) 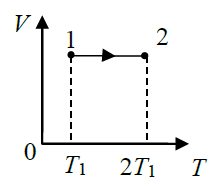 Дано: Найти: Решение Запишем уравнение Менделеева – Клапейрона для двух состояний газа, учитывая, что согласно условию задачи Из уравнений (1) и (2) можем записать: Отсюда: Подставим данные в (3): Ответ: 2. Два баллона с объемами V1 и V2 = 2V1 соединены трубкой с краном. Баллоны заполнены воздухом при давлении р1 = 0,3 МПа и р2 соответственно, и одинаковой температуре. Если кран открыть, то в баллонах установится давление 0,5 МПа. Чему равно давление воздуха во втором баллоне (в МПа)? Дано: Найти: Решение Запишем уравнение Менделеева – Клапейрона для газа первого и второго баллона, до открытия крана, учитывая, что согласно условию задачи температура в них одинакова: Запишем уравнение Менделеева – Клапейрона для газа, когда открыли кран, учитывая, что температура не изменилась: Из уравнение (1) находим: Из уравнение (2) находим: Подставим (4) и (5) в (3): Отсюда: Учитывая, что Подставим данные в (6): Ответ: 3. Определите среднюю кинетическую энергию поступательного движения и полную кинетическую энергию одной молекулы азота при температуре 600 К. Дано: Найти: Решение Средняя кинетическая энергия поступательного движения одной молекулы равна: Где Средняя энергия вращательного движения равна: Тогда среднее значение полной кинетической энергии Подставим данные в (1) и (3): Ответ: 5. Водород занимает объем Дано: Найти: Решение Согласно первому началу термодинамики, количество теплоты При изохорическом процессе работа равна нулю Известно, что изменение внутренней энергии Изменение внутренней энергии равно: где Запишем уравнение Менделеева-Клайперона: Где Запишем уравнение (4) сначала для состояния 1, а потом для состояния 2, учитывая, что Из уравнений (5) и (6) можем записать: Или Учитывая (7), выражение (3) можем записать так: Учитывая (7), выражение (2) можем записать так: Подставим данные в (9), учитывая, что для двухатомной молекулы, какой является молекула водорода i=5. Ответ: 6. Найдите показатель адиабаты Дано: Найти: Решение Показатель адиабаты Где Количество теплоты, необходимое для нагревания смеси газов при постоянном давлении на некоторую температуру Где С другой стороны это количество теплоты можем записать так: Где Из уравнений (2) и (3) можем записать: Отсюда: Удельная теплоемкость газа при постоянном давлении определяется формулой: где R =8,31 Дж/(моль⋅К) газовая постоянная; Запишем выражение (5) отдельно для двух газов: где Подставим выражения (6) и (7) в (4): 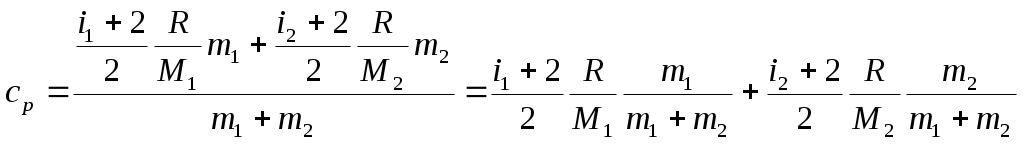 Количество теплоты, необходимое для нагревания смеси газов при постоянном объеме на некоторую температуру Где С другой стороны это количество теплоты можем записать так: Где Из уравнений (9) и (10) можем записать: Отсюда: Удельная теплоемкость газа при постоянном объеме определяется формулой: Запишем выражение (12) отдельно для двух газов: где Подставим выражения (13) и (14) в (11): 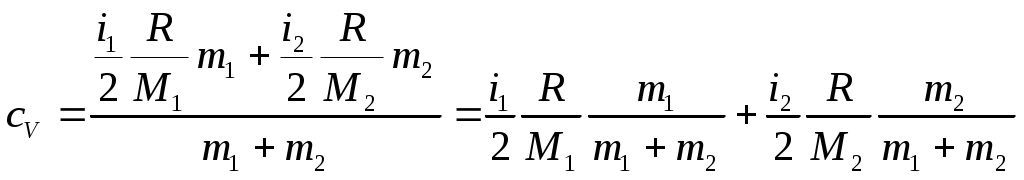 Подставим выражения (8) и (16) в (1): 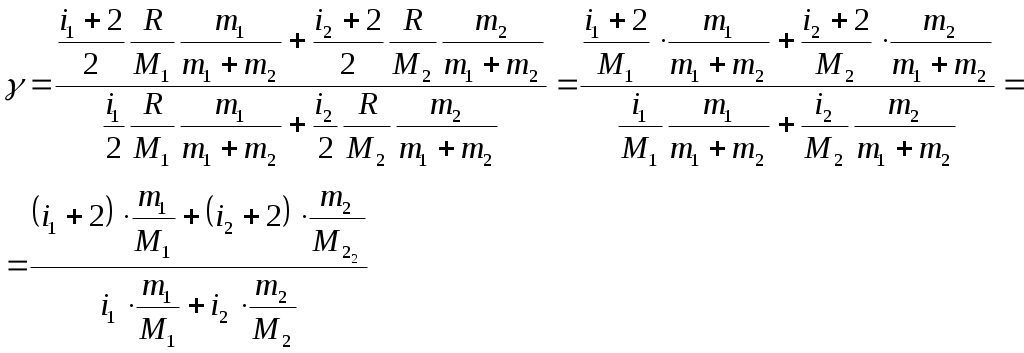 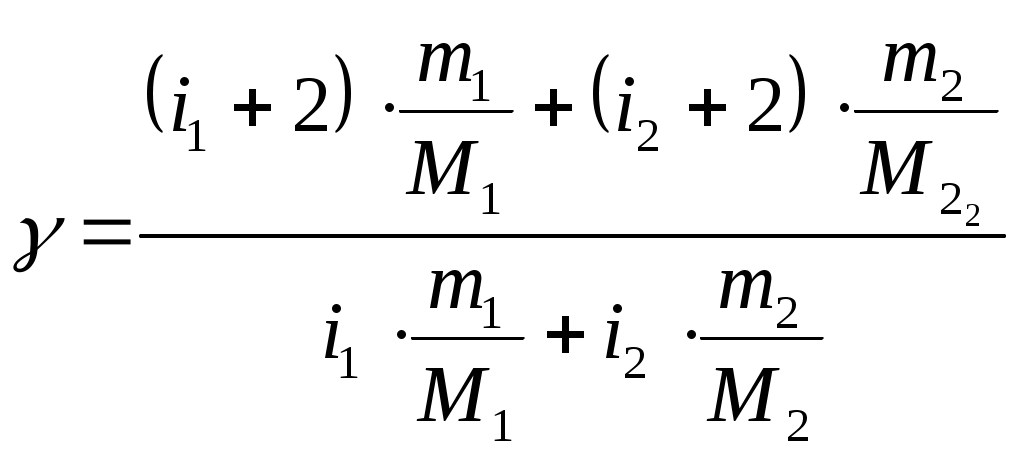 (17) (17)Подставим данные в формулу (17), учитывая, что для гелия количество степеней свободы равно 3: 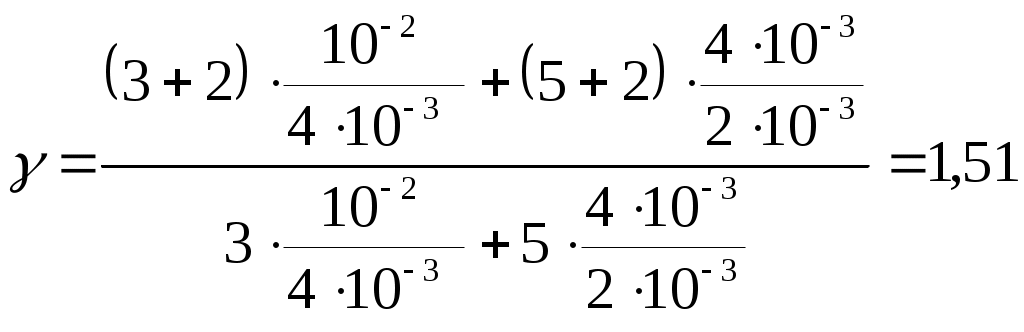 Ответ: 7. Температура нагревателя тепловой машины 500 К. Температура холодильника 400К. Определите КПД тепловой машины, работающей по циклу Карно, и полезную мощность машины, если нагреватель ежесекундно передает ей 1675 Дж теплоты. Дано: Найти: Решение Термический к.п.д. цикла Карно можно определить по формуле: где К.п.д. цикла Карно также можно определить по формуле: Работа, совершенная рабочим телом тепловой машины равна: Подставим выражение (3) в (2): Отсюда: Работа в единицу времени и есть мощность. Тогда полезная мощность тепловой машины при найденном нами её КПД может быть выражено следующим образом: Подставим (1) в (6): 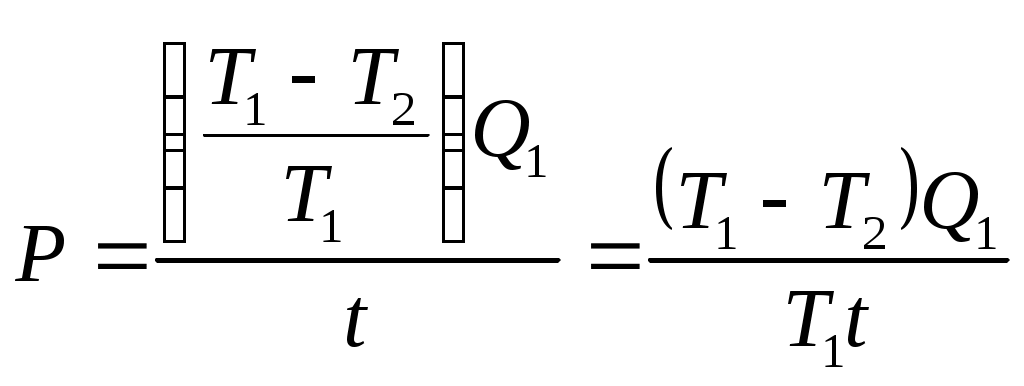 Подставим данные в (1) и (7): Ответ: 8. Кислород массой m = 2 кг увеличил свой объем в 5 раз сначала изотермически, затем – адиабатно. Найдите изменение энтропии. Дано: Найти: Решение Так как энтропия величина аддитивная, то общее изменение энтропии будет равно: Где По определению, изменение энтропии при переходе системы из состояния 1 в состояние 2 равно: где dQ – количества тепла, сообщенное газу, Т – абсолютная температура, S1 и S2 – значения энтропии в начальном и конечном состояниях системы. Поскольку при адиабатическом процессе Найдем изменение энтропии при изотермическом процессе. Согласно первому началу термодинамики, количество теплоты Для изотермического процесса все подводимое количество теплоты идет на работу по расширению, т.е. dQ = dA = pdV (5) Запишем уравнение Менделеева-Клайперона: Где Из уравнения (6) можем записать: Подставим (7) в (5): Подставляя (8) в (2), получим:  Подставим данные в (9): Ответ: |
