Каталитический крекинг. 1. Назначение и общая характеристика установки каталитический крекинг нефть бензин
 Скачать 0.93 Mb. Скачать 0.93 Mb.
|
|
Часть цеолитсодержащих катализаторов крекинга производят по технологии «со связующим», используя в стадии нанесения синтезированного цеолита на поверхность носителя (алюмосиликата) связующий компонент. В качестве «связующего» используют алюмо- или кремнегидрозоль. Затем осуществляют стадии распылительной сушки, ионного обмена термохимической обработкой, нанесения промоторов, вспомогательных добавок, прокаливанию. В этом случае наполнитель жестко фиксирует кристаллики цеолита, создавая пористую систему тончайших транспортных пор для диффузии углеводородов. Содержание цеолита в катализаторе достигает 20 % масс. Нормы технологического режима Таблица 4
4. Химизм процесса КК Химический состав продукта каталитического крекинга имеет характерные особенности: бензин содержит много изопарафинов и ароматических углеводородов; газ получается «тяжелый», с высокой концентрацией изобутана и олефинов С3 – С4; газойлевые фракции богаты полициклическими ароматическими углеводородами. Каталитический крекинг – типичный пример гетерогенного катализа. Реакции протекают на границе двух фаз: твердой (катализатор) и паровой или жидкой (сырье), поэтому решающее значение имеют структура и поверхность катализатора. [9] Каталитический крекинг сочетает в себе реакции, характерные как для термических, так и для термокаталитических процессов. Однако преобладающими реакциями являются реакции распада (или деалкилирования) и изомеризации осколков молекулы. Парафиновые углеводороды, как и при термическом крекинге, распадаются на олефин и парафин меньшей, чем олефин молекулярной массы. Причем распад молекул происходит в нескольких местах углеводородной цепи, но не на самом краю, так как ионы карбония +С2Н5 и +СН3 мало стабильны. Поэтому в реакционной смеси накапливаются газообразные углеводороды С3—С4, предельного и непредельного характера. Одной из отличительных черт процессов, протекающих в присутствии бифункциональных катализаторов, является возможность легко присоединять и передавать водород. Происходит это на металлических (гидрирование — дегидриование) и кислотных (миграция водородного атома) центрах катализатора: 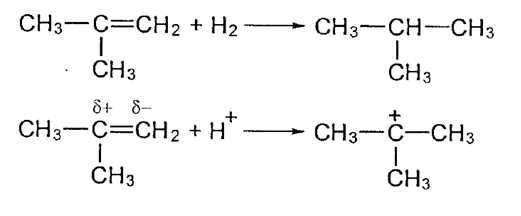 Индукционный эффект метальных групп повышает электронную плотность двойной связи, создавая своего рода отрицательный заряд на одном из атомов углерода. Очевидно, что и протон (положительно заряженный атом водорода) будет легче реагировать с такой «отрицательно заряженной» молекулой. Следствием миграции водорода на поверхности катализатора является развитие при каталитическом крекинге реакций изомеризации углеводородов. В результате жидкие продукты каталитического крекинга обогащены изомерными углеводородами, за счет чего октановое число бензинов каталитического крекинга повышено по сравнению с бензинами термического крекинга. В термокаталитических процессах ароматическим углеводородам свойственны реакции гидрирования, конденсации, но преимущественно реакции изомеризации алкильных заместителей и их последующей отрыв с образованием термически устойчивых моно- и полиметилированных ароматических углеводородов и олефинов. Например: 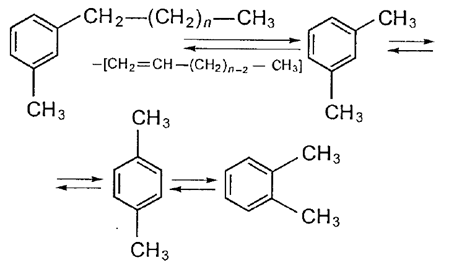 Ароматические углеводороды обладают высокой детонационной стойкостью, поэтому их присутствие в топливе повышает его октановое число. Это еще одно отличие бензинов каталитического крекинга от бензинов термического крекинга — повышенное содержание ароматических углеводородов. Реакции каталитического крекинга — это равновесные реакции, идущие с поглощением тепла и увеличением объема системы. Поэтому для смещения равновесия в сторону образования продуктов температуру процесса необходимо повышать. Давление при этом следует понижать. Добиваются этого разбавлением реакционной смеси водяным паром. Существенное влияние на процесс оказывает состав сырья. Широкие вакуумные фракции — это в основном парафинистое, относительно смолистое и сернистое сырье. Сырье вторичного происхождения отличается от прямогонных газойлей наличием непредельных углеводородов и повышенным содержанием ароматических углеводородов, серы и азота. Очевидно, что при повышенном содержании в исходном сырье непредельных углеводородов на поверхности катализатора будет отлагаться большее количество кокса, поскольку преобладающими станут реакции полимеризации и циклизации олефинов. Введение водяного пара позволяет решить и эту проблему. В ходе каталитического крекинга образуется газ, содержащий значительное количество углеводородов С3—С4 предельного и непредельного характера. Он является сырьем для производства высокооктанового автомобильного и авиационного бензина. В основе этого производства лежит процесс алкилирования, т. е. реакция присоединения к парафиновым углеводородам олефинов с образованием парафинов с разветвленным углеводородным скелетом (С-алкилирование):  Процесс алкилирования базируется на реакциях изомеризации, протекающих на кислотных центрах катализатора. Схематично это можно изобразить так: инициирование цепи — взаимодействие протона катализатора с исходным олефином с образованием карбкатиона:  развитие цепи — реакция карбкатиона с парафином и образование нового более устойчивого карбкатиона или скелетная изомеризация исходного карбкатиона: 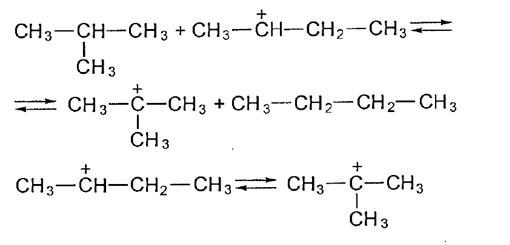 Образовавшийся таким образом карбкатион может прореагировать с исходным парафином: 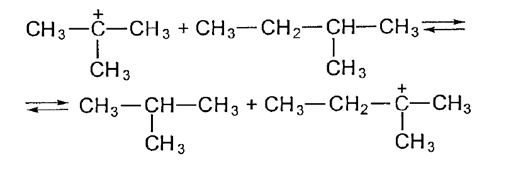 или олефином, присутствующим в реакционной смеси: 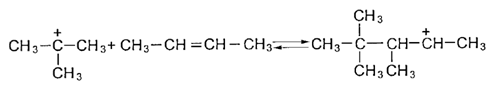 В дальнейшем разветвленные карбкатионы обмениваются протоном с анионом кислоты, регенерируя катализатор, либо с изоалканом с образованием целевого продукта процесса — алкилата (смеси алканов изостроения) — триметилпентанов различного строения.  Вид углеводорода, с которым преимущественно будет реагировать карбкатион, зависит от его концентрации в реакционной смеси. Если концентрация парафина будет многократно превышать концентрацию олефина, то карбкатион будет реагировать с парафином, если же олефина в исходной смеси будет больше, то — с олефином. Обычно алкилирование проводят при избытке изопарафина. Это позволяет избежать реакций полимеризации олефинов. Реакции алкилирования — это реакции присоединения, т. е. реакции, идущие с уменьшением объема системы и выделением тепла. Согласно правилу Jle-Шателье для смещения их равновесия в сторону образования продуктов необходимо по¬нижать температуру проведения процесса и повышать давление в зоне реакции. Такое сочетание параметров снижает вероятность деструктивных процессов. Алкилированием можно получать высокооктановое топливо не только за счет образования высокооктанового разветвленного парафина. Широкое распространение получил синтез метил- третбутилового эфира (МТБЭ) — высокооктанового компонента моторных топлив, в основе которого лежит процесс О-алкилирования изобутилена метанолом:  По сравнению с алкилатом (ОЧи = 89—96) МТБЭ обладает более высоким октановым числом (ОЧи = 115—135) и низкой температурой кипения, что позволяет повысить октановое число низкокипящих фракций. Бутан-бутиленовая фракция каталитического крекинга и пиролиза получила наибольшее применение в качестве сырья для синтеза МТБЭ. В отличие от С-алкилирования катализаторами О-алкилирования являются сульфированные ионообменные смолы, как правило, сульфокатионит со стиролдивинилбензольной основой. Такой катализатор обладает ярко выраженной кислотной функцией. Механизм О-алкилирования во многом схож с механизмом С-алкилирования. Первой стадией является взаимодействие протона (Н+ — ядро водорода) с олефином: инициирование цепи: | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
