Обменные реакции аминокислот. 24 вариант. 1. Общие химические свойства
 Скачать 0.63 Mb. Скачать 0.63 Mb.
|
|
Содержание
Введение По современным данным, биомасса единовременно живущих на Земле организмов составляет 1,8·1012-2,4·1012 т в пересчете на сухое вещество. В организмах, составляющих биомассу Земли, обнаружено свыше 60 химических элементов. Среди них условно выделяют группу элементов, встречающихся в составе любого организма. К их числу относят C, N, H, O, S, P, Na, K, Са, Mg, Zn, Fe, Mn и др. Первым шести элементам приписывают исключительную роль в биосистемах, так как из них построены важнейшие соединения, составляющие основу живой материи – белки, нуклеиновые кислоты, углеводы, липиды и др. Примерно 75% биомассы составляет вода. Вторым же по количественному содержанию в биологических объектах, но, несомненно, первым и главным по значению классом соединений являются белки. Белки состоят из мономерных единиц, т.е. аминокислот. Аминокислоты (аминокарбоновые кислоты) — органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы. Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминные группы. В данной работе мы рассмотрим общие химические свойства аминокислот, их изомерию, классификации α-аминокислот, а также некоторые химические свойства. Глава 1.Общие химические свойства1)Аминокислоты могут проявлять как кислотные свойства, обусловленные наличием в их молекулах карбоксильной группы -COOH, так и основные свойства, обусловленные аминогруппой -NH2. Растворы аминокислот в воде благодаря этому обладают свойствами буферных растворов. Цвиттер-ионом называют молекулу аминокислоты, в которой аминогруппа представлена в виде -NH3+, а карбоксигруппа — в виде -COO-. Такая молекула обладает значительным дипольным моментом при нулевом суммарном заряде. Именно из таких молекул построены кристаллы большинства аминокислот. Некоторые аминокислоты имеют несколько аминогрупп и карбоксильных групп. Для этих аминокислот трудно говорить о каком-то конкретном цвиттер-ионе. 2) Важной особенностью аминокислот является их способность к поликонденсации, приводящей к образованию полиамидов, в том числе пептидов, белков и нейлона-6. 3) Изоэлектрической точкой аминокислоты называют pH, при котором максимальная доля молекул аминокислоты обладает нулевым зарядом. При таком pH аминокислота наименее подвижна в электрическом поле, и данное свойство можно использовать для разделения аминокислот, а также белков и пептидов. 4) Аминокислоты обычно могут вступать во все реакции, характерные для карбоновых кислот и аминов. Глава 2.ИзомерияБольшинство аминокислот, участвующих в биохимических превращениях, содержат первичную аминогруппу, находящуюся в -положении к карбоксильной функции. Во всех природных аминокислотах, входящих в состав белков (за исключением глицина), ‑углеродный атом представляет собой хиральный центр (треонин и изолейцин содержит два ассиметричных атома) и аминокислоты обладают оптической активностью.. Для описания конфигурации в случае -аминокислот обычно используют относительную D,L-номенклатуру. Считают, что кислота относится к L-ряду, если в каноническом написании фишеровской проекции аминогруппа расположена слева (Рис.1).  Рис.1. Конфигурация α-аминокислот Все природные аминокислоты, входящие в состав белков, относятся именно к L-ряду. Данную особенность «живых» аминокислот трудно объяснить, так как в реакциях между оптически неактивными веществами или рацематами (из которых, видимо, состояла древняя Земля) L и D-формы образуются в одинаковых количествах. Креационисты, естественно, могут объяснить это божьим умыслом, остальным же приходится считать, что это — просто результат случайного стечения обстоятельств: самая первая молекула, с которой смог начаться матричный синтез, была оптически активной, а других пригодных молекул почему-то не образовалось. Оптические изомеры аминокислот претерпевают медленную самопроизвольную неферментативную рацемизацию. Например, в белке дентине (входит в состав зубов) L-аспартат переходит в D-форму со скоростью 0,1% в год, что может быть использовано для определения возраста биологических объектов. 3. АминокислотыВ процессе биосинтеза белка в полипептидную цепь включаются 20 важнейших α-аминокислот, кодируемых генетическим кодом.
Помимо этих аминокислот, называемых стандартными, в некоторых белках присутствуют специфические нестандартные аминокислоты, являющиеся производными стандартных. По физиологическому признаку аминокислоты делятся на незаменимые – те аминокислоты, которые не синтезируются в организме человека и высших млекопитающих (Val, Leu, Ile, Thr, Met, Lys, Phe, Trp), полузаменимые – те аминокислоты, которые синтезируются в организме человека, но в недостаточном количестве (Arg, Tyr, His) и обычные – те аминокислоты., которые синтезируются во всех организмах (все остальные). 3.1. Классификация стандартных аминокислот по R-группамТаким образом, -аминокислоты различаются лишь строением радикала R, который называют боковым радикалом или боковой группой. Поскольку с точки зрения абсолютной R,S-стереохимической номенклатуры боковой радикал всегда имеет меньшее старшинство, чем карбоксильная и аминогруппа, все L-аминокислоты имеют S-конфигурацию при -атоме. В зависимости от строения бокового радикала аминокислоты подразделяют на неполярные (содержат неполярный гидрофобный радикал), полярные не заряженные и полярные заряженные (содержат полярный гидрофильный боковой остаток). Часто в отдельную группу выделяют ароматические аминокислоты (фенилаланин, тирозин, триптофан и гистидин). Неполярные: аланин, валин, изолейцин, лейцин, метионин, пролин, триптофан, фенилаланин Полярные незаряженные: аспарагин, глицин, глутамин, серин, тирозин, треонин, цистеин Заряженные отрицательно при pH=7: аспарагиновая кислота, глутаминовая кислота Заряженные положительно при pH=7: аргинин, гистидин, лизин Наиболее распространенные -аминокислоты приведены на Рис.Общие химические свойства. Неполярные аминокислоты 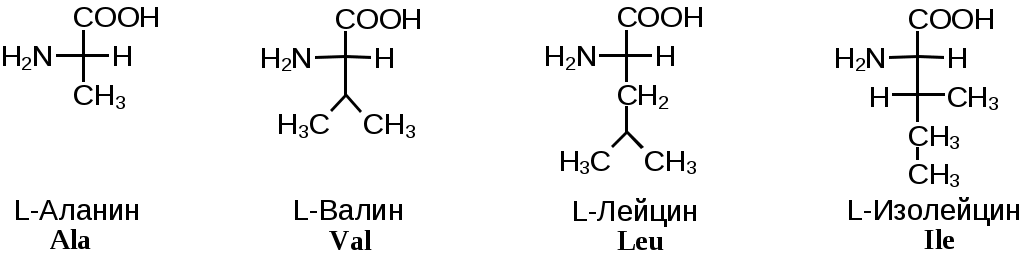 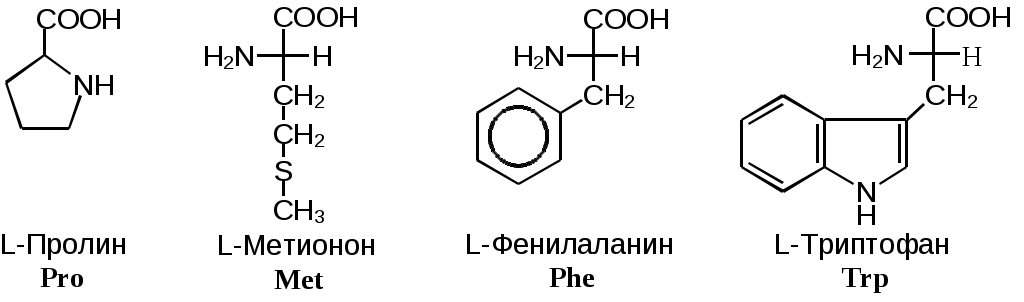 Полярные незаряженные аминокислоты 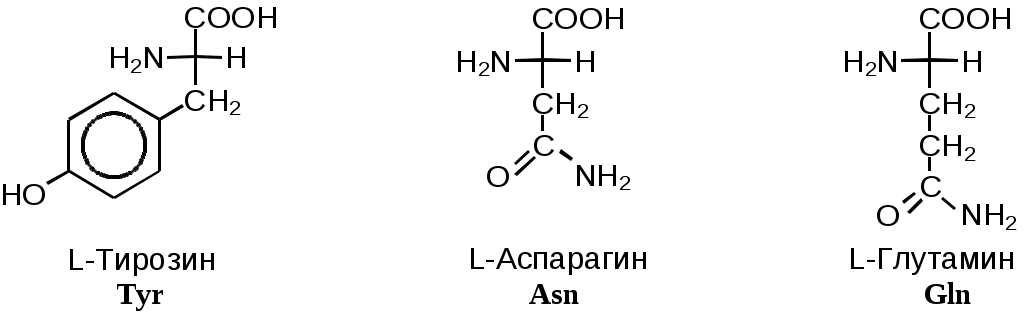 З  аряженные аминокислоты аряженные аминокислоты Рис.Общие химические свойства. Наиболее распространенные α-аминокислоты Сразу следует указать, что в нейтральных растворах все аминокислоты ионизованы (то есть, заряжены). Приведенный выше термин «заряженные аминокислоты» относится исключительно к боковому радикалу аминокислоты и отражает тот факт, что в боковом радикале содержится функциональная группа, которая либо теряет протон при рH, близком к 7, (отрицательно заряженные аминокислоты), либо, наоборот, присоединяет (положительно заряженные аминокислоты). Из 20 -аминокислот, приведенных на Рис.Общие химические свойства, 17 обладают одним хиральным центром (то есть, могут существовать в виде двух энантиомеров), одна ахиральна (глицин) и две имеют два хиральных центра (изолейцин и треонин). Каждая из этих двух аминокислот может существовать в виде четырех стереоизомеров. Рассмотрим стереохимию и номенклатуру этих соединений на примере треонина (Рис. 2).  Рис. 2. Стереоизомеры треонина Встречающийся в белках L-треонин является (2-S, 3‑R)-стереоизомером. Его энантиомер называют D‑треонином. Для обозначения их диастереомеров используют приставку «алло» (алло по-гречески означает другой). 3.2. Классификация стандартных аминокислот по функциональным группамАлифатические Моноаминомонокарбоновые: аланин, валин, глицин, изолейцин, лейцин Оксимоноаминокарбоновые: серин, треонин Моноаминодикарбоновые: аспарагиновая кислота, глутаминовая кислота, за счёт второй карбоксильной группы имеют несут в растворе отрицательный заряд Амиды моноаминодикарбоновых: аспарагин, глутамин Диаминомонокарбоновые: аргинин, гистидин, лизин, несут в растворе положительный заряд Серусодержащие: цистеин (цистин), метионин Ароматические: фенилаланин, тирозин Гетероциклические: триптофан, гистидин, пролин (также входит в группу иминокислот) Иминокислоты: пролин (также входит в группу гетероциклических) 4. Кислотно-основное равновесие в растворе -аминокислот-Аминокислоты обладают как минимум двумя ионогеннными группами — карбоксилом и аминогруппой. Поскольку атом азота и двойная связь C=O разделены двумя ординарными связями, сопряжение карбоксильной группы со свободной электронной парой азота невозможно по пространственным соображениям. Взаимное влияние функциональных групп может осуществляться только по механизму индуктивного эффекта. Поскольку аминогруппа проявляет –I-эффект, который существенно увеличивается при протонировании, она должна повышать кислотность карбоксила. 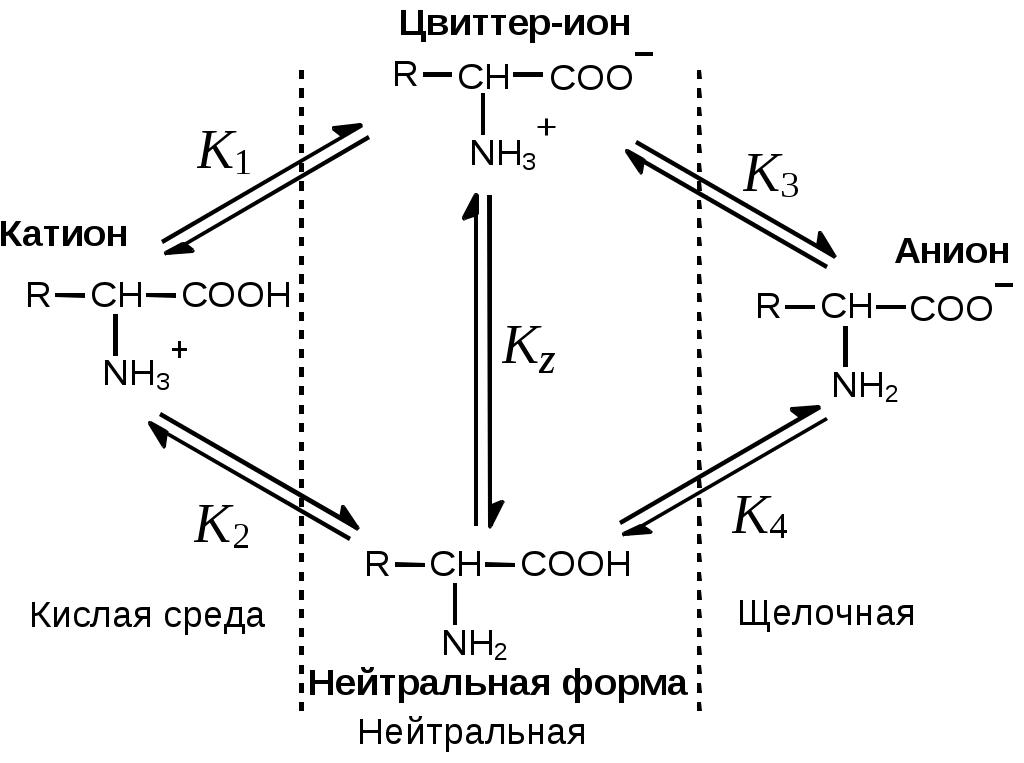 Рис. 3. Кислотно-основное равновесие в растворе α‑аминокислот В свою очередь, неионизованная карбоксильная группа (–I-эффект) должна понижать основность аминогруппы, а ионизованный карбоксил за счет сильного +I-эффекта будет усиливать основные свойства NH2-группы. В сильно кислой среде -аминокислоты существуют в виде двухосновной кислоты (катион на Рис. 3). В сильно щелочной среде будет преобладать анион. В нейтральных средах могут присутствовать две незаряженные формы — нейтральная и биполярная (последнюю часто называют цвиттер-ионом). Соотношение нейтральной и биполярной форм определяется относительной силой двух кислотных группировок катиона (-COOH и ‑NH3+). Чем больше кислотность карбоксильной группы по сравнению с аммонийной (или чем основнее аминогруппа по сравнению с карбоксилат-анионом), тем сильнее равновесие сдвинуто в сторону цвиттер-иона. Аминокислоты в нейтральных средах существуют практически полностью в виде цвиттер-иона. Характеристическое значение рH, при котором концентрация цвиттер-иона максимальна называют изоэлектрической точкой (pI).. Поскольку в целом молекула цвиттер-иона электронейтральна, электропроводность раствора в такой точке будет минимальной, а молекула аминокислоты не будет смещаться в электрическом поле. При отсутствии ионизирующихся групп в боковом радикале изоэлектрическая точка лежит при pH, численно равном среднему арифметическому двух величин pKэфф. В Табл. 1 приведены величины pKэфф и pI некоторых аминокислот. Табл. 1. Экспериментально измеренные pK и изоэлектрические точки -аминокислот
Практически важно, что в изоэлектрической точке аминокислоты обладают наименьшей растворимостью. 5. Некоторые химические свойства -аминокислотХимические свойства -аминокислот в основном определяются поведением содержащихся в них функциональных групп — карбоксильной группы, аминогруппы и функциональной группы бокового радикала (коль скоро таковая присутствует). Здесь мы остановимся на химических особенностях, интересных с биохимической точки зрения. Для обнаружения небольших количеств аминокислот наиболее широко используется нингидриновая реакция (Рис. 4). При нагревании аминокислот с избытком нингидрина образуется продукт лилового цвета, если аминокислота содержит свободную -аминогруппу, и желтый продукт, если, как у пролина, ее ‑аминогруппа защищена. Этот метод обладает высокой чувствительностью и используется как для качественного, так и для количественного (колориметрического) определения аминокислот.  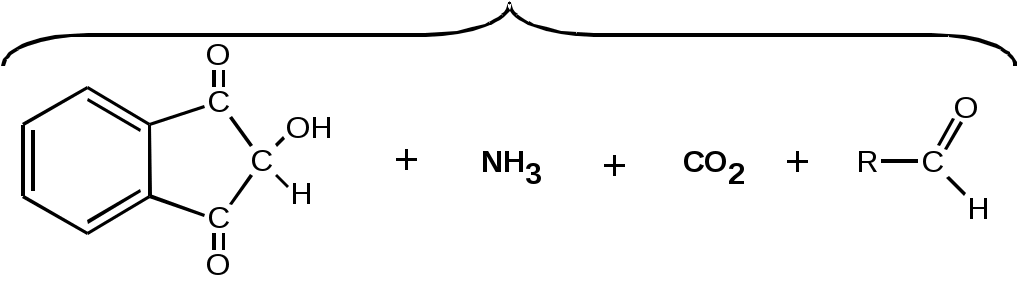 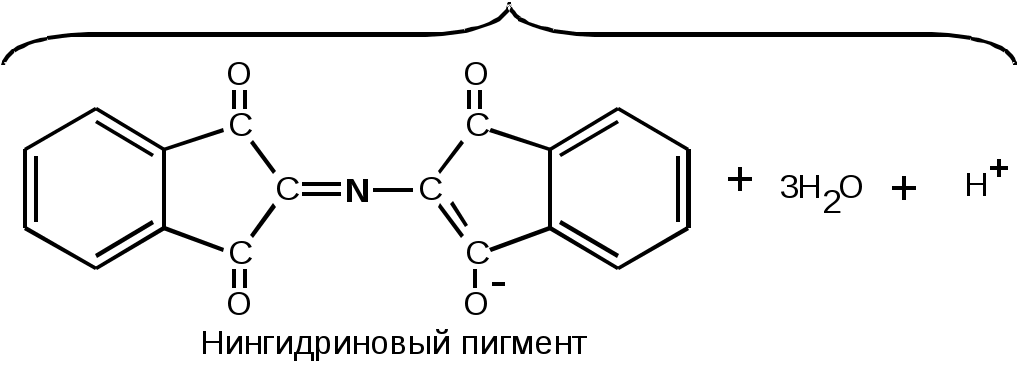 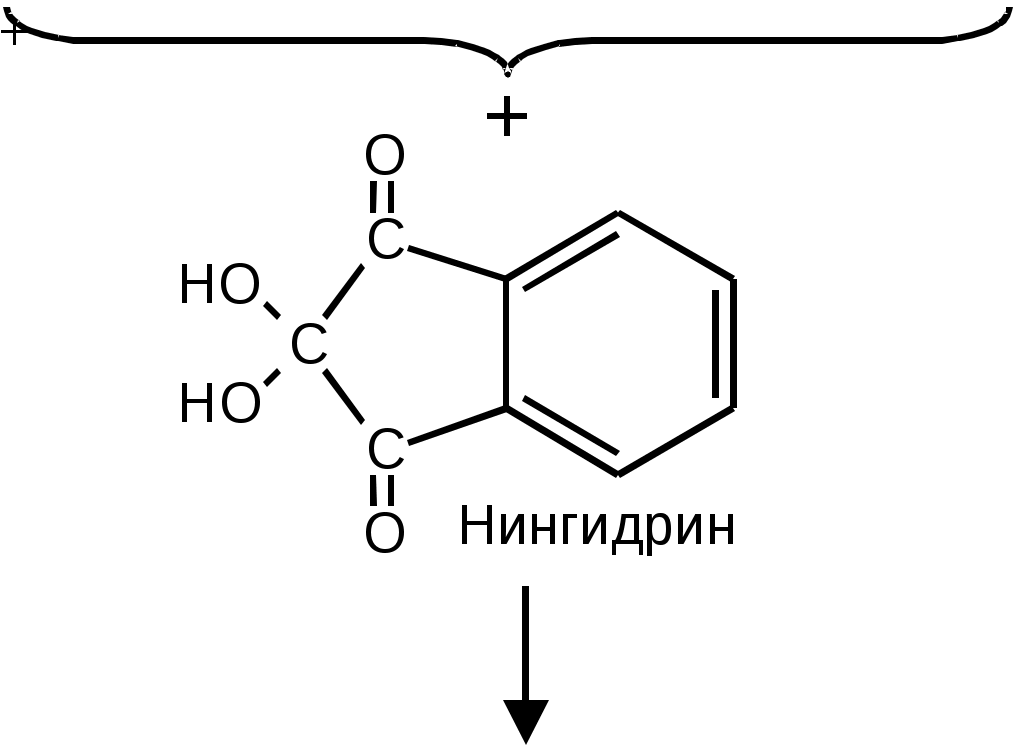 Рис. 4. Нингидриновая реакция, используемая для обнаружения и количественного определения α‑аминокислот. Атомы аминокислоты отмечены жирным шрифтом. Пигмент содержит две молекулы нингидрина и атом азота аминокислоты Для определения аминокислотной последовательности пептидов важное значение имеет реакция аминокислот с 1‑фтор-2,4-динитробензолом (Рис. 5). 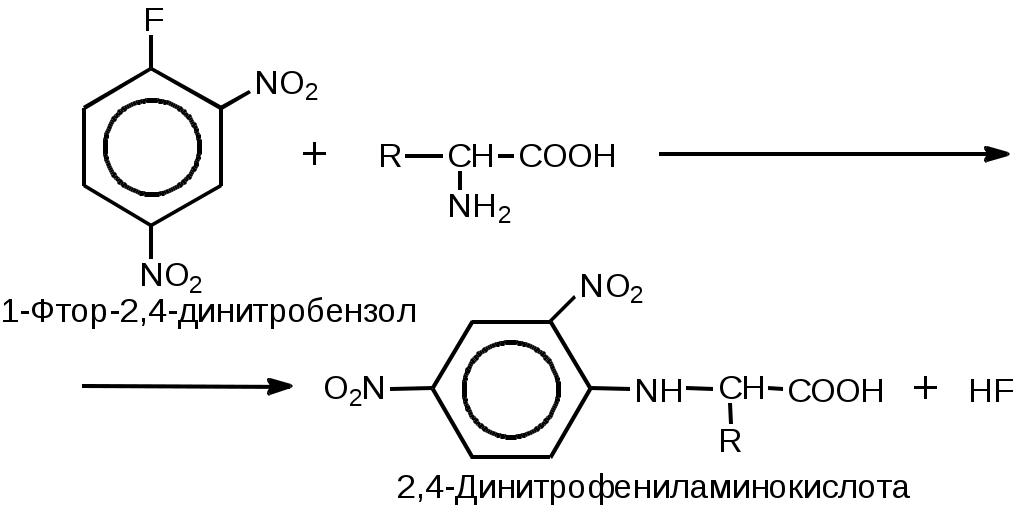 Рис. 5. Образование 2,4-динитрофенильных производных аминокислот SH-Группа цистеина чрезвычайно легко в окислительных условиях образует S–S-связь (Рис. 6).  Рис. 6. Цистеин и цистин. Образование S–S-мостиков. В белках встречается как цистин, так и цистеин Эта реакция проходит уже в присутствии газообразного кислорода. Обратная реакция легко протекает под действием даже слабых восстановителей. Образование S–S-связей играет важную роль в организации третичной структуры белка. Отметим, что все аминокислоты, входящие в состав белков, имеют атом водорода у ‑углеродного атома. Это очень важная особенность, на которой основан метаболизм ‑аминокислот в живых организмах. Заключение Аминокислоты – это «кирпичики», из которых построены молекулы важнейших биополимеров – белков. Многообразие функций, осуществляемых белками в живых организмах, определяется их химической структурой и физико-химическими свойствами. Для понимания строения и свойств аминокислот, которые являются соединениями со смешанными функциями и проявляют как свойства карбоновых кислот, так и свойства аминов, необходимо изучение и азотсодержащих органических соединений, и карбоновых кислот. Список использованных материалов 1. Дюга Т., Пенни К.. Биоорганическая химия. М.: Мир, 1983. 2. Ленинджер А.. Основы биохимии. М.: Мир, 1985. – Т.1-3. 3. Марри Р., Греннер Д., Мейес П., Родуэл В.. Биохимия человека. М.: Мир, 1993. – Т.1-3. 4. Мецлер Д.. Биохимия. М.: Мир, 1980. – Т.1-3. 5. Страйер Л.. Биохимия. М.: Мир, 1985. – Т.1-3. 6. Филиппович Ю. Б. Основы биохимии. М.: Высшая школа, 1985. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
