био 12. 1. По типу наследования
 Скачать 1.25 Mb. Скачать 1.25 Mb.
|
1 2 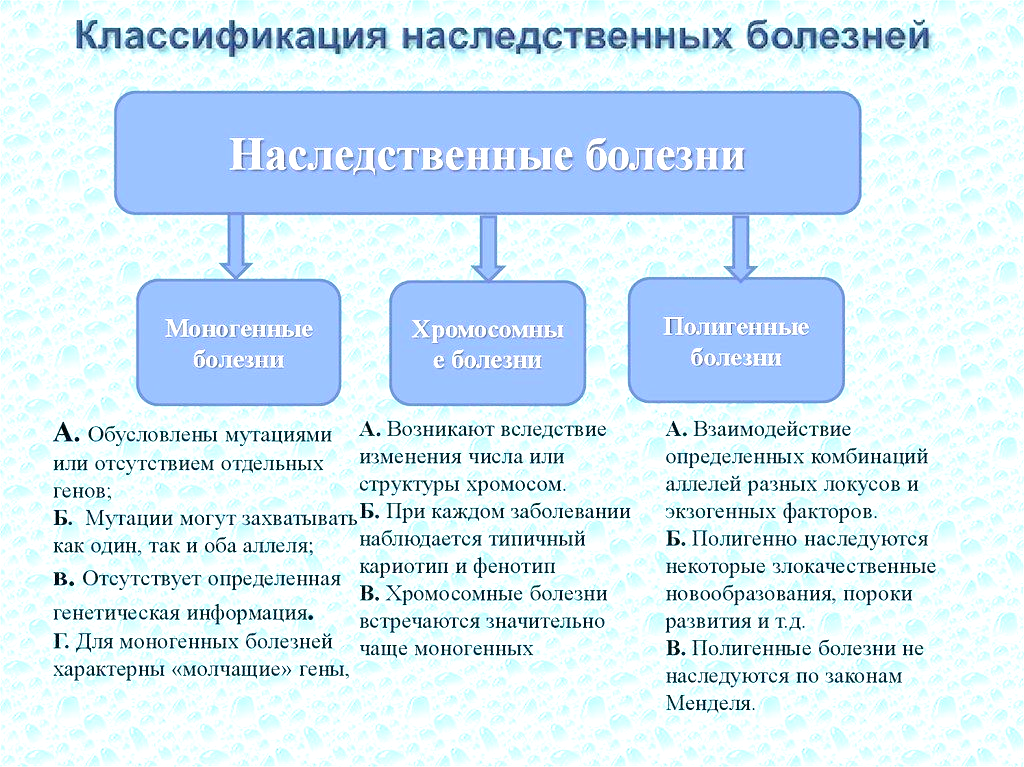 Моногенные болезни (МБ) – это заболевания, в основе этиологии которых лежит единичная генная мутация. 1. По типу наследования: - МЗ с аутосомно-доминантным типом наследования: хорея Гентингтона, нейрофиброматоз, синдромы Марфана, Крузона, Холт-Орама, ПМД лицелопаточноплечевая, оливопонтоцеребеллярная атрофия I типа, ахондроплазия и др.; -МЗ с аутосомно-рецессивным типом наследования: большинство наследственных болезней обмена веществ (фенилкетонурия, галактоземия, мукополисахаридозы и др.), атаксия Фридрейха, спинальная мышечная атрофия I-III типов, альбинизм и др.; -МЗ с Х-сцепленным рецессивным наследованием: ПМД Дюшенна/Беккера, ПМД Эмери-Дрейфуса, гемофилия А и В, бульбоспинальная амиотрофия Кеннеди и др; -МЗ с Х-сцепленным доминантным наследованием: невральная амиотрофия Шарко-Мари-Тус, витамин-Д резистентный рахит, синдром недержания пигмента и др.; -МЗ с митохондриальным (материнским) наследованием: синдромы MELAS, Кернс-Сейра, Пирсона, MERRF и др. 2. В зависимости от того, какая система организма поражается в большей степени: -болезни нервной системы: нервно-мышечные, с преимущественным поражением пирамидной, экстрапирамидной, координаторной систем, лейкодистрофии и др.; -болезни сердечно-сосудистой системы: семейные формы гиперхолестеринемии, гиперлипопротеидемии, сердечный гликогеноз, наследственный амилоидоз и др.; -болезни дыхательной системы: идиопатический диффузный фиброз легких, наследственный спонтанный пневмоторакс, изолированный легочный гемосидероз и др.; -болезни желудочно-кишечного тракта: синдром мальабсорбции, врожденная хлоридная диарея, врожденный дефицит лактазы, целиакия и др.; -болезни соединительной ткани и скелета: несовершенный остеогенез, ахондроплазия, различные формы хондродистрофии, синдром Элерса-Данлоса, мукополисахаридозы и др.; -болезни кожи и ее придатков: ладонно-подошвенная кератодермия, синдром недержания пигмента, пигментная ксеродерма, ихтиоз, синдром Блума и др.; -болезни почек и мочевыводящих путей: наследственный нефрит, поликистоз почек, несахарный диабет, почечный канальцевый ацидоз и др.; -болезни эндокринных органов: врожденный гипотиреоз, гипофизарный нанизм, гипертиреоз и др.; -болезни органов зрения: анофтальмия врожденная, -болезни органов слуха: рахличные типы наследственной глухоты, синдром микротии с атрезией наружного слухового прохода и др.; - болезни половой системы и др. 3.По этиологии: 3.1.Болезни с установленным первичным генетическим дефектом (т.е в зависимости от типа мутации). Этот принцип наиболее сложен, т.к. одно и то же заболевание может быть обусловлено сотнями различных мутаций (для муковисцидоза установлено около 1000 вариантов мутаций), однако он наиболее точен. В настоящее время доля заболеваний с установленным генетическим дефектом невелика, однако она постоянно растет (можно предположить, что у человека минимально может быть до 30-50 тыс. моногенных заболеваний). 3.2.Болезни с неустановленным первичным генетическим дефектом, т.е. около 90% известных на сегодняшний момент форм МЗ. 3.3.Болезни с установленным первичным биохимическим дефектом, т.е в зависимости от того, функция какого субстрата нарушена (белок, фермент и др.). На эту группу МЗ, как и в предыдущем случае приходится меньшая часть заболеваний – около 10%. 3.4.Болезни с неустановленным первичным биохимическим дефектом. В ближайшее десятилетие предполагается изучить первичные биохимические дефекты основной группы наследственных болезней обмена (НБО). Причины алкаптонурии Алкаптонурия относится к числу генетически обусловленных энзимопатий, наследуемых по аутосомно-рецессивному типу, т. е. для развития клинических проявлений заболевания ребенок должен получить от каждого из родителей по одной копии мутантного гена. При алкаптонурии мутации затрагивают ген оксидазы гомогентизиновой кислоты (HGD), локализованный на длинном плече 3 хромосомы (3q 21-23). В результате нарушается воспроизводство фермента гомогентизиназы (гомогентизиновой оксидазы), который участвует в расщеплении тирозина и фенилаланина. В норме гомогентизиновая кислота, являющаяся промежуточным метаболитом обмена тирозина и фенилаланина, под действием гомогентизиназы трансформируется в малеилацетоуксусную кислоту и далее расщепляется до ацетоуксусной и фумаровой кислот, которые затем участвуют в последующих биохимических циклах. При алкаптонурии, в условиях врожденного дефицита фермента, гомогентизиновая кислота не подвергается дальнейшему метаболизму, а превращается в хиноновые полифенолы (пигмент алкаптон), которые накапливаются в соединительных тканях и в больших количествах экскретируются с мочой (до 4-8 г в сутки). Симптомы алкаптонурии Алкаптонурия характеризуется следующими основными симптомокомплексами: гомогентизиновой ацидурией, охронозом и артропатией. Эти признаки возникают в разное время: окрашивание мочи существует с рождения, пигментация тканей становится выраженной к 30 годам, поражение суставов развивается на четвертом десятилетии жизни. Ранние признаки алкаптонурии можно заметить еще в раннем детском возрасте: на мокрых пеленках ребенка остаются темные разводы от мочи, которые невозможно отстирать. Из- за большого количества гомогентизиновой кислоты собранная моча при отстаивании также быстро приобретает темно-бурый цвет. В дальнейшем со стороны мочеполовых органов нередко развиваются пиелонефрит, мочекаменная болезнь, калькулезный простатит. Кожный синдром при алкаптонурии характеризуется появлением серо-коричневой пигментации на лице (в области спинки носа, вокруг губ и глаз), на шее, ладонях, животе, подмышечной и паховой области. Типичным признаком алкаптонурии служит уплотнение и серо-голубое окрашивание ушных раковин, пигментация склеры и конъюнктивы. Диффузное отложение пигмента отмечается в хрящах гортани, что сопровождается охриплостью голоса, одышкой, дисфагией и болью при глотании. Со временем развивается кальцификация аорты и клапанов сердца, следствием чего являются атеросклероз, приобретенные аортальный и митральный пороки. При тяжелых формах алкаптонурии отложение пигмента может встречаться в щитовидной железе, надпочечниках, яичках, поджелудочной железе, селезенке. Поражение опорно-двигательной системы при алкаптонурии, затрагивает, главным образом, крупные суставы нижних конечностей и позвоночник. Раньше всего изменения по типу деформирующего спондилеза развиваются в поясничном, затем в грудном отделе позвоночника. При этом постепенно нарастает сглаженность поясничного лордоза, боли и скованность при движениях, вплоть до полной потери подвижности в пораженных отделах позвоночника. Вслед за поражением позвоночника появляются признаки деформирующего остеоартроза коленных, плечевых и тазобедренных суставов. Характерны артралгии, припухлость суставов (реактивный синовит), крепитация, подвижность, развитие сгибательных контрактур. Нередко при алкаптонурии поражаются крестцово-подвздошные суставы и лонное сочленение Причины галактоземии Галактоземия является врожденной патологией, наследуемой по аутосомно-рецессивному типу, т. е. заболевание проявляется только в том случае, если ребенок наследует две копии дефектного гена от каждого из родителей. Лица, гетерозиготные по мутантному гену, являются носителями заболевания, однако у них тоже могут развиваться отдельные признаки галактоземии в легкой степени. Превращение галактозы в глюкозу (метаболический путь Лелуара) происходит при участии 3-х ферментов: галактоза-1-фосфатуридилтрансферазы (GALT), галактокиназы (GALK) и уридиндифосфат-галактозо-4-эпимеразы (GALE). В соответствии с дефицитом этих ферментов различают 1 (классический вариант), 2 и 3 тип галактоземии. Выделение трех типов галактоземии не совпадает с порядком действия ферментов в процессе метаболического пути Лелуара. Галактоза поступает в организм с пищей, а также образуется в кишечнике в процессе гидролиза дисахарида лактозы. Путь метаболизма галактозы начинается с ее превращения под действием фермента GALK в галактозо-1- фосфат. Затем при участии фермента GALT галактозо-1-фосфат преобразуется в УДФ- галактозу (уридилдифосфогалактозу). После этого с помощью GALE метаболит превращается в УДФ – глюкозу (уридилдифосфоглюкозу). При недостаточности одного из названных ферментов (GALK, GALT или GALE) концентрация галактозы в крови значительно повышается, в организме накапливаются промежуточные метаболиты галактозы, которые вызывают токсическое поражение различных органов: ЦНС, печени, почек, селезенки, кишечника, глаз и др. Нарушение метаболизма галактозы и составляет суть галактоземии. Наиболее часто в клинической практике встречается классический (1 тип) галактоземии, обусловленный дефектом фермента GALT и нарушением его активности. Ген, кодирующий синтез галактоза-1-фосфатуридилтрансферазы, находится в околоцентромерном участке 2-ой хромосомы. Симптомы галактоземии По тяжести клинического течения выделяют тяжелую, среднюю и легкую степени галактоземии. Первые клинические признаки галактоземии тяжелой степени развиваются очень рано, в первые дни жизни ребенка. Вскоре после кормления новорожденного грудным молоком или молочной смесью возникает рвота и расстройство стула (водянистый понос), нарастает интоксикация. Ребенок становится вялым, отказывается от груди или бутылочки; у него быстро прогрессируют гипотрофия и кахексия. Ребенка могут беспокоить метеоризм, кишечные колики, обильное отхождение газов. В процессе обследования ребенка с галактоземией неонатологом выявляется угасание рефлексов периода новорожденности. При галактоземии рано появляется стойкая желтуха различной степени выраженности и гепатомегалия, прогрессирует печеночная недостаточность. К 2-3 месяцу жизни возникают спленомегалия, цирроз печени, асцит. Нарушения процессов свертывания крови приводит к появлению кровоизлияний на коже и слизистых оболочках. Дети рано начинают отставать в психомоторном развитии, однако степень интеллектуальных нарушений при галактоземии не достигает такой тяжести, как при фенилкетонурии. К 1-2 месяцам у детей с галактоземией выявляется двусторонняя катаракта. Поражение почек при галактоземии сопровождается глюкозурией, протеинурией , гипераминоацидурией. В терминальной фазе галактоземии ребенок погибает от глубокого истощения, тяжелой печеночной недостаточности и наслоения вторичных инфекций. При галактоземии средней тяжести также отмечается рвота, желтуха, анемия, отставание в психомоторном развитии, гепатомегалия, катаракта, гипотрофия. Галактоземия легкой степени характеризуется отказом от груди, рвотой после приема молока, задержкой речевого развития, отставанием ребенка в массе и росте. Однако даже при легком течении галактоземии продукты обмена галактозы токсическим образом воздействуют на печень, приводя к ее хроническим заболеваниям. Галактоземия может протекать в моносимптомной форме, при которой обнаруживается только поражение ЦНС, катаракта или диспепсические расстройства. Описан вариант бессимптомной (асимптоматической) галактоземии Дюарте, при которой недостаточность ферментов выявляется только при биохимическом исследовании крови.
яичников. При галактоземии у 50% детей дошкольного возраста выявляется моторная алалия, характеризующаяся трудностью организации и координации речевых движений, бедностью словарного запаса, обилием парафазий и персевераций при сохранном понимании обращенной речи.
обусловленное мутацией гена трансмембранного регулятора муковисцидоза (МВТР) и характеризующееся поражением желез внешней секреции, тяжёлыми нарушениями функций органов дыхания и желудочно-кишечного тракта. Это самое распространенное среди известных наследственных заболеваний. Каждый 20-й житель планеты является носителем дефектного гена. Рождение больного ребенка возможно на 25%, если оба родителя являются носителями генетического дефекта. 70 % случаев муковисцидоза выявляются в течение первых 2 лет жизни ребёнка. С внедрением неонатального скрининга время выявления значительно сократилось. Слово «муковисцидоз» происходит от латинских слов mucus — «слизь» и viscidus — «вязкий». Это название означает, что секреты (слизь), выделяемые различными органами, имеют слишком высокую вязкость и густоту. В результате страдают все эти органы: бронхолегочная система, поджелудочная железа, печень, железы кишечника, потовые и слюнные железы, половые железы. В легких из-за скапливающейся вязкой мокроты развиваются воспалительные процессы. Нарушается вентиляция и кровоснабжение легких. Возникает мучительный кашель — это один из постоянных симптомов болезни. Легкие легко инфицируются, чаще всего стафилококком или синегнойной палочкой. У больных развиваются повторяющиеся бронхиты и пневмонии, иногда уже с первых месяцев жизни. Инфекция еще сильнее увеличивает вязкость мокроты. Такие состояния крайне опасны для жизни больного. Именно от дыхательной недостаточности погибает подавляющее большинство больных детей и взрослых. Из-занедостатка ферментов поджелудочной железы у больных муковисцидозом плохо переваривается пища, поэтому такие дети, несмотря на повышенный аппетит, отстают в весе. Из-за застоя желчи у некоторых детей развивается цирроз печени, могут сформироваться камни в желчном пузыре. Вы можете себе представить, что значит жить, не снимая противогаза? Противогаза, который с каждым днем работает все хуже и хуже. Примерно так живут больные муковисцидозом. Их легкие работают лишь на 25%. Существует несколько форм муковисцидоза: легочная форма, кишечная форма, но чаще всего наблюдается смешанная форма муковисцидоза с одновременным поражением желудочно-кишечного тракта и органов дыхания. Встречаются также и другие формы болезни. Больные муковисцидозом не заразны и умственно совершенно полноценны. Среди них много по-настоящему одаренных и интеллектуально развитых детей. Они особенно успешно занимаются делами, которые требуют покоя и сосредоточенности — изучают иностранные языки, много читают и пишут, занимаются творчеством, из них получаются замечательные музыканты, художники. Больные муковисцидозом могут создавать семьи. Если второй супруг не является носителем дефектного гена, такие пары могут иметь здоровых детей. Фенилкетонурия Фенилкетонурия (phenyiketonuria; фенилаланин + кетоны + греч. uron моча; синоним: фенилпировиноградная олигофрения, болезнь Феллинга) — наследственная болезнь, обусловленная нарушением обмена фенилаланина; проявляется отставанием в физическом развитии и прогрессирующим слабоумием, расстройствами движений и мышечного тонуса. Средняя частота встречаемости патологии по результатам массовых обследований новорожденных составляет 1:10 000; мальчики и девочки болеют одинаково часто, однако мальчики чаще погибают на 1-м году жизни.
L-фенилаланина в тирозин. Наследуется по аутосомно-рецессивному типу. Фенилаланин является незаменимой аминокислотой для построения белковой молекулы и, кроме того, служит предшественником гормонов щитовидной железы (в частности, тироксина), адреналина и меланина. Метаболический блок при отсутствии
прогрессирующего слабоумия; нарушения аминокислотного равновесия организма как в жидкостных его средах, так и клетках. Установлена не только генетическая и клиническая неоднородность аномалий обмена фенилаланина, но и обнаружены дефекты обмена или синтеза биоптерина, приводящие к развитию атипичных форм фенилкетонурии Несмотря на то, что последние встречаются нечасто и составляют не более 10% всех случаев фенилкетонурии, знание их чрезвычайно важно вследствие различий в биохимической картине патологии и специфической терапевтической тактике.
беспокойны, не фиксируют взгляд на предметах, не поворачиваются к источнику звука, поздно начинают гулить. Обычно ранними симптомами болезни являются запах плесени, исходящий от мочи и кожи ребенка, рвота, трудности вскармливания (часто в сочетании с пилоростенозом), а также повышенная возбудимость и двигательная гиперактивность, отставание в физическом развитии, отчетливо проявляющееся во втором полугодии жизни. В это время отмечается прогрессирование основного признака фенилкетонурии — задержка психического развития (фенилпировиноградная олигофрения); позднее присоединяются пирамидные знаки, атаксии, гиперкинезы. Значительно задерживается формирование моторных функций, примерно у четверти больных фенилкетонурией развиваются судороги.
поведения.Клинических отличий классической и атипичных форм фенилкетонурии не существует. Форма фенилкетонурии выявляется только в процессе лечения. Для атипичных форм характерно прогрессирование проявлений болезни, несмотря на адекватное лечение с помощью диеты. При классической форме под влиянием диеты с резким ограничением проектов, содержащих фенилаланин, клинические проявления редуцируются. Многофакторные (мультифакториальные) болезни, или болезни с наследственной предрасположенностью, развиваются в результате взаимодействия определенных комбинаций аллелей разных локусов и специфического воздействия факторов окружающей среды. К многофакторным болезням относят гипертоническую болезнь, нарушения мозгового кровообращения, тромбозы, большинство сердечно-сосудистых заболеваний и опухолей. Осложнения беременности также имеют многофакторную природу. При мультифакториальных болезнях важную роль играет как носительство «аллелей риска», так и наличие провоцирующих факторов. Заболевают не все носители «аллелей риска», а те, у кого вредные для данного индивидуума факторы накладываются на предрасполагающий генетический фон. Пусковым механизмом может стать беременность, особенности питания, прием лекарств, образ жизни и другие факторы. Просим учесть, что обнаруженные генетические особенности человека, называемые генетическими факторами риска, не означают наличия или отсутствия указанного заболевания. Выявление генетических полиморфизмов и составление индивидуального «генетического паспорта» позволяет реализовать концепцию индивидуальной медицины, дать персональные рекомендации по профилактике, оценить необходимость более пристального врачебного контроля, назначить дополнительные исследования и консультации специалистов. В ряде случаев своевременное изменение образа жизни, соблюдение диеты или прием фармакологических препаратов позволяет предотвратить или существенно снизить тяжесть многофакторного заболевания. При этом важно помнить, что только лечащий врач может ответить на вопрос: необходимы ли дополнительные исследования и/или консультации специалистов (и если да, то какие), необходимо ли изменение образа жизни или лечение. . Болезнь развивается при превышении определенных значений предрасположенности — «порога подверженности». Порог подверженности — это определенное значение непрерывно возрастающей восприимчивости к заболеванию, превышение которого приводит к развитию болезни при воздействии дополнительных средовых факторов (прерывистые мультифакториальные признаки). Таким образом, при благоприятных условиях среды может не заболеть индивид с высокой подверженностью, а при плохих — болезнь может развиться у индивида с относительно низкой подверженностью. 6. Понятие и классификация врожденных пороков развития. Врожденными пороками развития называют такие структурные нарушения, которые возникают до рождения (в пренатальном онтогенезе), выявляются сразу или через некоторое время после рождения и вызывают нарушение функции органа. Последнее отличает врожденные пороки развития органов от аномалий, при которых нарушение функции обычно не наблюдается. Врожденные пороки развития являются причиной приблизительно 20% смертей в неонатальном периоде, а также занимают значительное место в практике акушерства и гинекологии, медицинской генетике детской хирургии и ортопедии, патологической анатомии. В связи с этим знания по вопросам профилактики, этиологии, патогенеза, лечения и прогнозирования врожденных пороков развития имеют большое значение. Знакомство с закономерностями и механизмами нормального морфогенеза в процессе эмбрионального развития позволяет понять, какого рода нарушения могут привести к возникновению пороков. Кроме того, пороки развития представляют собой как бы природные эксперименты, обнаруживающие скрытые от глаз процессы. Таким образом, сами эти пороки представляют собой материал для научных поисков и обобщений. Примером могут служить такие врожденные пороки развития, которые напоминают некоторые черты строения, свойственные другим видам взрослых позвоночных животных или их зародышам. Они позволяют осознать теснейшую эволюционно-биологическую связь человека с животными и использовать ее для иллюстрации закономерностей макроэволюции, а также для формирования естественноисторического взгляда на возникновение и развитие человека. Существует несколько различных критериев, на основе которых классифицируют врожденные пороки развития. Основные из них следующие: причина, стадия, на которой проявляется воздействие, последовательность их возникновения в организме, распространенность и локализация. Мы дополнительно обращаем внимание на филогенетическую значимость и нарушения основных клеточных механизмов, приводящие к пороку развития. В зависимости от причины все врожденные пороки развития делят на наследственные, экзогенные ( средовые) и мультифакториальные. Наследственными называют пороки, вызванные изменением генов или хромосом в гаметах родителей, в результате чего зигота с самого возникновения несет генную, хромосомную или геномную мутацию. Генетические факторы начинают проявляться в процессе онтогенеза последовательно, путем нарушения биохимических, субклеточных, клеточных, тканевых, органных и организменных процессов. Время проявления нарушений в онтогенезе может зависеть от времени вступления в активное состояние соответствующего мутированного гена, группы генов или хромосом. Последствия генетических нарушений зависят также от масштаба и времени проявления нарушений. Экзогенными называют пороки, возникшие под влиянием тератогенных факторов (лекарственные препараты, пищевые добавки, вирусы, промышленные яды, алкоголь, табачный дым и др.), т.е. факторов внешней среды, которые, действуя во время эмбриогенеза, нарушают развитие тканей и органов. Историческими вехами являются работы Ц. Стоккарта в начале XX в., впервые показавшего тератогенное действие алкоголя, и работы офтальмолога Н. Грегга, открывшего тератогенное действие вируса краснухи (1941). Очень страшное событие имело место в 1959—1961 гг., когда после применения беременными талидомида в ряде стран Запада родились несколько десятков тысяч детей с тяжелыми врожденными пороками. Поскольку средовые экзогенные факторы в конечном итоге оказывают влияние на биохимические, субклеточные и клеточные процессы, механизмы возникновения врожденных пороков развития при их действии такие же, как при генетических причинах. В результате фенотипическое проявление экзогенных и генетических пороков бывает весьма сходным, что обозначается термином фенокопия. Для выявления истинных причин возникновения пороков в каждом конкретном случае следует привлекать множество различных подходов и критериев. Мультифакториальными называют пороки, которые развиваются под влиянием как экзогенных, так и генетических факторов. Вероятно, скорее всего бывает так, что экзогенные факторы нарушают наследственный аппарат в клетках развивающегося организма, а это приводит по цепочке ген — фермент — признак к фенокопиям. Кроме того, к этой группе относят все пороки развития, в отношении которых четко не выявлены генетические или средовые причины. Установление причины врожденных пороков имеет большое прогностическое значение для носителя этих пороков и профилактическое — в отношении последующего потомства. В настоящее время медицинские генетики и патологоанатомы существенно продвинулись в области так называемого синдромологического анализа. Синдромологический анализ — это обобщенный анализ фенотипа больных с целью выявления устойчивых сочетаний признаков. Овладение им помогает в установлении причины возникновения пороков и основных патогенетических механизмов. Взависимости от стадии, на которой проявляются генетические или экзогенные воздействия, все нарушения, происходящие в пренатальном онтогенезе, подразделяют на гаметопатии, бластопатии, эмбриопатии и фетопатии. Если нарушения развития на стадии зиготы (гаметопатия) или бластулы (бластопатия) очень грубые, то дальнейшее развитие, видимо, не идет и зародыш погибает. Эмбриопатии (нарушения, возникшие в период от 15 сут до 8 нед эмбрионального развития) как раз составляют основу врожденных пороков, о чем уже говорилось выше. Фетопатии (нарушения, возникшие после 10 нед эмбрионального развития) представляют собой такие патологические состояния, для которых, как правило, характерны не грубые морфологические нарушения, а отклонения общего типа: в виде снижения массы, задержки интеллектуального развития, различных функциональных нарушений. Очевидно, что наибольшее клиническое значение имеют эмбриопатии и фетопатии. Взависимости от последовательности возникновения различают первичные и вторичные врожденные пороки. Первичные пороки обусловлены непосредственным действием тератогенного фактора, вторичные — являются осложнением первичных и всегда патогенетически с ними связаны. Выделение первичных пороков из комплекса нарушений, обнаруженных у пациента, имеет большое значение для медико-генетического прогноза, поскольку риск определяется по основному пороку. По распространенности в организме первичные пороки подразделяют на изолированные, или одиночные, системные, т.е. в пределах одной системы, и множественные, т.е. в органах двух систем и более. Комплекс пороков, вызванный одной ошибкой морфогенеза, называют аномаладом. В основу классификации врожденных пороков, принятой Всемирной организацией здравоохранения (ВОЗ), положен анатомо-физиологический принцип (по месту локализации). По клеточным механизмам, которые преимущественно нарушены при том или ином врожденном пороке развития, можно выделить пороки, возникшие в результате нарушения размножения клеток, миграции клеток или органов, сортировки клеток, дифференцировки, а также гибели клеток. Нарушение перечисленных клеточных механизмов может привести к слишком малым или, наоборот, слишком большим размерам органов или их частей, к недостаточному или, напротив, очень сильному рассасыванию тканей в органах, к изменению положения отдельных клеток, тканей или органов относительно других органов и тканей, к нарушениям дифференцировки, так называемым дисплазиям. По филогенетической значимости можно все врожденные пороки развития разделить на филогенетически обусловленные и не связанные с предшествующим филогенезом, т.е. нефилогенетические. Филогенетически обусловленными называют такие пороки, которые по виду напоминают органы животных из типа Хордовые и подтипа Позвоночные. Если они напоминают органы предковых групп или их зародышей, то такие пороки называют анцестральными (предковыми) или атавистическими. Примерами могут служить несращение дужек позвонков, шейные и поясничные ребра, несращение твердого нёба, персистирование висцеральных дуг и др. Если пороки напоминают органы родственных современных или древних, но боковых ветвей животных, то их называют аллогенными. Филогенетически обусловленные пороки показывают генетическую связь человека с другими позвоночными, а также помогают понять механизмы возникновения пороков в ходе эмбрионального развития. + Нефилогенетическими являются такие врожденные пороки, которые не имеют аналогов у нормальных предковых или современных позвоночных животных. К таким порокам можно отнести, например, двойниковые уродства и эмбриональные опухоли, которые появляются в результате нарушения эмбриогенеза, не отражая филогенетических закономерностей. Так, известно, что в проксимальном участке хромосомы 15 имеются близко сцепленные, но противоположно импринтированные локусы, отвечающие за возникновение двух фенотипически разных синдромов - Прадера-Вилли и Энгельмана. Для синдрома 1 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
