12. Строение и биологические функции мононуклеотидов
 Скачать 258 Kb. Скачать 258 Kb.
|
|
12.Строение и биологические функции мононуклеотидов. Нуклеотиды состоят из нуклеозидов. Нуклеозид – это фрагмент нуклеотида, который состоит из азотистого основания и моносахаридного остатка, соединенные N-гликозидной связью. Азотистые основания в зависимости от строения разделяются на пуриновые (аденин, гуанин, два цикла, производные пурина) и пиримидиновые (урацил, тимин, цитозин, один цикл, производные пиримидина). Мононуклеотид состоит из одного азотистого основания — пуринового (аденин — А, гуанин — Г) или пиримидинового (цитозин — Ц, тимин — Т, урацил — У), сахара-пентозы (рибоза или дезоксирибоза) и 1—3 остатков фосфорной кислоты . По своему строению нуклеиновые кислоты являются полинуклеотидами, состоящими из мононуклеотидовили нуклеотидов. Нуклеотид сложное органическое соединение, состоящее из трех частей: азотистого основания, углевода и остатков фосфорной кислоты. Азотистые основания - это гетероциклические органические соединения, относящиеся к двум классам – пурины и пиримидины. Из пуринов в состав нуклеиновых кислот входят аденин и гуанин 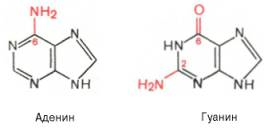 А из пиримидинов цитозин, тимин(ДНК) и урацил(РНК) . 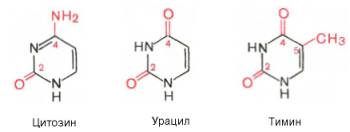 Углеводом, входящим в состав нуклеотидов может быть рибоза (РНК) и дезоксирибоза (ДНК) 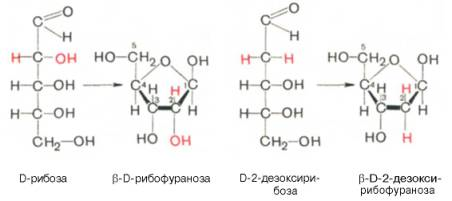 Азотистое основание, связанное с углеводом называется нуклеозидом.Фосфорная кислота присоединяется эфирной связью к пятому атому углерода рибозы или дезоксирибозы. Нуклеотиды, входящие в состав нуклеиновых кислот имеют один остаток фосфорной кислоты и называются мононуклеотидами. Однако в клетке встречаются ди- и тринуклеотиды. 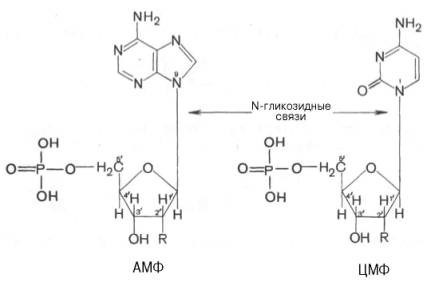 Например, нуклеотид, состоящий из аденина, рибозы и одного остатка фосфорной кислоты называется аденозинмонофосфат или АМФ, а из цитозина и одного остатка фосфорной кислоты цитозинмонофосфат или ЦМФ. Функции мононуклеотидов: 1) структурная -- построение нуклеиновых кислот, некоторых коферментов и простетических групп ферментов; 2) энергетическая -- аккумуляторы энергии за счет имеющихся макроэргических связей. АТ Ф -- универсальный аккумулятор энергии, энергия УТ Ф используется для синтеза гликогена, ЦТ Ф -- для синтеза липидов, ГТФ -- для движения рибосом в ходе трансляции (биосинтез белка) и передачи гормонального сигнала (G-белок); 3) регуляторная: мононуклеотиды -- аллостерические эффекторы многих ключевых ферментов, цАМФ и цГМФ -- посредники в передаче гормонального сигнала при действии многих гормонов на клетку (аденилатциклазная система), активируют протеинкиназы. 28. Витамин «P», химическое строение, биологическая роль, явление недостаточности, значение и суточная потребность. Витамин Р (рутин, биофлавоноиды) относится к веществам, которые организм человека не способен вырабатывать сам. Поэтому он представляет для него особую ценность. Регулярное применение витамина Р нормализует состояние стенок капилляров, повышая их прочность и эластичность, снижает артериальное давление, замедляет сердечный ритм. Считается, что ежедневное применение рутина в количестве 60 мг может снизить внутриглазное давление. Правда, при этом профилактический курс должен составлять не менее четырёх недель. Витамин P, также, участвует в желчеобразовании, помогает регулировать суточную норму выделения мочи и деликатно стимулирует функцию коры надпочечников. Он сдерживает выработку гистамина и серотонина, обладает противооттечным и обезболивающим действием. Тем самым, витамин Р облегчает и ускоряет течение аллергических реакций, в частности бронхиальной астмы. Строение Витамин Р, строго говоря, является не витамином, а группой витаминоподобных веществ (до 600 представителей) разнообразного строения, содержащих в своей основе бензапироновое кольцо, соединенное с гидроксилированным фенолом, также имеются метильные группы, производные различных остатков сахаров (рамноза, глюкоза и др.). 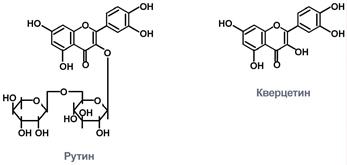 Суточная потребность в витамине P: в зависимости от образа жизни, 35-50 мг в день. Растущему организму, а также лицам занятым тяжелой работой (физической или умственной, не имеет значения), спортсменам, при различных заболеваниях и стрессах потребность организма в витамине Р увеличивается. Недостаток витамина P: недостаток флавоноидов в первую очередь приводит к слабости капилляров, что в дальнейшем может привести к развитию тяжёлых заболеваний, опасных для жизни. Симптомы недостатка рутина: кровоизлияния на слизистых оболочках, общая слабость и вялость, быстрая утомляемость, боли в ногах и руках, кровоточивость дёсен, мозговые кровотечения и отёк мозга, заболевание сердца, лёгких и других органов. Гиповитаминоз витамина P приводит к развитию угревой сыпи и синюшного оттенка кожи, также выпадение волос может стать сигналом о недостатке биофлавоноидов в организме. Биологическая роль:Функции витамина Р в организме во многом повторяют функции, выполняемые витамином С. В ряде процессов они участвуют вместе, усиливая полезные эффекты друг друга. Итак, роль витамина Р: 1.Укрепляет капилляры, уменьшает их ломкость, улучшает качество микроциркуляции. Это помогает добиться уменьшения кровоточивости и склонности к появлению синяков, повысить качество питания органов и тканей, добиться положительных косметических эффектов. Последние заключаются в улучшении микроциркуляции в дерме и волосяных луковицах, что положительно сказывается на состоянии кожи и волос. 2.Улучшает обмен веществ в тканях, их дыхание. Это обеспечивает витамину универсальное оздоровительное воздействие. 3.Антиоксидантный эффект рутина приводит к омоложению. Это может быть заметно не только внешне; во внутренних органах тоже происходят процессы, замедляющие старение. В частности, замедляется развитие атеросклероза в сосудах. 4.Способствует нормализации артериального давления. 5.Укрепляет иммунитет, усиливает его противодействие агрессивным инфекционным возбудителям. 44.Окислительное декарбоксилирование пировиноградной кислоты. Окисление пирувата до ацетил-КоА происходит при участии ряда ферментов и коферментов, объединенных структурно в мультиферментную систему, получившую название «пируватдегидрогеназный комплекс». На I стадии этого процесса пируват (рис. 10.8) теряет свою карбоксильную группу в результате взаимодействия с тиаминпирофосфатом (ТПФ) в составе активного центра фермента пируватдегидрогеназы (E1). На II стадии оксиэтильная группа комплекса E1–ТПФ–СНОН–СН3 окисляется с образованием ацетильной группы, которая одновременно переносится на амид липоевой кислоты (кофермент), связанной с ферментом дигидроли-поилацетилтрансферазой (Е2). Этот фермент катализирует III стадию – перенос ацетильной группы на коэнзим КоА (HS-KoA) с образованием конечного продукта ацетил-КоА, который является высокоэнергетическим (макроэргическим) соединением. На IV стадии регенерируется окисленная форма липоамида из восстановленного комплекса дигидролипоамид–Е2. При участии фермента дигидролипоилдегидрогеназы (Е3) осуществляется перенос атомов водорода от восстановленных сульфгидрильных групп дигидролипоамида на ФАД, который выполняет роль простетической группы данного фермента и прочно с ним связан. На V стадии восстановленный ФАДН2 дигидро-липоилдегидрогеназы передает водород на кофермент НАД с образованием НАДН + Н+. Процесс окислительного декарбоксилирования пирувата происходит в матриксе митохондрий. В нем принимают участие (в составе сложного мультиферментного комплекса) 3 фермента (пируватдегидрогеназа, ди-гидролипоилацетилтрансфераза, дигидролипоилдегидрогеназа) и 5 кофер-ментов (ТПФ, амид липоевой кислоты, коэнзим А, ФАД и НАД), из которых три относительно прочно связаны с ферментами (ТПФ-E1, ли-поамид-Е2 и ФАД-Е3), а два – легко диссоциируют (HS-KoA и НАД). 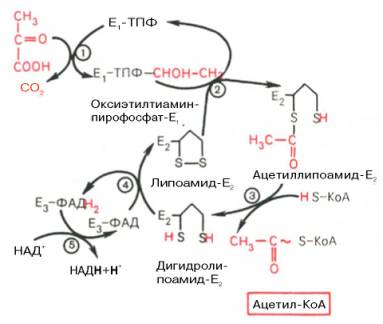 Рис. 10.8. Механизм действия пируватдегидрогеназного комплекса. 60.Дезаминирование аминокислот :окислительное дезаминирование глутаминовой кислоты.Обезвреживание аммиака в организме. Дезаминирование – процесс удаления аминогруппы из аминокислот и выделение ее в виде аммиака. Углеродный скелет аминокислоты превращается в кетокислоту. Трансаминирование и дезаминирование протекает в клетке одновременно и часто ключевой молекулой является глутамат. В природе известны четыре основных типа дезаминирования. Восстановительное дезаминирование: 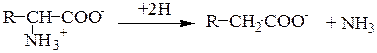 Гидролитическое дезаминирование: 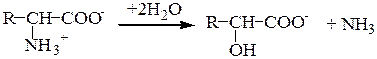 Внутримолекулярное дезаминирование: 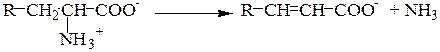 Окислительное дезаминирование: 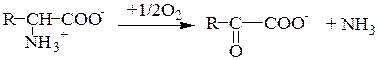 Окислительное дезаминирование глутамата -обратимая реакция и при повышении концентрации аммиака в клетке может протекать в обратном направлении, как восстановительное шинирование α-кетоглутарата. Глутаматдегидрогеназа очень активна в митохондриях клеток практически всех органов, кроме мышц. Глутаматдегидрогеназа играет важную роль, так как является регуляторным ферментом аминокислотного обмена. Аллостерические ингибиторы глутаматдегидрогеназы (АТФ, ГТФ, NADH) вызывают диссоциацию фермента и потерю глутаматдегидрогеназной активности. Высокие концентрации АДф активируют фермент. Таким образом, низкий энергетический уровень в клетках стимулирует разрушение аминокислот и образованиеα-кетоглутарата, поступающего в ЦТК как энергетический субстрат. Глутаматдегидрогеназа может индуцироваться стероидными гормонами (кортизолом). 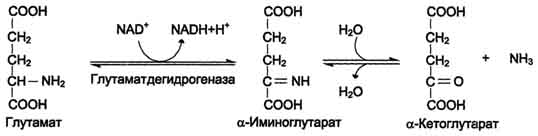 Обезвреживание аммиака в организме.Для удаления аммиака из организма используется включение его в состав мочевины в печени и выведение ее с мочой, и удаление почками в виде аммонийных солей. Однако, так как аммиак является чрезвычайно токсичным соединением, то предварительно в тканях (!) происходят реакции его обезвреживания (временного связывания) для переноса в печень и почки. – синтез глутаминовой кислоты и глутамина, синтез аспарагина: 1.Синтез глутаминовой кислоты (восстановительное аминирование) – взаимодействие α-кетоглутарата с аммиаком. Реакция по сути обратна реакции окислительного дезаминирования, однако в качестве кофермента используется НАДФН. Происходит практически во всех тканях, кроме мышечной, но имеет небольшое значение, т.к. для глутаматдегидрогеназы предпочтительным субстратом является глутаминовая кислота и равновесие реакции сдвинуто в сторону α-кетоглутарата, 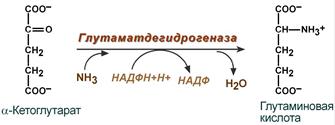 Реакция синтеза глутаминовой кислоты2. Синтез глутамина. – взаимодействие глутамата с аммиаком. Является главным способом уборки аммиака, наиболее активно происходит в нервной и мышечной тканях, в почках, сетчатке глаза, печени. Реакция протекает в митохондриях.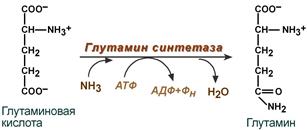 Реакция синтеза глутаминаОбразование большого количества глутамина обеспечивает высокие концентрации его в крови (0,5-0,7 ммоль/л). Так как глутамин проникает через клеточные мембраны путем облегченной диффузии, то он легко попадает не только в гепатоциты, но и в другие клетки, где есть потребность в аминогруппах. Азот, переносимый глутамином, используется клетками для синтеза пуринового кольца и гуанозинмонофосфата (ГМФ), синтеза цитидинтрифосфата (ЦТФ), аспарагина, глюкозамино-6-фосфата (предшественник всех остальных аминосахаров). 3.Синтез аспарагина – взаимодействие аспартата с аммиаком. Является второстепенным способом уборки аммиака, энергетически невыгоден, т.к. при этом тратятся 2 макроэргические связи, 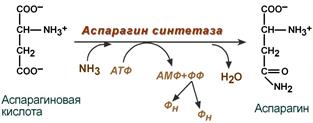 Реакция синтеза аспарагина |
