БжБ №3. 78 сынып оушыларына арналан жасспірімдер арасындаы жаратылыстану математикалы баыттаы облысты олимпиада Областная юниорская олимпиада естественноматематического цикла среди учащихся 78 классов Павлодар, 2013
 Скачать 2.31 Mb. Скачать 2.31 Mb.
|
|
Бұл қай құстың іздері екенін анықтаңыз (0,5-тен 2 ұпай)
  Химия пәнінен жасөспірімдер арасындағы ІІ облыстық олимпиаданың тапсырмалары Задания ІІ областной юниорской олимпиады по химии Жаттықтыру тапсырмалары/ Тренировочные задания I уровень 1.Из предложенного перечня выпишите пары веществ, которые являются друг другу химическими антонимами и пары веществ – химических синонимов: синтез, катод, гомологи, донор, акцептор, катион, испарение, катализатор, сублимация ионизация, ассоциация, анод, изомеры, анион, конденсация, ингибитор, возгонка, энзимы, , диссоциация, фермент, анализ, катод. 2. Ляпис, Бертоллетова соль, железный купорос, карборунд, питьевая сода, поташ, купоросное масло, цементит, каустическая сода. Напишите формулы этих веществ и укажите области их применения 3. Потеря слоя почвы толщиной в 1 мм означает, что 1 га почвы лишится 76 кг азота, 240 кг – фосфора и 80 кг – калия. Число атомов калия и азота, которые потеряет 1 га почвы, если при самых неблагоприятных условиях в Казахстане происходит разрушение 3 мм почвы в год 4. Литровая кружка теплого летнего воздуха вблизи от земли (не в горах) весит 1 1/5 г. Хватит ли 1 кубометра такого воздуха, чтобы из имеющегося азота получить 500 л аммиака? 5. При сгорании 1 моль метана выделяется 802 кДж. Сколько грамм метана нужно сжечь, чтобы вскипятить 1,5 л воды (для этого необходимо затратить 500 кДж)? II уровень 1.4 грамма газообразного бинарного соединения А разлагается при 1000°С на вещества В и С. Взаимодействие этих веществ с соединением черного цвета Д при нагревании ведет к образованию простого вещества Е красного цвета и двух сложных веществ Ж и З, которые являются продуктами сгорания А, а при разложении З одним из продуктов реакции является вещество С. Установите все зашифрованные вещества, запишите уравнения химических реакций и вычислите массу З. 2. Какой объем (н.у.) углекислого газа заполнит помещение кухни, если юный химик прокалил на электрической плите 500 г толченого мела, в котором 3% примесей? Хватит ли этого углекислого газа комнатным растениям для синтеза 15 г глюкозы? 3. Выведите формулы всех веществ состава ХНу, в которых массовая доля водорода составляет 0,125 4. Смесь водорода и дейтерия в 20 раз легче углекислого газа. Сколько молекул водорода приходится на одну молекулу дейтерия в такой смеси? 5. Сколько грамм медного купороса выпадет из 400 г насыщенного раствора (t = 60°С) при охлаждении до 20°С, если при 60°С растворимость сульфата меди 40 г на 100 г воды, а при 20°С – 20 г на 100 г воды. Хватит ли оставшейся соли в насыщенном (при 20°С) растворе для изменения массы железной пластинки на 1,6 г? III уровень 1. Осуществи цепочку превращений:  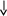 F F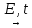 D D F Ft B  E E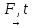 D D F FА – сложное вещество зеленого цвета. 2. Установите формулы бинарных соединений (не менее 2), молекулы которых содержат по 18 электронов и 14 нейтронов. Укажите методы получения этих веществ 3. Газообразный тритий (изотоп водорода 3H) подвергается радиоактивному распаду с образованием газообразного гелия согласно следующему уравнению: T2 → 23He + β (β — частица представляет собой электрон). Определите, во сколько раз изменится давление в сосуде по истечении двух периодов полураспада трития (периодом полураспада называется время, за которое распадается половина имеющегося радиоактивного вещества). 4. На гробнице китайского полководца Чжао Чжу, похороненного в 316 г., есть металлический орнамент. Когда химики сделали анализ сплава, то оказалось, что он имеет следующий состав: 5% магния, 10% меди и 85% алюминия. До сих пор наука не может объяснить, как удалось древним китайцам получить такой сплав. Определите, объём 10 % раствора серной кислоты (плотность 1,05 г/мл) , необходимый для реакции с 10 г этого сплава и массовые доли веществ в полученном растворе 5. При приливании к смеси карбоната кальция и карбоната натрия избытка соляной кислоты выделилось 16,8 л (н.у.) газа, который пропустили через 48г 62,5% раствора гидроксида натрия. 1) Определите количественный состав исходной смеси в % 2) Массовую долю соли в полученном растворе Нәтижеге дейінгі есептер Задачи довывода 1. Алтын – бағалы метал ғана емес, күшті катализатор, мысалы автомашиналардан шығатын қалдық газдардағы СО газын көмірқышқыл газына дейін каталитикалық тотықтыру процесінде белсенді катализатор. Алтын нанобөлшек түрінде болған кезде каталитикалық қасиет көрсетеді. 5.5 см3 металдан құрамы Au20 болатын қанша нанобөлшек алуға болады? Алтынның тығыздығы 19.32 г/см3 Золото – не только драгоценный металл, но и перспективный катализатор, например, в процессах каталитического окисления СО до углекислого газа в выхлопных газах автомобилей. Каталитические свойства проявляет золото, находящееся в виде наночастиц. Сколько наночастиц состава Au20 можно получить из 5.5 см3 металла? Плотность золота составляет 19.32 г/см3 2. Кальций оксидін суда еріту барысында (сөндірілген әкпен) оған оттекті үрлеген кезде түзілген затпен темір (ІІ) сульфатының әрекеттесуі нәтижесінде минералды бояулардың біреуі алынады. Түзілген тоқ сары түсті тұнбаны сүзеді, кептіреді және сусыздандырады (құрғатады). А) Алынған бояудың құрамын көрсетіңіздер. В) Оны алу үшін есептің барысында айтылған барлық реакция теңдеулерін жазыңыздар Одну из минеральных красок получают взаимодействием сульфата железа (II) с веществом, полученным при растворении оксида кальция в воде (гашеной известью) при продувании кислорода. Образовавшийся осадок оранжевого цвета отфильтровывают, сушат и прокаливают. А) Укажите состав полученной краски В) Напишите все уравнения реакции, описанные в задаче, для ее получения 3. 180 г 10% мыс (ІІ) сульфаты ерітіндісіне 20 г су және 25 г мыс купоросын (CuSO4·5H2O) қосты. Жаңа ерітіндінің концентрациясы қандай болды? К 180 г 10% раствора сульфата меди (II) добавили 20 г воды и 25 г медного купороса (CuSO4·5H2O). Какова концентрация нового раствора? 4. Анықтаңыздар: А) 16,25 г жезбен (40% Zn және 60% Cu) әрекеттесу үшін қажетті 10 %-тік күкірт қышқылының (тығыздығы 1,1 г/мл) көлемін; Б) Осы кезде алынған тұнбаның және газдың зат мөлшерін. Определите, А) Объём 10 % раствора серной кислоты (плотность 1,1 г/мл), необходимый для реакции с 16,25 г латуни (40% Zn и 60% Cu), Б) Количества вещества полученных при этом осадка и газа. 5. 100г магний мен литийдің қоспасын оттекпен әрекеттестірген кезде оксидтер түзіледі және соңғы қоспаның массасы 2 есе артады. Қоспадағы металдардың массалық үлестері қандай? При взаимодействии 100г смеси магния и лития с кислородом образуются оксиды, и масса конечной смеси увеличивается в 2 раза. Каковы массовые доли металлов в смеси? Нәтижеден кейінгі есептер Задачи вывода 1 тапсырма: Ағаштарды және бұталарды залалсыздандыру үшін қолданылатын А затының сулы ерітіндісін әмбебап индикатор қағазының түсін көк түске өзгертетін В затының түссіз ерітіндісіне құйды. В затының құрамында қайнатылған (поваренной) тұздың құрамына кіретін метал бар. А және В заттарының әрекеттесуі нәтижесінде түсті (боялған) С тұнбасы және Глаубер тұзының құрам бөлігі болып саналатын D заты түзілді. С затын қыздырған кезде Е және Ғ екі оксиді түзілді. Е оксиді G «купоросты метал» ерітіндісімен әрекеттескенде А және Ғ заттары түзіледі. А) Барлық жасырылған заттардың A, D,C,D,E,F,G формулаларын анықтаңыздар; В) Жүрілген реакция теңдеулерін жазыңыздар. Задание 1: Водный раствор вещества А, применяемый для обеззараживания деревьев и кустарников, прилили к бесцветному раствору вещества В, изменяющего окраску универсальной индикаторной бумаги на синий цвет. В состав вещества В входит тот же ион металла, что и в состав повареной соли. В результате взаимодействия веществ А и В выпал окрашенный осадок С и образовалось вещество D, которое является составной частью Глауберовой соли. При нагревании вещества С образовалось 2 оксида E и F. Взаимодействие оксида Е с раствором «купоросного масла» G дает вещества А и F. А) Установите формулы всех зашифрованных веществ A, D,C,D,E,F,G В) Напишите уравнения протекающих реакций. 2 тапсырма: Нөмірленген алты құтыда (стаканда) қатты зат бар (ұнтақ түрінде): натрий гидрокарбонаты, натрий хлориді, магний нитраты, темір (ІІ) сульфаты, кальций карбонаты, сусыз гипс (СаSO4). 1) Үстелдің үстіндегі реактивтерді және құрал-жабдықтарды пайдалана отырып әрбір құтыдағы (стакандағы) затты анықтаңыздар. Әрбір заттың химиялық формуласын жазыңыздар. 2) Барлық заттардың (жеке-жеке) тұз қышқылымен және сілтімен химиялық реакция теңдеулерін жазыңыздар. Егер сіздердің көзқарастарыңыз бойынша қандай да бір реакция жүрмейтін болса, онда оны келесі түрде жазыңыздар (Na2SO4 + NaOH ≠). Реагенттер: 2M HCl, 2M NaOH, H2O дистилденген Құрал-жабдықтар: сынауықтар (пробиркалар) орнатылған штатив (7-10 дана), қысқыш (шпатель), араластыруға арналған таяқшалар. Задание 2: В шести пронумерованных стаканах находятся твердые вещества (в виде порошков): гидрокарбонат натрия, хлорид натрия, нитрат магния, сульфат железа(II), карбонат кальция, безводный гипс (СаSO4). Используя имеющиеся на столе реактивы и оборудование, определите содержимое каждого стакана. Приведите химическую формулу каждого вещества. Напишите уравнения химических реакций всех веществ (по отдельности) с соляной кислотой и щёлочью. Если какие-либо реакции, на Ваш взгляд, не идут, это следует написать (Na2SO4 + NaOH ≠). Реагенты: 2M HCl, 2M NaOH, H2O дистиллированная Оборудование: штатив с пробирками (7-10 штук), шпатель, палочка для размешивания |


