Алкадиены
 Скачать 490.5 Kb. Скачать 490.5 Kb.
|
|
ЛЕКЦИЯ 6 АЛКАДИЕНЫ. Схема лекции. 1. Строение молекул, изомерия, номенклатура. 2. Способы получения. 3. Физические свойства. 4. Химические свойства. 4.1. Гидрирование. 4.2. Гидрогалогенирование. 4.3. Галогенирование 4.4. Радикальные реакции. 4.5. Реакция диенового синтеза. 4.6. Полимеризация. 1. Строение молекул, изомерия, номенклатура. Определение: Алкадиенами или просто диенами называются ненасыщенные углеводороды, содержащие две двойные связи. Алкадиены образуют гомологический ряд общей формулы СnН2n-2. Таким образом, алкадиены являются структурными изомерами алкинов. По систематической номенклатуре названия диеновых углеводородов образуют от названия соответствующего алкана с заменой суффскса «ан» на «диен». Например: 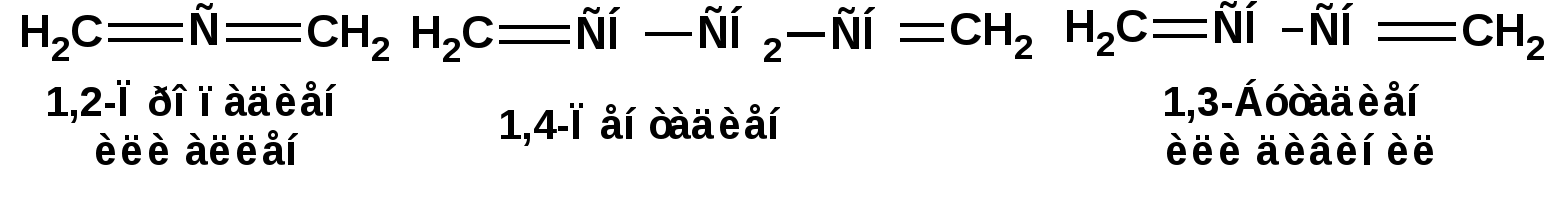 Главная цепь выбирается таким образом, чтобы двойные связи были в главной цепи, а локанты расставляются таким образом, чтобы атомы углерода, от которых начинаются двойные связи, имели бы наименьшие значения. Для основных диеновых углеводородов широко распространены тривиальные названия. Например аллен, дивинил, а также: 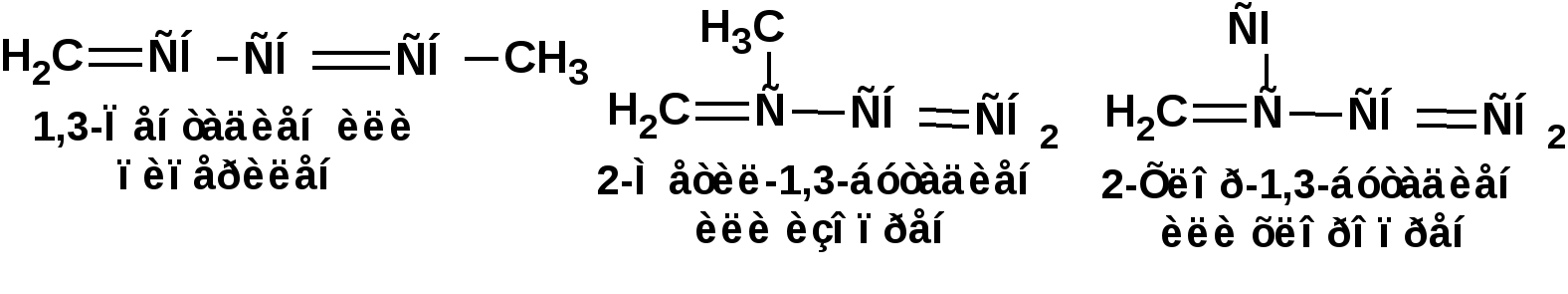 Названия по рациональной номенклатуре также употребляются. Например: 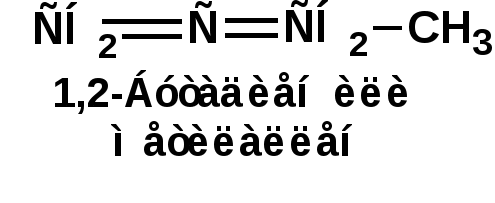 Диеновые углеводороды обладают двумя функциональными группами. Поэтому: 1. Должна быть изомерия положения функциональной группы. 2. Должна быть структурная изомерия, связанная со строением углеродного скелета. Структурная изомерия начинается с С5–углеводородов. Примером структурных изомеров являются пиперилен и изопрен. В одном случае углеводород с цепь нормального строения, в другом - изомерное строение цепи. Изомерия положения двойных связей различает три типа диеновых систем: 1. Углеводороды с изолированными двойными связями или просто «изолированные». Определение: Изолированными называют углеводороды, у которых двойные связи разделены хотя бы одним атомом углерода в состоянии sp3-гибридизации. Например 1,4-пентадиен. 2. Углеводороды с кумулированными двойными связями или просто «кумулированные» («кумулированные» - примыкающие к одному атому углерода). Примером кумулированного диена является аллен. Определение: кумулированными называют углеводороды, у которых в образовании двойных связей участвует атомом углерода в состоянии sp-гибридизации. В кумулированных системах π-связи располагаются в двух взаимно перпендикулярных плоскостях. (Как ацетилен с «растянутой » тройной связью). 3. Наибольший интерес представляют диеновые углеводороды с сопряженными двойными связями. Определение: Сопряженными называют углеводороды, у которых две двойные связи разделены одной простой связью и все четыре атома углерода находятся в состоянии sp2-гибридизации. Это 1,3-бутадиен, 1,3-пентадиен, 2-метил-1,3-бутадиен и 2-хлор-1,3-бутадиен – в общем 1,3-алкадиены. 2. Способы получения. 2.1. Способы получения диенов с изолированными двойными связями, такие как для обычных алкенов. 2.2. Получение диенов с кумулированными двойными связями. Например, получение аллена. Заключается в отщеплении брома от 2,3-дибромпропена действием металлического цинка:  2.3. Способы получения 1,3-алкадиенов 1,3-Алкадиены являются мономерами при производстве каучуков. Поэтому способы их получения являются, главным образом, промышленными. 2.3.1. Получение 1,3-бутадиена по Реппе и 2-метил-1,3-бутадиена по Фаворскому. Из существующих способов получения 1,3-алкадиенов один – с использованием ацетилена в качестве исходного - уже разобрали. Также из ацетилена получают хлоропрен. Димеризацией ацетилена получают винилацетилен. Далее к винилацетилену присоединяют хлористый водород: 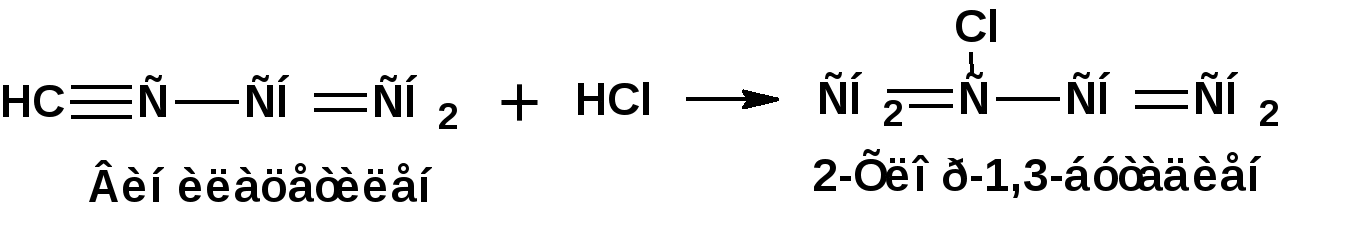 2.3.2. Получение 1,3-бутадиена по Лебедеву. Эта реакция промышленного значения уже практически не имеет, но имеет большое историческое значение, поскольку в канун второй мировой войны способ Лебедева противостоял способу Реппе. По С.В. Лебедеву 1,3-бутадиен получают из этилового спирта, который получают из крахмала. Крахмал получают из картофеля, а картофель хорошо растет в Татарстане. 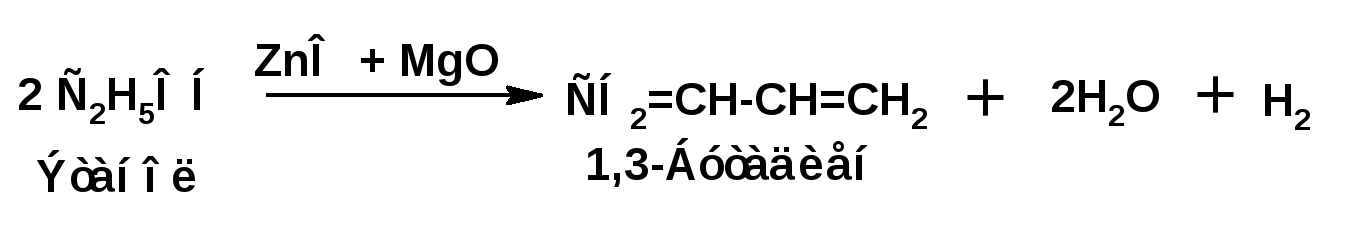 2.3.3. Дегидрогенизация (дегидрирование). Самым выгодным экономически способами производства 1,3-бутадиена и 2-метил-1,3-бутадиена является пиролиз бутана и 2-метилбутана. Реакция идет в две стадии. На первой стадии образуется смесь 1- и 2-алкена, от которых на второй стадии отщепляется еще одна молекула водорода: 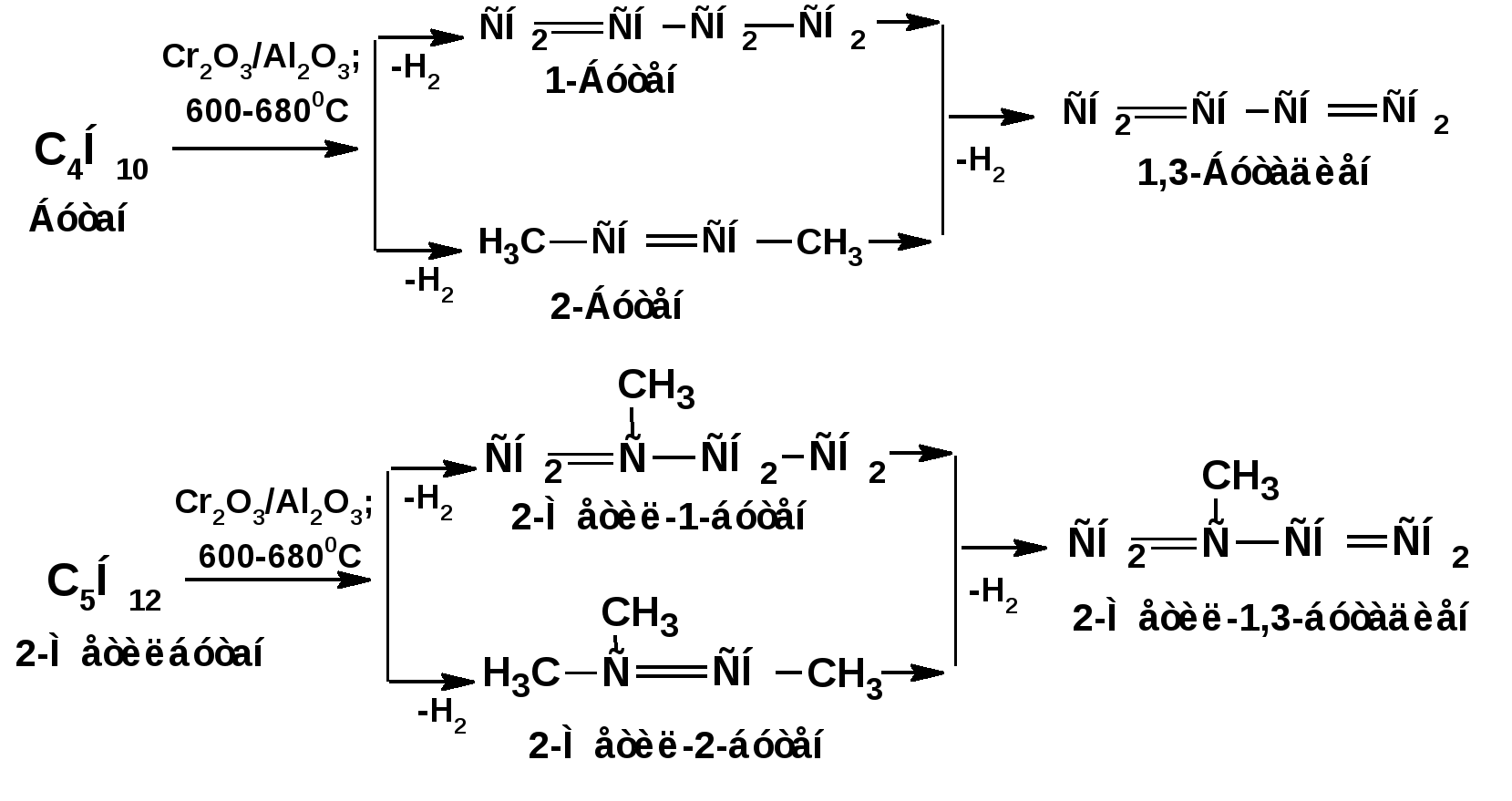 В качестве сырья могут быть использованы фракции, образующиеся при крекинге нефти, которые уже содержат смесь исходных алканов и алкенов. 2.3.4. Дегидратация алкандиолов Дегидратация соответствует одной из стадий в получении 1,3-бутадиена по Реппе. Эта реакция проводится в присутствии минеральных кислот, например: 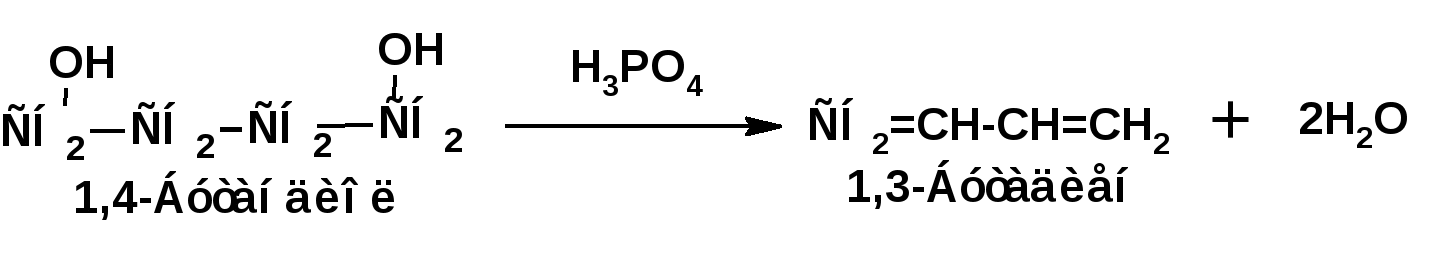 или в газовой фазе на гетерогенных катализаторах на основе оксида алюминия: 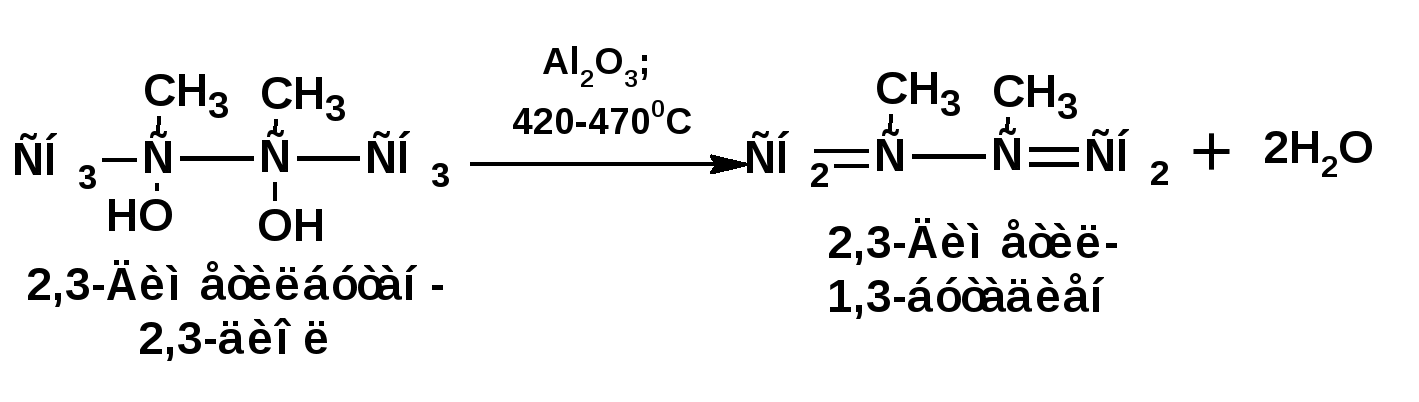 2.3.5. Получение 2-метил-1,3-бутадиена по реакции Принса. Используемый для производства основного массового каучука СКИ-3 изопрен получают в России (в СССР), в частности в Татарстане в г. Нижнекамск на АО «Нижнекамскнефтехим» - по реакции Принса из изобутилена и формальдегида: 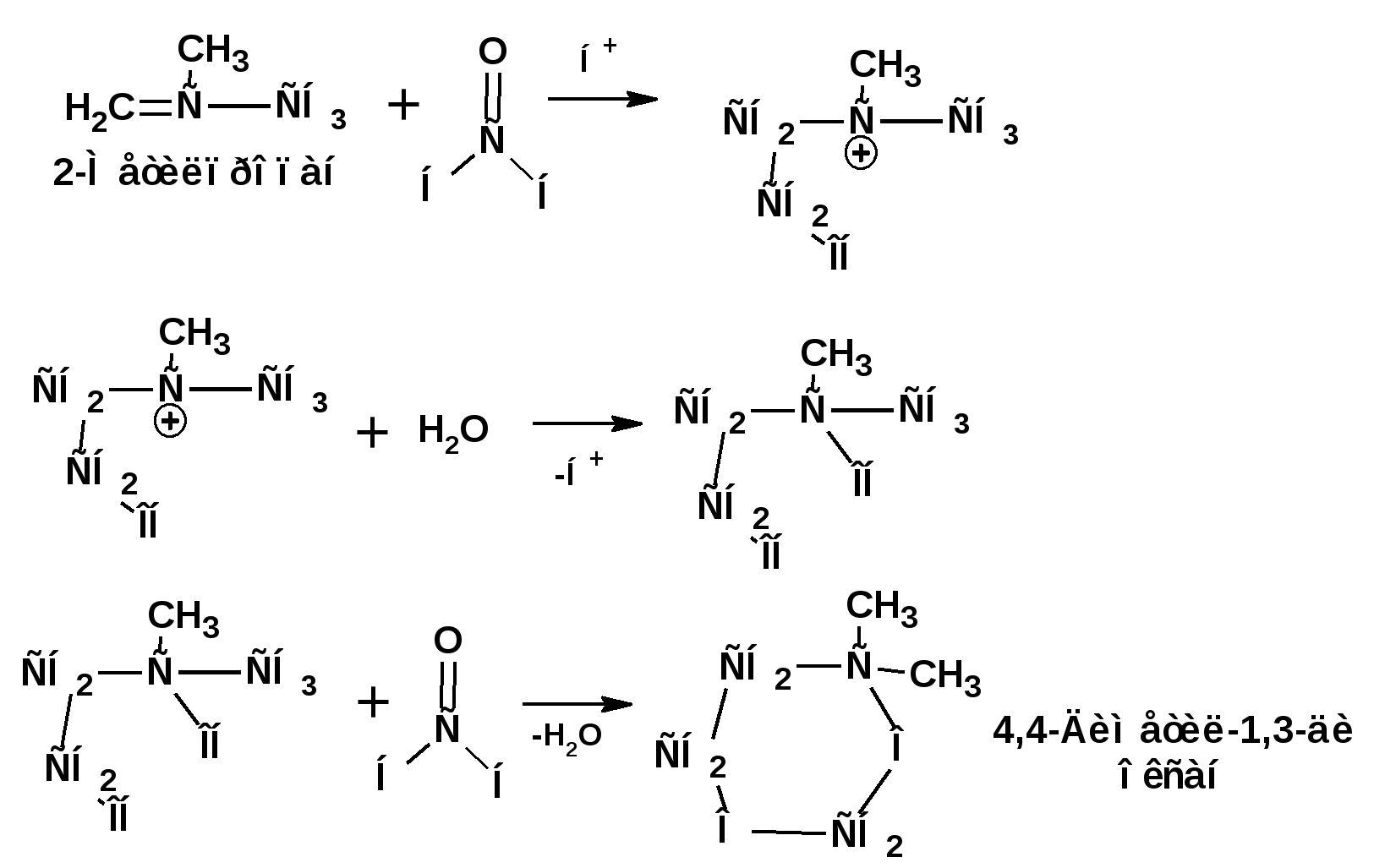 На первой стадии из изобутилена двух молекул формальдегида и воды получают 4,4-диметил-1,3-диоксан. На второй стадии диоксан разлагают на гетерогенном катализаторе на основе фосфата кальция. При этом образуется 2-метил-1,3-бутадиен формальдегид и вода. 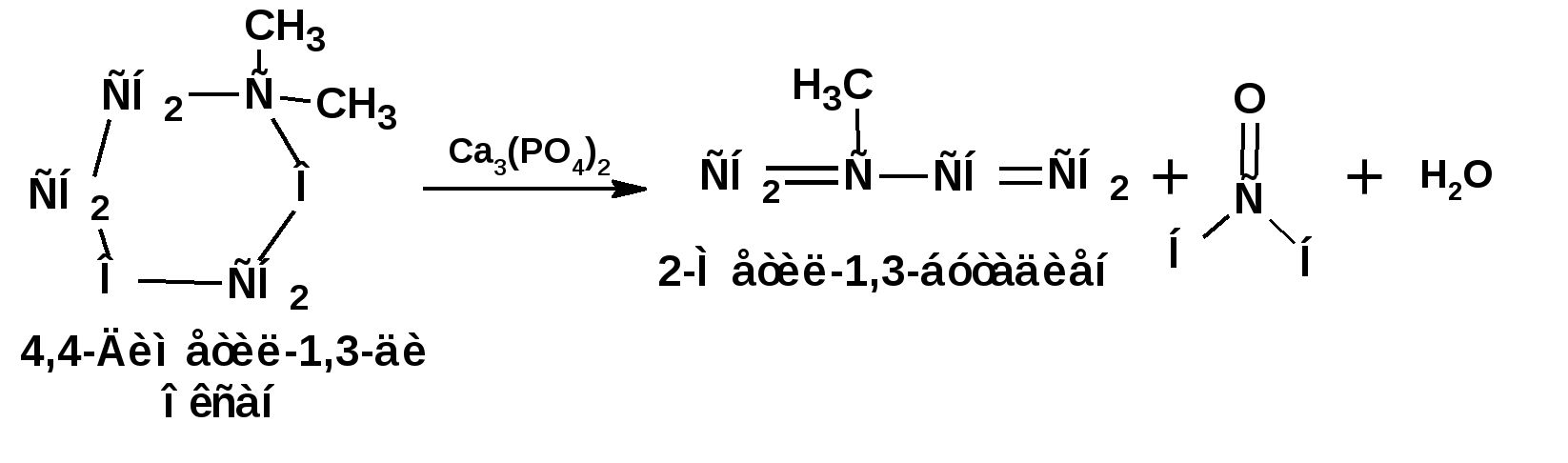 3. Физические свойства. 1,3-Бутадиен при обычных условиях является газом. Изопрен и другие простейшие алкадиены являются жидкостями. Для алкадиенов с сопряженными двойными связями наблюдаются аномально высокие значения показателя преломления света. С использованием показателя преломления составляет основу величины называемой молекулярной рефракцией. Молекулярная рефракция вычисляется по формуле Лорентц-Лоренца с использованием экспериментальных данных по показателю преломления и плотности: 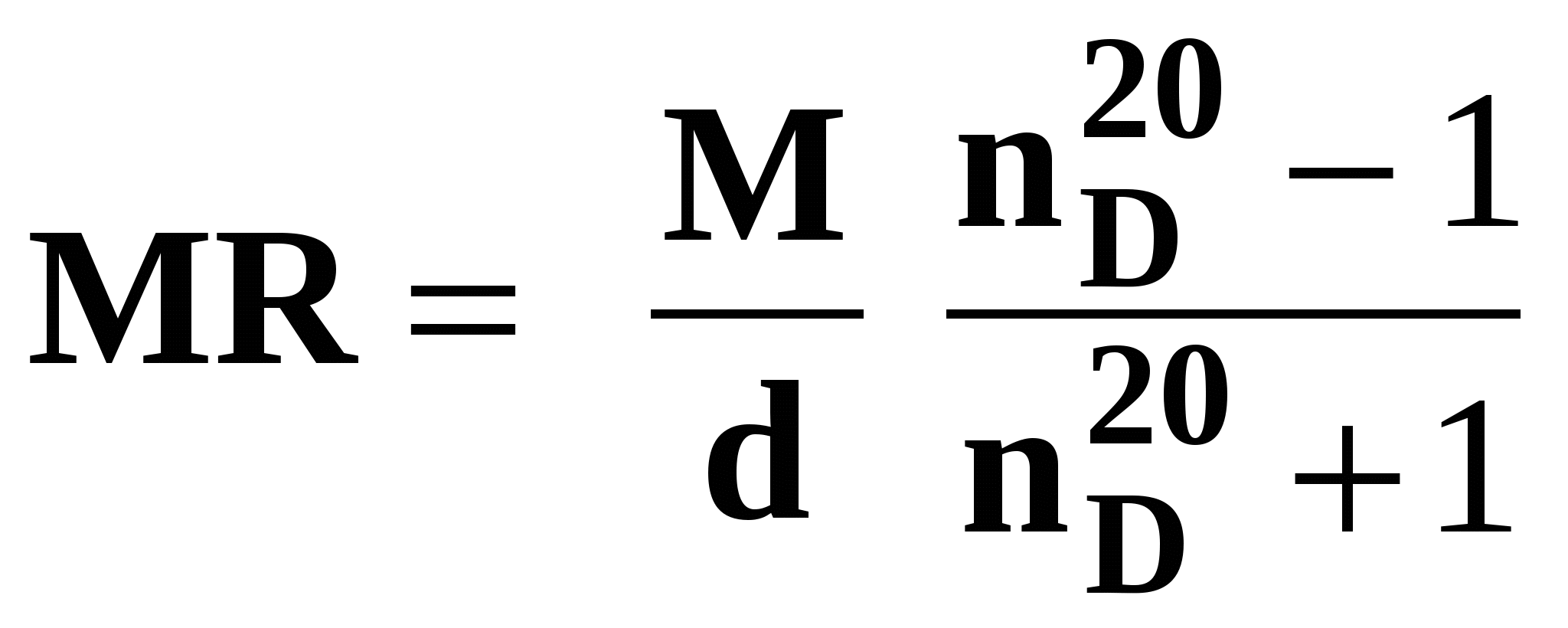 где: МR – молекулярная рефракция; М – молярная масса; D – плотность; n D 20 – показатель преломления. Но молекулярную рефракцию можно рассчитать по системе специальных инкрементов. Например, по системам инкрементов можно достаточно точно рассчитать молекулярную рефракцию алканов, алкенов и алкинов. Но расчеты по системам инкрементов молекулярной рефракции алкадиенов приводили к систематическому занижению результатов, по сравнению с экспериментальными данными. Разница между расчетными значениями и значениями, полученными на основании экспериментальных данных - составляет обычно 1 – 1.5 единицы. Эта разница называется молекулярной экзальтацией. Наличие системы сопряженных двойных связей в молекулах 1,3-алкадиенов обеспечивает возможность поглощения квантов электромагнитного излучения длинноволновой ультрафиолетовой части спектра. Введение заместителей позволяет поглощать кванты видимой части спектра. Поэтому наличие окрашивания органического соединения указывает на наличие системы сопряженных двойных связей. 4. Химические свойства. Две сопряженные π-связи образуют общее облако π-электронов. Наличие этого облака делает возможным присоединение не только к соседним атомам углерода, так называемое 1,2-присоединение: 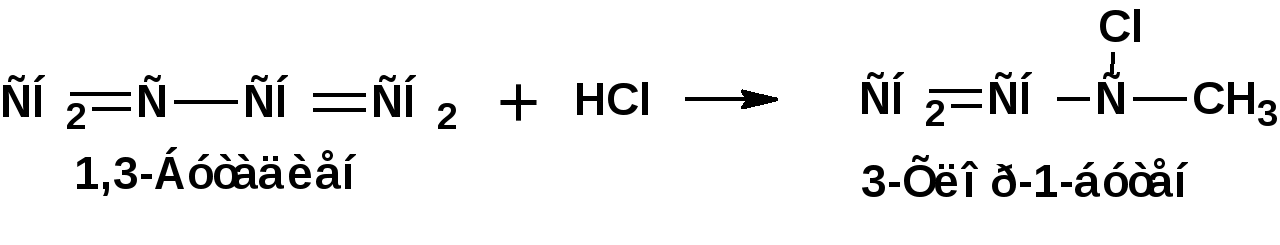 но и к крайним атомам сопряженной системы, так называемое 1,4-присоединение: 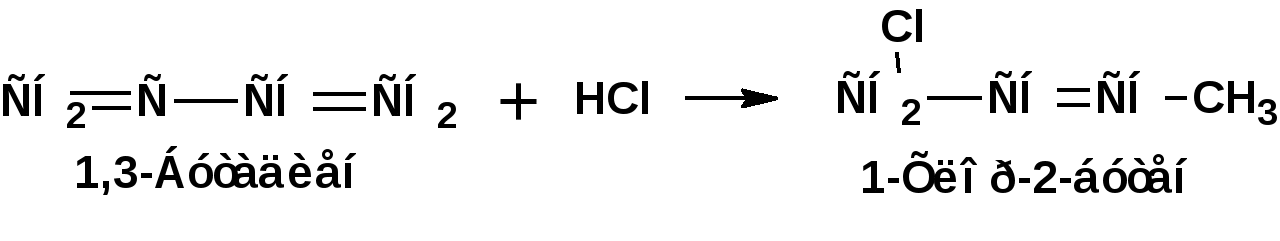 4.1. Гидрирование В условиях гетерогенного катализа, аналогичных гидрированию алкенов, водород присоединяется в 1,2- и 1,4-положения с образованием смеси продуктов: 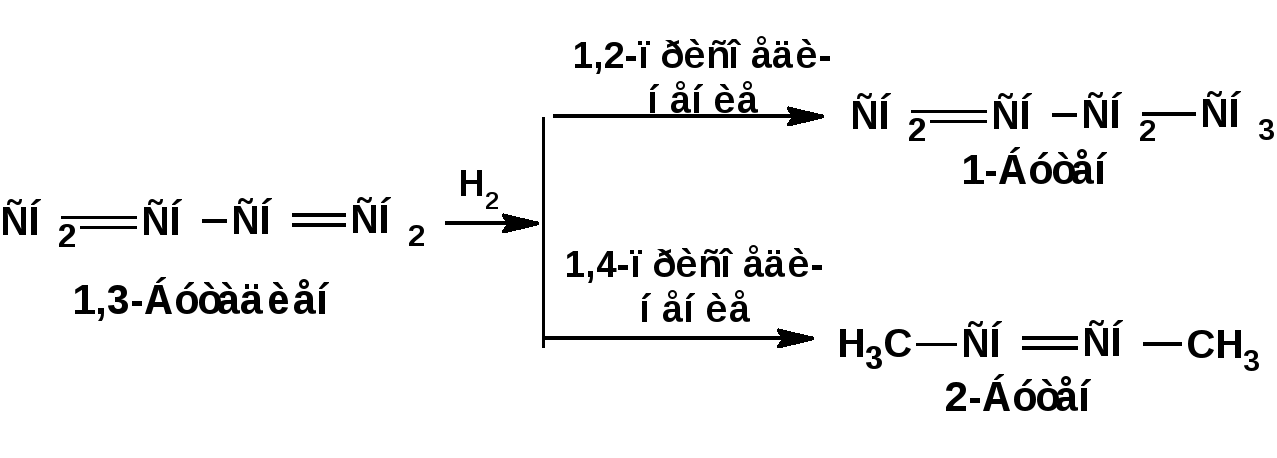 4.2. Гидрогалогенирование При присоединении галогенводородов к сопряженным диенам образуются два структурных изомера: 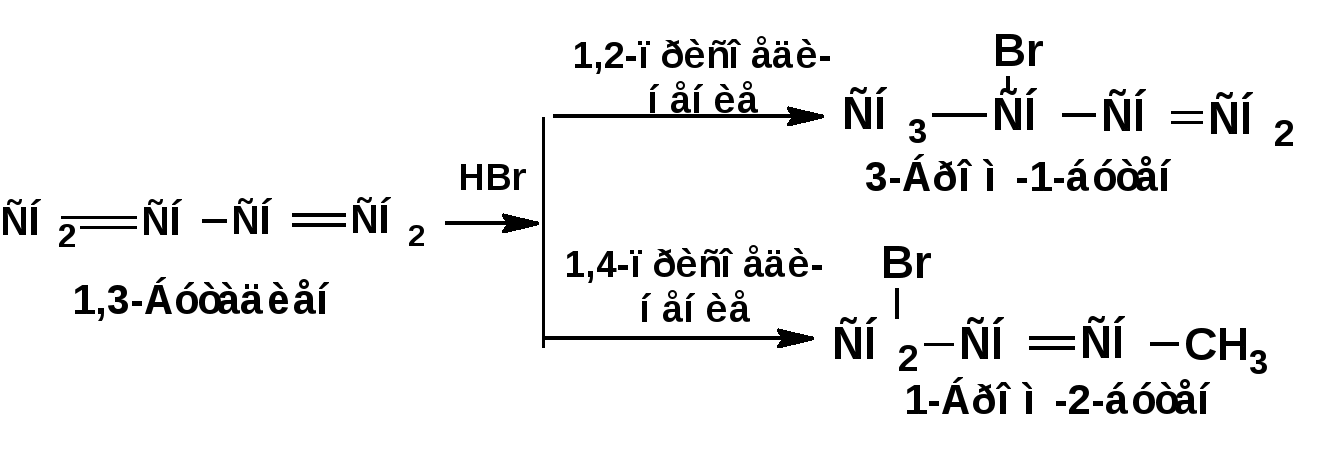 Механизм присоединения галогенводорода включает следующие стадии: 1. На первой стадии образуется π-комплекс: 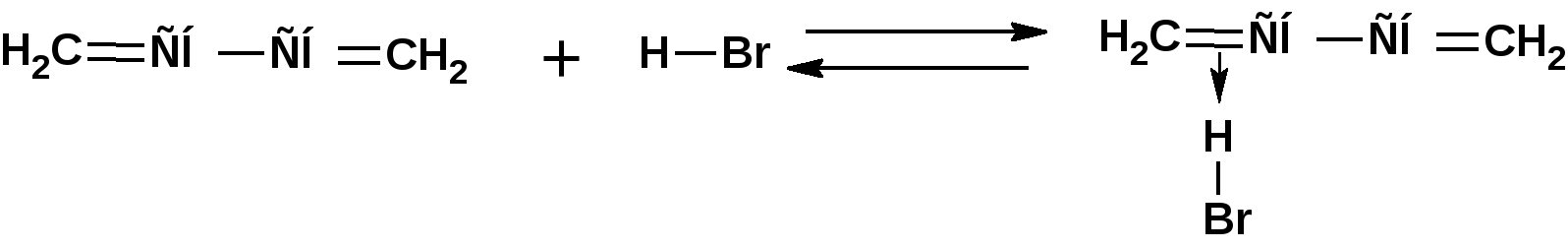 2. На второй стадии образование промежуточного карбкатиона. Эта стадия является медленной (скоростьлимитирующей). Особенностью карбкатиона является возможность представления его в форме резонансных структур: 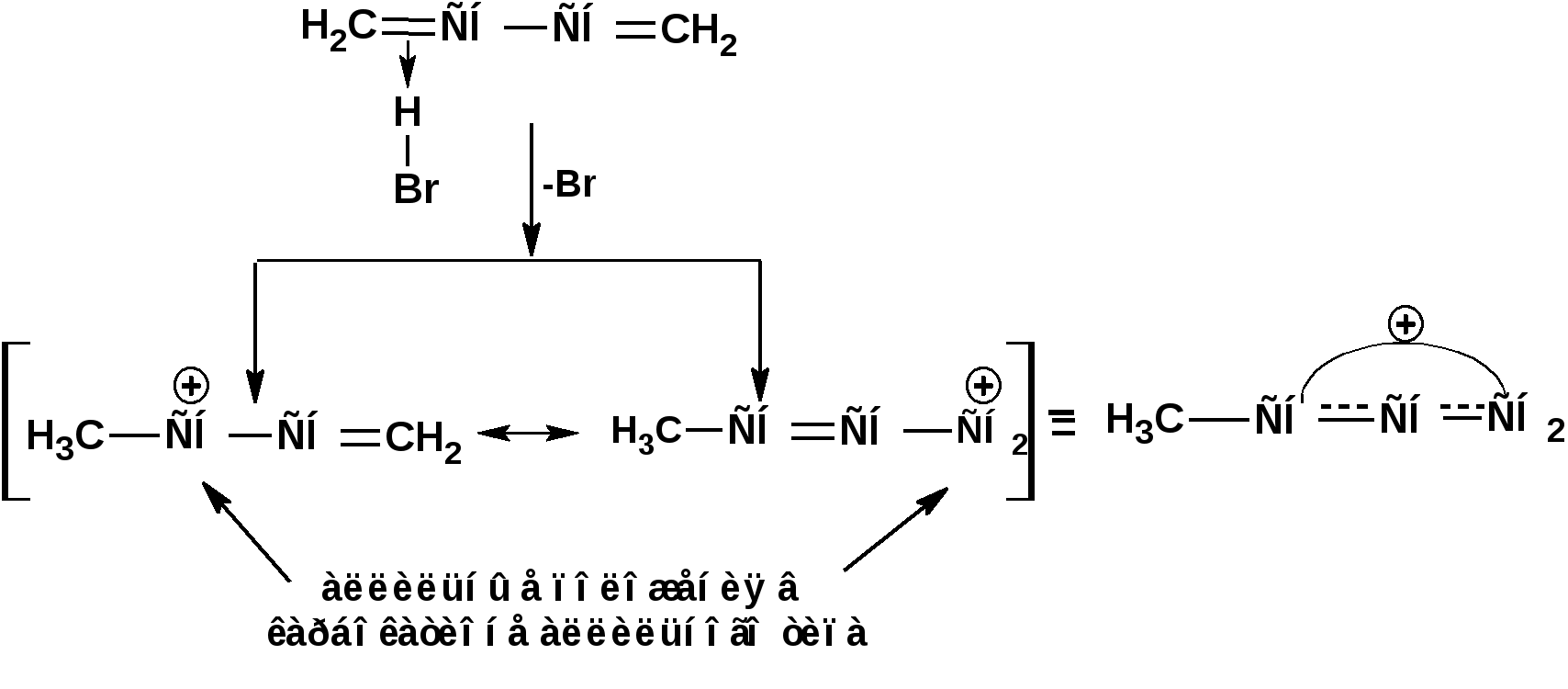 Образуются два сопряженных карбкатиона. 3. На третьей стадии бромид-ион, образовавшийся на второй стадии, быстро присоединяется к сопряженным карбкатионам с образованием двух возможных изомеров: 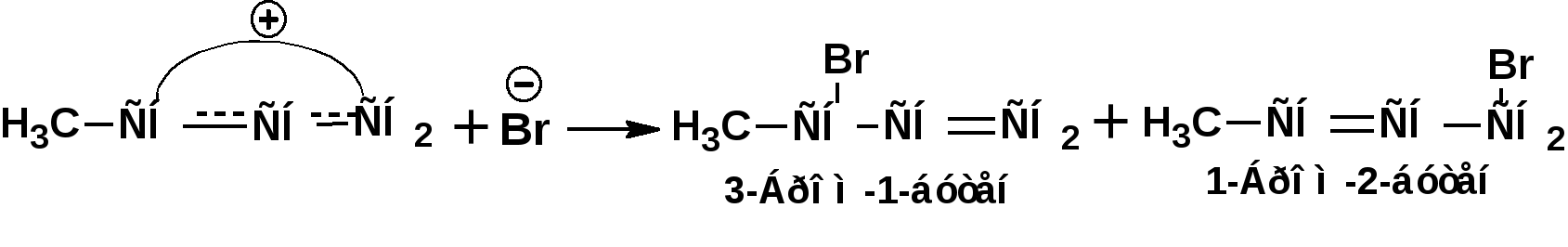 Карбкатионы, образующиеся в реакциях электрофильного присоединения к сопряженным диенам, принято называть карбкатионами аллильного типа. Такие карбкатионы характеризуются повышенной устойчивостью. Они более устойчивы, чем третичные карбкатионы. По этой причине сопряженные диены в реакциях электрофильного присоединения более реакционноспособны, чем алкены и алкины. 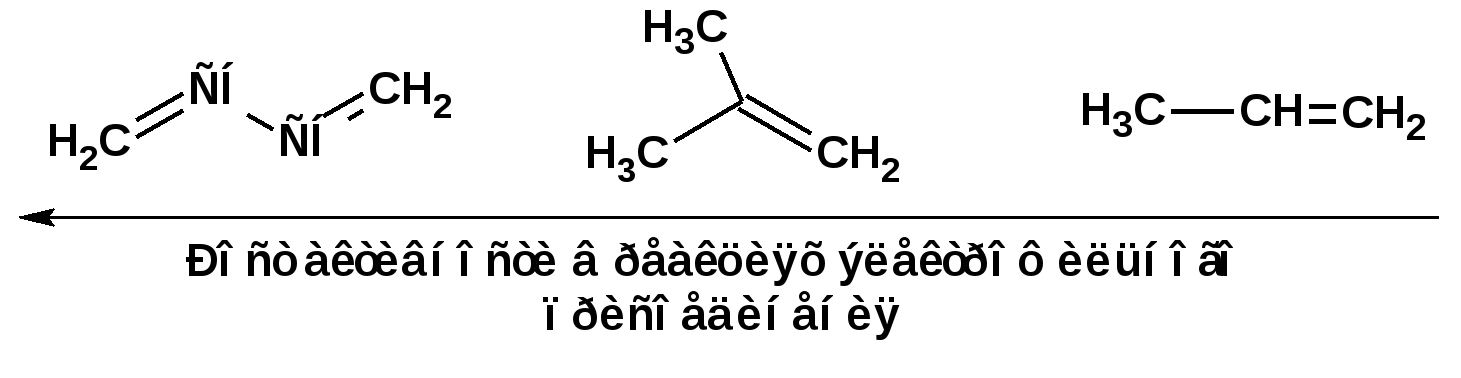 Поскольку в карбкатионе аллильного типа имеется два реакционных центра присоединение бромид-иона может протекать в двух направлениях. Соотвественно образуется смесь продуктов 1,2-присоединения (прямое присоединение и 1,4-присоединение (сопряженное присоединение). Однако из двух сопряженных карбкатионов один (с зарядом во втором положении) более стабильный поскольку алльный катион дополнительно стабилизирован метильным радикалом. Соответственно протекание реакции через стадию этого катиона будет более предпочтительным. Белее стабильный из двух карбкатионов приводит к образованию продукта 1,2-присоединения. Следствием большей стабильности карбкатиона является меньшая высота потенциального барьера на пути от реагентов к продуктам. Определение: Один из двух возможных продуктов, образование, которого связано с меньшей высотой потенциального барьера – называется кинетически контролируемым. О таком ходе реакции говорят как о кинетически контролируемой реакции. Повышенная стабильность карбкатиона приводит к тому, что катион образуется при обратной реакции. За счет резонанса более устойчивый катион может изомеризоваться в менее устойчивый, который также образует продукт. Но в силу меньшей стабильности катиона обратная реакция протекает очень медленно и постепенно идет накопление второго продукта. Такой продукт называется термодинамически контролируемым, а реакцию называют термодинамически контролируемой реакции. Различие кинетически и термодинамически контролируемых реакций в том, что кинетически контролируемый продукт образуется быстро и при низких температурах. Термодинамически контролируемый продукт накапливается медленно, а реакции идут при повышенных температурах. Так присоединение бромистого водорода к 1,3-бутадиену при –800С приводит к смеси продуктов, в которой 81% 3-бром-1-бутена и 19% 1-бром-2-бутена. При 200С образуется смесь, в которой 3-бром-1-бутена 44%, 1-бром-2-бутена 56%. 4.3. Галогенирование При галогенировании 1,3-диенов также образуется смесь продуктов кинетического и термодинамического контроля. При присоединении брома к 1,3-бутадиену при -800С основным продуктом является 3,4-дибром-1-бутен с примесью 1,4-дибром-2-бутена. При проведении реакции при 400С основным продуктом является 1,4-дибром-2-бутен, а в качестве примеси присутствует 3,4-дибром-1-бутен. 4.4. Радикальное присоединение Как и другие алкены, сопряженные диены способны присоединять свободные радикалы. Например, бром в условиях радикального процесса присоединяется к 1,3-бутадиену преимущественно по типу 1,4-присоединения независимо от температуры. 4.5. Реакция диенового синтеза. При взаимодействии 1,3-диеновой системы с акеном, у которого двойная связь имеет заместитель с отрицательным индуктивным и мезомерным эффектами, то во всех случаях образуется шестичленная циклическая система (производное циклогексена): 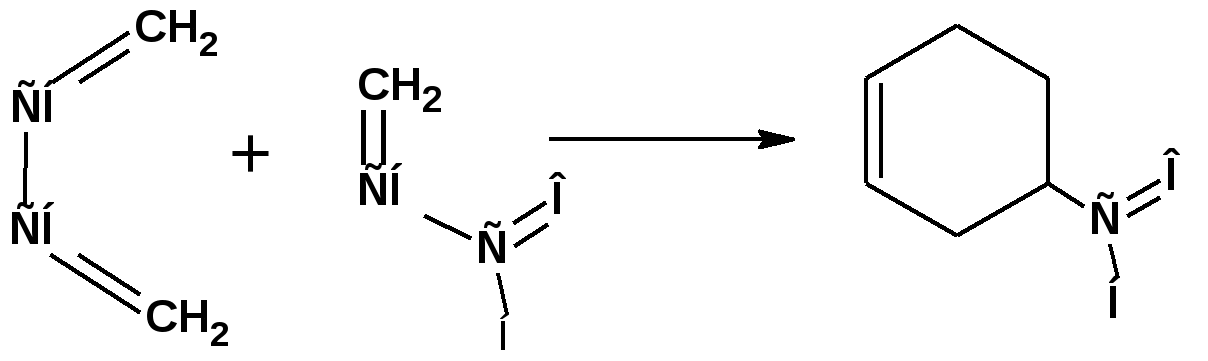 Реакция диенового синтеза является примером синхронной реакции, в которой происходит одновременный разрыв старых связей и образование новых. 4.6. Полимеризация Диеновые углеводороды с сопряженными двойными связями подобно алкенам легко вступают в реакции полимеризации. Причем именно цепной полимеризации. Реакции могут протекать по ионному и по радикальному механизму. Наличие двух двойных связей приводит к появлению новых возможностей в ходе процесса: 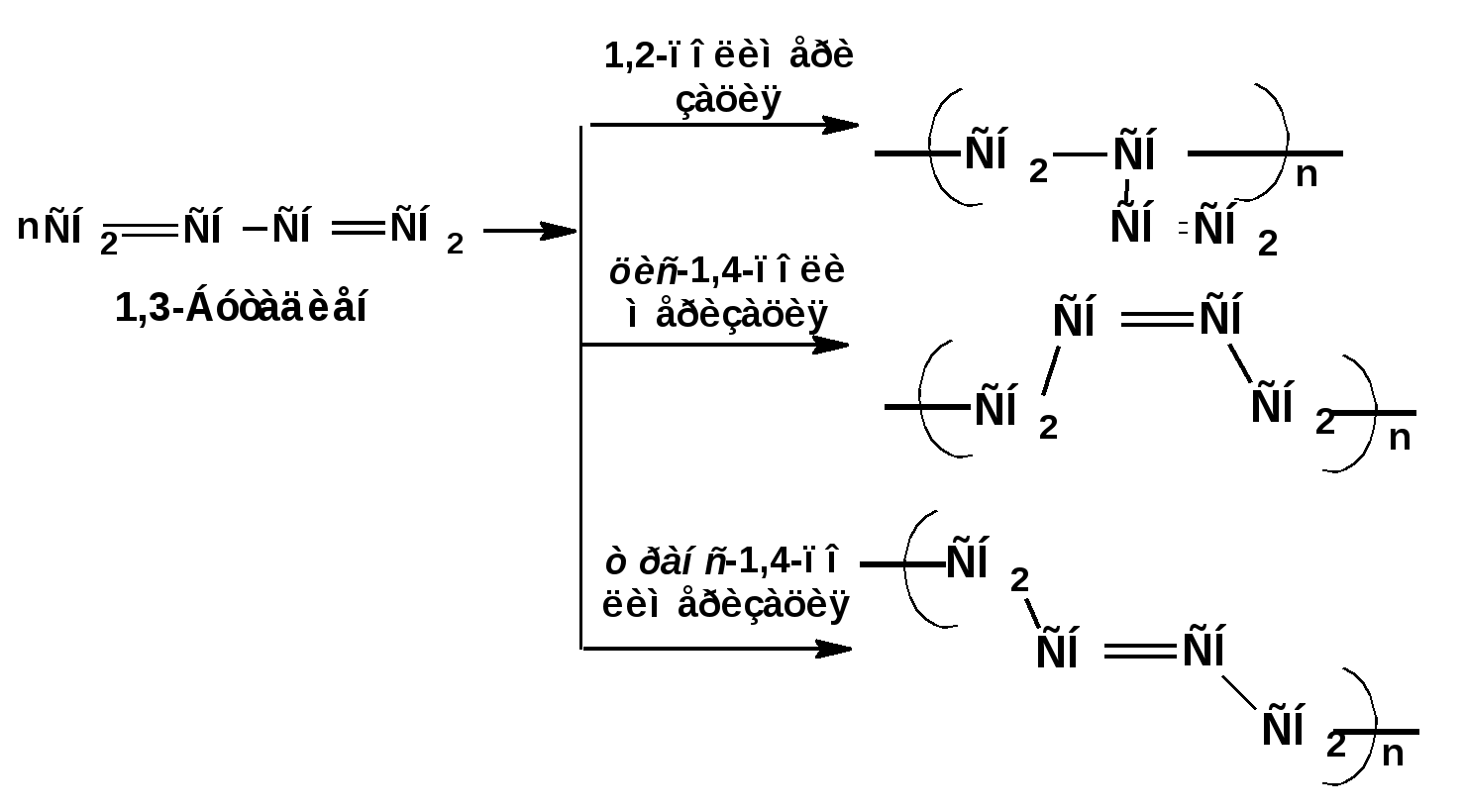 Полимеризацией 1,3-диенов получают каучуки или эластомеры. Нагреванием каучуков с серой или другими реагентами, например, оксидом магния – получают вулканизаты, в частном случае резины. За счет присоединения вулканизирующего агента по двойным связям соседних макромолекул происходит пространственная сшивка полимерных цепей и образование материалов с высокими физико-механическими свойствами. В природе получается цис-1,4-полиизопрен. Это так называемый натуральный каучук. Содержится в млечном соке дерева гевеи. Млечный сок представляет собой эмульсию полиизопрена в воде так называемый латекс. Каучук получают разлагая латекс соляной кислотой. Также в природе существует транс-1,4-полиизопрен. Этот полимерный материал имеет короткие полимерные цепи и известен под названием гуттаперчи. Эластичными свойствами транс-1,4-полиизопрен не обладает. 1,3-Бутадиен, полученный С.В. Лебедевым из спирта, был использован для получения каучука катионной полимеризацией: 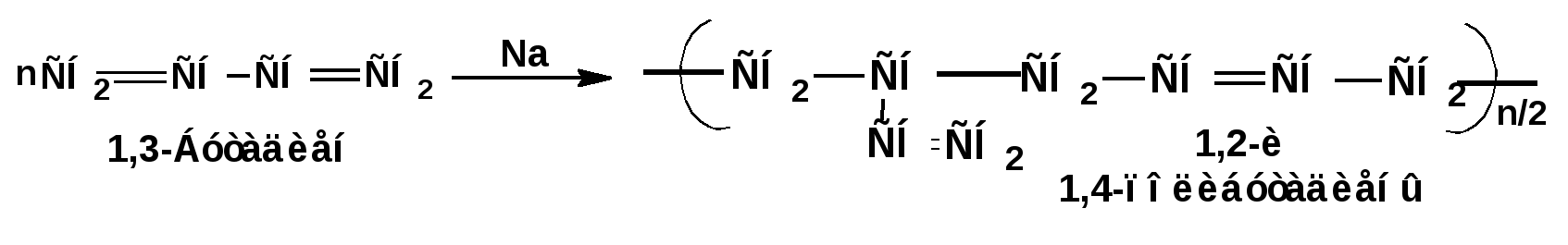 Бутадиеновый каучук уступает натуральному, по своим физико-химическим свойствам. Каучук по своим свойствам похожий на натуральный удалось получить из изопрена на катализаторах Циглера-Натта, где используется триизобутилалюминий (ТИБА): 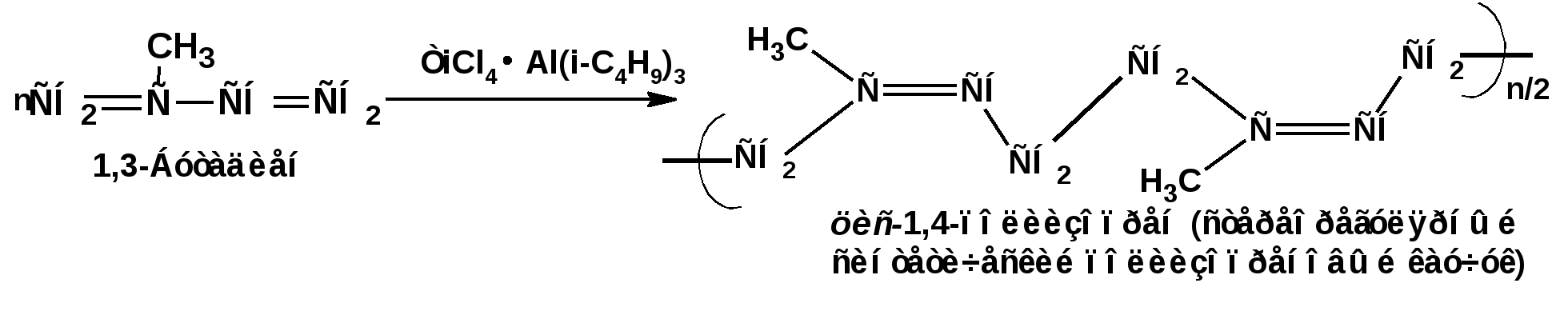 Большое практическое значение (маслобензостойкие резины) имеет неопрен – продукт свободнорадикальной полимеризации 2-хлор-1,3-бутадиена (хлоропрена): 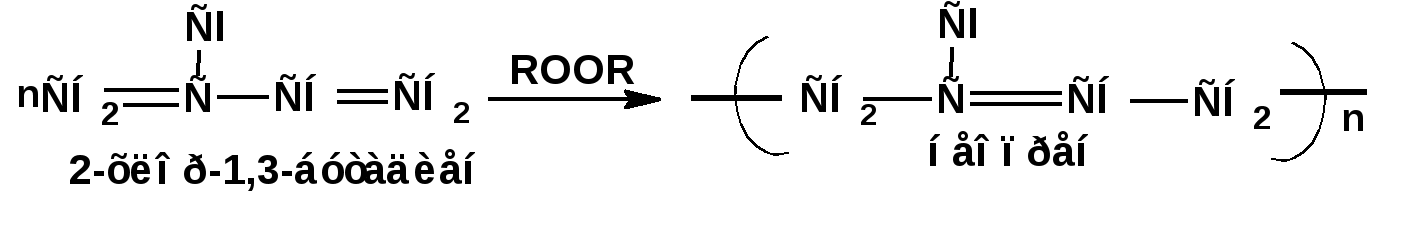 Также широкое применение имеет бутадиен-стирольный сополимер, получаемый радикальной полимеризацией: 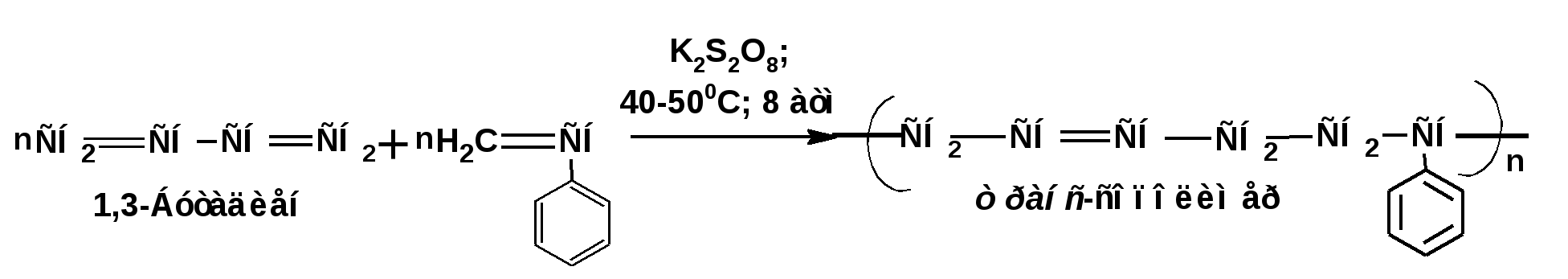 Из него делают искусственную кожу, а также используется в изготовлении шин. АЛИЦИКЛИЧЕСКИЕ УГЛЕВОДОРОДЫ или ЦИКЛОАЛКАНЫ Схема лекции. 1. Строение молекул, изомерия, номенклатура. 2. Способы получения. 3. Физические свойства. 4. Химические свойства. 1. Строение молекул, изомерия, номенклатура. Углеводороды с циклическим скелетом, содержащие атомы углерода в цикле только в состоянии sp3-гибридизации, называются циклоалканами. Общая формула (СН2)n. По номенклатуре ИЮПАК названия циклических соединений строятся подобно наименованиям соединений жирного ряда с добавлением приставки «цикло-»: 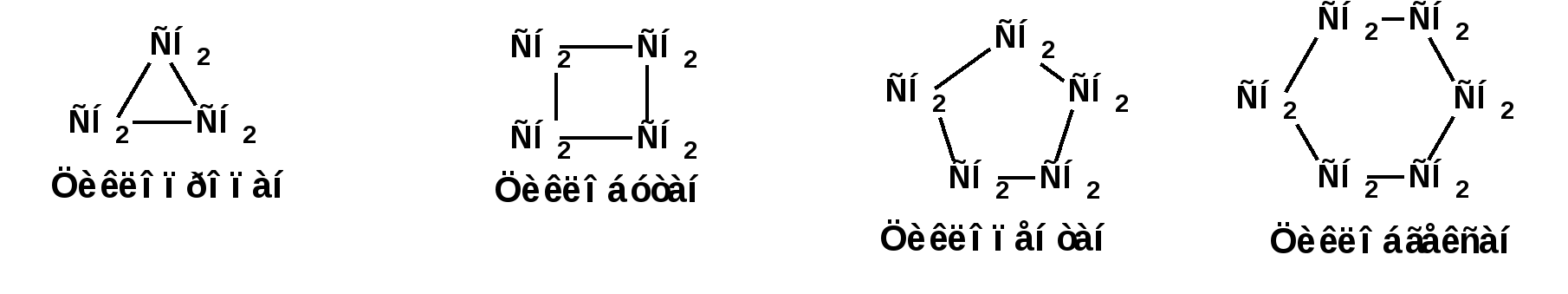 Два заместителя находящиеся в молекуле циклоалкана у различных атомов могут быть расположены по одну сторону плоскости цикла: Два заместителя находящиеся в молекуле циклоалкана у различных атомов могут быть расположены по одну сторону плоскости цикла: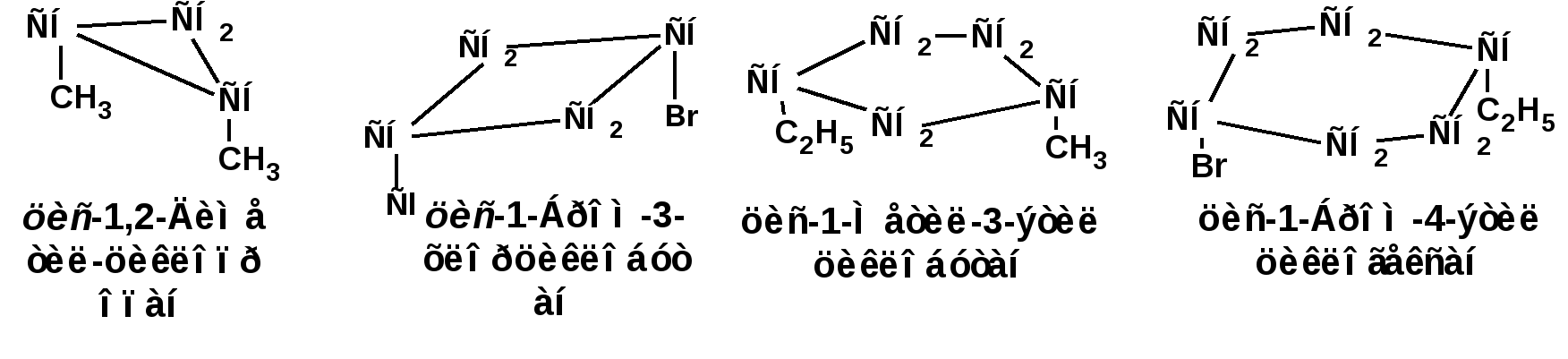 Два заместителя по разные стороны плоскости цикла образуют транс-изомер. Два заместителя по разные стороны плоскости цикла образуют транс-изомер.Кроме цис-, транс-изомерии циклоалеканам присуще: 1. изомерия по числу углеродных атомов в кольце. 2. изомерия по числу углеродных атомов в заместителях. 3. по расположению заместителей в кольце. Особенностью циклоалканов является так называемое «напряжение». Напряжение обусловлено: 1. искажением валентных углов по Байеру; 2. Торсионное напряжение, связанное с отклонением от наиболее выгодной заторможенной конформации по Питцеру; 3. Отталкивание сближенных атомов по Прелогу; 4. Изменение длин связей. Напряжение, вызванное изменением валентных углов наиболее ярко выражено для молекулы циклопропана. В циклопропане так называемые банановые связи. Искажение валентных углов существенным образом влияет на химические свойства циклоалканов. С увеличением числа углеродных атомов напряжение уменьшается. Наиболее напряженным является циклопропан, далее следуют циклобутан, циклопентан и циклогексан. Возможность свободного вращения вокруг ординарной связи углерод-углерод позволяет существовать циклогексану в форме двух конформаций : «кресло» и «ванна». В конформации «кресло» 12 связей С-Н разделяются на две группы аксиальные и экваториальные Заместитель в циклогексане стремится занять экваториальное положение. 2. Способы получения. Способы получения делятся на общие и специальные. К общим способам относятся: 1. Способы, приводящие к получению цикла с числом углеродных атомов таким же, как в исходном дигалоидалкане. Например, дегалогенирование дигалогенпроизводных с помощью цинка:  2. Способы, приводящие к получению цикла с числом углеродных атомов большим, чем в исходном дигалоидалкане. Например, взаимодействие дигалогенпроизводных с эфиром малоновой кислоты в присутствии щелочи. 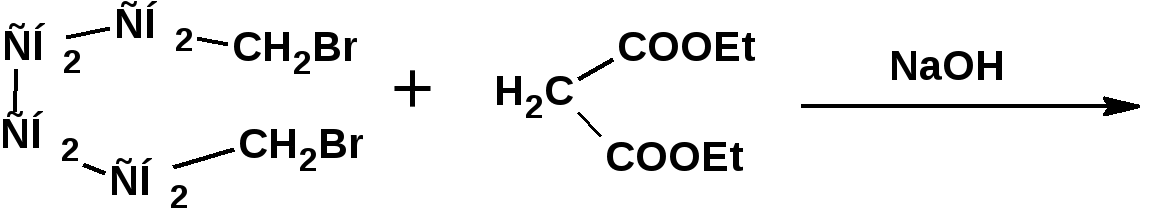 3. Способы, приводящие к получению цикла с числом углеродных атомов меньшим, чем в исходном дигалоалкане. Например, декарбоксилирование солей двухосновных кислот: 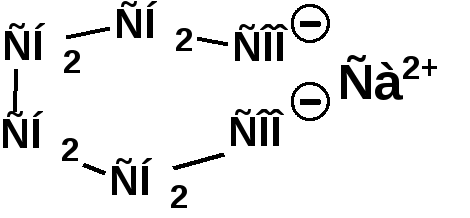 Специальные методы: 1. Соединения с трехчленным циклом получают присоединением карбена к алкенам. 2. Соединения с четерехчленным циклом получают димеризацией алленов (диметиленциклобутан). 3. соединения с шестичленным циклом получают по реакции диенового синтеза. 3. Физические свойства. Циклоалканы имеют более высокие температуры плавления и кипения чем ациклические соединения. 4. Химические свойства. Особенностью химических свойств циклоалканов является то, что малые напряженные циклы: циклопропан и циклобутан ведут себя подобно алкенам, а циклопентан и циклогексан ведут себя подобно алканам. 1. Гидрогалогенирование: Циклопропан и его гомологи реагируют с галогенводородами с раскрытием цикла в соответствии с правилом Марковникова. Остальные не реагируют. 2. Галогенирование: Циклопропан и его гомологи реагируют с галогенами с раскрытием цикла в соответствии с правилом Марковникова. Циклопентан и циклогексан вступают в обычное замещение. Циклобутан реагирует в обоих направлениях. 3. Реакции с водородом: Циклопропан и циклобутан присоединяют молекулу водорода с раскрытием цикла. Циклопентан в условиях малых циклов не реагирует. Для циклогексана устанавливаетися равновесие между ним и бензолом. 4. Окисление. Все циклы окисляются с раскрытием цикла и образованием дикарбоновых кислот Малоновая Янтарная Глутаровая Адипиновая |
