Борьба с гидратами на ОНГКМ. Борьба с гидратами. Анализ методов борьбы с образованием гидратов на газовых или газоконденсатных месторождениях онгкм
 Скачать 0.91 Mb. Скачать 0.91 Mb.
|
|
4.9 Выявление участков шлейфов и оборудования УКПГ, опасных с точки зрения образования кристаллогидратов Условия образования гидратов определяются составом природного газа. С увеличением молекулярной массы индивидуального газа или смеси газов, при меньших значениях давления, при одинаковой температуре более вероятно образование гидратов. Процесс гидратообразования в большинстве случаев протекает на границе раздела фаз ''газ - вода'' при условии полного насыщения природного газа влагой, Процессы могут протекать и в условиях недонасыщения природного газа парами воды. В этой связи возникает необходимость прогнозирования мест образования и интенсивности возникновения гидратов в системах добычи, подготовки и транспорта газа, а это обусловлено влагосодержанием природного газа и его изменением при различных термодинамических условиях. Практически образование гидратов в стволе скважины можно обнапужить по снижению рабочего давления на устье и уменьшению дебита газа. Место образования гидратной пробки обычно удается определить по росту перепада давления на данном участке газопровода. Определение зон возможного образования гидратов проводят путем расчета давления и температуры по стволу простаивающей или работающей газовой скважины, длине газопровода с построением графических зависимостей давления и температуры от глубины скважины. Сравнивая температуру и давление начала гидратообразования газа данного состава с температурой и давлением в стволе газовой скважины, газопроводе, определяют места образования гидратной пробки. 5 Предупреждение процесса гидратообразования Образование гидратов в скважинах и промысловых газопроводах и выбор метода борьбы с ними в значительной степени зависят от пластовых температур, климатических условий и режима эксплуатации скважины. Часто в стволе скважины имеются условия для образования гидратов, когда температура газа при его движении вверх от забоя до устья становится ниже температуры гидратообразования. В результате скважина забивается гидратами. Вследствие снижения температуры газа при движении его по стволу скважины, в потоке всегда имеется конденсационная вода. Поэтому образование гидратов обусловлено только отношением давления и температуры. Место начала образования гидратов в скважинах определяют по точке пересечения равновесной кривой образования гидратов с кривой изменения температуры газа по стволу скважин. Если гидраты перекрывают сечение скважины не полностью, разложения их проще всего достигнуть с помощью ингибиторов. Значительно труднее бороться с отложениями гидратов, полностью перекрывающих сечение фонтанных труб и образовавших сплошную гидратную пробку. При небольшой длине пробки ее ликвидацию обычно осуществляют продувкой скважины. При значительной длине выбросу пробки в атмосферу предшествует некоторый период, в течение которого она частично разлагается в результате снижения давления. Продолжительность периода разложения гидратов зависит от длины пробки, температуры газа и окружающих горных пород. Твердые частицы (песок, шлам, окалина, частицы глинистого раствора и т.п.) замедляют разложение пробки. Для ускорения этого процесса используют ингибиторы. Следует учитывать также, что при образовании гидратной пробки в зоне отрицательных температур только при понижении давления получают эффект. Дело в том, что вода, выделяющаяся при разложении гидратов при низкой концентрации ингибитора, может замерзнуть и вместо гидратной образуется ледяная пробка, ликвидировать которую затруднительно. Если пробка большой длины образовалась в стволе скважины, ее можно ликвидировать, применяя замкнутую циркуляцию ингибитора над пробкой. В результате механические примеси размываются, и на поверхности гидратной пробки постоянно содержится ингибитор высокой концентрации. Для борьбы с отложениями гидратов в промысловых и магистральных газопроводах применяют те же способы, что и на скважинах. Кроме того, предупредить образование гидратов можно путем ввода ингибиторов и теплоизоляцией шлейфов. 5.1 Классификация методов борьбы с гидратами газов Для предупреждения образования гидратов в потоке газа необходимо устранить одно из основных условий гидратообразования: - высокое давление; - низкую температуру; - свободную влагу. В связи с этим основными методами борьбы с гидратами являются понижение давления, повышение температуры, осушка газа, а также изменение условий равновесия системы газ-гидрат-вода путем ввода антигидратных ингибиторов. Ввод ингибиторов, используемых при ликвидации гидратных пробок Место образования гидратной пробки можно определить по росту перепада давления на данном участке газопровода. Если пробка не сплошная, то в трубопровод через специальные патрубки, штуцера для манометров или через продувочную свечу вводят ингибитор. Если в трубопроводе образовались сплошные гидратные пробки небольшой длины, их иногда удается ликвидировать таким же путем. Для быстрого разложения гидратной пробки применяют комбинированный способ; одновременно с вводом ингибитора в зоне образования гидратов снижают давление. Ликвидация гидратных пробок методом снижения давления Сущность этого метода заключается в нарушении равновесного состояния гидратов, в результате чего происходит их разложение. Давление снижают тремя способами: - отключают участок газопровода, где образовалась пробка, и с двух сторон через свечи пропускают газ; - перекрывают линейный кран с одной стороны и выпускают в атмосферу газ, заключенный между пробкой и одним из перекрытых кранов; - отключают участок газопровода с обеих сторон пробки и выпускают в атмосферу газ, заключенный между пробкой и одним из перекрытых кранов. После разложения гидратов учитывают следующее: возможность накопления жидких углеводородов на продуваемом участке и образование повторных гидратоледяных пробок за счет резкого снижения температуры. При отрицательных температурах по методу снижения давления в некоторых случаях не получают должного эффекта, так как вода, образовавшаяся в результате разложения гидратов, переходит в лед и образует ледяную пробку. В этом случае метод снижения давления используют в комбинации выводом в трубопровод ингибиторов. Количество ингибитора должно быть таким, чтобы при данной температуре раствор из введенного ингибитора и воды, получившийся при разложении гидратов, не замерзал (рисунок 5.1). 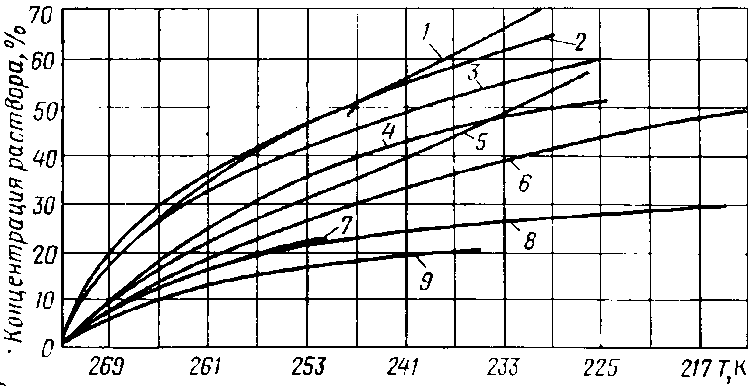 Рисунок 5.1 - Зависимость температуры замерзания воды от концентрации раствора. Ингибиторы: 1 - глицерин; 2 - ТЭГ; З - ДЭГ, 4 - ЭГ; 5 - С2Н5ОН; 7 - NaCI; 8 - CaCI2; 9 - MgCl2 Ликвидация гидратных пробок в трубопроводах природных и сжиженных газов методом подогрева При этом способе повышение температуры выше равновесной температуры образования гидратов приводит к их разложению. На практике трубопровод подогревают горячей водой или паром. Исследования показали, что повышение температуры в точке контакта гидрата и металла до 30 - 40°С достаточно для быстрого разложения гидратов. Ингибиторы для борьбы с образованием гидратов Для борьбы с образованием гидратов широко применяется метанол и гликоли. Иногда используют жидкие углеводороды, ПАВ, пластовую воду, смесь различных ингибиторов, например метанола с растворами хлористого кальция и т.д. Метанол обладает высокой степенью понижения температуры гидратообразования, способностью быстро разлагать уже образовавшиеся гидратные пробки и смешиваться с водой в любых соотношениях, малой вязкостью и низкой температурой замерзания. 5.2 Основы ингибирования процесса гидратообразования Ввод метанола Наиболее распространен на газовых промыслах способ подачи метанола (СН3ОН) в струю газа. При этом он образует с парообразной и жидкой влагой спиртоводные смеси, температура замерзания которых значительно ниже нуля. Пары воды поглощаются из газа, что значительно снижает точку росы, и, следовательно, создаются условия для разложения гидратов или для предупреждения их образования. Основным условием эффективного действия метанола является взаимодействие паров воды с парами метанола и дальнейшая конденсация их, что приводит к значительному понижению влагосодержания газа. Наибольшая эффективность метанола может быть достигнута с применением его в качестве средства, предупреждающего гидратообразование, а не для разрушения уже образовавшихся гидратов. При этом метанол необходимо впрыскивать в газовый поток, обеспечив хорошее распыление и смешение с общим газовым потоком. Ввод электролитов Для борьбы с гидратообразованием все большее применение находят электролиты, в частности, водные растворы хлористого кальция. Это недорогой, безопасный и достаточно эффективный антигидратный ингибитор. Ввод гликолей В качестве антигидратных ингибиторов применяются этиленгликоль (ЭГ), диэтиленгликоль (ДЭГ) и триэтиленгликоль (ТЭГ). В таблице 4.1 приведена характеристика гликолей. Гликоли являются более сильными, но и более дорогими ингибиторами по сравнению с растворами хлористого кальция и метанолом. При использовании отработанный раствор регенерируется и используется вновь. Это значительно снижает стоимость применения гликолей. Выбор гликоля зависит от состава газа. Так, в магистральном газопроводе, где присутствует природный газ, лучше применять ЭГ. Однако в сепараторах, теплообменниках и других дегидраторных аппаратах использовать ЭГ невыгодно из-за высокой упругости его паров. Для этих условий более подходят ДЭГ и ТЭГ. Следует отметить, что в единой системе сбора и транспорта газа следует применять один вид гликоля, что упрощает сбор и регенерацию отобранного раствора. С этой точки зрения целесообразнее всего применять ДЭГ. Гликоли (этиленгликоль, диэтиленгликоль, триэтиленгликоль) часто используют для осушки газа и в качестве ингибитора для борьбы с отложениями гидратов. Наиболее распространен как ингибитор диэтиленгликоль, хотя применение этиленгликоля более эффективно: его водные растворы имеют более низкую температуру замерзания, меньшую вязкость, а также малую растворимость в углеводородных газах, что значительно снижает его потери. Гликоли с водой также смешиваются в любых соотношениях. Наиболее низкие температуры замерзания растворов гликодей находятся в пределах концентрации 60 - 70%, которые являются оптимальными при использовании гликолей в качестве ингибиторов гидратов. Так как упругость паров гликолей при температуре образования гидратов небольшая, то они при вводе в трубопровод практически полностью остаются в жидкой фазе, что упрощает их улавливание для повторного использования. Понижение температуры образования гидратов, а также расход того или иного ингибитора (из расчета на 1 кг выделившейся из газа влаги) можно определить по графику (рисунок 5.2). 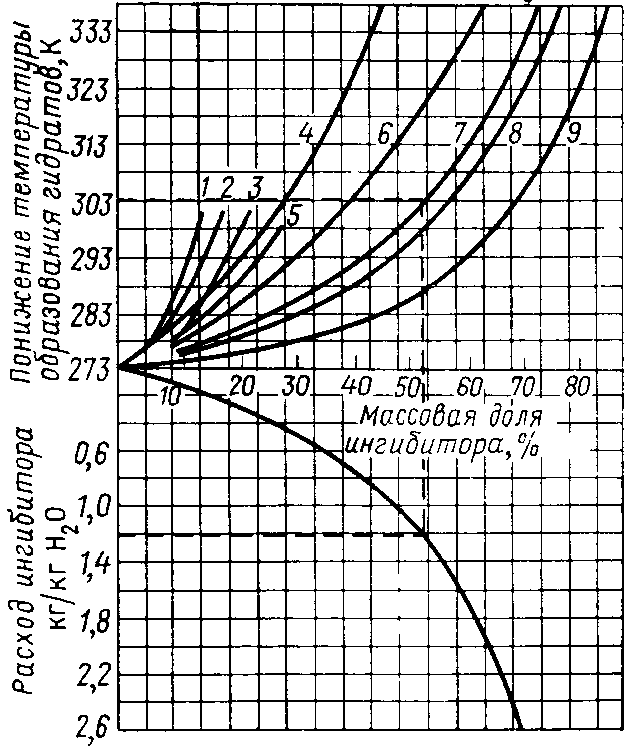 Рисунок 5.2 - Номограмма для определения понижения температуры образования гидратов природных газов и расхода ингибиторов. 1 - LiCl; 2 - MgCl2; 3 - NaCl; 4 - NН4; 5 - CaCl2; 6 - СН3ОН; 7 - ЭГ; 8 - ДЭГ; 9 – ТЭГ 5.3 Физико-химические свойства ингибиторов гидратообразования (метанол, гликоли, хлористый кальций, этилкарбитол, эфироальдегидная фракция) Физико-химические свойства метанола и гликолей приведены в таблицах 5.1 и 5.2. Таблица 5.1 - Физико-химические свойства метанола
Таблица 5.2 - характеристика гликолей
Эфироальдегидная фракция Побочный продукт, получаемый при ректификации спирта-сырца. Прозрачная, бесцветная или с желтоватым (зеленоватым) оттенком жидкость, крепостью не менее 92% об. (при получении спирта-ректификата). Эфироальдегидная фракция выводится из конденсата эпюрационной колонны соответственно в объеме 1,5—5% и 0,5—3% от введенного в установку сырья по абсолютному алкоголю. Состоит в основном из этилового спирта; содержит также сложные эфиры, метиловый спирт и небольшое количество органических кислот. Эфироальдегидную фракцию подвергают разгонке с получением технического спирта, который используют в химических промышленности, и концентрата эфироальдегидной фракции, применяющегося как топливо, пеногаситель и для питания кормовых дрожжей. Кальций хлористый (хлорид кальция, кальциевая соль соляной кислоты) гост 450-77 Представляет собой бесцветные тригональные кристаллы без запаха, горько-соленого вкуса, хорошо растворимые в воде и спирте. Чрезвычайно гигроскопичен. Энергично поглощает водяные пары, сначала образуя твёрдые гидраты, а затем расплываясь в жидкость. Водные растворы хлорида кальция замерзают при низких температурах (20%-ный при -18,57° С, 30%-ный при -48° С). Несовместим с солями тяжелых металлов, кислотами, йодидами и бромистыми солями. Плотность: 2,15 г/см³. Температура плавления 772° C, температура кипения 1935° C. Этилкарбитол технический (моноэтиловый эфир диэтиленгликоля) Химическое название: 2-(2-Этоксиэтокси)этанол Эмпирическая формула: C6H14O3 Технические условия: ТУ 2422-125-05766801-2003 Этилкарбитол технический (моноэтиловый эфир диэтиленгликоля) получают оксиэтилированием этилового спирта и этилцеллозольва. Предназначен для получения эфиров, приготовления тормозных и специальных гидравлических жидкостей. Физико-химические свойства этилкарбитола приведены в таблице 5.3. Таблица 5.3 - характеристика этилкарбитола
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
