апоптоз реферат. Апоптоз уникальный механизм сигналиндуцированной запрограммированной гибели одной клетки или группы клеток многоклеточного организма
 Скачать 239.91 Kb. Скачать 239.91 Kb.
|
|
Введение Апоптоз – уникальный механизм сигналиндуцированной запрограммированной гибели одной клетки или группы клеток многоклеточного организма. Сигналы, запускающие механизмы апоптоза, активируют ферменты, которые вызывают фрагментацию ДНК на участки 50–300 п.н. и разрушение клетки. После этого начинаются фагоцитоз и элиминация апоптозных телец (дебриса) макрофагами. Признаками апоптоза являются уменьшение размеров клетки, уплотнение и фрагментация хроматина, скопление его возле ядерной мембраны, уменьшение объема цитоплазмы. При этом гибель клеток не сопровождается воспалением и повреждением тканей. Апоптоз индуцируется большинством веществ (в малых концентрациях), вызывающих некроз, а также сигналами, поступающими от регуляторных клеточных молекул (гормонов, цитокинов, антигенов, суперантигенов, моноклональных антител). Апоптоз ИКК развивается вследствие поступления «неполных» или недостаточно полных костимуляторных сигналов извне. Сигнал к апоптозу реализуется при взаимодействии его индукторов с мембранной молекулой – антигеном АРО-l/Fas(CD95), относящейся к семейству рецепторов ФНО. APO-MFas экспрессируется на клетках многих типов, a Fas лиганд – в основном па активированных Т-лимфоцитах. Активация Fas обусловливает его взаимодействие с Fas-ассоциированным белком, содержащим домен, индуцирующий смерть клетки. Связывание прокаспазы 8 с этим доменом сопровождается ее активацией. В свою очередь, активированная форма каспазы 8 разрушает (активирует) еще 9 других прокаспаз, которые завершают процесс апоптоза. Функцией каспазы 3 являются активация 2, 6, 7 и 9 каспаз, конденсация хроматина и фрагментация ДНК. Она наиболее изучена. Процесс апоптоза может быть блокирован рядом белков ингибиторов (bcl-2 и др.). Апоптоз служит регулятором количества клеточных популяций организма и важным фактором селекции клонов лимфоцитов. Он также играет исключительно важную роль во многих физиологических процессах – эмбриогенезе, формировании нейронов, системы иммунитета, тканевого гомеостаза, иммунологической толерантности. Противоположным апоптозу процессом является некроз – повреждение нормальных тканей. Актуальность темы В последние годы ученые различных биологических и медицинских специальностей заинтересовались проблемой апоптоза – запрограммированной гибели клеток. Клеточный состав большинства органов всех живых особей практически идентичен, колебания относительно невелики. Жизненный цикл клеток разных систем неодинаков, при этом происходит постоянная их смена. Этот закономерный клеточный феномен, наблюдаемый во всех ядросодержащих клетках организма человека и животных, J. Кerr и соавторы (1972) назвали апоптозом (греч. – осеннее опадание листьев с деревьев). Клеточное постоянство регулируется генетическими программами организма, одна из которых определяет интенсивность клеточного деления, другая – клеточную гибель. В литературе встречаются два термина – «программированная клеточная смерть» и «апоптоз». Большинство авторов используют их как синонимы. Однако они характеризуют различные стороны гибели клеток. Запрограммированная гибель клеток – это более широкое понятие, определяющее совокупность сложных биохимических процессов, а апоптоз – морфологическое понимание смерти. J. Kerr и соавторы выдвинули концепцию о принципиальном различии нормальной клеточной гибели в зрелом организме как формы клеточного обновления и патологической гибели – некроза клеток при различных повреждениях тканей (травма, ишемия и др.). Для некроза характерно набухание и разрыв клеточной оболочки, выход клеточного содержимого в окружающую среду и развитие воспаления. При апоптозе происходит конденсация клеточных элементов (ядро, протоплазма), но клеточная мембрана сохраняется целой, погибшие клетки фагоцитируются макрофагами, воспаление не развивается. Непосредственные причины апоптической гибели клеток окончательно не установлены, но большинство авторов полагают, что значение имеет истощение энергетических ресурсов клетки. Наиболее распространенный путь реализации апоптоза – это инициация физиологическими сигналами-индукторами, которые воспринимаются специализированными клеточными рецепторами. Их активация вызывает последовательные этапы внутриклеточных биохимических процессов. Сигналами являются многие факторы (биологически активные вещества, дисгормональные ситуации, антигенные перегрузки, антитела к рецепторам клеток для антигенов, некоторые цитокины и др.). Сигналами может быть как наличие, так и отсутствие необходимого вещества в среде, окружающей клетку. Характер ответа на эти сигналы неоднозначен и, как указывает А.А. Ярилин (1996), зависит от ряда факторов (особенности и состояние клеток, стадия их активации и дифференцировки). Восприятие сигналов осуществляется через белковые молекулы на мембране клеток – рецепторы, состоящие из трех частей (внеклеточной, внутриклеточной и промежуточной, пронизывающей мембрану клетки). Внеклеточная (наружная) часть рецептора может воспринимать сигналы определенного строения, находящиеся либо в свободном состоянии, либо на мембране других клеток. Среди механизмов биологической гибели наиболее универсальным является механизм специфических рецепторов Fas (Fas R2, Apo1, CD95). Fas экспрессируется на поверхности многих типов клеток: активированных Т- и В-лимфоцитов, антигенпрезентирующих клеток, фибробластов, кератиноцитов, трансформированных вирусами и т.д. Он относится к семейству рецепторов фактора некроза опухоли (ФНО; TNF – tumor necrosis factor). Это мембранный белок, имеющий в своей структуре внеклеточный, трансмембранный и цитоплазматический участки (домены). Этот рецептор активируется соответствующим антигеном – Fas-лигандом (Fas-L). Fas-лиганд (Apo 1 L, CD 95 L) – индуктор апоптоза; это цитокин, имеющий две формы – нерастворимую, связанную с мембраной клетки, и растворимую, которая получается при отщеплении его от эффектора. Fas-L реагирует с тремя молекулами Fas, вызывает активацию каспазного каскада и апоптоза. Fas-L – мембранный протеин второго типа, аминотерминал которого находится в цитоплазме, а С-концевой участок – во внеклеточном пространстве. Связывание Fas-L и Fas, или соединение Fas с антителами IgM или IgG3, вызывает апоптоз в клетках, несущих Fas. В цитоплазматическом участке Fas имеется гомологичный домен, который вызывает индукцию сигнала гибели (death domen (DD) – домен смерти). В процессе активации возможно усиление экспрессии Fas-рецептора. Внутриклеточная часть рецептора связана с определенными клеточными ферментами, поэтому в результате действия наружного сигнала в клетке происходят биохимические сдвиги, гидролиз липидов клеточной мембраны, изменение уровня в молекулах белковых регуляторов, что ведет к изменению набора внутриклеточных РНК и белков. Каспазы обусловливают расщепление антиапоптозных белков из семейства Bcl-2, протеолиз ингибитора ДНК-азы и фрагментацию, нарушение цитоскелета клетки. Следствием этого является уплотнение хроматина – главного внутриядерного компонента, содержащего ДНК и белки. Ядро распадается на фрагменты – хроматиновые тельца, разрушается цитоплазма. Апоптоз может происходить и без участия каспаз, но при повышенном синтезе белков – промоутеров апоптоза семейства Вах и Ваk. Регуляция апоптоза определяется концентрацией в клетке белков-регуляторов. Это белки семейства Вах, молекулы которых могут образовывать димеры. Повышенное содержание их способствует апоптозу. Белок Bcl-2 тоже образовывает димеры, но он может соединяться с белком Вах, образуя гетеродимер Вах/Bcl-2, и апоптоз задерживается, т.е. увеличение содержания белка Вах способствует гибели клетки (если есть сигнал из окружающей среды), а при преобладании Bcl-2 клетка от гибели защищена. В мембране митохондрий локализуются протеины ядерных генов Ced9/Bcl-2, одни из которых (Bcl-2, Bcl-xa) ингибируют апоптоз, другие (Вах, Ваk) – стимулируют его. Соотношение ингибиторов и стимуляторов определяет способность клетки к апоптозу. Известный ген р53 ответственен за синтез протеина р53, он локализуется в ядре клетки и регулирует экспрессию генов, блокирующих клеточный цикл. Белок р53, вызывая остановку деления клетки, предупреждает появление мутантных клеток. Гены семейства Bcl-2 контролируются геном р53, но эффект последнего неоднозначен, он может стимулировать и пролиферацию, и апоптоз, поэтому исход зависит от особенности программы клеточной линии, наличия цитокинов, а также ряда других факторов. Поскольку передача апоптогенных сигналов индуцируется разнообразными факторами и воздействиями, следовательно, и пути их поступления внутрь клетки различны. В зависимости от характера пускового сигнала различают несколько разновидностей апоптоза. Если сигнал передается через клеточные рецепторы, то происходит активация тирозинкиназ, фосфолипазы С, включаются ионы кальция, Са2+/кальмодулин-зависимая протеинфосфатаза, протеинкиназы. Это ведет к активации Т-клеток, их митозу. При другой разновидности апоптоза, вызванной глюкокортикоидами, участвует система циклического АМФ. При повышении его уровня вследствие активации аденилатциклазы и фосфолипазы А2 или при ингибировании фосфодиэстеразы цАМФ усиливается фрагментация ДНК и наступает гибель клетки – эффект через активацию протеинкиназы А. Если сигнал происходит от цитокинов (ФНО-a), то это ведет к каскаду реакций, формирующих транскрипционные факторы, активации генов и апоптозу через Fas-рецепторы. Важная роль в развитии апоптоза отводится ионам кальция и активаторам протеинкиназы С. Одним из основных механизмов реализации апоптоза является деградация ДНК, проходящая ряд этапов с участием Са2+, Mg2+-зависимой эндонуклеазы, что ведет к фрагментации хроматина и ядра. Основная причина гибели клеток – истощение пула АТФ вследствие активации поли (АДР-рибоза) полимеразы в ответ на повреждение ДНК. Расщепление ДНК сопровождается энергетическим голоданием, которое развивается в связи с увеличением расхода АТФ на репарацию поврежденной ДНК, усиливается активация фермента поли (АДР-рибоза) полимеразы, истощается АДР-рибозный комплекс. Проявления апоптоза в основном биохимические, морфологические и цитофлюорометрические. Биохимическими проявлениями апоптоза являются активация ферментов (эндонуклеаз, трансглутаминазы), фрагментация ДНК – расщепление в результате ее разрыва при электрофорезе выявляется в виде «лесенки». При некрозе же признак деградации ДНК – «размазанный» характер миграции ДНК при электрофорезе, изменение структуры клеточной мембраны. Морфологические признаки апоптоза: сморщивание клеток и уплотнение мембран, что обусловливается активацией трансглутаминазы, которая вызывает перекрестное сшивание мембранных белков. Можно выделить 2 стадии клеточных изменений: – первая стадия – преапоптоз – уменьшение размеров и сморщивание клетки, уплотнение и фрагментация хроматина; изменения в ядре (появляются осьмиофильные скопления хроматина по периферии). Эти изменения обратимы. На стадии преапоптоза процесс гибели клетки может быть задержан специфическими регуляторами, блокирующими каспазы-индукторы либо их разрушающими. Активация же эффекторных каспаз приводит к гибели клетки; – вторая стадия – инвагинация в ядерной мембране, хроматиновые фрагменты отходят от ядра (апоптические тельца). В цитоплазме происходит конденсация и сморщивание гранул, расширение эндоплазматического ретикулума, отмечается потеря клеточной мембраной ворсинок и нормальной складчатости, формирование на поверхности клетки пузырей. Следовательно, наиболее значимые изменения при апоптозе происходят в ядре клетки и выражаются в конденсации и фрагментации хроматина, что является результатом деградации ДНК вследствие активации эндонуклеаз. Цитофлюорометрическое изменение структуры мембран ведет к экспрессии на поверхности клеток детерминантных групп (они необычны), благодаря чему апоптические клетки быстро распознаются фагоцитами (макрофагами, нейтрофилами, мезангиальными клетками почек) как чужеродные, поглощаются ими и разрушаются. Особую роль в жизнедеятельности иммунной системы играет запрограммированная гибель клеток. На всех этапах клеточного развития – пролиферации и дифференцировки – она является методом отбора иммунокомпетентных клеток (ИКК), регулирует их ответ на антигенные стимулы, определяет характер иммунного ответа или формирование иммунологической толерантности. На ранних этапах кроветворения в отборе ИКК регулирующую функцию выполняет фактор стволовых клеток (SCF). На дальнейших этапах дифференцировка клеток определяется очень многими факторами, выполняющими роль как индуктора, так и факторов выживания. Существуют две альтернативные формы ответа различных популяций клеток иммунной системы на антигенную стимуляцию – пролиферация или апоптоз. Апоптоз – активная форма реакции ИКК не только на неблагоприятные, но и на физиологические, и на активирующие (антигены, митогены) воздействия. Апоптоз ИКК обусловлен взаимодействием рецептора Fas (CD 95/Apo 1) и его лиганда Fas-L, которые экспрессируются на них. Экспрессия Fas увеличивается под влиянием интерферона-γ и ИЛ-2. Индукция Fas-L наступает при антигенной стимуляции (Moulian N. et al., 1998). Установлено, что более 95% тимоцитов, поступающих в вилочковую железу (тимус), удаляются путем апоптоза в ходе их селекции и облучения (Wylle A.H., 1980). Апоптоз в тимусе совершается без системы Fas/Fas-L. Апоптоз Т-клеток внутри тимуса обусловлен действием агентов, среди которых глюкокортикоиды или продукты со сходным действием, а также комплексы рецепторовTCR-CD3 с антигенами. Большинство незрелых Т-лимфоцитов погибает на ранних этапах своего развития из-за неправильного направления Т-рецептора, или аутореактивности. На периферии зрелые Т-клетки распознают собственные антигены и гибнут при периферической клональной делеции с участием Fas-рецепторов в силу активации их аутоантигенами. Имеются и мембранные молекулы, способные модифицировать активационный сигнал (CD4 и CD8), их перекрестное сшивание активирует апоптоз через TCR-CD3. Защищают клетки от активационного апоптоза мембранные молекулы: для В-лимфоцитов – CD40, для Т-лимфоцитов – CD28. Морфологические проявления апоптоза Апоптоз имеет свои отличительные морфологические признаки, как на светооптическом, так и на ультраструктурном уровне. При окраске гематоксилином и эозином апоптоз определяется в единичных клетках или небольших группах клеток. Апоптотические клетки выглядят как округлые или овальные скопления интенсивно эозинофильной цитоплазмы с плотными фрагментами ядерного хроматина. Поскольку сжатие клетки и формирование апоптотических телец происходит быстро и также быстро они фагоцитируются, распадаются или выбрасываются в просвет органа, то на гистологических препаратах он обнаруживается в случаях его значительной выраженности. К тому же апоптоз - в отличие от некроза - никогда не сопровождается воспалительной реакцией, что также затрудняет его гистологическое выявление. Таблица 1. Сравнительная характеристика некроза и апоптоза
Апоптоз - это механизм гибели клеток, который имеет ряд биохимических и морфологических отличий от некроза. Наиболее четко морфологические признаки выявляются при электронной микроскопии. Для клетки, подвергающейся апоптозу характерно (рис.1): 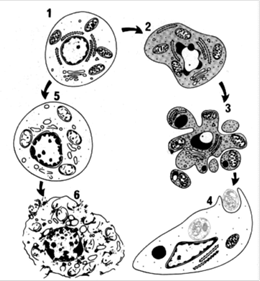 Рис.1. Последовательность ультраструктурных изменений при апоптозе (справа) и некрозе (слева): 1 - нормальная клетка; 2 - начало апоптоза; 3 - фрагментация апоптотической клетки; 4 - фагоцитоз апоптотических телец окружающими клетками; 5 - гибель внутриклеточных структур при некрозе; 6 - разрушение клеточной мембраны. Сжатие клетки Клетка уменьшается в размерах; цитоплазма уплотняется; органеллы, которые выглядят относительно нормальными, располагаются более компактно. Предполагается, что нарушение формы и объема клетки происходит в результате активации в апоптотических клетках трансглютаминазы. Этот фермент вызывает прогрессивное образование перекрестных связей в цитоплазматических белках, что приводит к формированию своеобразной оболочки под клеточной мембраной, подобно ороговевающим клеткам эпителия. Конденсация хроматина Это наиболее характерное проявление апоптоза. Хроматин конденсируется по периферии, под мембраной ядра, при этом образуются четко очерченные плотные массы различной формы и размеров. Ядро же может разрываться на два или несколько фрагментов. Механизм конденсации хроматина изучен достаточно хорошо. Он обусловлен расщеплением ядерной ДНК в местах, связывающих отдельные нуклеосомы, что приводит к развитию большого количества фрагментов, в которых число пар оснований делится на 180-200. При электрофорезе фрагменты дают характерную картину лестницы. Эта картина отличается от таковой при некрозе клеток, где длина фрагментов ДНК варьирует. Фрагментация ДНК в нуклеосомах происходит под действием кальций чувствительной эндонуклеазы. Эндонуклеаза в некоторых клетках находится постоянно (например, в тимоцитах), где она активируется появлением в цитоплазме свободного кальция, а в других клетках синтезируется перед началом апоптоза. Однако еще не установлено, каким образом после расщепления ДНК эндонуклеазой происходит конденсация хроматина. Формирование в цитоплазме полостей и апоптотических телец В апоптотической клетке первоначально формируются глубокие впячивания поверхности с образованием полостей, что приводит к фрагментации клетки и формированию окруженных мембраной апоптотических телец, состоящих из цитоплазмы и плотно расположенных органелл, с или без фрагментов ядра. Фагоцитоз апоптотических клеток или телец Фагоцитоз апоптотических клеток или телец осуществляется окружающими здоровыми клетками, или паренхиматозными, или макрофагами. Апоптотические тельца быстро разрушаются в лизосомах, а окружающие клетки либо мигрируют, либо делятся, чтобы заполнить освободившееся после гибели клетки пространство. Фагоцитоз апоптотических телец макрофагами или другими клетками активируется рецепторами на этих клетках: они захватывают и поглощают апоптотические клетки. Один из таких рецепторов на макрофагах - рецептор витронектина, который является β3-интегрином и активирует фагоцитоз апоптотических нейтрофилов. Апоптоз принимает участие в следующих физиологических и патологических процессах: Запрограммированном разрушении клеток во время эмбриогенеза (включая имплантацию, органогенез). Несмотря на то, что при эмбриогенезе апоптоз не всегда является отражением “запрограммированной смерти клетки”, это определение апоптоза широко используют различные исследователи. Гормон-зависимой инволюции органов у взрослых, например, отторжение эндометрия во время менструального цикла, атрезии фолликулов в яичниках в менопаузе и регрессия молочной железы после прекращения лактации. Удалении некоторых клеток при пролиферации клеточной популяции. Гибели отдельных клеток в опухолях, в основном при ее регрессии, но также и в активно растущей опухоли. Гибели клеток иммунной системы, как В-, так и Т-лимфоцитов, после истощения запасов цитокинов, а также гибели аутореактивных Т-клеток при развитии в тимусе. Патологической атрофии гормон-зависимых органов, например, атрофии предстательной железы после кастрации и истощении лимфоцитов в тимусе при терапии глюкокортикоидами. Патологической атрофии паренхиматозных органов после обтурации выводных протоков, что наблюдается в поджелудочной и слюнных железах, почках. Гибели клеток, вызванных действием цитотоксических Т-клеток, например, при отторжении трансплантата и болезни “трансплантат против хозяина”. Повреждении клеток при некоторых вирусных заболеваниях, например, при вирусном гепатите, когда фрагменты апоптотических клеток обнаруживаются в печени, как тельца Каунсильмана. Механизм апоптоза TNF-α и Fas-лиганд (CD178) запускают каскад биохимических реакций, финальным этапом которых является дефрагментация хромосом и гибель клетки. На поверхности клеток организма имеются специальные рецепторы для TNF-α, это TNF-RI (с молекулярной массой 55-60 кДа) и TNF-RII (с молекулярной массой 75-80 кДа), а для Fas-лиганда рецептор Fas / APO-1 (CD95). TNF-R и Fas / APO-1(CD95) имеют гомологию в экстрацеллюлярных доменах, представленную в виде цистеин богатых доменов и гомологичную последовательность в интрацеллюлярной части рецептора. 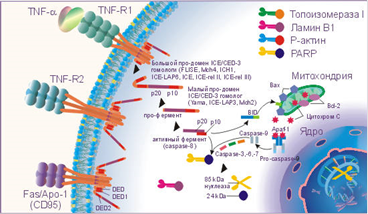 Рис.2. Апоптоз Связывание TNF-α и Fas-лигандов с рецепторами апоптоза активирует интрацеллюлярные "домены смерти" (DED - death effector domain) этих рецепторов: DED, DED1 и DED2 и ряд посредников, включая церамиды, ras, SAPK / JNK, протеиновые тирозинкиназы, катепсин D и протеазы ICE / CED-3 семейства, которые каскадно проводят смертельный сигнал. Цистеиновые протеазы ICE / CED-3 семейства находятся в составе интрацеллюлярной части рецептора апоптоза в неактивной форме, они относятся к интерлейкин-lβ расщепляющим ферментам (ICE). Это семейство включает ряд различных типов протеаз, многие протеазы имеют несколько обозначений. Семейство цистеин-аспартат протеаз ещё называют каспазами. Кроме семейства каспаз, в регуляции апоптоза принимает участие семейство Bcl-2 белков, в котором Bcl-2, Bcl-XL, Ced-9, Bcl-w, и Mcl-1 белки ингибируют апоптоз, а Bcl-2 гомологи (BH) 1-3, Bax подобный белок, Bak, Bok, и состоящие только из BH3 региона, Bad подобный белок, Bid, Bik, Bim, и Hrk выполняют проапоптозную функцию. Активация DED, DED1 и DED2 вызывает каскадную перестройку и активацию протеаз ICE / CED-3 семейства. Первым этапом является превращение не активной про-каспазы-8 в активную каспазу-8. Каспаза-8 активирует каспазу-3 и Bid. Bid взаимодействуя с Bax способствует выходу из митохондрий цитохрома C, который активизирует каспазу-9. В свою очередь активная каспаза-9 приводит к появлению активных каспаз-3, - 6, - 7. В свою очередь активные ICE начинают взаимодействовать с рядом внутриклеточных субстратов: поли-(АДФ-рибозо) полимеразой (PARP), участвующей в репарации ДНК и модификации активности некоторых ядерных белков, ламином В1, топоизомеразой I и Р-актином. Все члены семейства ICE / CED-3 протеаз содержат каталитический остаток цистеина и расщепляют субстраты после аспарагиновой кислоты. Специфическое расщепление PARP, ламина В1, топоизомеразы I и Р-актина под действием ICE-подобных протеаз на большие и малые фрагменты приводит клетку к гибели, так как большие фрагменты этих субстратов и являются активными нуклеазами, которые разрезают хромосомы на фрагменты. Например, PARP расщепляется CPP32 / Yama на два фрагмента 85 и 24 кДа, из которых апоптоз-специфическим является фрагмент 85 кДа. Активация протеаз ICE / CED-3 семейства может происходить и под действием фосфолипидов, например, церамидов, которые способны активировать CPP32 / Yama. Свободный сфингозин образуемый из церамидов в результате его гидролиза церамидазой так же активирует ICE-подобные протеазы и ускоряет апоптоз. 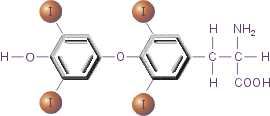 Рис.3. Тироксин Важная роль в осуществлении апоптоза принадлежит тироксину (Т4). Он регулирует функционирование протеиновой тирозинкиназы, важного элемента реализации сигнала смерти. При недостатке этого гормона щитовидной железы происходит подавление апоптоза. IL-lβ блокирует апоптоз. ICE-подобные протеазы взаимодействуют с IL-lβ, а не с PARP, ламином В1, топоизомеразой I и Р-актином. В результате чего не происходит образования активных нуклеаз, и клетка избегает апоптоза. На взаимодействие TNF-α и Fas-лигандов с TNF-R и Fas / APO-1(CD95) и проведение апоптотического сигнала оказывают влияние Bcl и Bax белки. Так белки Bcl семейства: Bcl-2, Bcl-xL и Bcl-xS блокируют выход цитохрома С из митохондрий и таким образом предотвращают превращение про-каспазы-9 в активную форму, отменяют атоптотический сигнал. В свою очередь Bax белки способствуют выходу цитохрома С из митохондрий и образованию активной каспазы-9, которая инициирует продолжение и активацию апоптотическог каскада, начавшегося с присоединения TNF-α или Fas-лигандов к TNF-R и Fas / APO-1(CD95). Быть или не быть апоптозу зависит от соотношения Bcl и Bax белков в митохондриях. Преобладание экспрессии белков Bcl семейства блокирует запуск апоптоза, а преобладание экспрессии Bax белков способствует реализации сигнала смерти. Регуляция апоптоза Апоптоз - это генетически контролируемая смерть клетки. В настоящее время выявлено большое число генов, которые кодируют вещества, необходимые для регуляции апоптоза. Многие из этих генов сохранились в ходе эволюции - от круглых червей до насекомых и млекопитающих. Некоторые из них обнаруживаются также в геноме вирусов. Таким образом, основные биохимические процессы апоптоза в разных экспериментальных системах (исследования ведутся на круглых червях и мухах) являются идентичными, поэтому результаты исследований можно прямо переносить на другие системы (например, организм человека). Апоптоз может регулироваться: внешними факторами, автономными механизмами. Воздействие внешних факторов Апоптоз может регулироваться действием многих внешних факторов, которые ведут к повреждению ДНК. При невосстановимом повреждении ДНК путем апоптоза происходит элиминация потенциально опасных для организма клеток. В данном процессе большую роль играет ген супрессии опухолей р53. К активации апоптоза также приводят вирусные инфекции, нарушение регуляции клеточного роста, повреждение клетки и потеря контакта с окружающими или основным веществом ткани. Апоптоз - это защита организма от персистенции поврежденных клеток, которые могут оказаться потенциально опасными для многоклеточного организма. При стимуляции тканей каким-либо митогеном ее клетки переходят в состояние повышенной митотической активности, которая обязательно сопровождается некоторой активацией апоптоза. Судьба дочерних клеток (выживут они или подвергнутся апоптозу) зависит от соотношения активаторов и ингибиторов апоптоза: ингибиторы включают факторы роста, клеточный матрикс, половые стероиды, некоторые вирусные белки; активаторы включают недостаток факторов роста, потерю связи с матриксом, глюкокортикоиды, некоторые вирусы, свободные радикалы, ионизирующую радиацию. При воздействии активаторов или отсутствии ингибиторов происходит активация эндогенных протеаз и эндонуклеаз. Это приводит к разрушению цитоскелета, фрагментации ДНК и нарушению функционирования митохондрий. Клетка сморщивается, но клеточная мембрана остается интактной, однако повреждение ее приводит к активации фагоцитоза. Погибшие клетки распадаются на небольшие, окруженные мембраной, фрагменты, которые обозначаются как апоптотические тельца. Воспалительная реакция на апоптотические клетки не возникает. Автономный механизм апоптоза При развитии эмбриона различают три категории автономного апоптоза: морфогенетический, гистогенетический и филогенетический. Морфогенетический апоптоз участвует в разрушении различных тканевых зачатков. Примерами являются: разрушение клеток в межпальцевых промежутках; гибель клеток приводит к разрушению избыточного эпителия при слиянии небных отростков, когда формируется твердое небо. гибель клеток в дорсальной части нервной трубки во время смыкания, что необходимо для достижения единства эпителия двух сторон нервной трубки и связанной с ними мезодермы. Гистогенетический апоптоз наблюдается при дифференцировке тканей и органов, что наблюдается, например, при гормональнозависимой дифференцировке половых органов из тканевых зачатков. Так, у мужчин клетками Сертоли в яичках плода синтезируется гормон, который вызывает регрессию протоков Мюллера (из которых у женщин формируются маточные трубы, матка и верхняя часть влагалища) путем апоптоза. Филогенетический апоптоз участвует в удалении рудиментарных структур у эмбриона, например, пронефроса. При различных состояниях может наблюдаться как ускорение, так и замедление апоптоза. Несмотря на то, что апоптоз могут активировать различные факторы, характерные для определенных типов клеток, однако конечный путь апоптоза регулируется точно установленными генами и является общим, независимо от причины активации апоптоза. Все факторы, усиливающие или ослабляющие апоптоз, могут действовать прямо на механизм гибели клетки или опосредованно, путем влияния на регуляцию транскрипции. В некоторых случаях влияние этих факторов на апоптоз является решающим (например, при глюкокортикоид-зависимом апоптозе тимоцитов), а в других не имеет особой важности (например, при Fas - и TNF-зависимом апоптозе). В процессе регуляции принимает участие большое количество веществ. Наиболее изученными из них являются вещества из семейства bcl-2. Bcl-2 ген впервые был описан как ген, который транслоцируется в клетках фолликулярной лимфомы и ингибирует апоптоз. При дальнейших исследованиях оказалось, что Bcl-2 является мультигеном, который обнаруживается даже у круглых червей. Гомологичные гены были также обнаружены в некоторых вирусах. Все вещества, относящиеся к данному классу делятся на активаторы и ингибиторы апоптоза. К ингибиторам относятся: bcl-2, bcl-xL, Mcl-1, bcl-w, аденовирусный E1B 19K, Эпштейн-Барр-вирусный BHRF1. К активаторам относятся bax, bak, Nbk / Bik1, Bad, bcl-xS. Члены этого семейства взаимодействуют друг с другом. Одним из уровней регуляции апоптоза является взаимодействие белок-белок. Белки семейства bcl-2 формируют как гомо - так и гетеродимеры. Например, bcl-2-ингибиторы могут образовать димеры bcl-2-активаторами. Таким образом, жизнеспособность клеток зависит от соотношения активаторов и ингибиторов апоптоза. Например, bcl-2 взаимодействует с bax; при преобладании первого жизнеспособность клетки повышается, при избытке второго - уменьшается. К тому же белки семейства bcl-2 могут взаимодействовать с белками, не относящимися к этой системе. Например, bcl-2 может соединятся с R-ras, который активирует апоптоз. Другой белок, Bag-1, усиливает способность bcl-2 ингибировать апоптоз. В настоящее время принято считать, что гены, участвующие в регуляции роста и развития опухолей (онкогены и гены-супрессоры опухолей), играют регулирующую роль в индукции апоптоза. К ним относятся: bcl-2 онкоген, который ингибирует апоптоз, вызванный гормонами и цитокинами, что приводит к повышению жизнеспособности клетки; Белок bax (также из семейства bcl-2) формирует димеры bax-bax, которые усиливают действие активаторов апоптоза. Отношение bcl-2 и bax определяет чувствительность клеток к апоптотическим факторам и является “молекулярным переключателем”, который определяет, будет ли происходить рост или атрофия ткани. c-myc онкоген, чей белковый продукт может стимулировать либо апоптоз, либо рост клеток (при наличии других сигналов выживания, например, bcl-2) Ген р53, который в норме активирует апоптоз, но при мутации или отсутствии (что обнаружено в некоторых опухолях) повышает выживаемость клеток. Установлено, что р53 необходим для апоптоза при повреждении клетки ионизирующим излучением, однако при апоптозе, вызванном глюкокортикоидами и при старении, он не требуется. Снижение и ускорение апоптоза Продукт р53 гена следит за целостностью генома при митозе. При нарушении целостности генома клетка переключается на апоптоз. Наоборот, белок bcl-2 ингибирует апоптоз. Таким образом, недостаток р53 или избыток bcl-2 приводит к накоплению клеток: эти нарушения наблюдаются в различных опухолях. Изучение факторов регулирующих апоптоз имеет важное значение в разработке лекарственных препаратов, усиливающих гибель клеток злокачественных новообразований. Аутоиммунные заболевания могут отражать нарушения в индукции апоптоза лимфоидных клеток, способных реагировать с собственными антигенами. Например, при системной красной волчанке наблюдается нарушение Fas-рецепторов на клеточной поверхности лимфоцитов, что ведет к активации апоптоза. Некоторые вирусы повышают свою выживаемость путем ингибирования апоптоза инфицированных клеток, например, вирус Эпштейна-Барра может воздействовать на обмен bcl-2. Ускорение апоптоза доказано при синдроме приобретенного иммунодефицита (СПИД), нейротрофических заболеваниях и некоторых заболеваниях крови, при которых наблюдается дефицит каких-либо форменных элементов. При СПИДе вирус иммунодефицита может активировать CD4 рецептор на неинфицированных Т-лимфоцитах, ускоряя, таким образом, апоптоз, что приводит к истощению клеток данного типа. Значение апоптоза в развитии организма и патологических процессах Апоптоз играет важную роль в развитии млекопитающих и в различных патологических процессах. Функционирование bcl-2 требуется для поддержания жизнеспособности лимфоцитов, меланоцитов, эпителия кишечника и клеток почек во время развития эмбриона. bcl-x необходим для ингибирования смерти клеток в эмбриогенезе, особенно в нервной системе. Bax необходим для апоптоза тимоцитов и поддержания жизнеспособности сперматозоидов во время их развития. р53 является геном супрессии опухолей, поэтому в эмбриогенезе особой роли не играет, но обязательно необходим для супрессии опухолевого роста. Мыши, у которых отсутствовали оба р53 гена, проявляли чрезвычайно высокую склонность к развитию злокачественных опухолей в результате полного или частичного нарушения апоптоза предопухолевых клеток. Усиленный синтез белка, кодируемого bcl-2 геном, приводит к подавлению апоптоза и, соответственно, развитию опухолей; данный феномен обнаружен в клетках В-клеточной фолликулярной лимфомы. При лимфопролиферативных заболеваниях и похожей на системную красную волчанку болезни у мышей наблюдается нарушение функции Fas-лиганда или Fas-рецептора. Повышенный синтез Fas-лиганда может предупреждать отторжение трансплантата. Апоптоз является частью патологического процесса при инфицировании клетки аденовирусами, бакуловирусами, ВИЧ и вирусами гриппа. Ингибирование апоптоза наблюдается при персистировании инфекции, в латентном периоде, а при усиленной репликации аденовирусов, бакуловирусов, возможно герпесвирусов, вируса Эпштейн-Барра и ВИЧ наблюдается активация апоптоза, что способствует широкому распространению вируса. При нейродистрофических заболеваниях отмечается нарушение функции гена (iap-гена), сходного с ингибитором апоптоза бакуловирусов. Роль апоптоза в защите от онкологических заболеваний Современная химиотерапия опухолей часто базируется на усилении апоптоза в раковых клетках исходя из того, что они более чувствительны к нему, нежели обычные не-раковые клетки. К сожалению, на продвинутых стадиях опухолевого процесса апоптоз в раковых клетках, как правило, подавлен. Некоторые интерфероны усиливают экспрессию гена p53, помогая апоптозу. В результате эти интерфероны помогают борьбе с раком. Новое лекарство от рака лёгких гефитиниб ингибирует белок-рецепторную протеинкиназу EGFR-тирозинкиназа (EGFR tyrosine kinase), которая производится в раковых клетках лёгких и запускает каскад реакций, активирующих апоптоз. В результате гефитиниб используется для лечения рака лёгких с минимумом побочных эффектов. Лилинг Янг (Liling Yang) и др. [1] обнаружили, что в одном из типов раковых клеток лёгких, NCI-H460, апоптоз блокируется избыточным выделением вещества, которое назвали X-linked inhibitor of apoptosis protein (XIAP). Этот ингибитор, связываясь с каспазой-9, подавляет действие цитохрома С. Янг и её соавторы синтезировали пептид SmacN7, уничтожающий XIAP-ы, благодаря чему апоптоз снова начал действовать, и раковые опухоли у мышей стали уменьшаться. |
