Тема 24. Ариламины и другие азотсодержащие соединения. Аренмонокарбоновые кислоты Ароматические нитросоединения Методы получения
 Скачать 295.7 Kb. Скачать 295.7 Kb.
|
|
2 H2SO4 + NaNO2 --- O=N-OSO3H + NaHSO4 + H2O Диазотирование всегда проводят в кислой среде, где протолитическое равновесие сильно смещено вправо. Тем не менее диазотированию подвергается амин в виде свобoдного основания. Механизм диазотирования включает образование нитрозамина, таутомерное превращение его в диазогидроксид, протонированная форма которого отщепляет молекулу воды с образованием катиона диазония. 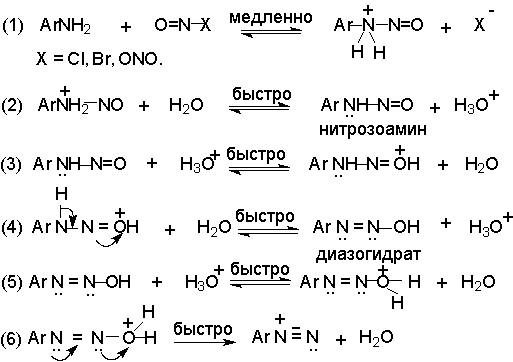 Лимитирующей стадией процесса является образование катиона N-арилнитрозоаммония. Далее следует ряд быстрых протолитических равновесий. На стадии (4) происходит отщепление протона от азота или кислорода, поскольку исходный катион формально является аналогом аллильного катиона. Депротонирование кислорода приводит к исходному субстрату - нитрозамину, тогда как депротонирование азота ведет к образованию конечного продукта - соли арендиазония. Условия проведения реакции диазотирования Диазотирование - экзотермическая реакция, сопровождающаяся выделением большого количества теплоты, поэтому процесс проводят при охлаждении, поддерживая температуру в интервале 0-5о, чтобы не допустить разложения термически неустойчивой соли арендиазония. В реакции используют избыток минеральной кислоты, так чтобы по окончании диазотирования рН не превышал 0,5-1,5. Высокая кислотность среды необходима для подавления побочных процессов с участием образующегося катиона арендиазония и исходного ароматического амина. 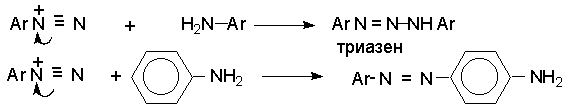 азосоединение В растворе с низким значением рН резко снижается концентрация свободного амина и тем самым подавляются оба нежелательных процесса с его участием. От кислотности среды зависит скорость процесса диазотирования. С увеличением кислотности растет концентрация образующихся из азотистой кислоты активных нитрозирующих агентов, что должно приводить к увеличению скорости. Однако одновременно снижается концентрация свободного амина, что замедляет реакцию. Для успешного проведения процесса необходимо поддерживать оптимальную концентрацию кислоты, соизмеряя ее с основностью амина. Диазотирование осуществляется четырьмя основными методами, выбор каждого из которых определяется природой исходного амина. 1. Метод "прямого" диазотирования применим для диазотирования анилина, алкил-, галоген - и алкоксианилинов. Раствор одного эквивалента нитрита натрия при охлаждении до 0 - 5о постепенно добавляют к водному раствору одного эквивалента амина с тремя эквивалентами сильной минеральной кислоты. 2. "Обратный" метод диазотирования используют для плохо растворимых в кислотах аминов, например, сульфаниловой и антраниловой кислот, для которых характерно образование внутренних солей. В этом случае щелочной раствор диазотируемого амина и нитрита натрия постепенно вводят в водный раствор охлажденной до +5о разбавленной минеральной кислоты. 3. Для диазотирования аминофенолов, которые легко окисляются азотистой кислотой, реакцию проводят с добавлением солей меди, препятствующих окислению амина. 4. Для диазотирования слабоосновных аминов, содержащих одну или несколько нитрогрупп, три- или тетрагалогенанилинов (Hal=Cl,Br), амин растворяют в смеси концентрированных H2SO4 - H3PO4 или H2SO4 - CH3COOH и полученный раствор при охлаждении прибавляют к нитрозилсерной кислоте. Полученный одним из описанных выше методов водный раствор соли диазония сразу используют для дальнейших превращений. Предварительно следует убедиться в полноте протекания диазотирования, т.е. проверить отсутствие в реакционной массе непрореагировавших исходных веществ. При добавлении к порции диазораствора ацетата натрия, снижающего кислотность среды, при наличии исходного амина образуется триазен – нерастворимый в воде оранжевый осадок. Азотистую кислоту обнаруживают с помощью иодкрахмальной бумаги. Избыток азотистой кислоты удаляют добавлением мочевины до прекращения выделения газообразных продуктов из реакционной смеси. 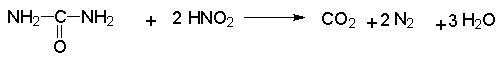 Физические свойства и строение Соли арендиазония – бесцветные кристаллические вещества. Хлориды, гидросульфаты и нитраты хорошо растворимы в воде и используются в основном в виде водных растворов. В твердом виде они неустойчивы и взрываются от трения и от нагревания. Соли арендиазония с некоторыми комплексными анионами (PF6-, SbF6-, BF4-) нерастворимы в воде и достаточно стабильны при хранении их в сухом виде в течение длительного времени. В целом соли арендиазония гораздо устойчивее алифатических аналогов, что обусловлено стабилизирующим влиянием p -системы ароматического ядра, которое участвует в делокализации положительного заряда. 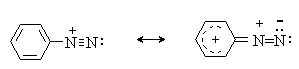 Электронодонорные заместители в о- и п-положениях обеспечивают дополнительную стабилизацию арендиазониевого катиона. 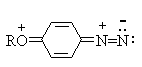 Сама диазониевая группа может быть представлена набором из двух резонансных структур. 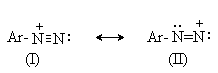 Наибольший вклад в резонанс вносит структура (I). По данным рентгеноструктурного анализа связь азот-азот по длине соответствует тройной (0,11 нм). ИК-спектры содержат полосу поглощения в области 2100-2300 см-1, что соответствует валентным колебания связи Nº N. Второй атом азота несет частичный положительный заряд (структура (II)) и является электрофильным центром в реакциях диазониевых солей. Диазониевая группа является сильнейшим электроноакцептором и превосходит в этом отношении нитрогруппу. Химические свойства 1. Равновесия между различными формами диазосоединений в водных растворах. Образование и строение диазотатов Форма существования диазосоединений в растворе зависит от рН. Катионы диазония могут существовать в кислой среде и в средах, близких к нейтральной. При обработке растворов солей диазония щелочью образуются диазотаты. ArN2+X- + 2NaOH ® Ar-N=N-O- Na+ + NaX + H2O Процесс протекает в две стадии. Сначала катион диазония, как кислота Льюиса, взаимодействует с гидроксид-ионом с образованием диазогидроксида, который, будучи кислотой Бренстеда, быстро реагирует с еще одним эквивалентом щёлочи с образованием диазотат- аниона Для приведенных выше равновесий К2>К1, поэтому концентрация диазогидрата в водном растворе очень мала. Диазотат-анионы существуют в анти- и син-формах. При взаимодействии катиона арендиазония со щелочью первоначально образуется менее стабильный син-диазотат, который медленнно изомеризуются в более стабильную анти-форму. Изомеризацию ускоряет нагревание и присутствие в бензольном кольце электроноакцепторных групп. Обратная изомеризация наблюдается только при УФ облучении. 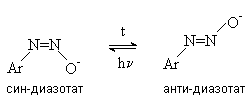 Диазотат-ионы являются амбидентными ионам с двумя нуклеофильными центрами - кислородом и азотом. анти-Диазотат протонируется исключительно по атому азота с образованием N-нитрозоамина. 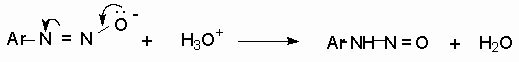 Далее N-нитрозоамин в кислой среде медленно превращается в катион арендиазония, как это было описано ранее в соответствии со стадиями (2 - 6) при обсуждении механизма диазотирования. син-Диазотаты при протонировании образуют диазогидраты в результате протонирования по кислороду. Диазогидрат далее очень быстро превращается в кислой среде в катион арендиазония. 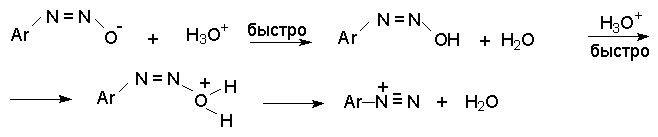 Общую схему протолитических превращений ароматических диазосоединений в водном растворе можно представить следующим образом. 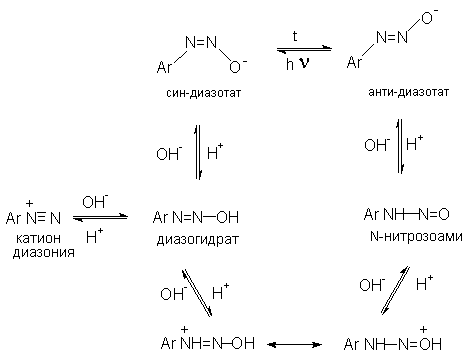 2. Реакции солей арендиазония Все реакции солей диазония можно разделить на четыре большие группы, различающиеся по механизму взаимодействия катиона диазония с нуклеофильным агентом Х-. 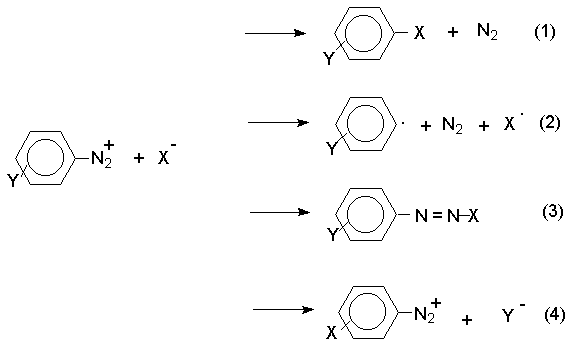 Реакции типа (1) и (4) - нуклеофильное ароматическое замещение. В реакциях группы (1) имеет место замещение самой диазогруппы. В реакциях типа (4) диазогруппа, как очень сильный акцептор, активирует нуклеофильное замещение группы Y в орто- или пара-положении к диазогруппе. В реакциях группы (2) происходит радикальный распад соли диазония. Образующийся при этом арильный радикал Ar претерпевает затем дальнейшее превращение. Третий тип реакций предполагает атаку нуклеофильным агентом крайнего атома азота диазониевого катиона. По формальному признаку реакции солей диазония можно разделить на две большие группы: реакции идущие с выделением (1,2) и без выделения (3,4) азота. Реакции, идущие с выделением азота Замещение диазогруппы – один из основных методов введения заместителей в ароматическое кольцо. Замещение протекает как по гетеролитическому, так и по гомолитическому механизму. Характер разрыва связи углерод-азот в катионе арендиазония зависит прежде всего от природы нуклеофильного агента. Гетеролиз связи С-N имеет место при взаимодействии с жесткими нуклеофильными агентам - водой, фторид-ионом и при проведении реакции в растворителях с электрофильными или малонуклеофильными свойствами. Гомолитическому расщеплению связи углерод-азот благоприятствует рост нуклеофильных свойств растворителя и использование мягких нуклеофильных агентов (J- , SCN-). Все эти анионы относятся к сильным восстановителям, что облегчает перенос одного электрона от реагента к катиону диазония. Эту же функцию в отдельных случаях может выполнять и растворитель. Для многих реакций переход от гетеролитического к гомолитическому механизму происходит очень легко при введении в раствор солей одновалентной меди. а) Замещение диазогруппы на гидроксил. 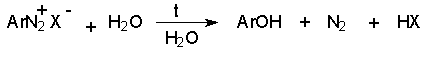 Реакцию обычно проводят путем разложения соли диазония в 40-50 %-ном растворе серной кислоты. Реакция протекает как процесс мономолекулярного ароматического нуклеофильного замещения (SN1). Для получения фенолов используют соли диазония с малонуклеофильными или комплексными анионами (X=HSO4-, BF4-), что избежать образования продуктов арилирования противоиона промежуточно образующимся арилкатионом. Образующийся из Ar+ и HSO4- эфир серной кислоты ArОSO3H в условиях реакции гидролизуется до фенола. Как во всех процессах SN1 - типа стадия, определяющая скорость реакции, и стадия, определяющая состав продуктов реакции, не совпадают. 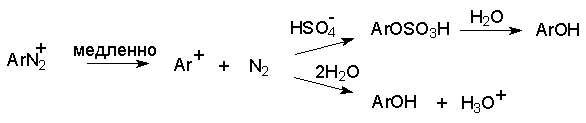 б) Замещение диазогруппы на фтор (реакция Шимана). Замещение диазогруппы на фтор происходит при термическом разложении тетрафторборатов арендиазония. ArN2 +BF4 - ® ArF + N2 + BF3 Реакция протекает, вероятно, через промежуточное образование арилкатиона. Выходы арилфторидов сильно колеблются в зависимости от природы заместителя в бензольном кольце арендиазокатиона. Увеличению выхода способствует наличие в бензольном кольце электронодонорных заместителей. Реакция Шимана – один из основных методов введения фтора в ароматическое кольцо. с) Замещение диазогруппы на иод ArN2 +X - + KI ® ArI + N2 + KX Замещение диазогруппы на йод осуществляется по принципиально иному механизму и представляет собой ион-радикальный процесс, в котором иодид-ион выступает в роли одноэлектронного восстановителя. 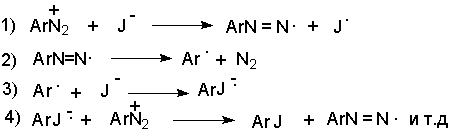 В препаративном отношении это одна из самых простых реакций ароматических диазосоединений. д) Замещение диазогруппы на хлор-, бром-, циан- и нитрогруппу (реакция Зандмейера). Выходы арилхлоридов, арилбромидов и арилцианидов в реакциях солей арендиазония с хлорид-, бромид- и цианид-ионами в отсутствие катализаторов невелики и редко превышают 20%. Для получения этих соединений используют реакцию Т. Зандмейера, который обнаружил, что такое замещение эффективно катализируется солями меди (I). Для введения хлора и брома используют раствор галогенида меди (I) в соответствующей галогеноводородной кислоте. 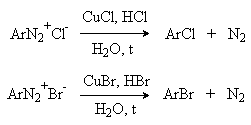 Для введения цианогруппы нейтральный раствор соли диазония смешивают с раствором комплексного цианида. 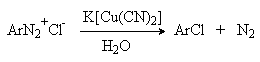 Механизм реакции Зандмейера достоверно не установлен. Считается, что катион меди (I) выступает в роли восстановителя катионов диазония, поскольку сами ионы Cl- и Br- в отличие от иодид-ионов трудно окисляются. Образующиеся при одноэлектронном восстановлении арилрадикалы Ar или арилдиазорадикалы Ar - N = N далее окисляются солью двухвалентной меди. Предполагают, что радикалы образуются и реагируют в реакционном комплексе соль диазония–соль меди и в растворе как кинетически независимые частицы не появляются. Вместо солей меди (I) может использоваться медный порошок (реакция Гаттермана). Метод дает особенно хорошие результаты при замене диазогруппы в тетрафторборатах или гексафторфосфатах арендиазония на нитрогруппу. 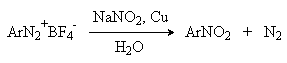 е) Замещение диазогруппы на водород (дезаминирование первичных ароматических аминов). Замещение диазогруппы на водород происходит при действии восстановителей. В качестве восстановителей используют спирты. ArN2+X- + RCH2OH ® ArH + R-CH=O + N2 + HX Реакция протекает по цепному радикальному механизму. Зарождениецепи: ArN2+ + CH3OH ® ArN2. + CH3OH.+ ArN2. ® Ar. + N2 CH3OH. + ®.CH2OH + H+ Развитиецепи : Ar. + CH3OH ® ArH + .CH2OH .CH2OH + ArN2+® ArN2. + CH2OH+ т.е. (H2-C=O+H) CH2OH+ ® H-C(H)=O + H+ ArN2. ® Ar . + N2 и т.д. Параллельно протекает замещение диазозогруппы на алкоксильную. 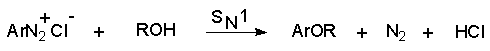 Эта реакция, также как и взаимодействие катиона диазония с водой, протекает по гетеролитическому мономолекулярному механизму. Соотношение продуктов в двух конкурирующих процессах - гетеролитическом и гомолитическом - зависит от природы заместителя в бензольном кольце катиона арендиазония и от рН среды. Протеканию гомолитического процесса восстановления способствует наличие электроноакцепторных заместителей в ароматическом кольце и среда, близкая к нейтральной, в которой доминируют гомолитические процессы разложения ковалентных форм диазосоединений. В общем же случае образуется смесь эфира фенола и углеводорода, поэтому восстановительное дезаминирование осуществляют другими методами. Универсальным восстановителем при замещении диазогруппы на водород является фосфорноватистая кислота H3PO2. |
