Физиология экзамен. Билет 1 Физиология возбудимости ткани потенциал покоя (ПП) и потенциал действия (ПД). Фазы изменения возбудимости. (1602516632620. Физиология возбудимых тканей)
 Скачать 1.1 Mb. Скачать 1.1 Mb.
|
|
БИЛЕТ № 1 1. Физиология возбудимости ткани: потенциал покоя (ПП) и потенциал действия (ПД). Фазы изменения возбудимости. (1602516632620. Физиология возбудимых тканей) Возбудимость– способность клетки переходить из состояния покоя в состояние возбуждения при действии раздражителя. Разные клетки имеют различную возбудимость. Возбудимость одной и той же клетки меняется в зависимости от ее функционального состояния. Физико-химические механизмы возникновения потенциала покоя Потенциал покоя (ПП) — мембранный потенциал возбудимой клетки в невозбужденном состоянии. Он представляет собой разность электрических потенциалов, имеющихся на внутренней и наружной сторонах мембраны и составляет у теплокровных от -55 до -100 мВ. У нейронов и нервных волокон обычно составляет -70 мВ. При возбуждении клетки её мембрана повреждается, и ионы К+ вытекают из клетки по концентрационному градиенту до тех пор, пока потенциал мембраны не становится равным нулю. Затем мембрана восстанавливает свою целостность, и потенциал возвращается к уровню потенциала покоя. ПП формируется в два этапа. Первый этап: создание незначительной (-10 мВ) отрицательности внутри клетки за счёт неравного асимметричного обмена Na+ на K+ в соотношении 3 : 2. В результате этого клетку покидает больше положительных зарядов с натрием, чем возвращается в неё с калием. Такая особенность работы натрий-калиевого насоса, осуществляющего взаимообмен этих ионов через мембрану с затратами энергии АТФ, обеспечивает его электрогенность. Результаты деятельности мембранных ионных насосов-обменников на первом этапе формирования ПП: 1. Дефицит ионов натрия (Na+) в клетке. 2. Избыток ионов калия (K+) в клетке. 3. Появление на мембране слабого электрического потенциала (-10 мВ). Второй этап: создание значительной (-60 мВ) отрицательности внутри клетки за счёт утечки из неё через мембрану ионов K+. Ионы калия K+ покидают клетку и уносят с собой из неё положительные заряды, доводя отрицательность до -70 мВ. Итак, мембранный потенциал покоя - это дефицит положительных электрических зарядов внутри клетки. Обнаружить МПП можно с помощью второго опыта Гальвани, т.е. зарегистрировать ток покоя между поврежденным и неповрежденным участками мембраны. Для измерения потенциала покоя используют микроэлектродную технику. Физико-химические механизмы возникновения потенциала действия Потенциал действия — волна возбуждения, перемещающаяся по мембране живой клетки в процессе передачи нервного сигнала. По сути своей представляет электрический разряд — быстрое кратковременное изменение потенциала на небольшом участке мембраны возбудимой клетки (нейрона, мышечного волокна или железистой клетки), в результате наружная поверхность этого участка становится отрицательно заряженной по отношению к соседним участкам мембраны, тогда как его внутренняя поверхность становится положительно заряженной по отношению к соседним участкам мембраны. Потенциал действия является физической основой нервного или мышечного импульса, играющего сигнальную (регуляторную) роль. Потенциал действия – это быстрое колебание МПП, возникающее при возбуждении нервных, мышечных и секреторных клеток. Фазы потенциала действия: 1. Локальный ответ (местная деполяризация), предшествующий развитию ПД. 2. Фаза деполяризации. Во время этой фазы МП быстро уменьшается и достигает нулевого уровня. Уровень деполяризации растет выше нуля. Поэтому мембрана приобретает противоположный заряд – внутри она становится положительной, а снаружи отрицательной. 3. Фаза реполяризации. Она начинается при достижении определенного уровня МП (примерно +20 мВ). Мембранный потенциал начинает быстро возвращаться к потенциалу покоя. Длительность фазы 3-5 мс. 4. Фаза следовой деполяризации или следового отрицательного потенциала. Период, когда возвращение МП к потенциалу покоя временно задерживается. Он длится 15-30 мс. 5. Фаза следовой гиперполяризации или следового положительного потенциала. В эту фазу МП на некоторое время становится выше исходного уровня ПП. Ее длительность 250-300 мс. Фазы изменения возбудимости 1. Абсолютный рефрактерный период. В этот период ни на какие раздражения извне ткань не отвечает. Продолжительность этого периода, для: - нервного волокна – 1-2 мсек; - мышечного – 4-5 мсек; - мионеврального синапса – 8-10 мсек. 2. Относительный рефрактерный период. В этот период ответные реакции возникают только при воздействии раздражителей выше пороговой силы. 3. Супернормальный период. В этот период ткань отвечает и на низко пороговые раздражения. 4.Субнормальный период. В этот период происходит снижение возбудимости и ткань отвечает на выше пороговые раздражения. 2. Цикл сердечной деятельности, структура сердечного цикла. Систола предсердий, систола желудочков, общая пауза сердца. (физиология сердечной деятельности) Цикл сердечной деятельности включает систолу (греч. systole — сокращение) предсердий, систолу желудочков и общую паузу сердца. Общая пауза - это часть сердечного цикла, когда совпадают по времени диастола (греч. Dyastole - расширение) желудочков с диастолой предсердий. Структура цикла сердечной деятельности Систола предсердий — 0,1 с. Систола желудочков — 0,33 с, она включает: • период изгнания крови — 0,25 с (фаза быстрого изгнания — 0,12 с и фаза медленного изгнания — 0,13 с); • период напряжения — 0,08 с (фаза асинхронного сокращения — 0,05 с и фаза изометрического сокращения — 0,03 с). Общая пауза сердца — 0,37 с, которая включает: • период расслабления желудочков — 0,12 с (протодиастола — 0,04 с и фаза изометрического расслабления — 0,08 с); • период наполнения желудочков кровью — 0,25 с (фаза быстрого наполнения — 0,08 с и фаза медленного наполнения — 0,17 с). Весь цикл сердечной деятельности при частоте сокращений 75 в минуту длится 0,8 с. 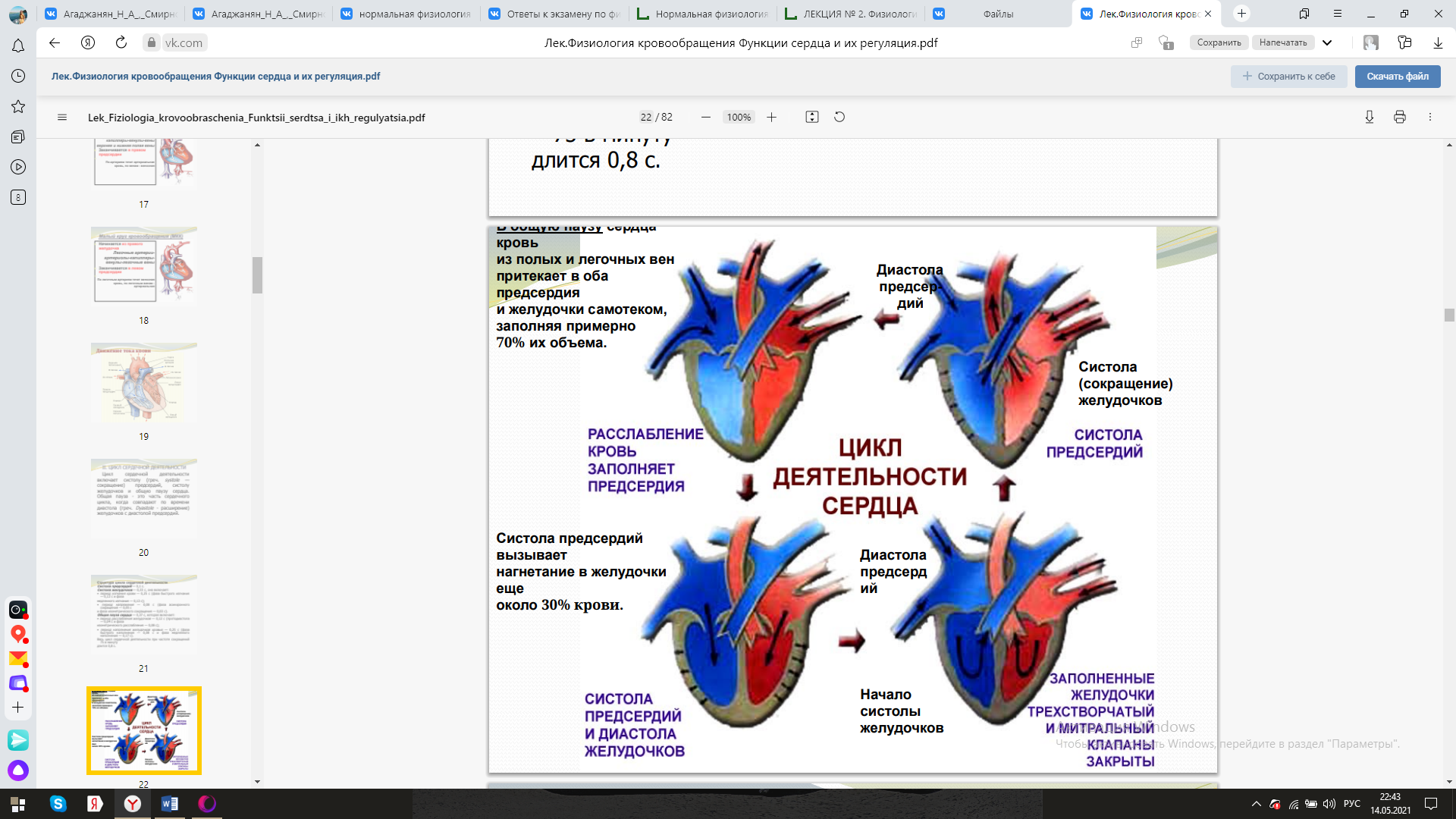 Систола предсердий начинается после общей паузы сердца и обеспечивает дополнительную подачу крови в желудочки. К началу систолы предсердий вся мускулатура предсердий и желудочков расслаблена. Открыты атриовентрикулярные клапаны, они провисают в желудочки, расслаблены сфинктеры, представляющие собой кольцевую мускулатуру в области впадения полых вен в предсердия и выполняющие функцию клапанов. Поскольку весь рабочий миокард расслаблен, давление в полостях сердца равно нулю. Из-за градиента давления в полостях сердца и в артериальной системе полулунные клапаны закрыты. Возбуждение предсердий начинается в области впадения полых вен, поэтому одновременно с сокращением рабочего миокарда предсердий сокращается мускулатура сфинктеров в области устьев впадающих в сердце вен: они закрываются, давление в предсердиях начинает расти, и дополнительная порция крови поступает в желудочки. К концу систолы предсердий давление в левом предсердии возрастает до 10–12 мм рт. ст., в правом — до 4–8 мм рт. ст. Такое же давление к концу систолы предсердий создается и в желудочках. Вслед за систолой предсердий происходит их диастола, которая длится 0,7 с. Предсердия при этом наполняются кровью (резервуарная функция предсердий), поскольку расслаблены также и сфинктеры предсердий. Через 0,007 с (интерсистолический интервал) после окончания систолы предсердий начинается систола желудочков. Систола желудочков обеспечивает выброс крови в артериальную систему. Общая пауза сердца начинается с протодиастолы. Она продолжается от начала расслабления мышц желудочков до закрытия полулунных клапанов. Давление в желудочках становится несколько ниже, чем в аорте и легочной артерии, поэтому полулунные клапаны закрываются. БИЛЕТ №2 1. Физиология нервных волокон, механизм проведения возбудимости по нервному волокну. Физиологические свойства нервных волокон: 1) возбудимость – способность приходить в состояние возбуждения в ответ на раздражение; 2) проводимость – способность передавать нервные возбуждение в виде потенциала действия от места раздражения по всей длине; 3) рефрактерность (устойчивость) – свойство временно резко снижать возбудимость в процессе возбуждения. Нервная ткань имеет самый короткий рефрактерный период. Значение рефрактерности – предохранять ткань от перевозбуждения, осуществляет ответную реакцию на биологически значимый раздражитель; 4) лабильность – способность реагировать на раздражение с определенной скоростью. Лабильность характеризуется максимальным числом импульсов возбуждения за определенный период времени (1 с) в точном соответствии с ритмом наносимых раздражений. Нервные волокна не являются самостоятельными структурными элементами нервной ткани, они представляют собой комплексное образование, включающее следующие элементы: 1) отростки нервных клеток – осевые цилиндры; 2) глиальные клетки; 3) соединительнотканную (базальную) пластинку. Главная функция нервных волокон – проведение нервных импульсов. Отростки нервных клеток проводят сами нервные импульсы, а глиальные клетки способствуют этому проведению. По особенностям строения и функциям нервные волокна подразделяются на два вида: безмиелиновые и миелиновые. Безмиелиновые нервные волокна не имеют миелиновой оболочки. Их диаметр 5–7 мкм, скорость проведения импульса 1–2 м/с. Миелиновые волокна состоят из осевого цилиндра, покрытого миелиновой оболочкой, образованной шванновскими клетками. Осевой цилиндр имеет мембрану и оксоплазму. Миелиновая оболочка состоит на 80 % из липидов, обладающих высоким омическим сопротивлением, и на 20 % из белка. Миелиновая оболочка не покрывает сплошь осевой цилиндр, а прерывается и оставляет открытыми участки осевого цилиндра, которые называются узловыми перехватами (перехваты Ранвье). Длина участков между перехватами различна и зависит от толщины нервного волокна: чем оно толще, тем длиннее расстояние между перехватами. При диаметре 12–20 мкм скорость проведения возбуждения составляет 70—120 м/с. В зависимости от скорости проведения возбуждения нервные волокна делятся на три типа: А, В, С. Наибольшей скорость проведения возбуждения обладают волокна типа А, скорость проведения возбуждения которых достигает 120 м/с, В имеет скорость от 3 до 14 м/с, С – от 0,5 до 2 м/с. Не следует смешивать понятия «нервное волокно» и «нерв». Нерв – комплексное образование, состоящее из нервного волокна (миелинового или безмиелинового), рыхлой волокнистой соединительной ткани, образующей оболочку нерва. Механизм проведения возбуждения по нервным волокнам зависит от их типа. Существуют два типа нервных волокон: миелиновые и безмиелиновые. Процессы метаболизма в безмиелиновых волокнах не обеспечивают быструю компенсацию расхода энергии. Распространение возбуждения будет идти с постепенным затуханием – с декрементом. Декрементное поведение возбуждения характерно для низкоорганизованной нервной системы. Возбуждение распространяется за счет малых круговых токов, которые возникают внутрь волокна или в окружающую его жидкость. Между возбужденными и невозбужденными участками возникает разность потенциалов, которая способствует возникновению круговых токов. Ток будет распространяться от «+» заряда к «—». В месте выхода кругового тока повышается проницаемость плазматической мембраны для ионов Na, в результате чего происходит деполяризация мембраны. Между вновь возбужденным участком и соседним невозбужденным вновь возникает разность потенциалов, что приводит к возникновению круговых токов. Возбуждение постепенно охватывает соседние участки осевого цилиндра и так распространяется до конца аксона. В миелиновых волокнах благодаря совершенству метаболизма возбуждение проходит, не затухая, без декремента. За счет большого радиуса нервного волокна, обусловленного миелиновой оболочкой, электрический ток может входить и выходить из волокна только в области перехвата. При нанесения раздражения возникает деполяризация в области перехвата А, соседний перехват В в это время поляризован. Между перехватами возникает разность потенциалов, и появляются круговые токи. За счет круговых токов возбуждаются другие перехваты, при этом возбуждение распространяется сальтаторно, скачкообразно от одного перехвата к другому. Сальтаторный способ распространения возбуждения экономичен, и скорость распространения возбуждения гораздо выше (70—120 м/с), чем по безмиелиновым нервным волокнам (0,5–2 м/с). 2. Особенности возбудимости, проводимости и сократимости сердечной мышцы и ее энергитического обеспечения. Сердечная мышца, как и всякая другая мышца, обладает рядом физиологических свойств: возбудимостью, проводимостью, и сократимость (рефрактерностью и автоматией). Возбудимость — это способность кардиомиоцитов и всей сердечной мышцы возбуждается при действии на нее механических, химических, электрических и других раздражителей, что находит свое применение в случаях внезапной остановки сердца. Особенностью возбудимости сердечной мышцы является то, что она подчиняется закону “все — или ничего”. Это значит, что на слабый, до пороговой силы раздражитель сердечная мышца не отвечает, (т.е. не возбуждается и не сокращается) (“ничего”), а на раздражитель пороговой, достаточной для возбуждения силы сердечная мышца реагирует своим максимальным сокращением (“все”) и при дальнейшем увеличении силы раздражения ответная реакция со стороны сердца не изменяется. Это связано с особенностями строения миокарда и быстрым распространением по нему возбуждения через вставочные диски — нексусы и анастомозы мышечных волокон. Таким образом, сила сердечных сокращений в отличие от скелетных мышц не зависит от силы раздражения. Однако этот закон, открытый Боудичем, в значительной степени условен, так как на проявление данного феномена влияют определенные условия — температура, степень утомления, растяжимость мышц и ряд других факторов. Проводимость — это способность сердца проводить возбуждение. Скорость проведения возбуждения в рабочем миокарде разных отделов сердца неодинакова. По миокарду предсердий возбуждение распространяется со скоростью 0,8-1 м/с, по миокарду желудочков — 0,8-0,9 м/с. В атриовентрикулярной области на участке длиной и шириной в 1 мм проведение возбуждения замедляется до 0,02-0,05 м/с, что почти в 20-50 раз медленнее, чем в предсердиях. В результате этой задержки возбуждение желудочков начинается на 0,12-0,18 с позже начала возбуждения предсердий. Существует несколько гипотез, объясняющих механизм атриовентрикулярной задержки, но этот вопрос требует своего дальнейшего изучения. Однако эта задержка имеет большой биологический смысл — она обеспечивает согласованную работу предсердий и желудочков. Сократимость. Сократимость сердечной мышцы имеет свои особенности. Сила сердечных сокращений зависит от исходной длины мышечных волокон (закон Франка–Старлинга). Чем больше притекает к сердцу крови, тем более будут растянуты его волокна и тем большая будет сила сердечных сокращений. Это имеет большое приспособительное значение, обеспечивающее более полное опорожнение полостей сердца от крови, что поддерживает равновесие количества притекающей к сердцу, и оттекающей от него крови. Здоровое сердце уже при небольшом растяжении отвечает усиленным сокращением, в то время как слабое сердце даже при значительном растяжении лишь немного увеличивает силу своего сокращения, а отток крови осуществляется за счет учащения ритма сокращений сердца. Кроме того, если по каким–либо причинам произошло чрезмерное сверх физиолочески допустимых границ растяжение сердечных волокон, то сила последующих сокращений уже не увеличивается, а ослабляется. Сила и частота сердечных сокращений меняется и под действием различных нервно–гуморальных факторов без изменения длины мышечных волокон. Особенностями сократительной деятельности миокарда является то, что для поддержания этой способности необходим кальций. В безкальциевой среде сердце не сокращается. Поставщиком энергии для сокращений сердца являются макроэргические соединения (АТФ и КФ). В сердечной мышце энергия (в отличие от скелетных мышц) выделяется, главным образом, в аэробную фазу, поэтому механическая активность миокарда линейно связана со скоростью поглощения кислорода. При недостатке кислорода (гипоксемия) активируются анаэробные процессы энергетики, но они только частично компенсируют недостающую энергию. Недостаток кислорода отрицательно влияет и на содержание в миокарде АТФ и КФ. В сердечной мышце, имеется так называемая атипическая ткань, образующая проводящую систему сердца Эта ткань имеет более тонкие миофибриллы с меньшей поперечной исчерченностью. Атипические миоциты более богаты саркоплазмой. Ткань проводящей системы сердца более возбудима и обладает резко выраженной способностью к проведению возбуждения. В некоторых местах миоциты этой ткани образуют скопления или узлы. Первый узел располагается под эпикардом в стенке правого предсердия, вблизи впадения полых вен — синоатриальный узел. Особенности энергетического обеспечения сердечной мышцы Главным источником энергии для сердца является процесс аэробного окисления. Анаэробное окисление (анаэробный гликолиз) для сердца в отличие от скелетной мышцы играет незначительную роль. Потенциальными носителями энергии являются главным образом неуглеводные субстраты. Это свободные жирные кислоты и молочная кислота (около 60 %), пировиноградная кислота, кетоновые тела и аминокислоты (менее 10 %). Только около 30 % расходуемой сердцем энергии покрывается за счет глюкозы; при физической нагрузке увеличивается энергетическая доля жирных и молочной кислот при одновременном снижении энергетической доли глюкозы. Таким образом, сердце утилизирует недо-окисленные продукты, накапливающиеся в результате интенсивной мышечной работы, и тем самым препятствует закислению внутренней среды организма. Большая зависимость деятельности сердечной мышцы от аэробного окисления делает сердце весьма зависимым от поступления кислорода к кардиомиоцитам. Сердце массой 300 г потребляет около 30 мл О2 в минуту, что составляет 10—12 % от общего количества потребляемого организмом кислорода в покое (масса сердца составляет 0,5 % от массы тела). На 1 кг массы весь организм потребляет около 4 мл О2 в 1 мин, а сердце — около 100 мл, т.е. в 25 раз больше. Скелетная мышца может некоторое время работать вообще без кислорода (в долг) за счет гликолиза. Коэффициент полезного действия сердца в среднем составляет около 30 %, т.е. несколько больше, нежели скелетной мышцы, — 20—25 %. При ухудшении коронарного кровотока и недостаточном поступлении кислорода к сердечной мышце в ней могут развиваться патологические процессы, вплоть до инфаркта. Однако это случается относительно редко благодаря миоглобину, имеющемуся в сердечной мышце в количестве около 4 мг/г ткани. Он обладает большим сродством к О2, запасает его во время диастолы и покоя сердца и отдает во время систолы, когда кровоток в коронарных артериях желудочков прекращается: 1 г миоглобина связывает 1,34 мл О2, что составляет 0,005 мл на 1 г ткани. Этого количества кислорода хватает для работы сердца в течение 3—4 с (в норме систола желудочков длится 0,3 с). Даже в случае кратковременного спазма коронарных сосудов, например, при сильных отрицательных эмоциях кислород, связанный с миоглобином, смягчает трудную для сердца ситуацию. БИЛЕТ№3 1. Физиология нервно-мышечного синапса: структурно-функциональная организация, механизм и характеристика синаптической передачи в химических синапсах. (Физиология ЦНС) Синапс (греч. synapsis — соединение) — это специализированная структура, обеспечивающая передачу сигнала от клетки к клетке. Посредством синапса реализуется действие многих фармакологических препаратов. Структурно-функциональная организация. Каждый синапс имеет пре- и постсинаптическую мембраны и синаптическую щель (рис. 17). 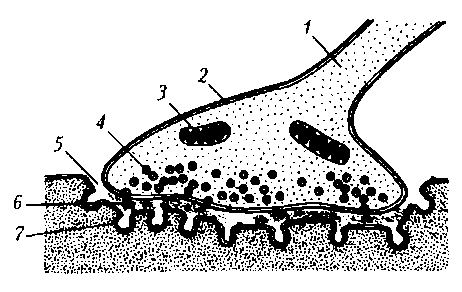 Рис. 17. Нервно-мышечный синапс скелетной мышцы: 1 – ветвь аксона; 2 – пресинаптическое окончание аксона; 3 – митохондрия; 4 – синаптические пузырьки, содержащие ацетилхолин; 5 – синаптическая щель; 6 – молекулы медиатора в синаптической щели; 7 – постсинаптическая мембрана мышечного волокна с N-холинорецепторами Пресинаптическая мембрана нервно-мышечного синапса представляет собой часть мембраны пресинаптического окончания аксона мотонейрона. Через нее осуществляется выброс (экзоцитоз) медиатора (лат. mediator — посредник) в синаптическую щель. В нервно-мышечном синапсе медиатором является ацетилхолин. Медиатор пресинаптического окончания содержится в синаптических пузырьках (везикулах), диаметр которых составляет около 40 нм. Они образуются в комплексе Гольджи, с помощью быстрого аксонного транспорта доставляются в пресинаптическое окончание, где заполняются медиатором и АТФ. В пресинаптическом окончании содержится несколько тысяч везикул, в каждой из которых имеется от 1 тыс. до 10 тыс. молекул химического вещества. Постсинаптическая мембрана (концевая пластинка в нервно-мышечном синапсе) — это часть клеточной мембраны иннервируемой мышечной клетки, содержащая рецепторы, способные связывать молекулы ацетилхолина. Особенность этой мембраны: множества мелких складок, увеличивающих ее площадь и количество рецепторов на ней до 10—20 млн в одном синапсе. Синаптическая щель в нервно-мышечном синапсе имеет ширину в среднем 50 нм. Она содержит межклеточную жидкость, ацетилхолинэстеразу и мукополисахаридное плотное вещество в виде полосок, мостиков, в совокупности образующих базальную мембрану, соединяющую пре- и постсинаптическую мембраны. Механизмы синаптической передачи включают три основных этапа (рис. 18). 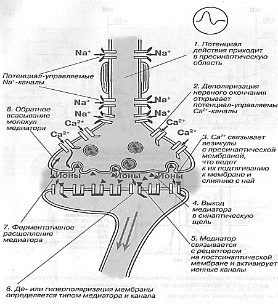 Рис. 18. Механизм проведения импульса через химический синапс: 1-8 – этапы процесса (Чеснокова, 2007) Первый этап — процесс выброса медиатора в синаптическую щель, который запускается посредством ПД пресинаптического окончания. Деполяризация его мембраны ведет к открытию потенциалуправляемых Са-каналов. Са2+ входит в нервное окончание согласно электрохимическому градиенту. Часть медиатора в пресинаптическом окончании локализуется на пресинаптической мембране изнутри. Са2+ активирует экзоцитозный аппарат пресинапса, представляющий собой совокупность белков (синапсин, спектрин и др.), пресинаптического окончания, активация которых обеспечивает выброс ацетилхолина посредством экзоцитоза в синаптическую щель. Количество высвобождаемого ацетилхолина из пресинаптического окончания пропорционально в четвертой степени количеству поступившего туда Са2+. На один ПД из пресинаптического окончания нервно-мышечного синапса выбрасывается 200—300 квантов (везикул) медиатора. Второй этап — диффузия ацетилхолина в течение 0,1—0,2 мс к постсинаптической мембране и действие его на N-холинорецепторы (стимулируются также никотином, вследствие чего и получили свое название). Удаление ацетилхолина из синаптической щели осуществляется путем разрушения его под действием ацетилхолинэстеразы, расположенной в базальной мембране синаптической щели, в течение нескольких десятых долей миллисекунды. Около 60% холина захватывается обратно пресинаптическим окончанием, что делает синтез медиатора более экономичным, часть ацетилхолина рассеивается. В промежутках между ПД из пресинаптического окончания происходит спонтанное выделение 1— 2 квантов медиатора в синаптическую щель в течение 1 с, формируя так называемые миниатюрные потенциалы (0,4—0,8 мВ). Они поддерживают высокую возбудимость иннервируемой клетки в условиях функционального покоя и выполняют трофическую роль, а в ЦНС — способствуют поддержанию тонуса ее центров. Третий этап — взаимодействие ацетилхолина с N-холинорецепторами постсинаптической мембраны, в результате чего открываются ионные каналы на 1 мс и, вследствие преобладания входа N+ в клетку, происходит деполяризация постсинаптичедкой мембраны (концевой пластинки). Эту деполяризацию в нервно-мышечном синапсе называют потенциалом концевой пластинки (ПКП) (рис. 19). Особенностью нервно-мышечного синапса скелетного мышечного волокна является то, что при одиночной его активации формируется ПКП большой амплитуды (30—40 мВ), электрическое поле которого вызывает генерацию ПД на мембране мышечного волокна вблизи синапса. Большая амплитуда ПКП обусловлена тем, что нервные окончания делятся на многочисленные веточки, каждая из которых выбрасывает медиатор. Характеристика проведения возбуждения в химических синапсах. Одностороннее проведение возбуждения от нервного волокна к нервной или эффекторной клетке, так как пресинаптическое окончание чувствительно только к нервному импульсу, а постсинаптическая мембрана — к медиатору. Неизолированное — возбуждение рядом расположенных постсинаптических мембран суммируется. Синаптическая задержка в передаче сигнала к другой клетке (в нервно-мышечном синапсе 0,5-1,0 мс), что связано с высвобождением медиатора из нервного окончания диффузией его к постсинаптической мембране и возникновением постсинаптических потенциалов, способных вызвать ПД. Декрементность (затухание) возбуждения в химических синапсах при недостаточном выделении медиатора из пресинаптических окончаний в синаптические щели. Низкая лабильность (в нервно-мышечном синапсе составляет 100 Гц), которая в 4 - 8 раз ниже лабильности нервного волокна. Это объясняется синаптической задержкой. Проводимость нервно-мышечного синапса (как и химических синапсов ЦНС) угнетается или, наоборот, стимулируется различными веществами. Например, кураре и курареподобные вещества (диплацин, тубокурарин) обратимо связываются с N-холинорецепторами постсинаптической мембраны, блокируют действие на нее ацетилхолина и передачу в синапсе. Напротив, некоторые фармакологические препараты, например прозерин, подавляют активность ацетилхолинэстеразы, способствуя умеренному накоплению ацетилхолина и облегчению синаптической передачи, что используется в лечебной практике. Утомляемость (синаптическая депрессия) — ухудшение проводимости вплоть до полной блокады проведения возбуждения при длительном функционировании синапса (главная причина — истощение медиатора в пресинаптическом окончании). 2. Автоматия сердца, проводящая система сердца, механизм автоматии, градиент автоматии. (физиология сердечной деятельности) Сердечной мышце свойственны возбудимость, проводимость, сократимость и автоматия. Особое свойство – автоматия– это способность сердца к самопроизвольным сокращениям, без внешних раздражителей. Причиной, вызывающей автоматию, являются изменения обмена веществ, происходящие в самом органе. В сердце есть 4 водителя ритма. I порядка – сино – атриальный узел, в устье полых вен, ЧСС – 60 – 80 ударов в минуту. II порядка – атрио – вентрикулярный узел – 40 – 50 ударов в минуту. III порядка – ножки пучка Гисса – 30 – 40 ударов в минуту. IV порядка – волокна Пуркинье – 20 ударов в минуту. Снижение способности к автоматии от основания к верхушке называется убывающим градиентом автоматии. От положения водителя ритма зависит ЧСС. Градиент автоматии – это уменьшение способности к автоматии по мере удаления от синоатриального узла, то есть от места непосредственной генерализации импульсов. Наиболее высокой способностью к автоматии обладает синусно-предсердный узел, где генерируется ритм, который усваивается остальными элементами проводящей системы и сократительным миокардом. У человека он равен 60-70 уд/мин в состоянии покоя. Если работа синусно-предсердного узла нарушена, функция водителя ритма переходит к предсердно-желудочковому узлу, который генерирует более медленный сердечный ритм (около 40 уд/мин), но он в состоянии обеспечить нормальную работу сердца и нормальное кровоснабжение организма. Другие элементы проводящей системы, и в первую очередь пучок Гиса, также способны к автоматии, но генерируемое здесь возбуждение возникает с еще более низкой частотой и проявляется только в условиях патологии, например при гипоксии и ишемии. В этих условиях ненормальные очаги автоматии могут формироваться и в сократительных клетках сердца, создавая источники аритмии сердца. Нарушение автоматии. В норме – 60 – 80 уд/мин. (у новорожденных до 140). Патология – синусовая тахикардия 90 100 уд/мин. синусовая брадикардия 40 – 50 уд/мин. (у спортсменов это норма) Наибольшей способностью к автоматии обладает водитель ритма нормального сердца - синоатриальный узел. Автоматия обнаружена в волокнах, близких по структуре к волокнам синоатриального узла, расположенных вблизи него в предсердиях. Эти волокна обладают несколько меньшей способностью к автоматии, чем клетки синоатриального узла. Их называют скрытыми водителями ритма. Автоматия свойственна также атриовентрикулярному узлу. Синоатриальный узел называют центром автоматии первого порядка, атриовентрикулярный узел — центром автоматии второго порядка. Анатомическим субстратом автоматии являются мышечные клетки в проводящей системе сердца. Для выяснения природы автоматии проводились различные исследования, в результате которых была установлена характерная особенность пейсмекерных клеток. Эта особенность состояла в том, что в промежутке между двумя систолами (в диастолу), в автоматически возбуждающейся пейсмекерной клетке происходило постепенное уменьшение мембранного потенциала (разности потенциалов между протоплазмой и внешней поверхностью клетки). Для того, чтобы в клетке вновь возникло возбуждение, мембранный потенциал должен был уменьшиться на 20-30 мВ. Чем быстрее во время диастолы достигалось такое уменьшение мембранного потенциала, тем чаще возникало возбуждение клетки-водителя ритма, и тем чаще происходило сокращение сердца. В проводящей системе сердца выделяют узлы и пути: 1. синоатриальный узел. Он расположен в устье полых вен, т.е. в венозных синусах; 2. межузловые и межпредсердные проводящие пути. Проходят по миокарду предсердий и межпредсердной перегородке; 3. атриовентрикулярный узел. Находится в нижней части межпредсердной перегородки под эндокардом правого предсердия; 4. пучок Гиса. Идет от атриовентрикулярного узла по верхней части межжелудочковой перегородки. Затем делится на две ножки – правую и левую. Они образуют ветви в миокарде желудочков; 5. волокна Пуркине. Это концевые разветвления ветвей ножек пучка Гиса. Образуют контакты с клетками сократительного миокарда желудочков. Чем дальше центр автоматии сердца расположен от его венозного конца и ближе к артериальному, тем меньше его способность к автоматии-принцип убывающего градиента автоматии. БИЛЕТ№4 1. Назначение и структурные элементы скелетной мышцы. Механизм сокращения скелетной мышцы, виды мышечных сокращений. Показатели физической деятельности мышц. (Физиология мышечной ткани) Основным элементом скелетной мышцы является мышечная клетка. В связи с тем, что мышечная клетка по отношению к своему поперечному сечению (0,05-0,11мм) относительно длинна (волокна бицепса, например, имеют длину до 15 см), ее называют также мышечным волокном. Скелетная мышца состоит из большого количества этих структурных элементов, составляющих 85-90% от ее общей массы. Так, например, в состав бицепса входит более одного миллиона волокон. Между мышечными волокнами расположена тонкая сеть мелких кровеносных сосудов (капилляров) и нервов (приблизительно 10% от общей массы мышцы). От 10 до 50 мышечных волокон соединяются в пучок. Пучки мышечных волокон и образуют скелетную мышцу. Мышечные волокна, пучки мышечных волокон и мышцы окутаны соединительной тканью. Мышечные волокна на своих концах переходят в сухожилия. Через сухожилия, прикрепленные к костям, мышечная сила воздействует на кости скелета. Сухожилия и другие эластичные элементы мышцы обладают, кроме того, и упругими свойствами. При высокой и резкой внутренней нагрузке (сила мышечной тяги) или при сильном и внезапном внешнем силовом воздействии эластичные элементы мышцы растягиваются и тем самым смягчают силовые воздействия, распределяя их в течение более продолжительного промежутка времени. Поэтому после хорошей разминки в мускулатуре редко происходят разрывы мышечных волокон и отрывы от костей. Сухожилия обладают значительно большим пределом прочности на растяжение (около 7000 Н/кв см), чем мышечная ткань (около 60 Н/кв см), где Н – ньютон, поэтому они гораздо тоньше, чем брюшко мышцы. В мышечном волокне содержится основное вещество, называемое саркоплазмой. В аркоплазме находятся митохондрии (30-35% от массы волокна), в которых протекают процессы обмена веществ и накапливаются вещества, богатые энергией, например фосфаты, гликоген и жиры. В саркоплазму погружены тонкие мышечные нити (миофибриллы), лежащие параллельно длинной оси мышечного волокна. Миофибриллы составляют в совокупности приблизительно 50% массы волокна, их длина равна длине мышечных волокон, и они являются, собственно говоря, сократительными элементами мышцы. Они состоят из небольших, последовательно включаемых элементарных блоков, именуемых саркомерами Так как длина саркомера в состоянии покоя равна приблизительно лишь 0,0002 мм, то для того, чтобы, к примеру, образовать цепочки из звеньев миофибрилл бицепса длиной 10-15 см, необходимо "соединить" огромное количество саркомеров. Толщина мышечных волокон зависит главным образом от количества и поперечного сечения миофибрилл. В миофибриллах скелетных мышц наблюдается правильное чередование более светлых и более темных участков. Поэтому часто скелетные мышцы называют поперечнополосатыми. Миофибрилла состоит из одинаковых повторяющихся элементов, так называемых саркомеров. Саркомер ограничен с двух сторон Z-дисками. К этим дискам с обеих сторон прикрепляются тонкие актиновые нити. Нити актина обладают низкой плотностью и поэтому под микроскопом кажутся более прозрачными или более светлыми. Эти прозрачные, светлые области, располагающиеся с обеих сторон от Z-диска, получили название изотропных зон (или I-зон). В середине саркомера располагается система толстых нитей, построенных преимущественно из другого сократительного белка, миозина. Эта часть саркомера обладает большей плотностью и образует более темную анизотропную зону (или А-зону). В ходе сокращения миозин становится способным взаимодействовать с актином и начинает тянуть нити актина к центру саркомера. Вследствие такого движения уменьшается длина каждого саркомера и всей мышцы в целом. Важно отметить, что при такой системе генерации движения, получившей название системы скользящих нитей, не изменяется длина нитей (ни нитей актина, ни нитей миозина). Укорочение является следствием лишь перемещения нитей друг относительно друга. Сигналом для начала мышечного сокращения является повышение концентрации Са 2+ внутри клетки. Концентрация кальция в клетке регулируется с помощью специальных кальциевых насосов, встроенных в наружную мембрану и мембраны саркоплазматического ретикулума, который оплетает миофибриллы. Механизм сокращения скелетной мышцы После генерации ПД в мышечном волокне вблизи синапса возбуждение распространяется по мембране миоцита в обе стороны, в том числе по мембранам поперечных Т-трубочек. Механизм проведения ПД по мышечному волокну такой же, как и по безмиелиновому нервному волокну, — возникший ПД вблизи синапса посредством своего электрического поля обеспечивает возникновение новых ПД в соседнем участке волокна и т.д. (непрерывное проведение возбуждения). ПД Т-трубочек за счет своего электрического поля активирует электроуправляемые кальциевые каналы мембраны СПР, вследствие чего Са2+ выходит из цистерн СПР согласно электрохимическому градиенту. В межфибриллярном пространстве Са2+ контактирует с тропонином, что приводит к его конформации и смещению тропомиозина, в результате чего на нитях актина обнажаются активные участки, с которыми соединяются головки миозиновых мостиков. В результате взаимодействия с актином АТФазная активность головок миозиновых нитей усиливается, обеспечивая высвобождение энергии АТФ, которая расходуется на сгибание миозинового мостика, внешне напоминающего движение весел при гребле (гребковое движение) обеспечивающее скольжение актиновых нитей относительно миозиновых. После этого головки поперечных мостиков в силу своей эластичности возвращаются в исходное положение и устанавливают контакт со следующим участком актина; далее вновь происходит очередное гребковое движение и скольжение актиновых и миозиновых нитей. Подобные элементарные акты многократно повторяются. Виды мышечных сокращений (в зависимости от характера сокращений) Ауксотоническое сокращение мышцы встречается чаще других и заключается в одновременном изменении длины и напряжения мышцы. Этот вид сокращения характерен для натуральных двигательных актов и бывает двух видов: эксцентрическое, когда напряжение мышцы сопровождается ее удлинением — например, в процессе приседания (опускания), и концентрическое, когда напряжение мышцы сопровождается ее укорочением — например, при разгибании нижних конечностей после приседания (подъем). Изометрическое сокращение мышцы — когда напряжение мышцы возрастает, а длина ее не изменяется. Этот вид сокращения можно наблюдать в эксперименте, когда оба конца мышцы зафиксированы и отсутствует возможность их сближения, и в естественных условиях — например, в процессе приседания и фиксации положения. Изотоническое сокращение мышцы — заключается в укорочении мышцы при ее постоянном напряжении; возникает, когда сокращается ненагруженная мышца с одним закрепленным сухожилием, не поднимая (не перемещая) никакого внешнего груза либо поднимая груз без ускорения. Виды мышечных сокращений (в зависимости от длительности сокращений) Одиночное и тетаническое. Одиночное сокращение мышцы — возникает при однократном раздражении нерва или самой мышцы. Обычно мышца укорачивается на 5–10% от исходной длины. Три основных периода: 1) латентный — время от момента нанесения раздражения до начала сокращения; 2) период укорочения (или развития напряжения); 3) период расслабления. Тетаническое сокращение — это длительное сокращение мышцы, возникающее под действием ритмического раздражения, когда каждое последующее раздражение или нервные импульсы поступают к мышце, пока она еще не расслабилась. В основе тетанического сокращения лежит явление суммации одиночных мышечных сокращений — увеличение амплитуды и длительности сокращения при нанесении на мышечное волокно или целую мышцу двух и более быстро следующих друг за другом раздражений. |
