Цель работы ознакомление с физическими основами спектрального анализа и приобретение навыков работы с простейшим спектральным прибором. Основные сведения о спектрах
 Скачать 290.68 Kb. Скачать 290.68 Kb.
|
|
Цель работы - ознакомление с физическими основами спектрального анализа и приобретение навыков работы с простейшим спектральным прибором. 1. ОСНОВНЫЕ СВЕДЕНИЯ О СПЕКТРАХ При анализе физических явлений приходится использовать идсализированные модели, передающие не все свойства реальных объектов, а только те из них, которые существенны в рассматриваемом круге вопросов. К ним относится широкоиспользуемая в оптике плоская монохроматическая волна (ПМВ). Таких волн в действительности не существует. Математически ПМВ описывается как простейшая периодическая функция координаты и времени:  Реальный волновой процесс ограничен во времени и в пространстве в отличие от ПМВ, которая задана при всех значениях аргументов (х,t). Однако часто встречаются ситуации, в анализе которых важно учесть только факт наличия пространственно-временной периодичности некоторой физической величины. Практическая выгода от использования ПМВ основана на возможности представить любой волновой процесс как результат сложения (суперпозицию) некоторого количества ПМВ с надлежащим образом подобранными амплитудами и частотами. Совокупность амплитуд и частот слагаемых, из которых состоит волна, называется спектром. Оптическим спектром (в узком смысле слова) иногда называют цветные полосы, получающиеся в результате разложения волны призмой (или другим прибором) по длине волн. Спектральный анализ. Виды спектров Спектральный анализ - совокупность методов определения количественного и качественного состава вещества, основанная на изучении его спектров испускания и поглощения. Количественный спектральный анализ определяет концентрации химических элементов, содержащихся в исследуемом образце. Качественный спектральный анализ предназначен для выяснения химического состава вещества. Атомы каждого химического элемента имеют присуший только им набор позможных стационарных знергстических состояний, При перехоле из одного состояния в другос атом излучаст или поглошает квант систа, энергия которого определястся разностью энергий атома начальном 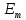 , и конечном состоянии , и конечном состоянии 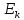 : : где h - постоянная Планка; v - частота излучения. Каждому возможному переходу соответствует линия в спектре. Количество линий в спектре атома очень велико и может достигать десятков тысяч. Следовательно, возможно случайное совнадение некоторых линий в спектрах различных атомов, поэтому спектральный анализ следует проводить по нескольким наиболее интенсивным линиям. Совпадение длин волн этих линий с табличными значениями надежно указывает на присутствие элемента в источнике излучения. Различают непрерывные, линейчатые и полосатые спектры. Все вещества в газообразном состоянии дают линейчатые спектры. В этом случае свет излучают атомы, которые практически не взаимодействуют друг с другом. Изолированные атомы испускают излучение строго определенных длин волн. Обычно для наблюдения линейчатых спектров используют свечение паров вещества в пламени или свечение газового разряда в трубке, наполненной исследуемым газом. Слабосвязанные друг с другом молекулы жидкости дают спектр, состоящий из большого числа близко расположенных линий, которые группируются в отдельные полосы. Такие спектры называются полосатыми. Раскаленные твердые тела, а также сильно сжатые газы дают сплошной спектр, состоящий из всехспектральных цветов, непрерывно переходящих друг в друга. Спектр поглощения можно получить, если на пути излучения, имеющего сплошной спектр, поместить вещество, которое само не излучает свет, но поглощает излучение определенных длин волн. Спектр погло-шения обнаруживается по появлению темных линий или темных полос нафоне сплошного спектра источника света. Можно сказать, что спектр поглощения это зависимость способности вещества поглощать свет от длины волны. Спектры поглощения, как и спектры излучения, могут быть сплошными, полосатыми и линейчатыми. Оптические спектры неодима В работе исследуются спектры поглощения неодимового стекла и раствора NdCl2. Неодим принадлежит к редкоземельным элементам. Внешняя часть электронных оболочек в группе редкоземельных элементов почти одинакова, Этим объясняется схожесть их химических свойств. Электроны с наименьней энергией связи принадлежат внутрсиней лостраивающейся 4f-оболочке, которая защищена от висшних возлействий завершенными подслоями 5s, 5p и 6s. Оптические спектры группы редкоземельных элементов получаются именно за счет возбуждения этих наименес прочно связанных электронов, поэтому спектры поглошсния атомов Nd в растворе их солей, а также в твердом теле в искоторой мерс сохраняют свою дискретную структуру, похожую на структуру спсктров этих атомов в газе. В спектрах других элементов в тех же условиях дискретность не сохраняется и могут сильно различаться уровни энергии. Поглощение излучения водным раствором двухромовокислого калия K2Cr2O7 Некоторые твердые и жидкие вещества поглощают падающее на них излучение в очень широком диапазоне ллин волн, сильно меняя его спектральный состав. Именно таким свойством обладают широко использусмыс светофильтры. Примером жидкого светофильтра может служить водный раствор двухромовокислого калия K-Cr2O1. Он пропускает излучение только в желто-красной области спектра, полностью поглощая синефиолетовую область. Объясняется это явление следующим образом. Молекулы K2Cr2O7 в воде диссоциируют, образуя ионы К+ и Cr2O-27: 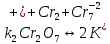 Квант света, ссли его энергия достаточна, поглощается и вызывает расщепление иона 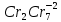 , на ионы , на ионы 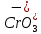 , и , и 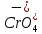 : :Минимальную энергию кванта, расщепляющего ион 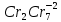 , можно считать равной энергии связи ∆Е ионов , можно считать равной энергии связи ∆Е ионов 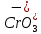 , и , и 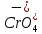 : :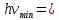 ∆Е ∆Еоткуда получаем максимальную длину волны излучения, поглощаемого раствором: 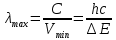 Все излучение с Amax полностью поглощается, что приводит к появлению темной области с границей Аmах в спектре поглощения на фоне сплошного излучения лампы. 2. УСТРОЙСТВО СПЕКТРАЛЬНОГО ПРИБОРА Назначение спектральных приборов - исследовать спсктральный состав излучения, т. с. определить, из каких ПМВ оно состоит. Действие спектральных приборов основано на том, что в искоторых физических системах условия прохождения света разной длины волны оказываются различными. Принципиальная схема простейшего спектрального прибора показана на рис. 1. 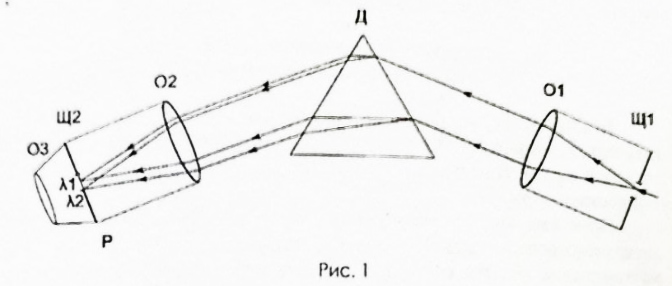 Рис. 1 Рис. 1Входная щель Щ1, на которую падает исследуемое излучение, находится в фокальной плоскости линзы О1. Эта часть прибора называется коллиматором. Выходящий из линзы параллельный пучок света падает на призму Д. Вследствие дисперсии в веществе призмы свет разных длин волн выходит из призмы под разными углами. Линза О2 фокусирует па раллельные пучки лучей, и в результате образуются изображения входной щели в разных местах фокальной плоскости для разных длин волн. В фокальной плоскости линзы О2, помещается регистратор спектра Р. Если спектр регистрирустся визуально, как в данном приборе через окуляр О3, то прибор называется спектроскопом, если с помощью фотопластинки - спектрографом. Чтобы получить монохроматический свет, на месте регистратора ставят выходную щель Щ2. В этом случае прибор называется монохроматором. Приборы, в которых оптические спектры регистрируются с помощью фотоэлектрических приемников излучения, называются спектрофотометрами. Идеальный прибор при падении монохроматического излучения давал бы на выходе единственную бесконечно узкую спектральную линию. Однако в реальном приборе получается некоторое распределение освещенности, характеризуемое контуром определенной формы. Этот контур имеет конечную ширину, что ограничиваст способность прибора разделять две близко расположенные спектральные линии. барабана N) всех видимых линий спектра испускания начиная с красного цвета. 5. Данные занести в табл. 1. 6. Выключить тумблер «Сеть», снять источник излучения 1 с оптической скамьи. 7. Используя таблицу, построить градуировочный график (график ависимости N( λ)). 8. Поставить на оптическую скамью источник излучения 2 – лампу накаливания, включить ес в сеть. 9. Вращая барабан монохроматора 12, исследовать визуально спектр испускания. Сравнить спектры испускания, полученные от этих двух исочников излучения. Сделать выводы.  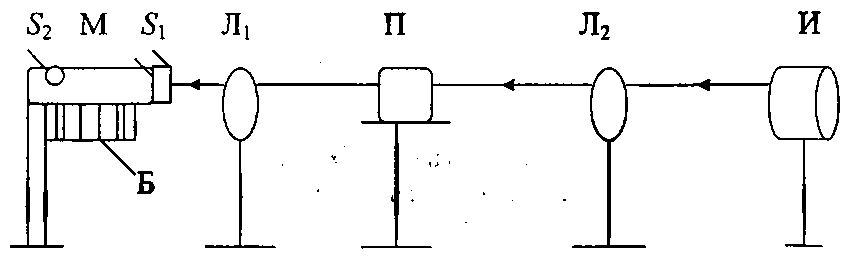 Рис. 2. Монохроматор: 1 - окуляр; 2 - призма; 3 - поворотный столик; 4 - шкала фокусировки объектива; 5 - тумблер «Сеть»; 6 - кнопка «Пуск»; 7 - тумблер «Вкл, лампа ДРШ»; 8 - блок питания; 9 - барабан установки ширины входной щели; 10 – затвор коллиматора; 11 - маховичок фокусировки обьектива; 12 - барабан поворота столика с отсчетными делениями угла поворота; 13 - указатель делений Таблица 1
Исследование спектров поглощения 1. Получить у лаборанта исследусмыс образцы. Поместить между источником излучения 2 и входной щелью раствор NdCl2. 2. Убедиться, что излучение попадает на входную шель. 3. Вращая барабан монохроматора 12, сделать по шкале отсчеты N положения центральной, наиболее темной части каждой полосы. Повторить измерения при вращении барабана в противоположную сторону. Усреднить полученные значения. 4. По градуировочному графику найти соответствующие длины волн. 5. По формуле v рассчитать частоты. 6. Данные измерений и вычислений занести в табл. 2. 7. Заменить раствор NdCl2 на неодимовое стекло и повторить исследование (п. 2-6). 9. Сравнить спектры поглощения для неодимового стекла и раствора NdCl2 по значениям длин волн и ширине линий поглощения. Сделать выводы. Таблица 2
Погрешность ∆ λ находится с помощью градуировочного графика N(λ) по абсолютной погрешности отсчета с шкалы барабана. Считая отно сительные погрешности и ∆ λ / λ одинаковыми, найти абсолютную по-грешность ∆ λv. Определение постоянной Планка 1. Поместить между источником света 2 (лампой накаливания) и щелью кювету с водным раствором двухромовокислого калия. 2. Сделать по шкале отечет N границы поглошасмой области спектра. Измерения провести пять раз. Результат усреднить. 3. Данные занести в табл. 3. 4. По градуировочному графику найти длину волны дату, соответствующую границе поглощаемой области спектра. Полученное значение занести в таблицу. 5. Пользуясь формулой (1), вычислить постоянную Планка h. Значсние ∆ Е = 2,292 эВ. 6. Оценить абсолютные погрешности и 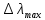 и ∆h. и ∆h.7. Полученное значение h сравнить с табличным значением. Таблица 3
Контрольные вопросы 1. Что такое спектр? 2. Почему различаются спектры различных химических элементов? 3. Какие виды спектров существуют? 4. Объясните принцип работы спектральных приборов. 5. Каковы цели спектрального анализа вещества? 6. Как получить спектр поглощения? 7. В чем сходство и различие спектров излучения и поглощения? | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

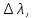 Дж’с
Дж’с