Материальный баланс получения карбида кальция. 25 вариант переделанный. Cодержание Введение 3 Исходные данные 4
 Скачать 182.2 Kb. Скачать 182.2 Kb.
|
|
89248923422- егор Cодержание Введение 3 1.Исходные данные 4 2.Обзор вариантов промышленного получения карбида кальция 5 3.Сырье, используемое в производстве 8 4. Технологическая схема производства 11 5. Оборудование для производства карбида кальция13 6. Химические процессы и реакции 14 7. Продукты производства 15 8. Составление материального баланса производства 16 9. Расчет основных технических показателей 19 Заключение 22 Список использованных источников 23 Введение Любое промышленное производство можно представить как технологическую схему, т.е. совокупность аппаратов, машин и других устройств, а также материальных, энергетических и других потоков между ними, функционирующих как единое целое и предназначенных для переработки исходных веществ (сырья) в продукцию. Исходными веществами для промышленных продуктов является сырье, полупродукты и вторичное сырье. Подготовка сырья включает в себя его предварительную обработку, затем подготовленное сырье проходит ряд превращений, в результате чего образуется необходимый продукт производства. Целью курсовой работы является рассмотрение технологии производства карбида кальция сплавлением обожженной извести с антрацитом. Для этого были сформулированы следующие задачи: 1. описать схему синтеза карбида кальция 2. рассмотреть сырье, используемое в производстве, а также промежуточные продукты; 3. составить материальный баланс изучаемого производства; 4. рассчитать основные технические показатели производства (расходные коэффициенты, степень конверсии, выход продукта по сырью). 1. Исходные данные 1. Производительность установки по уксусному ангидриду: 3500 т/год; 2. Число рабочих дней в году: 340 дней; 3. Концентрация углерода в антраците (остальное сера): 99%; 4.Выделение газа на 1 т. карбида (считая на объем при н.у.): 250 м3; 5. Потеря известняка (от его веса): 3%. 2. Обзор вариантов промышленного получения карбида кальция сплавлением обожженной извести с антрацитом. Один из способов производства карбида кальция основан на введении в электродуговую печь исходной шихты, состоящей из извести и углеродсодержащего материала в виде кокса или антрацита, и плавлении шихты электрической дугой. Получаемый при плавке шихты оксикарбидный расплав удаляют из печи в изложницы или в охлаждаемый барабан путем выпуска струей. Исходную шихту вводят в печь в виде кусков размерами в пределах 20-60 мм. Содержание карбида кальция в продукте составляет 70-85 мас.%. Недостатком способа является малая интенсивность взаимодействия извести и углерода по реакции СaO + 3C = CaC2 + CO. Существует усовершенствованный способ получения карбида кальция. Способ заключается во введении в электродуговую печь исходной шихты, состоящей из извести и углеродсодержащего продукта, например в виде кокса, угля и тому подобного продукта, плавлении исходной шихты с последующей кристаллизацией полученного оксикарбидного расплава путем выпуска струи расплава в изложницу или охлаждаемый барабан. При этом кусковую шихту дробят, рассеивают по размерам и крупные куски (размером 10-40 мм) вводят на колошник печи, а более мелкую крошку вдувают через полый электрод. Недостатком способа так же является низкая интенсивность реакций синтеза карбида кальция, поскольку основная часть вводимой исходной шихты крупно-кусковая, что обусловливает низкую реакционную способность шихты в целом. Для современных печей производительность единицы в плавильной поверхности печи, определяемая отношением производительности печи к площади поперечного сечения ванны, составляет от 200 до 380 кг/ч/м2. Это преимущественно определяет производительность промышленных печей. В настоящее время, в промышленной технологии производства карбида кальция расплав выпускают из печи в охлаждаемый барабан или в изложницы, что приводит к потере литража продукта. В первом случае потери литража карбида кальция составляют от 5 до 30 л/кг, во втором - от 2 до 3 л/кг в зависимости от содержания СаС2 в карбиде. Это происходит за счет контакта расплава и кристаллического материала с воздухом при его выпуске и охлаждении и протекания следующих реакций: 2CaC2 + 5O2 = 2CaO + 4CO2, (1) СaC2 + 2H2O = Ca(OH)2 + C2H2,(2) 2 CaC2 + 6CO2 = 2CaO + 10 CO.(3) При выпуске расплава в барабан образующиеся гранулы имеют большую поверхность контакта с воздухом и большие потери литража. В результате снижается выход годного продукта. Экономическим результатом отмеченных недостатков является необходимость увеличения габаритов печей для достижения требуемого выпуска продукции, что ведет к высоким капитальным затратам. Интенсификация синтеза получения карбида кальция и повышения выхода годного продукта достигается тем, что в известном способе получения карбида кальция в электропечь вводится шихта. Она состоит из извести и углеродсодержащего продукта. Для плавления шихты и кристаллизации оксикарбидного расплава, в качестве электрической печи используют индукционную печь с охлаждаемым металлическим тиглем. В тигле нагревают получаемый оксикарбидный расплав в электромагнитном поле индуктора, а шихту вводят в тигель в виде мелкодисперсного порошка с размерами частиц менее 3 мм, при этом толщину слоя шихты на колошнике печи поддерживают в пределах 5-60 мм, а кристаллизацию оксикарбидного расплава осуществляют непосредственно в тигле.[4] Применение индукционной печи с охлаждаемым металлическим тиглем обеспечивает равномерный нагрев ванны оксикарбидного расплава по всему объему и интенсивное перемешивание расплава. Тем самым весь объем ванны расплава становится реакционной зоной и достигается высокий тепловой поток к исходной шихте по всему зеркалу расплава. Введение в печь мелкодисперсной шихты, имеющей развитую поверхность, приводит к высокой скорости реакций синтеза, которые происходят вблизи и на зеркале ванны расплава. Высокие значения теплового потока от расплава к шихте и отсутствие местных перегревов расплава обеспечивают послойное поступление шихты в реакционную зону. В свою очередь, это обеспечивает равномерное протекание реакций синтеза по всему зеркалу ванны расплава и равномерное поглощение теплоты от расплава, что препятствует его перегреву.[7] Таким образом, взаимно обусловленные процессы в совокупности обеспечивают повышение интенсивности протекания реакций синтеза карбида кальция. При расплавлении в печи шихты образуется оксикарбидный расплав, который одновременно выполняет две функции: является средой для преобразования электромагнитной энергии индуктора в тепловую и реакционной зоной протекания реакций синтеза карбида кальция. Поступающая на поверхность расплава мелкодисперсная шихта под воздействием отходящих газов образует квазикипящий слой на колошнике печи, обеспечивая широкий и равномерный фронт плавления и синтеза. При этом нижние слои шихты постепенно переходят в расплав, а верхние защищают от потери энергии на излучение. Нагрев расплава осуществляется равномерно по всему объему ванны, что достигается благодаря применению индукционного способа нагрева и интенсивному перемешиванию расплава. [12] 3. Сырье, используемое в производстве Окси́д ка́льция (окись кальция, негашёная и́звесть) — белое кристаллическое вещество, формула CaO. Негашёная известь и продукт её взаимодействия с водой — Ca(OH)2 (гашёная известь, или «пушонка») находят обширное использование в строительном деле. До второй половины XX века известь широко использовали в качестве строительной побелки — прокаленный мел или известняк (оксид кальция) при смешивании с водой образует ярко-белую гашеную известь (Ca(OH)2), обладающую хорошими адгезионными свойствами к различным поверхностям. Далее известь медленно поглощает из воздуха углекислый газ, покрываясь коркой карбоната кальция. В настоящее время известковый раствор при строительстве жилых домов практически не применяется в виду значительной гигроскопичности (склонности поддерживать высокую влажность, провоцирующую рост плесени) и сложности производства работ, уступив место более эффективным материалам.[14] В лабораторной практике оксид кальция используется как дешевый и эффективный агент для осушения растворителей и жидких веществ. В пищевой промышленности зарегистрирован в качестве пищевой добавки E-529. В промышленности водный раствор используют в одном из способов удаления диоксида серы из дымовых газов. В результате реакции гашеной извести Са(OH)2 и диоксида серы получается осадок сульфита кальция СаSO3. В настоящее время вытеснен современными абсорберами на основе четвертичных аммонийных соединений, способных обратимо связывать SO2 и CO2.[10] Использовался в «саморазогревающейся» посуде. Оксид кальция, помещенный между двух стенок емкости, при прокалывании капсулы с водой реагирует с ней с выделением тепла. Промышленным способом получения данного вещества является термическое разложение известняка (кальция карбоната): CaCO3 = CaO + CO2 (4) Также кальция оксид можно получить посредством взаимодействия простых веществ: 2Ca + O2 = 2CaO (5) Третий способ получения оксида кальция заключается в термическом разложении кальция гидроксида (Ca(OH)2) и кальциевых солей нескольких кислородсодержащих кислот: 2Ca(NO3)2 = 2CaO + 4NO2 + O2 (6) Антрацит. Наибольшее количество антрацита образовалось в результате регионального метаморфизма при погружении угленосных толщ в область повышенных температур и давлений. Температура при формировании антрацита в условиях регионального метаморфизма находилась в интервале 350–550°С, что, наряду с изменением давления, особенностями исходного материала и другими причинами, привело к образованию антрацита с различными свойствами. В зависимости от содержания углерода и по своему технологическому применению антрацит также принято подразделять на следующие градации: стандартное качество (SG); высокое качество (HG) сверхвысокое качество (UHG). Таблица 1― Классификационные свойства антрацита 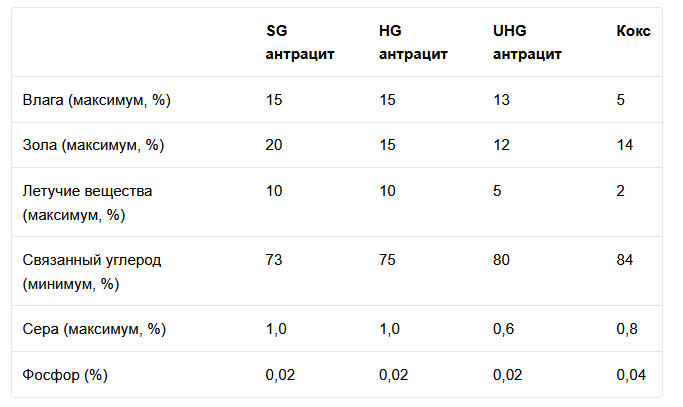 Общие запасы антрацита составляют 1 % от мировых запасов угля (по данным 2006 года). Антрацит залегает в пластах разной мощности обычно на средней и малой глубинах, в отложениях многих геологических систем. По объёму запасов (по состоянию на 2009 г.) Россия находится на 1 месте, за ней следуют Китай, Украина и Вьетнам. Крупнейший производитель антрацита — Китай, другие значимые производители — Северная Корея (в основном для внутреннего потребления), Россия, Украина, Вьетнам, Польша, Англия, Австралия, США.[13] До 1980-х годов антрацит относительно редко употребляли для технологических целей, в основном же антрацит разновидности standard grade использовался как топливо в энергетике, на транспорте и в быту. В настоящее время антрацит, помимо использования в энергетике, применяется для чёрной и цветной металлургии, а также для производства адсорбентов, электродов, электрокорунда, микрофонного порошка.[11] Антрациты UHG используются в качестве заменителя кокса и коксовой мелочи (в составе смеси с коксом) в доменных печах при пылеугольном вдувании (PCI), в производстве агломератов железной руды, железорудного окатыша, электродов. Требования к качеству антрацита по сравнению с топливно-энергетическим использованием являются наиболее высокими. Даже сравнительно небольшое ухудшение некоторых свойств антрацита часто отрицательно влияет на качество промышленной продукции. Согласно принятым в России и СНГ межгосударственным стандартам на угли и антрациты, (классификация по генетическим и технологическим параметрам), антрациты используются в производстве водяного газа, термоантрацита, карбида кальция, электрокорунда, в пылевидном сжигании, слоевом сжигании в стационарных котловых установках и кипящем слое, топках судов, паровозов, для коммунальных и бытовых нужд, производстве извести, цемента, в агломерации руд, производстве электродов.[8] 4. Технологическая система производства Чистый карбид кальция плавится при 2433 К (2160 ?С), следовательно, теоретическая температура начала реакции при рСО равном 100 кПа ниже температуры его плавления. Поскольку в системе СаО-СаС2 образуется эвтектика и растворы, то электропечной технический карбид кальция представляет собой закристаллизованный расплав, содержащий более 80 % СаС2 и 10-15 % СаО. Примеси, содержащиеся в извести, и зола кокса являются источником поступления в карбид нежелательных оксидов (не более 2 % Al2O3, не более 2 % SiO2). При подготовке шихты к плавке известь должна содержать 92-95 % СаО и 1-2 % СО2. Содержание твердого углерода в коксе 85-89 %, а влажность не более 1 %, поэтому кокс следует сушить. Известь применяют крупностью 8-40 мм, а кокс 8-25 мм [12]. Электропечи для выплавки карбида кальция. На современных заводах карбид кальция выплавляют, в рудовосстановительных электропечах с круглой и прямоугольной ваннами единичной мощностью 60 МВ•А. В результате реконструкции мощность может, достигнуть, 80 МВ•А. Ванна печи укрыта водоохлаждаемыми элементами. Вокруг каждого электрода в укрытии ванны имеются щели (воронки) шириной 300 мм для подачи шихты. Межэлектродное пространство перекрывается газоулавливающими воронками, позволяющими улавливать до 80 % колошникового газа. На 1 т карбида кальция выделяется 250-330 м3 газа. Запыленность газа составляет 100-150 мг/м3. Газ подвергают очистке. На очистку 1000 м3 газа расходуется 2,7-3,5 м3 воды. Жидкий карбид кальция выпускается через летку в водоохлаждаемые барабаны. В настоящее время разработаны устройства для автоматического регулирования мощности печи, скорости питания ванны шихтой, положением электродов печи. Разработаны программы, алгоритм и схемы управления процессом выплавки карбида кальция. Компьютерная схема рассчитывает и поддерживает оптимальную температуру процесса при помощи регулирования положения электродов, подаваемой мощности, а также управления подачей извести и коксика и их соотношением. Шихта подается в измельченном виде через полый электрод в реакционную зону при помощи газаносителя. Такая система управления позволяет получать карбид кальция с большим содержанием СаС2 на единицу расходуемой извести [12]. 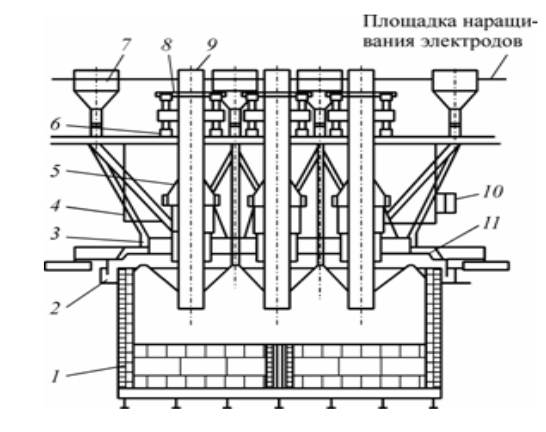 Рис. 1― Закрытая карбидная печь с прямоугольной ванной 1 – ванна; 2 – затвор сухой; 3 – сальник сухой; 4 – зонт; 5 – электрододержатель; 6 – механизм перемещения электродов; 7 – тракт шихтоподачи; 8 – механизм перепуска; 9 – электроды; 10 – короткая сеть; 11 –укрытие 5 Оборудование для производства карбида кальция Процесс получения карбида кальция проводят в мощных руднотермических печах непрерывного действия прямого нагрева. В таких печах электрическая энергия преобразуется в тепловую непосредственно в нагреваемом материале. Электроэнергия вводится в реакционное пространство с помощью электродов, сама реакционная зона является электрическим проводником, доля электрической дуги при этом довольно мала, не превышает 10–20% от полной мощности печи. Печи для производства карбида кальция подразделяются по конструктивным особенностям: – по форме ванны: круглые, прямоугольные и круглые со скошенной передней стенкой; – по состоянию колошника: открытые, частично укрытые и закрытые; ―по типу электродов: печи с круглыми электродами и печи с плоскими электродами; – по расположению электродов: печи с линейным расположением электродов и печи с расположением электродов по углам треугольника. На рисунке 1 представлена конструктивная схема закрытой прямоугольной печи. Основными узлами любого типа карбидной печи являются: ванна, электроды, электрододержатель, механизм перепуска электродов, короткая сеть, тракт шихтоподачи, узлы слива расплавов, зонт. Закрытые карбидные печи имеют, кроме того, дополнительный узел – укрытие с соответствующими элементами.[13] Использование закрытых печей предпочтительно, с точки зрения обеспечения безопасных условий работы персонала и экологической безопасности. 6. Химические процессы и реакции Процесс получения исходного материала (шихты) для производства карбида кальция идет в две стадии: сначала проводят пиролиз при 400-800°С, а затем кальцинирование при 1000-1300°С образовавшегося на первой стадии продукта, представляющего собой смесь оксида кальция и пиролизного кокса. После охлаждения до 500°С мелкие фракции (менее 3 мм) смеси карбида кальция с коксом отделяют, а крупные (более 3 мм) подают в закрытую карбидную печь как исходный материал для получения карбида кальция. Полученный карбид кальция содержит СаС2. [7] Кроме того, в среде, создаваемой в трубчатой печи, будет в качестве восстановителя образовываться сажа - вещество с пониженной активностью как восстановитель в системе взаимодействия СаО:С, а на второй стадии - прокаливание смеси оксида кальция и пиролизного кокса при температуре 1000-1300°С - будет происходить графитизация углерода, то есть снижение его восстановительной активности в процессе получения карбида кальция, что отрицательно скажется на интенсивности процесса.[8] 7. Продукты производства Карбид кальция (CaC2) представляет собой твердое кристаллическое вещество. Химически чистый карбид кальция бесцветен, цвет технического продукта, содержащего 20-25% примесей (в основном – негашеной извести), изменяется от светло-бурого до черного. Температура плавления карбида кальция равняется 2160°C, температура его кипения – 2300°C, плотность – 2,2 г/см3. Вещество бурно реагирует с водой, с разбавленными минеральными кислотами и водными растворами щелочей с выделением ацетилена и значительного количества тепла (127,3 кДж/моль). С водородом (Н2) выше 2200°C карбид кальция образует ацетилен и СаН2, с азотом (N2) и аммиаком (NH3) при нагревании – цианамид (CaCN2). Окисляется на воздухе выше 700°C, взаимодействует с хлором (Cl2) и хлористым водородом (HCl) выше 250°C. [11] Карбид кальция – сильный восстановитель, восстанавливает при нагревании почти все оксиды металлов до карбидов или свободных металлов. По степени воздействия на организм карбид кальция относится к веществам 1-гокласса опасности. Получают карбид кальция преимущественно восстановлением негашеной извести (СаО) углеродом (антрацитом, коксом) в специальных карбидных электрических дуговых печах при температуре 2000 2300ºС по эндотермической реакции. Технический карбид кальция широко применяют в технике, главным образом для промышленного производства ацетилена и продуктов его переработки, а так же цианамида кальция, из которого получают удобрения, цианистые соединения. Кроме того, его используют для восстановления металлов, снижения содержания кислорода (раскисления) и серы (десульфурации) стали, для получения карбидно-карбамидного регулятора роста растений, изготовления порошкового карбидного реагента, при проведении автогенных работ и для освещения (ацетиленовые горелки).[14] 8. Составление материального баланса Материальный баланс рассчитывается на основании химических реакций, описываемых формулами: 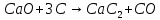 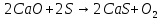 Расчеты материальных балансов технологических процессов, в результате которых происходит химическое превращение веществ, ведутся, учитывая основные стехиометрические законы (закон постоянства состава и закон кратных отношений). Эти законы выражают собой взаимное отношение атомов и молекул веществ при их химическом взаимодействии друг с другом.    М4   М5 М1   М6  M2 M2    М7 M3  М8  М1-СaO расход M2-антрацит расход М3-S примеси M4-СO M5-O2 М6-- CaC2 продукт М7-CaS побочный продукт М8-потери СаО Рис.7―Материальные потоки производства. Производительность установки составляет 3500 т/год, что равно соответственно 428,92 кг/ч следовательно М6=428,92 кг/ч Зная, что на выходе в реакционной смеси содержится в весовых процентах: антрацита 99%, серы 1% найдем: 428,92 кг/ч-99% Х-1% Следовательно, М3-4,33 кг/ч По уравнению химической реакции (1) находим количество антрацита, Пошедшего на образование карбида кальция 36 кг/моль—64 кг/кмоль Х—428,92 кг/ч Х—241,27 кг/ч Следовательно М2—241,27 кг/ч По уравнению химической реакции (1) находим количество СаО, пошедшего на образование карбида кальция 56кг/кмоль—64 кг/кмоль Х--428,92 кг/ч Х—375,305 кг/ч По уравнению химической реакции (2) находим количество СаО, пошедшего на образование сульфида кальция 112 кг/кмоль – 64 кг/кмоль х кг/ч—4,33 кг/ч Х—7,5775 кг/ч СаО: 7,5775 кг/ч+375,305 кг/ч=383 кг/ч Находим потери СаО 394,1375 кг/ч—97% Х—3% Х-12,19 кг/ч Следовательно М8=12,19 кг/ч Найдем массу кислорода 112 кг/кмоль—32 кг/кмоль 7,5775 кг/ч—х кг/ч Х—2,165 кг/ч Следовательно М5—2,165 кг/ч По уравнению химической реакции (2) находим количество СаS 112 кг/кмоль –144 кг/кмоль 7,5775 кг/ч—хкг/ч Х—9,7425 кг/ч Следовательно М7—9,7425 кг/ч Посчитаем массу выделившихся газов 64—28 428,92—х Х-187,6525 М4=187,6525 64—32 4,33—х Следовательно М5=2,165 кг/ч Таблица 7.1 Типовая таблица материального баланса
9. Расчет основных технических показателей Расчет основных технических показателей 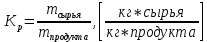 1) Для обоженной извести: 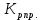 = 395,13/428,92= 0,92 = 395,13/428,92= 0,92 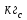 / / 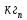 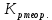 = 375,305 /428,92= 0,875 = 375,305 /428,92= 0,875 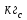 / /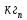 2) Для антрацита: 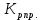 = 241,27/428,92=0,56 = 241,27/428,92=0,56 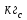 / /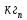 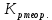 = 245,6 /428,92= 0,57 = 245,6 /428,92= 0,57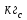 / /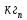 Реальный выход продукта составляет: из 395,13 кг обожженной извести –428,92 кг карбида кальция из 245,6 кг антрацита –428,92 кг карбида кальция. Выход продукта, как показатель эффективности: Потери обожженной извести + сырье на побочную реакцию [1] 12,19+7,5775=19,7675 кг/ч 19,7675 кг/ч- 56 кг/кмоль Х- 64 кг/кмоль Х=22,59 кг/кмоль 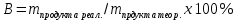 B=428,92/428,92+22,59 х 100%= 95% Степень конверсии рассчитывается как отношение количества переработанного сырья к исходному количеству сырья [1]: 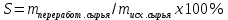 S=383/395,13х 100%=97% для обожженной извести S= 241,27/245,6=0,98 или 98% для антрацита Заключение В курсовой работе было рассмотрено производство карбида кальция из гашенной извести и антрацита, описаны технологическая схемы и сырье, используемое в производстве синтеза карбида кальция. Получение карбида кальция из обоженную известь является наиболее целесообразным, поэтому данная методика применяется многими компаниями. Следует отметить высокую степень конверсии сырья. Метод создаѐт экологические проблемы, так как синтез происходит при высоких температурах. В настоящее время ведутся поиски решения этой проблемы посредством модернизации оборудования. Кроме того, был составлен материальный баланс изученного производства и рассчитаны основные технические показатели эффективности производства (расходные коэффициенты, степень конверсии, выход продукта по сырью). Список использованных источников 1. Бесков В.С. Общая химическая технология и промышленная экология. Учебник для ВУЗов. – М.: ИКЦ «Академкнига», 2005 2. «Общая химическая технология». В 2-х томах под ред. акад. Вольфковича С. И. – М.: Госхимиздат,1952 – 1959. 3. Вольфкович С.И. Общая химическая технология. Т1, Т2 – М.: Химия, 1966 4. Казарновский С. Н., Козлов В. Н. «Альбом технологических схем процессов основного органического синтеза». – Горький: 1958. – 123 с. 5. Плановский А.Н., Рамм В.М. Процессы и аппараты химической технологии. – М.: Химия, 1968 – 846 с. 6. Глинка Н.Л. «Общая химия», М.: Химия, 1974. – 720 с. 7. Иванов Г.Н. «МЕТОДИЧЕСКИЕ УКАЗАНИЯ к курсовой работе по дисциплине «Промышленная экология»» Тверь 2008 . 8. Бесков С. Д. «Технологические расчеты» - М.: Высшая школа, 1962.-468 с. 9. Файшщкий М.З. Вероятностные модели определения параметров руднотермических печей. Л.: ЛенНИИГипрохим, 1977. - 28 с. 10. Сергеев П.В. Энергетические закономерности руднотермических печей, электролиза и электрической дуги. Алма-Ата: Изд-во АН КазССР, 1963. -248 с. 11. Платонов Г.Ф. Параметры и электрические режимы металлургических электродных печей. -М.-Л.: Энергия, 1965. 50 с. 12. Савицкий С.К. Анализ взаимосвязи основных параметров фосфорной печи при статическом режиме. // Процессы и аппараты производства фосфора. / Сб. научн. тр. ЛенНИИГипрохим. Л., 1980. - С. 69-76. 13. Ершов В.А. Зависимость напряжения с низкой стороны трансформатора руднотермической печи от технологических параметров: Проблемы рудной электротермии. // Сб. труд, научн.-технич. совещания «Электротермия-96». СПб.: СПбГТИ (ТУ), 1996. - С. 163. 14. Ефреймович Ю.Е. Оптимальные электрические режимы дуговых сталеплавильных печей. -М.: Металлургиздат, 1956. 76 с. |
