Фарм. Экспрессанализ
 Скачать 29.9 Kb. Скачать 29.9 Kb.
|
|
Экспресс-анализ В общей единой системе государственного контроля за качеством лекарств в нашей стране большая роль принадлежит внутриаптечному контролю качества лекарств, который осуществляется непосредственно в аптеках. Процент готовых лекарственных форм в аптеках в настоящее время составляет 85%, остальные 15% составляют экстемпоральную рецептуру, которая должна подвергаться анализу. До 15% лекарств, входящих в готовые лекарственные формы, составляют внутриаптечные заготовки, которые также должны подвергаться анализу. Среди экстемпоральной рецептуры 20-25% составляют глазные капли. Большой процент (70-80%) составляют инъекционные растворы, которые должны подвергаться обязательно не только качественному, но и количественному анализу. Таким образом, объем работы аналитических кабинетов аптек чрезвычайно большой и, если учесть, что в нашей стране все без исключения лекарства, изготовленные в аптеке, должны подвергаться различным видам контроля, естественно, что необходимым условием анализа лекарств в аптеке является быстрота выполнение анализа, в связи с этим методы анализа должны быть просты, не требовать сложного оборудования, затрата лекарства и реактивов должна быть минимальной (0,5-2 мл жидкой лекарственной формы или 0,05-0,1 г порошка), чтобы отпадала необходимость в повторном изготовлении лекарства. Этим требованиям отвечает химический экспресс-анализ, который среди других видов внутриаптечного контроля заминает ведущее место. Качественный экспресс-анализ проводится капельным методом в маленькой фарфоровой чашечке, на предметном стекле или фильтровальной бумаге. Фильтровальную бумагу кладут на стекло, капилляр набирают раствор исследуемого вещества и, прикладывая его к фильтровальной бумаге, выпускают из него жидкость. Из другого, более крупного капилляра в центр на образовавшееся пятно исследуемого вещества выпускают соответствующий реактив, в результате на фильтрованной бумаге появляется окраска (продукт взаимодействия исследуемого вещества с реактивом). При использовании крепких кислот и щелочей реакции рекомендуется проводить на предметном стекле, так как крепкие кислоты и щелочи разрушают бумагу. Часто для качественных реакций используют реактивные бумажки, пропитанные соответствующими реактивами и высушенные. Например, реактивные бумажки, пропитанные раствором сульфата меди, служат для идентификации сульфаниламидных препаратов, карбоновых кислот, барбитуратов. Количественный экспресс-анализ выполняется с применением объемных методов исследования, отличающих необходимой точностью, простотой и быстротой выполнения. При анализе порошков из приготовленной порошковой массы отвешивают на ручных весах 0,05-0,1 г с таким расчетом, чтобы на титрование ушло 1-2 мл титрованного раствора. При анализе жидкостей к 1-2 мл испытуемого раствора прибавляют 1-2 капли индикатора и титруют 0,1 или 0,05 н. соответствующим титрантом. При анализе концентрированных растворов на титрование 1 мл должно быть израсходовано сравнительно большое количество титрованного раствора, поэтому концентрированные растворы предварительно разбавляют. Микстуры, в которых концентрация исследуемого ингредиента не превышает 4%, обычно не разбавляют. Для количественного определения ингредиентов в мазях навеску берут пергаментной бумаге и помещают в колбу, куда добавляют 3-5 мл спирта и эфира. По растворении мазевой основы полученный раствор титруют. Обработка результатов анализа в зависимости от решаемой задачи осуществляется по нескольким расчетным формулам. За основные обозначения, рекомендуемые ГФХ, а именно: V - объем раствора в миллиметрах (мл); a - масса препарата в граммах(г); K – поправочный коэффициент к стандартному (титрованному) раствору; T – титр стандартного раствора по определяемому веществу в г/мл; c – концентрация растворов в процента, граммах и миллиграммах в 1 миллилитре. Если в расчетную формулу необходимо ввести еще некоторые обозначения, то пользуются, как правило, прописными, но не заглавными, буквами. Таким образом, наиболее употребительны следующие расчетные формулы:
V*K*T*100 Х= —————— , a где V – объем стандартного (титрованного) раствора определенной нормальности, мл; Т – титр, г/мл; К – поправочный коэффициент; а - масса препарата, г;
V*K*T*100 Х= —————— , a где V, К, Т имеют те же наименования, но а – объем препарата, взятого для определения, мл;
V*K*T*V1*100 Х= ———————— , a*V2 где V, К, Т и а имеют те же наименования; V1 – объем раствора препарата первого разведения, мл; V2 – объем аликвотной части разведения, взятый для определения, мл;
V*K*T*б Х= ————— , a где б – масса одного порошка или одной таблетки, г; или общий объем микстуры, мл;
Устройство микробюретки. Для титрования экспресс-методом применяют микробюретку, предложенную Всесоюзным научно-исследовательским институтом фармации (ВНИИФ). Порядок работы. 1) Заполнение титрованным раствором микробюретки и спускной изогнутой пипетки с резиновой насадкой. При закрытом кране средним и большим пальцем левой руки сжать резиновый баллончик таким образом, чтобы указательным пальцем закрыть отверстие для воздуха в нем и, постепенно отпуская баллончик, набрать в бюретку титрованный раствор. Закрыть кран и повернуть резиновую насадку вверх, нажать на бусинку и добиться заполнения пипетки титрованным раствором. Воздуха в спускной пипетке быть не должно. При плохом поступлении раствора в капилляр целесообразно одновременно сжать резиновый баллончик и бусинку и под давлением заполнить изогнутую пипетку. 2. Заполнение титрованным раствором микробюретки и установление на нулевой отметке. Привести пипетку в первоначальное положение, открыть кран и с помощью резинового баллончика, как и первом случае, набрать в бюретку титрованный раствор. Закрыть кран, спустить при его помощи титрованный раствор до нуля, и микробюретка готова к работе. Для удобства и быстроты заполнения бюретки необходимо соблюдать следующее правила: А) резиновый баллончик должен иметь наибольшее отверстие для входа и выхода воздуха; Б) не рекомендуется резко и с силой сжимать и отпускать резиновый баллончик, в противном случае жидкость попадает баллончик; В) не допускать попадания титрованного раствора и резиновый баллончик, иначе при титровании раствор будет попадать в бюретку и точное титрование будет невозможно; при попадании титрованного раствора в баллончик необходимо вынуть бюретку из склянки и путем частых сжатий баллончика освободиться от жидкости; Г) во избежание попадания воздуха в изогнутую пипетку сжимать резиновую насадку только в месте нахождения бусинки; Д) во избежание создания повышенного давления в склянке с титрованным раствором необходимо периодически вынимать бюретку из склянки. Рефрактометрия Рефрактометрический метод является одним из самых простых физическо-химических методов анализа с затратой очень небольших количеств анализируемого вещества и проводится за очень короткое время. В фармацевтическом анализе этот метод применяется для идентификации лекарственных веществ, установления их чистоты и количественного анализа. Рефрактометрический метод анализа основан на измерении показателя преломления анализируемого вещества. Показатель преломления – одно из основных физических свойств вещества: индивидуальное вещество, свободное от примесей характеризуется определенным показателем преломления. Когда луч света переходит из одной прозрачной среды в другую, на границе сред направление его изменяется – луч преломляется. Отношение скорости распространения света в воздухе к скорости распространения света в веществе, равное отношение синуса угла падения луча света к синусу угла его преломления, называется показателем преломления и является величиной постоянной для данной длины волны: ʋ1 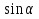 n = —— = ——— ʋ2 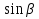 Величина показателя преломления зависит от природы вещества, длины световой волны, концентрации раствора, температуры. Определения показателя преломления производят с помощью специального прибора, называемого рефрактометром. На практике применяются рефрактометры различных систем: лабораторный – РЛ, универсальный – РЛУ и др. Принцип работы на рефрактометрах основан на определении показателя преломления методом предельного угля. Устройство рефрактометра. Главной деталью рефрактометра является измерительная призма из оптического стекла, показатель преломления которого известен. Входная грань измерительной призмы, соприкасающаяся с исследуемым веществом, служит границей раздела, на которой происходит преломление и полное внутреннее отражение луча. Через выходную грань измерительной призмы в зрительную трубу наблюдают преломление или отражение света. Порядок работы.1. До начало измерении применяют чистоту соприкасающихся поверхностей призм. 2. Проверка нулевой точки. На поверхность измерительной призмы нанести 2-3 капли дистиллированный воды, осторожно закрыть осветительной призмой. Открыть осветительное оконце и установить в направлении наибольшей интенсивности источника света с помощью зеркала. Путем вращения винтов получить резкое, четкое, бесцветное разграничение светлого темного поля в поле зрения окуляра. Вращая винт, нанести линию света и тени точного до совпадения с точкой пересечения линии в верхнем оконце окуляра. Вертикальная линия в нижнем оконце окуляра указывает результат измерения – показатель преломления воды при 20°С – 1,333. В случае других показаний показатель преломления устанавливают винтом на 1,333, а при помощи ключа (регулировочный винт снять) приводят границу света и тени к точке пересечения линий. 3. После установки прибора на нулевую точку приподнимают камеру осветительной призмы, фильтровальной бумагой, марлевой или фланелевой салфеткой снимают воду. Затем наносят 1-2 капли исследуемого раствора на плоскость измерительной призмы, камеру закрывают. Вращают винты до совпадения границы света и тени с точкой пересечений линий. По шкале нижнем оконце окуляра производят отсчет коэффициента преломления раствора. Концентрацию раствора определяют по соответствующим таблицам. При измерении концентрации растворов, температура которых отличается от 20°С, следует пользоваться иной таблицей. 4. После каждого определения необходимо обе камеры промыть водой и вытереть досуха фильтровальной бумагой или салфеткой, между камерами заложить прокладку из тонкого слоя ваты. 5. Определение концентрации по таблицам. Существуют таблицы для определения концентрации лекарственных средств, изготовленных весовым или весо-объемным методом. В таблицах приведены коэффициенты преломления и соответствующие им концентрации. В некоторых таблицах приведены коэффициенты преломления с точностью до третьего знака. В этом случае концентрация, соответствующая значению показателя преломления, взятому с четвертым знаком, определяется интерполированием. Меры предосторожности при работе. Быстрее всего в приборе выходят из строя призмы, необходимо соблюдать следующие меры предосторожности при обращении с ними:
|
