Экзаменационные вопросы по курсу минералогии с основами кристаллографии
 Скачать 343 Kb. Скачать 343 Kb.
|
|
Билет 20. Средняя категория
Координационные числа и координационные многогранники. Координационное число равно числу соседей. Координационный полиэдр – многогранник, описанный вокруг данной частицы, в вершинах которого расположены е ближайшие соседи.
Основные типы гидротермальных ассоциаций: I) Плутоногенные гидротермальные месторождения: - глубина 0,5 – 5 км. - повышенные давления - пространственная и генетическая связь с интрузивами - связь с поверхностью отсутствует. - температура 420 – 500С. Высокотемпературная (420 – 300С) минерализация, подобна грейзеновой, пространственно и генетически связана с грейзенами: касситерит, вольфрамит, молибденит, берилл, висмутин, кварц, флюорит, топаз. Среднетемпературные (300 -150С) жилы – пятиэлементная формация: Au, Co, Ni, Bi, U. Также месторождения Сo-Ni-арсенидной формации (Хову-Аксы). Сo-Ni-Ag формация (Канада). Среднетемпературному этапу принадлежат многие полиметаллические месторождения: Zn, Pb, Cu, Ag (Рудный Алтай, Забайкалье). II)Вулканогенные гидротермальные ассоциации: Связаны с вулканическими процессами, протекают на малых глубинах. В гидротермальных растворах имеется как ювенильная, так и метеорная составляющая. Резкие изменения термобарических параметров. Большая скорость отложения. Мелкозернистые, скрытозернистые агрегаты, коллоидные структуры. Так с подводным вулканизмом связаны колчеданные залежи сульфидов. III)Телетермальные ассоциации минералов. С магматизмом видимая связь не установлена. Растворы сместились далеко от источника. Приурочены к зонам глубинных разломов и к определенным вмещающим породам. Обычно низкие температуры – 150-50С. Ассоциации: киноварь + реальгар + аурипигмент + флюорит + барит + кварц + антимонит (SbS). Имеется много промежуточных вариантов ассоциаций. IV)Вторичные кварциты – образуются в результате замещения вмещающих алюмосиликатных пород кислыми растворами в близповерхностных условиях. Выносятся легкорастворимые щелочные металлы, кальций, железо, магний. Остаются труднорастворимые: кремний (в виде кварца), алюминий (алунит, серицит, корунд, каолинит), титан (титанит, сфен, титаноильменит), ванадий (изоморфная примесь в титаноильмените), циркон, самородная сера образуется за счет восстановления алунита, взаимодействий сероводорода с серной кислотой. Полная ассоциация: кварц, алунит, пирит, серицит, каолинит, корунд, флюорит, сера, рутил, на периферии гидроокислы железа-алюминия. Билет 21. Высшая категория Ж) Кубическая сингония Примитивный: куб, ромбододекаэдр, пентагон-додекаэдры, тетраэдры, тригон-тритетраэдры, тетрагон-тритетраэдры, пентагон-тритетраэдры Центральный: куб, ромбододекаэдр, пентагон-додекаэдры, октаэдр, тетрагон-триоктаэдры, тригон-триоктаэдры, дидодекаэдры. Планальный: куб, ромбододекаэдр, тетрагексаэдры, тетраэдры, тригон-тритетраэдры, тетрагон-тритетраэдры, гексатетраэдры. Аксиальный: куб, ромбододекаэдр, тетрагексаэдры, октаэдр, тетрагон-триоктаэдр, тригон-триоктаэдры, гексоктаэдры Типы химической связи в структурах кристаллов Связи обусловлены электронными переходами между атомами. Металлическая – ненаправленная, низкая твердость, вязкость, электропроводность, кч – 8 – 12. Ковалентная – направленная, высокая твердость, высокие температуры кипения и плавления, диэлектрики, КЧ 4 – 6. Ионная – ненаправленная, низкие твердости, низкие температуры плавления, расплавы электропроводны, средние КЧ 6 – 8. Ван-дер-Ваальсова – остаточная, тизкие температуры кипения и плавления, низкие твердости, возникновение градиента спайности. Возникает в результате ориентационно-дисперсионного смещения. Гидротермальные изменения вмещающих пород. А) Серицитизация – образование мелкочешуйчатого мусковита за счет полевых шпатов. Б) Эпидотизация – образование эпидота по породам, богатым Ca в зонах тектонического дробления. В) Березитизация – ассоциация серицит + анкерит + пирит, за счет алюмосиликатных пород. Г) Лиственитизация – изменение ультраосновных пород с образованием кварцево-карбонатных метасоматитов с зеленым фукситом (хромовая слюда) + пирит + гематит. Д) Хлоритизация – образование хлорита за счет биотита. Д) Серпентинизация, оталькование – гидротермальные изменения ультраосновных пород. Гидротермальные метасоматиты сами могут быть могут быть сырьем для добычи или индикаторами рудного проявления. Билет 22. Кристаллографические разновидности простых форм: Под названием одной простой формы объединяются многогранники, отличающиеся по своей симметрии. Но рассмотрим для примера кубы галенита и сравним с кубическими кристаллами пирита. На первый взгляд кажется, что кубики этих минералов обладают равной симметрией, однако это утверждение несостоятельно: грани пирита и галенита несут на себе разные системы штриховки, что непосредственно указывает на симметрию этих кристаллов. Действительно кубы пирита относят к центральному виду, а галенита к планаксиальному. Итак, для кубов делаем вывод: А) Взаимно-перпендикулярная на одной грани, параллельная ребрам штриховка – планаксиальный вид. Б) Взаимно-перпендикулярная на одной грани, но не параллельная ребрам штриховка – аксиальный вид. В) Односторонняя, развитая под углом 45 градусов к ребрам штриховка – планальный вид. Г) Односторонняя штриховка параллельная двум параллельным ребрам штриховка – центральный вид. Д) Косая штриховка – примитивный вид. Полный вывод всех возможных кристаллографически различных простых форм основывается на 32 видах симметрии, причем, отличающиеся по симметрии многогранники принимаются во внимание, как самостоятельные разновидности. В результате подробного пересмотра 47 простых форм было выведено 146 их кристаллографических аналогов. Так пинакоид – 21 разновидность, гексагональная призма – 11 разновидностей, моноэдр – 10 разновидностей. Изучение штриховки, вициналей помогает различать между собой вышеупомянутые разновидности простых форм. И наоборот знание последних дает ключ к пониманию морфологии кристаллов, условий их роста, моделирования геодинамической обстановки. Структуры галита и пирита. Анионы хлора в структуре галита образуют ПКУ. На один ион хлора приходится одна октаэдрическая пустота, которую занимает катион натрия. Помещаем ионы хлора во всех вершинах и центрах всех граней элементарной ячейки минерала. Находим центры октаэдрических пустот – в центре кубической ячейки и на серединах всех ее ребер. На ячейку приходится четыре иона хлора, четыре натрия. Число формульных единиц – 4. КЧ – 8. Кубический кристалл. Пирит – FeS2 имеет решетку производную от галита. Спаренные атомы серы образуют гантели S2, направленные параллельно осям третьего порядка. Чило формульных единиц – 4. Координационное число – 6. аналогично пириту рассматривается кобальтин – FeCoS2. Метаморфические процессы. Факторы метаморфизма. Метаморфизм – процесс твердофазного минерального и (или) структурного изменения пород под воздействием высоких температур, давлений и флюидов. Метаморфизм подразделяется на космогенный и эндогенный. Последний в свою очередь подразделяется на региональный, контактовый. Региональный – осуществляется за счет погружения продуктов различного генезиса на глубину с изменением их минерального состава и структуры. Охватывает большие регионы земной коры. Факторы: температура, давление, флюиды. Масштаб массопереноса незначителен. Тенденции минералообразования: образование новых минералов при повышении давления и уменьшение роли воды при повышении температуры. Факторы метаморфизма: - Температура от 200С до 1000 – 1100С (условно). Степень повышения температуры с глубиной называется геотермальным градиентом. Линия, отражающая изменение температуры с глубиной называется геотермой. Вариации теплового потока из недр Земли зависят от трех источников тепла: 1. Мантийный тепловой поток. 2.Глубинный радиоактивный распад. 3.Внедрение интрузий. -Давление от 2,5 до 12 кбар (при ультаметаморфизме до 12 -18 и 40 кбар). Литостатическое давление растет от 0,26 до 0,32 кбар/км. Флюидальное давление превышает литостатическое – «флюидное сверхдавление». Флюиды: вода, углекислота, аммиак, углеводороды. Присутствие флюидов дает возможность к протеканию метаморфических реакций. Многие минералы содержат в кристаллической решетке воду. Присутствие воды резко ускоряет процессы. Флюид также необходим для переноса компонентов. В составе флюидов доля углекислоты увеличивается с повышением температуры. Билет 23 Параметры граней Значение элементов симметрии и простых форм не всегда дает однозначное представление о кристалле. Помимо ранее указанных данных необходимо выяснить взаимное расположение граней в пространстве. С этой целью примечаются кристаллографические символы, определяющие положение любой грани данного кристалла. Параметрами граней называются отрезки, отсекаемые гранями на трех выбранных ребрах. Разделив, параметры какой-либо грани на соответственные параметры другой грани и взяв отношение между ними, получим отношение целых и сравнительно малых чисел. Получаются двойные отношения: сначала отношения между соответственными ребрами (получаются дроби), а затем отношения между этими дробями по типу: ОА1/ОА2:ОВ1/ОВ2:ОС1/ОС2 = p:q:r. Структуры а-железа, хлорида цезия, самородной меди. Медь Возможность выбора в трехслойной плотнейшей упаковке из атомов меди кубической гранецентрированной элементарной ячейки подтверждает ее высокую симметрию. В проекции на плоскость можно легко различить оси симметрии 4-го, 3-го и второго порядка. Начало координат выбирается в позиции с федоровской группой симметрии: m3m. Получаем, что атомы меди занимают гранецентрированную элементарную ячейку. Расстояние между атомами – 3,615 ангстрем. Координационное число – 12. Координационный многогранник - кубоктаэдр. Аналогичен тип структуры у многих самородных металлов: серебро, золото, гамма-железо, альфа-кобальт, никель, платина. Железо Выделяется объемноцентрированная ячейка Браве. Плотнейшая упаковка отсутствует. КЧ – 8. Присутствие координатных и диагональных зеркальных плоскостей симметрии, а также осей второго порядка указывает на кубическую симморфную пространственную группу. Наиболее симметричные позиции заняты атомами железа. Хлорид цезия Структуру хлорида цезия можно представить в виде двух примитивных кубов, в вершинах которых расположены ионы хлора и цезия. Кубы вложены друг в друга на ½ диагонали элементарной ячейки. По аналогии с а-железом структурный тип характеризуется КЧ – 8. Плотнейшая упаковка отсутствует. Сюда можно отнести галогениды (не фториды!) цезия, таллия, аммония, сплавы: серебро+кадмий, алюминий+железо, бериллий+медь. Метаморфические реакции. Для углерода: графит – алмаз. Для кварца – кристобалит – тридимит – коэсит – стишовит. Для Al2SiO5.: 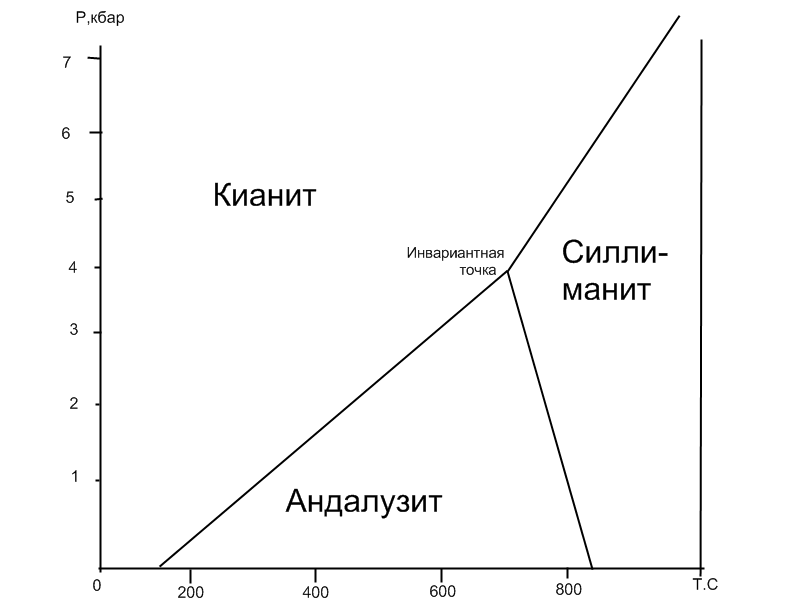 Реакции с появлением новых минеральных фаз: Na[AlSi3O8] = NaAl[Si2O6] + SiO2 Альбит = жадеит + кварц. Реакции обмена без появления новых минеральных фаз: Не приводят к изменению минерального состава, но изменяют химический состав минералов при изменении давления и температуры. Так, в ассоциации диопсид (геденбергит) + гранат при увеличении температуры происходит распределение железа-магния. При реакции краевых частей в центре одни параметры, на периферии – совсем другие. Билет 24. Закон целых чисел или закон рациональности параметров. Двойные отношения, отсекаемые двумя любыми гранями кристалла на трех пересекающихся ребрах его, равны отношениям целых и сравнительно малых чисел. Следует выделять два подпункта: А) Двойные отношения параметров пропорциональны целым числам. Б) Получающиеся числа невелики и редко превышают 10. Структуры алмаза, сфалерита, вюрцита и флюорита. Флюорит CaF2 Полиэдрическая модель молекулы флюорита представляет собой заполненные атомами кальция трехмерные кубы, чередующиеся с вакантными кубами по закону шахматной доски. Плотнейшая упаковка отсутствует так как КЧ анионов – 8 не характерно для плотнейшей упаковки. Структура похожа на структуру оксида лития, только узлы занимает кальций, в «пустотах» размещается фтор. Такое строение обуславливает спайность у флюорита по октаэдру. Вюрцит ZnS Гексагональная модификация сульфида цинка. Атомы серы создают двухслойную ПГУ. Атомы цинка занимают половину тетраэдрических пустот. Все Т-пустоты ориентированы одинаково относительно оси шестого порядка, в другую сторону они же вакантны. Это создает полярность оси шестого порядка. Симметрия нарушается заполнением атомами цинка половины тетраэдрических пустот одной ориентации. Ликвидируются горизонтальные плоскости симметрии. Имеем планальный вид симметрии гексагональной сингонии. Число формульных единиц равно двум. Сфалерит ZnS Кубичная модификация сульфида цинка. Имеет в основе трехслойную упаковку из атомов серы. Катионы цинка занимают также половину тетраэдрических пустот одной ориентации, полярность в данном случае направлена вдоль осей третьего порядка. Такое расположение частиц в структуре понижает симметрию до планального вида. Число формульных единиц – 4. Тип решетки Браве – гранецентрированный. Алмаз Можно представить, что структура алмаза является геометрическим аналогом структуры сфалерита. Имеем две гранецентрированные элементарные ячейки Браве, каждая из которых представлена атомами углерода. Вторая вдвинута в первую на четверть трансляции. Системы точек при этом правильные симметрия повышается до планаксиального вида. Фации метаморфизма. Метаморфичекая фация – ограниченная определенными термобарическими параметрами область, характеризующаяся определенной минеральной ассоциацией, устойчивой при этих параметрах, а также, сама эта ассоциация. Существуют фации низкой, средней и высокой ступеней метаморфизма. Фации низких давлений не превышают 2 - 2,5 кбар. Фации умеренных давлений: 2,5 – 12 кбар - Цеолитовая (менее 250С) - Пренит-пумпеллитовая (250 – 300С) - Зеленосланцевая (350 – 550С) – актинолит, эпидот, хлорит, альбит. - Амфиболитовая (550 – 700С) – амфибол, плагиоклаз, гранат. - Гранулитовая (более 750С) – клинопироксен, ортопироксен, плагиоклаз, гранат. Фации высоких давлений: более 12 кбар - Глаукофан-сланцевая (синие сланцы) – (менее 500С) – глаукофан (натриевый амфибол), альбит. - Эклогитовая (более 500 С) пироксен (омфацит), гранаты (гроссуляр, пироп, альмандин), кварц, рутил. Фации сверхвысоких давлений – фации верхней мантии: Эклогитовая переходит в коэситовую, а затем в фацию алмазоносных эклогитов. |
