|
|
ик спектроскопия. Инфракрасная спектроскопия. Факультет пищевой биотехнологии и товароведения
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ ОРЛОВСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ
УНИВЕРСИТЕТ
ФАКУЛЬТЕТ ПИЩЕВОЙ БИОТЕХНОЛОГИИ И ТОВАРОВЕДЕНИЯ
Р е ф е р а т
Инфракрасная спектроскопия
Выполнил: студент группы 11ТЭ,
факультета пищевой биотехнологии и товароведения
Лежепеков И. С.
Научный руководитель:
Климова Н.В.
Орел, 2009г
Оглавление
Введение…………………………………………………….3
Принцип метода…………………………………………3
Теоретические основы метода………………….............4
Приборы, аппаратура……………………………………6
Применение……………………………………………...10
Заключение…………………………………………………12
Список использованной литературы………………………13
Приложение
Введение.
Современное производство пищевых продуктов гарантированного качества требует использования хорошо воспроизводимых и точных экспресс-методов контроля показателей состава и свойств. Достижение стабильного высокого качества выпускаемой продукции неразрывно связано с организацией своевременного контроля качества сырья и полуфабрикатов на всех этапах технологического процесса. В этой связи, оснащение производственных лабораторий приборами экспресс-контроля позволяет своевременно реагировать на любое отклонение технологических параметров, основным преимуществом приборного контроля является оперативность. К таким методам оперативного анализа следует, безусловно, отнести широко распространенный во многих странах мира метод спектроскопии.
Метод ИК-спектроскопии играет важнейшую роль в идентификации химических и органических веществ, благодаря тому, что каждое химическое соединение имеет неповторимый ИК-спектр
1.Принцип метода
Инфракрасная спектроскопия (ИК спектроскопия), раздел молекулярной оптической спектроскопии, изучающий спектры поглощения и отражения электромагнитного излучения в ИК области, т.е. в диапазоне длин волн от 10-6 до 10-3 м. ИК спектр представляет собой сложную кривую с большим числом максимумов и минимумов. Основные характеристики спектра ИК-поглощения: число полос поглощения в спектре, их положение, определяемое частотой (или длиной волны ), ширина и форма полос, величина поглощения — определяются природой (структурой и химическим составом) поглощающего вещества, а также зависят от агрегатного состояния вещества, температуры, давления и др Спектральные характеристики (положения максимумов полос, их полуширина, интенсивность) индивидуальной молекулы зависят от масс составляющих ее атомов, геом. строения, особенностей межатомных сил, распределения заряда и др. Поэтому ИК спектры отличаются большой индивидуальностью, что и определяет их ценность при идентификации и изучении строения соединений. Инфракрасная спектроскопия дает очень важную информацию о частотах колебаний ядер, зависящих от строения молекул и от прочности валентных связей. Частоты колебаний определенной пары химически связанных атомов (валентных колебаний), обычно лежат в определенных пределах. Так, например, частоты колебаний С–Н имеют различные диапазоны, зависящие от остальных связей атомов углерода, что часто позволяет определять наличие соответствующих групп в органическом соединении.
2. Теоретические основы метода
Атомы в молекуле испытывают непрерывные колебания, а сама молекула вращается как целое, поэтому у нее возникают новые энергетические уровни, отсутствующие в изолированных атомах Молекула может находиться в нескольких энергетических состояниях с большей (E2) или меньшей (E1) колебательной энергией. Эти энергетические состояния называют квантованными. Поглощение кванта света с энергией Е, равной E2 – E1, переводит молекулу из низшего энергетического состояния в более высокое. Это называют возбуждением молекулы.
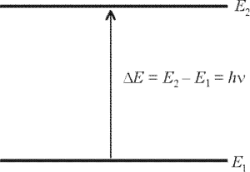
В результате атомы, связанные друг с другом в молекуле, начинают более интенсивно колебаться относительно некоторых исходных положений. Если рассматривать молекулу как систему из атомов-шариков, сцепленных между собой пружинками, то пружинки сжимаются и растягиваются, вдобавок изгибаются.
Хотя ИК-спектр является характеристикой всей молекулы, оказывается, что некоторые группы атомов имеют полосы поглощения при определенной частоте независимо от структуры остальной части молекулы. Эти полосы, которые называют характеристическими, несут информацию о структурных элементах молекулы.
Имеются таблицы характеристических частот, по которым многие полосы ИК-спектр могут быть связаны с определенными функциональными группами, входящими в состав молекулы (Приложение). Характеристическими будут колебания групп, содержащих легкий атом водорода (С–Н, О–Н, N–Н), колебания групп с кратными связями (С=С, С=N, С=O) и т. д. Такие функциональные группы проявляются в диапазоне спектра от 4000 до 1600 см–1.
Область спектра от 1300 до 625 cм–1 известна как область «отпечатков пальцев». Сюда попадают полосы поглощения, отвечающие колебаниям групп С–С, С–О, С–N, а также деформационные колебания. В результате сильного взаимодействия этих колебаний отнесение полос поглощения к отдельным связям невозможно. Однако весь набор полос поглощения в этой области является индивидуальной характеристикой соединения. Совпадение всех полос неизвестного (исследуемого) вещества со спектром заведомо известного эталона является прекрасным доказательством их идентичности. Параметрами молекулярных моделей служат массы составляющих систему атомов, длины связей, валентные и торсионные углы, характеристики потенциальной поверхности (силовые постоянные и др.), дипольные моменты связей и их производные по длинам связей и др.
Инфракрасная спектроскопия позволяет идентифицировать пространственные и конформационные изомеры, изучать внутри- и межмолекулярные взаимодействия, характер химических связей, распределение зарядов в молекулах, фазовые превращения, кинетику химических реакций, регистрировать короткоживущие (время жизни до 10-6 с) частицы, уточнять отдельные геометрические параметры, получать данные для вычисления термодинамических функций и др.
Необходимый этап таких исследований - интерпретация спектров, т.е. установление формы нормальных колебаний, распределения колебательной энергии по степеням свободы, выделение значимых параметров, определяющих положение полос в спектрах и их интенсивности. Расчеты спектров молекул, содержащих до 100 атомов, в том числе полимеров, выполняются с помощью ЭВМ. При этом необходимо знать характеристики молекулярных моделей (силовые постоянные, электрооптические параметры и др.), которые находят решением соответствующих обратных спектральных задач или квантово-химическими расчетами. И в том, и в другом случае обычно удается получать данные для молекул, содержащих атомы лишь первых четырех периодов периодической системы.
3. Приборы, аппаратура
Основные части классического спектрофотометра - источник непрерывного теплового излучения, монохроматор, неселективный приемник излучения. Кювета с веществом (в любом агрегатном состоянии) помещается перед входной (иногда за выходной) щелью. В качестве диспергирующего устройства монохроматора применяют призмы из различных материалов (LiF, NaCl, KCl, CsF и др.) и дифракции решетки. Последовательное выведение излучения различных длин волн на выходную щель и приемник излучения (сканирование) осуществляется поворотом призмы или решетки.
Работа прибора по двух лучевой схеме основана на нулевом методе. Радиация от источника излучения 1 направляется с помощью зеркал 2 - 5 по двум каналам: в одном канале (I) помещается исследуемый образец (6), в другом (II) - фотометрический клин (7) и образец сравнения (8).
С помощью прерывателя (9) пучки света из каналов I и II попеременно проходят через диспергирующую систему монохроматора, образуемую призмой 10 из солей LiF, NaCl или KBr, разлагаются в спектр и поступают на приемник радиации болометр. Когда интенсивность пучков в обоих каналах одинакова, на болометр поступает постоянная тепловая радиация и сигнал на входе усилителя не возникает. При наличии поглощения, на болометр падают лучи разной интенсивности и на нем возникает переменный сигнал. Этот сигнал после усиления смещает фотометрический клин, сводя до нуля разность поглощения образца и фотометрического клина. Фотометрический клин механически связан с пером, перо регистрирует величину поглощения.
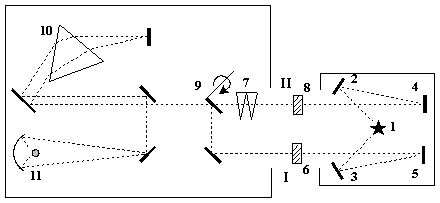 Оптическая схема. Оптическая схема.
Источники излучения - накаливаемые электрическим током стержни из различных материалов. Приемники: чувствительные термопары, металлические и полупроводниковые термосопротивления (болометры) и газовые термопреобразователи, нагрев стенки сосуда которых приводит к нагреву газа и изменению его давления, которое фиксируется. Выходной сигнал имеет вид обычной спектральной кривой. Достоинства приборов классической схемы: простота конструкции, относительная дешевизна.
Недостатки: невозможность регистрации слабых сигналов из-за малого отношения сигнал: шум, что сильно затрудняет работу в далекой ИК-области; сравнительно невысокая разрешающая способность длительная (в течение минут) регистрация спектров.

Фурье-спектрометр
В фурье-спектрометрах отсутствуют входная и выходная щели, а основной элемент - интерферометр. Поток излучения от источника делится на два луча, которые проходят через образец и интерферируют. Разность хода лучей варьируется подвижным зеркалом, отражающим один из пучков.
Первоначальный сигнал зависит от энергии источника излучения и от поглощения образца и имеет вид суммы большого числа гармоничных составляющих. Для получения спектра в обычной форме производится соответствующее фурье-преобразование с помощью встроенной ЭВМ. Достоинства фурье-спектрометра: высокое отношение сигнал: шум, возможность работы в широком диапазоне длин волн без смены диспергирующего элемента, быстрая (за секунды и доли секунд) регистрация спектра, высокая разрешающая способность (до 0,001 см1). Недостатки: сложность изготовления и высокая стоимость.
Все спектрофотометры снабжаются ЭВМ, которые производят первичную обработку спектров: накопление сигналов, отделение их от шумов, вычитание фона и спектра сравнения (спектра растворителя), изменение масштаба записи, вычисление экспериментальных спектральных параметров, сравнение спектров с заданными, дифференцирование спектров и др. Кюветы для ИК спектрофотометров изготовляют из прозрачных в ИК-области материалов. В качестве растворителей используют обычно ССl4, СНСl3, тетрахлорэтилен, вазелиновое масло. Твердые образцы часто измельчают, смешивают с порошком КВr и прессуют таблетки. Для работы с агрессивными жидкостями и газами применяют специальные защитные напыления (Ge, Si) на окна кювет. Мешающее влияние воздуха устраняют вакуумированием прибора или продувкой его азотом. В случае слабо поглощающих веществ (разреженные газы и др.) применяют многоходовые кюветы, в которых длина оптического пути достигает сотен метров благодаря многократным отражениям от системы параллельных зеркал.
Большое распространение получил метод матричной изоляции, при котором исследуемый газ смешивают с аргоном, а затем смесь замораживают. В результате полуширина полос поглощения резко уменьшается, и спектр получается более контрастным.
Применение специальной микроскопической техники позволяет работать с объектами очень малых размеров (доли мм). Для регистрации спектров поверхности твердых тел применяют метод нарушенного полного внутреннего отражения. Он основан на поглощении поверхностным слоем вещества энергии электромагнитного излучения, выходящего из призмы полного внутреннего отражения, которая находится в оптическом контакте с изучаемой поверхностью.
4. Применение
Инфракрасная спектроскопия широко применяют для анализа смесей и идентификация чистых веществ. Количественный анализ основан на зависимости интенсивности полос поглощения от концентрации вещества в пробе. При этом о количестве вещества судят не по отдельным полосам поглощения, а по спектральным кривым в целом в широком диапазоне длин волн. Если число компонентов невелико (4-5), то удается математически выделить их спектры даже при значительном перекрывании последних.
Для идентификации новых веществ (молекулы которых могут содержать до 100 атомов) применяют системы искусственного интеллекта. В этих системах на основе спектроструктурных корреляций генерируются молекулы структуры, затем строятся их теоретические спектры, которые сравниваются с экспериментальными данными. Исследование строения молекул и других объектов методами инфракрасной спектроскопии подразумевает получение сведений о параметрах молекулярных моделей и математически сводится к решению точки назначения обратных спектральных задач. Решение таких задач осуществляется последовательным приближением искомых параметров, рассчитанных с помощью специальной теории спектральных кривых к экспериментальным.
ИК-спектры измеряют для газообразных, жидких и твердых соединений, а также их растворов в различных растворителях. Некоторые области применения ИК спектроскопии
Химия и нефтехимия.
Качественный и количественный анализ сырья, промежуточных и конечных продуктов синтеза. Фракционный и структурно-групповой состав нефтепродуктов. Анализ топлив: эфиры, спирты, ароматика, октановое число. Фурье-спектрометры могут быть использованы для экспресс-анализ нефтей, газоконденсатов, природного газа и продуктов их переработки.
Химия полимеров.
Анализ сополимеров. Синтетические каучуки: состав, структурные характеристики. Анализ модифицирующих добавок: пластификаторы, антиоксиданты.
Фармацевтическая промышленность.
Определение подлинности субстанций по ИК-стандартам, контроль качества лекарственных форм и сырья.
Газовый анализ. Анализ многокомпонентных газовых смесей.
Контроль качества продукции газовой промышленности, анализ состава и влажности природного газа.
Электронная промышленность.
Контроль качества полупроводникового кремния и параметров тонких слоев. Анализ состава технологических газов.
Пищевая и парфюмерная промышленность.
Экспрессный контроль сырья и готовой продукции: содержание белков, клетчатки, жира, влаги.
Экологический контроль.
Контроль нефтепродуктов в воде и почве. Контроль атмосферного воздуха, воздуха рабочей зоны и выбросов промышленных предприятий.
Криминалистический, судебно-медицинский и биоклинический анализ.
Качественный и количественный анализ природных веществ и продуктов синтеза. Идентификация наркотиков, ОВ и ВВ. Анализ следовых остатков веществ.
Заключение
Метод инфракрасной спектроскопии дает возможность с высокой вероятностью предсказывать качественный количественный состав химических соединений. Современные приборы позволяют осуществлять процедуру измерения этих показателей с достаточной точностью и высокой воспроизводимостью результатов измерений.
Основными достоинствами данного метода являются
1.значительное сокращение времени на проведение анализа;
2. существенная экономия энергоресурсов;
3.приборы не требуют применения дорогостоящих расходных материалов и химических реактивов;
4. гораздо менее жесткие требования по специальной подготовке предъявляются к обслуживающему персоналу, производящему рутинные измерения (по сравнению с их коллегами, осуществляющие традиционные лабораторные методы анализа).
Список использованной литературы.
1. Беллами Л., Инфракрасные спектры молекул, пер. с англ., М., 1957;
2. Кросс А., Введение в практическую инфракрасную спектроскопию, пер. с англ., М., 1961;
3. Казицына Л.А., Куплетская Н.Б. Применение УФ, ИК, ЯМР и масс-спектроскопии в органической химии. М.: Изд-во Моск. ун-та, 1979, 240 с.;
4. Сильверстейн Р., Басслер Г., Моррил Т. Спектрометрическая идентификация органических соединений. М.: Мир, 1977, 590 с. спектроскопии в химии, пер. с англ., М., 1959;
5. Чулановский В. М., Введение в молекулярный спектральный анализ, 2 изд., М.—Л., 1951.
Приложение
Таблица «Частоты характеристических колебаний с участием одинарных связей»
Группа
|
ν, см-1
|
Iотн
|
Отнесение и примечания
|
C–C
|
1050 ± 10
|
с - ср
|
С-С связей. Обычно наблюдается несколько полос. Для целей идентификации не применяется
|
C–О–C
|
1105 ± 45
|
с
|
νas(C–О–C) в ациклических эфирах
|
C–О–C
|
1050 ± 10
|
с
|
νas(C–О–C) в алкилариловых и алкилвиниловых эфирах
|
C–О(Н)
|
1050
|
ср
|
ν(C–О) соответственно в первичных, вторичных и третичных спиртах, указания ориентировочны
|
1100
|
|
1150
|
|
C–О(Н)
|
1200 ± 20
|
|
ν(C–О) в фенолах
|
C–N
|
1305 ± 55
|
с
|
ν(C–N) в ароматических аминах и амидах
|
1230 ± 50
|
ср
|
ν(C–N) в алифатических аминах и амидах
|
870 ± 10
|
ср
|
ν(C–N) в нитросоединениях
|
C–F
|
1050 ± 50
|
с
|
В монофторзамещенных
|
1250 ± 150
|
оч.с
|
В ди- и полифторзамещенных. Чем выше степень замещения, тем выше частота
|
C–Cl
|
725 ± 25
|
с
|
В монохлорзамещенных. В полихлорзамещенных выше - до 800 см-1
|
C–Br
|
650 ± 30
|
с
|
|
C–I
|
500
|
с
|
|
P–O
|
1000
|
ср
|
В ароматических соединениях
|
Si–CH3
|
800 ± 50
|
оч.с
|
Наблюдается наряду с δ(СН3) при 1360 см-1
|
Si–Ph
|
1430
1115 ± 25
|
оч.с
оч.с
|
Точное отнесение неизвестно
|
P–O–С
|
1040 ± 10
|
оч.с
|
в алифатических эфирах
|
Таблица ХАРАКТЕРИСТИЧЕСКИЕ ЧАСТОТЫ КОЛЕБАНИЙ
НЕКОТОРЫХ ГРУПП
|
Группа (тип колебаний)
|
Волновое число, см–1
|
O–H (валентные)
|
3350–3250
|
N–H (валентные)
|
3460–3280
|
C–H (валентные)
|
2980–2850
|
C C (валентные)
|
2300–2100
|
C=O (валентные)
|
1870–1650
|
C=N (валентные)
|
1620–1560
|
C=C (валентные)
|
1645–1615
|
N–H (деформационные)
|
1650–1590
|
C–H (деформационные)
|
1470–1360
|
O–H (деформационные)
|
1440–1260
|
Инфракрасные спектры органических соединений
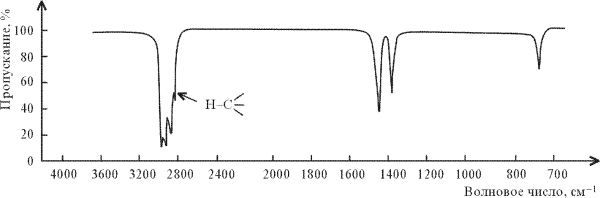
ИК-спектр н-гексана СН3(СН2)4СН3
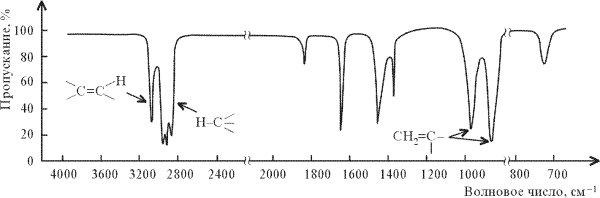
ИК-спектр гексена-1 СН2=СН(CH2)3СН3
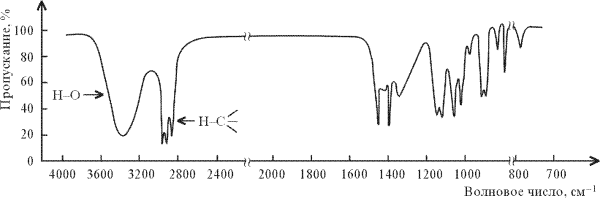
ИК-спектр гексанола-2 СН3(CH2)3СН(ОН)СН3
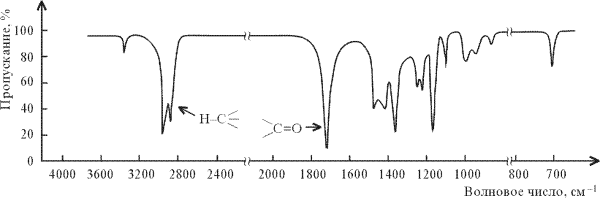
ИК-спектр гексанона-2 СН3(CH2)3С(О)СН3
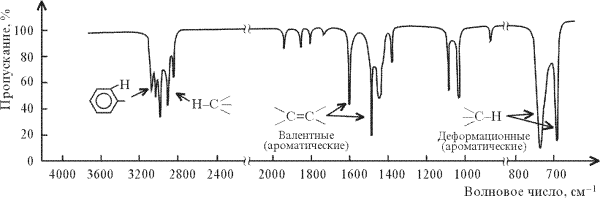
ИК-спектр толуола  СН3 СН3
Задача. Какому из приведенных ниже соединений принадлежит ИК-спектр, показанный на рис Объясните ваш выбор.
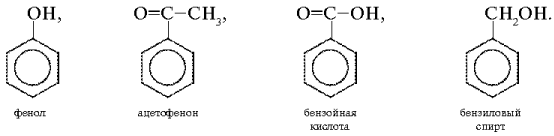
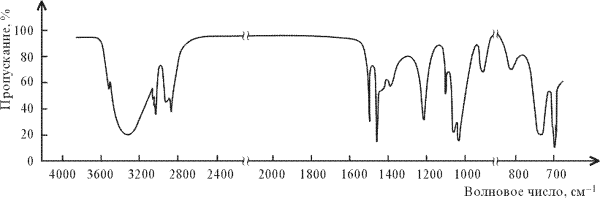
ИК-спектр неизвестного соединения
Решение. В области 1800–1650 см–1 поглощение отсутствует, поэтому соединение не содержит С=О-группы. Из двух остающихся веществ – фенола и бензилового спирта – выбираем спирт, т. к. в спектре есть полоса C–H=2950–2850 см–1 группы СН2 (углерод в состоянии sp2-гибридизации).
|
|
|
 Скачать 180.5 Kb.
Скачать 180.5 Kb.








 Оптическая схема.
Оптическая схема.