Тема занятия:
Фазы иммунной реакции
Рассматриваемые вопросы темы:
Антигенпрезентирующие клетки. Типы, характеристика.
Взаимодействие антигенпрезентирующих клеток с антигенами: процессирование и презентация антигена. Активированный макрофаг и регуляция его функций.
Т-лимфоциты и их характеристика. Субпопуляции Т-клеток.
Т-клеточный рецептор, структура. Роль Т-клеточного рецептора и др. ко-стимуляционных макромолекул (CD28, CD80, CD81, CD40, CD4, CD8, CD20), вовлекаемых в процесс активации Т-лимфоцитов. Т-зависимые и регуляторные механизмы.
Клеточный иммунный ответ и его проявления.
Фагоцитоз осуществляют две системы клеток —гранулоциты и мононуклеарные фагоциты, к
которым относятся макрофаги и моноциты. Макрофаги возникают из содержащихся в костном мозге предшественников, общих для макрофагов и гранулоцитов. Все этапы их созревания до моноцитов происходят в костном мозге.
Стадии дифференцировки макрофагов: Гемопоэтическая стволовая клетка → клетка предшественник миелопоэза → клетка предшественник →гранулоцитов-макрофагов → промоноцит → моноциты (циркулируют в крови) → макрофаги (тканевые).
Все макрофаги, по классификации ВОЗ (1972 г), объединены в МОНОНУКЛЕАРНУЮ ФАГОЦИТАРНУЮ СИСТЕМУ (МФС). К ней отнесены макрофаги тканей: гистиоциты, звездчатые ретикулоэндотелиоциты печени (синоним, который легче запоминается - клетки Купфера), свободные и фиксированные макрофаги селезенки, лимфатических узлов, лимфатических сосудов, серозных полостей, плевральные и перитониальные, легочные макрофаги представлены альвеолярными и интерстициальными макрофагами. Макрофаги мозга – микроглиальные клетки.
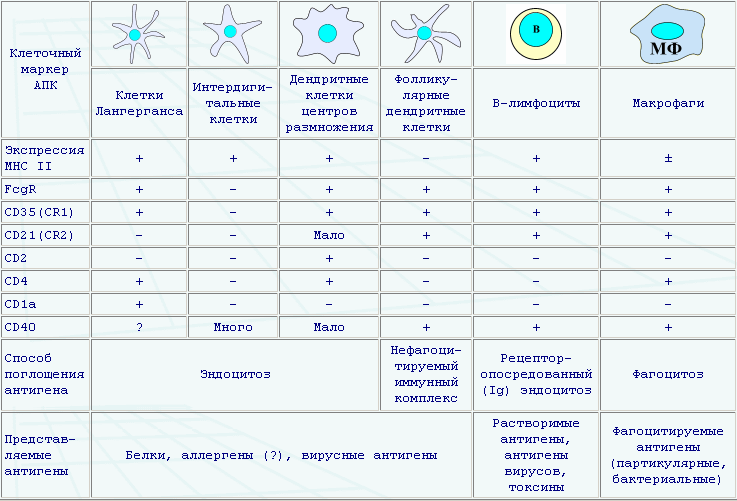
Рис. . Разновидности антигенпрезентирующих клеток и их характеристики.
В наибольшем количестве макрофаги содержатся в костном мозге, в печени, в селезенке, легких, серозных полостях, в соединительной ткани. Мононуклеарные фагоциты (моноциты/макрофаги) являются важной системой врожденного неспецифического иммунитета. Значительна их роль на доиммунном этапе защиты. В то же время они нужны для презентации антигена Т-лимфоцитам, так как с «диким» антигеном Т-лимфоциты не взаимодействуют.
В настоящее время признано, что ведущую роль в представлении антигена играют дендритные клетки, это – система специализированных клеточных популяций, которые распознают и представляют антигены Т- и В-лимфоцитам в ассоциации с антигенами главного комплекса гистосовместимости (и костимулирующими молекулами). С современной точки зрения дендритные клетки играют ключевую роль в обеспечении направленного иммунного ответа и именно у них важнейшей функцией является ПРЕДСТАВЛЕНИЕ АНТИГЕНА (у макрофагов эта функция вторична).Все органы и ткани человека содержат дендритные клетки, которые имеют различные названия, но обладают схожими свойствами. В крови их менее 2 %. В селезенке в паракортикальной Т-зависимой зоне они называются интердигитальными дендритными клетками и представляют антиген Т-клеткам. В В-зависимой области селезенки они называются фолликулярными дендритными клетками. В коже они представлены в большом количестве и называются клетками Лангерганса. Из кожи, поглотив антиген, они мигрируют в лимфоидные органы. Презентируя антиген в комплексе с антигенами HLA Т-лимфоцитам.
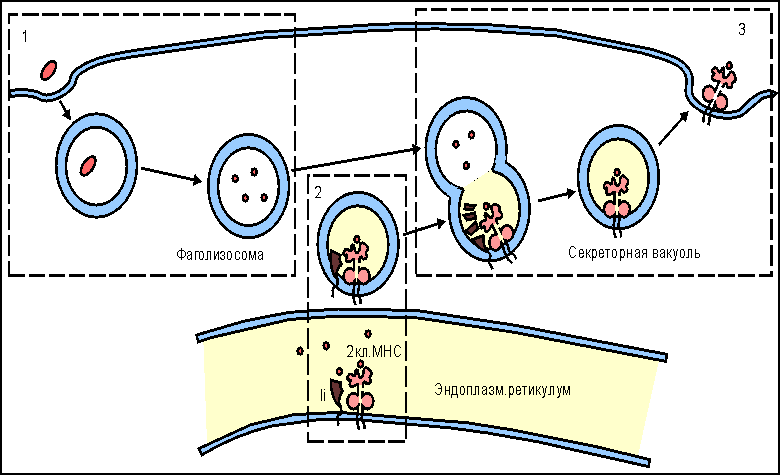
Рис. Процессирование антигена
I этап - поглощение бактерий или их токсинов фагоцитирующей, способной к презентации антигена клеткой и разрушение захваченного материала до отдельных пептидов в фаголизосомах.
II этап - во внутреннем пространстве эндоплазматического ретикулума происходит сборка молекул II класса, которые до встречи с пептидом комплексированы со специальным белком, получившим название инвариантной цепи (Ii). Этот белок защищает молекулу II класса от случайной встречи с бактериальными пептидами в эндоплазматическом ретикулуме. Комплекс молекулы II класса с Ii покидает эндоплазматический ретикулум в составе вакуоли.
III этап - вакуоль, содержащая комплекс молекулы II класса с Ii, сливается с фаголизосомой. Кислые протеазы фаголизосом разрушают Ii белок и таким образом снимают запрет на взаимодействие молекул II класса с бактериальными пептидами. Образовавшийся новый комплекс пептид:молекула II класса в составе секреторной вакуоли перемещается к мембране клетки. Результатом всех этих процессов является экспрессия чужеродного пептида в комплексе с молекулой II класса на клеточной поверхности, что и обеспечивает доступность бактериального пептида для антигенраспознающих рецепторов Т-клеток.
Моноциты, активированные in vitro гранулоцитарно-макрофагальным колониестимулирующим фактором и интерлейкином-4 , теряют способность к фагоцитозу и превращаются в АПК, приобретая морфологию дендритных клеток, и начинают экспрессировать белки MHC класса II. Относительно ФДК первичных и вторичных лимфоидных фолликулов предполагается, что они имеют мезенхимное, а не костномозговое происхождение.
КЛЕТОЧНЫЙ ИММУНИТЕТ
Иммунная система млекопитающих обеспечивает защиту организма двумя основными специфическими способами. Во-первых, это образование специфических антител, а во-вторых, образование и функционирование клеточных факторов приобретенного иммунитета, не только оказывающих ЭФФЕКТОРНОЕ ДЕЙСТВИЕ (разрушение клеток мишеней: опухолевых, мутировавших, и др.), но и осуществляющих РЕГУЛЯЦИЮ иммунного ответа. А так же участвующих в формировании иммунологической памяти, распознавании антигена и индукции иммунного ответа. Клетками, выполняющими такие многообразные функции, являются в первую очередь Т-ЛИМФОЦИТЫ. Причем среди Т-лимфоцитов существуют субпопуляции, основные из которых Т-хелперы и Т-эффекторы (цитотоксические Т-лимфоциты). Приобретение ими специфических функций происходит в центральном органе иммунной системы — тимусе. Важной особенностью Т-лимфоцитов является способность распознавать только антигены презентированные (представленные) на поверхности вспомогательных антигенпредставляющих клеток (дендритных, макрофагов или В-лимфоцитов) в комплексе с собственными антигенами гистосовместимости. ТИМУС важный лимфопоэтический и эндокринный орган. Главная функция тимуса это регулирующее влияние на Т-клеточный иммуногенез.
Гемопоэтические стволовые клетки (предшественники Т- лимфоцитов) из костного мозга через кровяное русло мигрируют в тимус. Установлено, что гормоны тимуса, а точнее растворимые факторы тимуса, создают гуморальное микроокружение тимическим лимфоцитам (последние называют тимоцитами). Значительную роль на внутритимическое развитие Т-лимфоцитов оказывают эпителиальные клетки тимуса и дендритные клетки тимуса. Межклеточные взаимодействия тимоцитов с ними обеспечивают созревание и селекцию Т-клеток. Влияние гормонов тимуса на иммуногенез происходит не только в процессе внутритимической дифференцировки лимфоцитов, но и на расстоянии, поступая в кровь, они оказывают влияние на предшественников лимфоцитов в костном мозге и циркулирующие лимфоциты. В итмусе происходят основные начальные этапы дифференцировки Т-лимфоцитов (тимоцитов), с последующим поступлением зрелых лимфоцитов в кровь. Среди этих лимфоцитов не должно быть аутореактивных – способных взаимодействовать с аутологичными антигенами организма индивидуума. Необходимо отметить, что до сих пор окончательно не установлена биологическая роль гормональных веществ тимуса. Их эффекты не ограничиваются лимфопоэзом, они оказывают влияние на метаболизм кальция и фосфора, обмен и утилизацию глюкозы, мышечный тонус, рост и половое созревание, обладают обезболивающим действием, влияют на пигментный обмен.
Дифференцировка Т-лимфоцитов.
В процессе дифференцировки Т-лимфоцитов выделяют два основных этапа (как Вы помните, такие же два этапа выделяют в процессе дифференцировки В-лимфоцитов):
1. Антигеннезависимая дифференцировка – происходит постоянно в тимусе.
2. Антигензависимая дифференцировка – происходит в периферических органах иммунной системы только при контакте Т-лимфоцита с антигеном.
АНТИГЕННЕЗАВИСИМАЯ ДИФФЕРЕНЦИРОВКА Т-ЛИМФОЦИТОВ
 Родоначальной клеткой Т-лимфоцитов, как и всех клеток крови, является полипотентная стволовая гемопоэтическая клетка. Её маркером является CD 34. Родоначальной клеткой Т-лимфоцитов, как и всех клеток крови, является полипотентная стволовая гемопоэтическая клетка. Её маркером является CD 34.
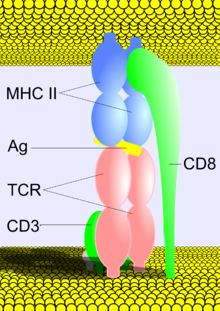
Ранние предшественники Т-лимфоцитов мигрируют из костного мозга в тимус, где происходит антигеннезависимая дифференцировка Т-клеток под влиянием «клеток нянек», эпителиальных клеток тимуса, а так же гормонов тимуса (α- и β-тимозины, тимулин /сывороточный фактор тимуса/, тимопоэтин, тимический гуморальный фактор). Самыми ранними маркерами тимоцитов являются CD7, CD2. В тимусе Т-лимфоциты дифференцируются в иммунокомпетентные клетки и приобретают важную способность к распознаванию антигена. На их наружной мембране появляется (экспрессируется) особый рецептор - Т-клеточный рецептор (ТКР, англ. - TcR, T-cell receptor) для антигена. Причем для каждого антигена (эпитопа) в организме предназначен отдельный лимфоцит или его клональные дочерние лимфоциты-потомки, которые имеют специфичный антигену TcR. Тимоциты одновременно с TcR в процессе дифференцировки приобретают CD3, который тесно связан с Т-клеточным рецептором. CD3 необходим для передачи сигнала от ТКР в цитоплазму. На поверхности тимоцитов появляются также молекулы CD8 и CD4. Это двойные позитивные клетки, т.е. их фенотип (ТКР+, CD3+, CD4+, CD8+) и они α β Место связывания антигена являются молодыми тимоцитами. По своему строению молекулы TcR (ТКР) напоминают иммуноглобулины (Fab-фрагмент) и состоят и альфа- и бета- цепей (TcR αβ их подавляющее большинство) или гамма- и дельта- цепей (TcR γδ). αβ- и γδ – формы TcR весьма сходны по структуре. Каждая цепь ТКР состоит из двух областей (доменов): наружный вариабельный (V) , второй – константный (С). Отдельные гены кодирующие всю вариабельную область (V) α и β цепей TcR отсутствуют. Фрагменты вариабельных доменов кодируются тремя группами генов обозначаемых V, D, J. В клеточном геноме гены, кодирующие V-, J- и D-сегменты вариабельной области, представлены в виде многочисленных вариантов. Именно различные сочетания V-, J- и D-сегментов V области, образующиеся в процессе генной перестройки, называемой реаранжировкой, обеспечивают разнообразие молекул ТКР. Таким образом, ограниченное число генов (около 400) может кодировать рецепторы для почти бесконечного числа антигенов (многих миллионов). Причем различные комбинации генов V, D, J –сегментов - это только один из способов достижения многообразия антигенных рецепторов Т-лимфоцитов. Основная функция зрелых Т-лимфоцитов – распознавание чужеродных антигенных пептидов в комплексе с собственными антигенами главного комплекса гистосовместимости (ГКГС) на поверхности антигенпрезентирующих клеток или на поверхности любых клеток-мишеней организма. Для выполнения этой функции Т-лимфоциты должны быть способны распознавать собственные антигены ГКГС. В то же время, Т- клетки не должны распознавать аутоантигены самого организма, связанные с собственными антигенами ГКГС. В связи с этим в тимусе молодые тимоциты проходят селекцию («отбор»), TcR которых соответствует вышеуказанным условиям. Суть позитивной и негативной селекции состоит в следующем:
Позитивная селекция. Т-лимфоциты, ТКР которых обладает способностью распознавать HLA (молекулы ГКГС) стромальных клеток тимуса, выживают, а если нет – то гибнут путем апоптоза. Позитивная селекция – поддержка избирательной выживаемости. Таким образом, выживают только лимфоциты способные распознавать собственные HLA! И эта способность в последующем является важной в функционировании Т-клеток. Кроме этого в тимусе погибают путем апоптоза аутореактивные лимфоциты (лимфоциты имеющие ТКР к антигенным детерминантам собственных тканей). Важно, что при контакте с эпителиоидными клетками тимуса Т-лимфоциты, реагирующие на «своё», разрушаются путем запуска апоптоза (запрограммированной клеточной смерти при активации через CD95 – Fas рецептор). Это отрицательная селекция. В итоге, исчезают аутореактивные клоны клеток и возникает толерантность (неотвечаемость) к «своему». В тимусе около 95 – 97% лимфоцитов погибают в результате процесса селекции. В последующем одна из молекул CD4 или CD8 утрачивается и клетки становятся зрелыми.
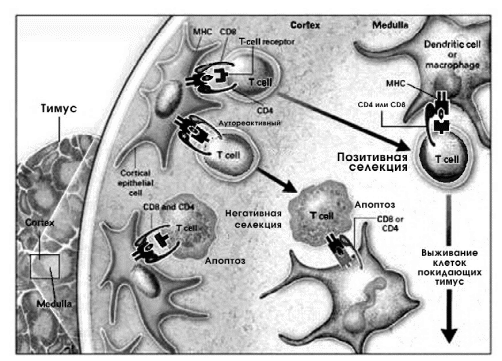
Клетки, сохранившие CD4 являются Т-хелперами (Тh) и их ТКР распознает HLA II класса, а сохранившие CD8 – цитотоксическими Т-лимфоцитами и их ТКР обладает способностью распознавать HLA I класса. Из тимуса они мигрируют в периферические лимфоидные органы, где заселяют преимущественно Т-зависимые зоны. На одном Т-лимфоците только один вариант рецептора и только к одномуантигену. TcR прочно связан с CD3.
В частности в лимфоузлах – паракортикальную. Зрелые лимфоциты рециркулируют. Таким образом, АНТИГЕННЕЗАВИСИМАЯ дифференцировка Т-лимфоцитов включает в себя пролиферацию, приобретение специфических маркеров Т-лимфоцитами и образование дифференцированных, зрелых субпопуляций, способных осуществлять характерные для той или иной субпопуляции функции (индукция иммунного ответа, его регуляция, цитотоксичность). В порцессе антигеннезависимой дифференцировки образуются лимфоциты, которые генетически детерминированы к взаимодействию с определенным антигеном и иммунному ответу на этот антиген.
АНТИГЕНЗАВИСИМАЯ ДИФФЕРЕНЦИРОВКА Т-ЛИМФОЦИТОВ
Антигензависмая дифференцировка происходит в периферических органах иммунной системы, если Т-лимфоцит провзаимодействовал с антигеном. Начинается она с момента распознавания антигена и заканчивается образованием клона лимфоцитов, способных _____оказывать специфическое действие как по отношению к антигену, так и к другим иммунокомпетентным клеткам, вступившим во взаимодействие с антигеном. Причем хелперы и цитотоксические лимфоциты распознают антиген по-разному. Так, ХЕЛПЕРЫ (CD4–клетки) распознают АНТИГЕН в комплексе с HLA II КЛАССА, КИЛЛЕРЫ (CD8-клетки) - в комплексе антиген с HLA 1 КЛАССА. Распознавание антигена Т-хелпером является центральным процессом, как в гуморальном иммунном ответе, так и в усилении клеточной формы иммунного ответа.
Специфическими МАРКЕРАМИ для ВСЕЙ ПОПУЛЯЦИИ Т-ЛИМФОЦИТОВ являются имеющиеся на наружной мембране этих клеток антигены CD 3. (Раньше использовался маркер CD 2 - рецептор для эритроцитов барана, что не совсем корректно. Параметры CD антигенов смотри в приложении.)
Маркер Т-лимфоцитов - структура, которая свойственна только Т-лимфоцитам (всем субпопуляциям Т-лимфоцитов) – CD3.
СУБПОПУЛЯЦИИ ЛИМФОЦИТОВ:
Тh лимфоциты. Примерно половина из числа циркулирующих Т-лимфоцитов несут на своей поверхности антиген CD4 . Эти Т-лимфоциты функционируют как ХЕЛПЕРЫ, то есть помощники (от англ. To help — помогать), «включающие» популяцию В-лимфоцитов в процесс выработки антител, а Т-эффекторы – в реализацию клеточного иммунитета. Т-хелперы опосредуют свою функцию гуморальными факторами - цитокинами, которые синтезируются этими лимфоцитами в ответ на антигенный стимул. Недостаточность хелперной функции Т-лимфоцитов, наблюдаемая при синдроме приобретенного иммунодефицита (СПИД, одной из важнейших мишеней ВИЧ являются Т-лимфоциты хелперы), приводит к «неотвечаемости» организма на антигенную стимуляцию, что, в конечном итоге, способствует персистенции в организме человека микроорганизмов, развитию злокачественных новообразований и является причиной летального исхода.
Т-хелперы (Th) – стимулируют пролиферацию и дифференцировку как Т-, так и В-лимфоцитов, выделяя цитокины. В зависимости от того, какие цитокины они продуцируют (в зависимости от цитокинового профиля) среди них различают:
Th1 (Т-хелперы первого типа), выделяют ИЛ-2 и γ-интерферон, и в итоге обеспечивают реакции Т-клеточного иммунитета – стимулируют иммунный ответ против внутриклеточных бактерий, противовирусный, противоопухолевый, трансплантационный иммунитет.
Th2 (Т-хелперы второго типа), секретируют ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-10, ИЛ-13 и стимулируют синтез антител, способствуют развитию гуморального иммунного ответа против внеклеточных бактерий, их токсинов, а также образование IgE-антител. Между Th1 и Th2 существует антагонизм: при повышении активности одних, угнетается функция других. В итоге преобладает Т-клеточный (Th1→ T киллеры) или В-клеточный (Th2 →В-лимфоциты →антитела) иммунитет, что во многом зависит от вида антигена. Таким образом, Т-хелперы выполняют хелперно-регуляторную функцию во взаимодействии иммунокомпетентных клеток, направленную на развитие эффекторной фазы иммунного ответа. Именно от Th зависит будет преобладать гуморальный или клеточный иммунный ответ.
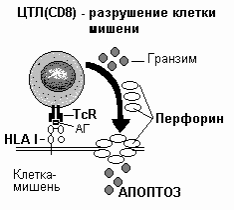 Тk. Среди субпопуляций Т-лимфоцитов различают эффекторные клетки. В связи с тем, что эти эффекторные клетки способны специфически разрушать клетки-мишени, их называют ЦИТОТОКСИЧЕСКИМИ Т-ЛИМФОЦИТАМИ, или Т-КИЛЛЕРАМИ - убийцами (от англ. to kill - убивать). Т-киллер — одна из основных эффекторных клеток клеточноопосредованного иммунитета, которая наряду с другими клетками способна осуществлять лизис клеток мишеней. Роль Т-киллеров очень велика в реализации трансплантационного иммунитета, развитии аутоиммунных заболеваний, в противоопухолевой защите. Тk-лимфоциты (CD8+ клетки) составляют около 20 – 25% от числа циркулирующих Т-лимфоцитов (абсолютноеколичество - 500 – 1200 в 1 мм3 (мкл)), они несут маркерный антиген CD8 . Макромолекула CD8 служит корецептором для антигенов главного комплекса гистосовместимости I класса (ГКГС-1). Активированные антигеном цитотоксические клетки – Т-киллеры связываются с антигенами на поверхности клеток и, выделяя белок перфорин, разрушают их. При этом Т-киллер остается жизнеспособным и может разрушать следующую клетку. Действие перфорина подобно МАК системы комплемента. Белок перфорин, полимеризуясь в мембране клетки-мишени, образует поры – каналы, тем самым, вызывая её осмотический лизис. Кроме того, цитотоксический Т-лимфоцит через пору, образованную перфорином в клетке-мишени, вбрасывает гранзимы (ферменты – сериновые протеазы), которые запускают программу апоптоза. Установлено также, что своё цитотоксическое действие Т- лимфоциты могут реализовывать путем экспрессии FasL и с его помощью индуцировать Fas-опосредованный апоптоз мишени. Тk. Среди субпопуляций Т-лимфоцитов различают эффекторные клетки. В связи с тем, что эти эффекторные клетки способны специфически разрушать клетки-мишени, их называют ЦИТОТОКСИЧЕСКИМИ Т-ЛИМФОЦИТАМИ, или Т-КИЛЛЕРАМИ - убийцами (от англ. to kill - убивать). Т-киллер — одна из основных эффекторных клеток клеточноопосредованного иммунитета, которая наряду с другими клетками способна осуществлять лизис клеток мишеней. Роль Т-киллеров очень велика в реализации трансплантационного иммунитета, развитии аутоиммунных заболеваний, в противоопухолевой защите. Тk-лимфоциты (CD8+ клетки) составляют около 20 – 25% от числа циркулирующих Т-лимфоцитов (абсолютноеколичество - 500 – 1200 в 1 мм3 (мкл)), они несут маркерный антиген CD8 . Макромолекула CD8 служит корецептором для антигенов главного комплекса гистосовместимости I класса (ГКГС-1). Активированные антигеном цитотоксические клетки – Т-киллеры связываются с антигенами на поверхности клеток и, выделяя белок перфорин, разрушают их. При этом Т-киллер остается жизнеспособным и может разрушать следующую клетку. Действие перфорина подобно МАК системы комплемента. Белок перфорин, полимеризуясь в мембране клетки-мишени, образует поры – каналы, тем самым, вызывая её осмотический лизис. Кроме того, цитотоксический Т-лимфоцит через пору, образованную перфорином в клетке-мишени, вбрасывает гранзимы (ферменты – сериновые протеазы), которые запускают программу апоптоза. Установлено также, что своё цитотоксическое действие Т- лимфоциты могут реализовывать путем экспрессии FasL и с его помощью индуцировать Fas-опосредованный апоптоз мишени.
«Наивные» Т-лимфоциты – это те лимфоциты, которые не встретились с антигеном и они составляют часть общего пула рециркулирующих Т-клеток.
Т-клетки иммунологической памяти – это долгоживущие лимфоциты, потомки клеток, встречавшихся с антигенами и сохраняющие к ним рецепторы. Т-ЛИМФОЦИТЫ ИММУНОЛОГИЧЕСКОЙ ПАМЯТИ - после стимуляции антигеном способны сохранять информацию о нем до 10—15 лет и передавать ее другим клеткам. Эти клетки защищены от апоптоза. Благодаря наличию в организме Т-клеток памяти обеспечивается ускоренный иммунный ответ по вторичному типу при повторном попадании данного антигена в организм. Этим объясняется форсированная динамика вторичного иммунного ответа. Маркером Т- лимфоцитов памяти является мембранный антиген CD45RO.
Раньше ошибочно выделяли субпопуляцию Т-супрессоров, которые считались ответственными за
подавление иммунного ответа. Однако в настоящее время показано, что самостоятельной субпопуляции Т-супрессоров нет. В угнетении, подавлении иммунного ответа решающее значение играет апоптоз простимулированных лимфоцитов, а также цитокин – трансформирующий фактор роста β.
Около 10 % лимфоцитов не имеют ни Т-, ни В-маркеров, они не относятся ни к Т-, ни к В-лимфоцитам и ранее получили название НУЛЕВЫЕ ЛИМФОЦИТЫ . Эта разнородная популяция лимфоцитов в зависимости от их морфофункциональных особенностей подразделяется на: l ЕСТЕСТВЕННЫЕ (natural) КИЛЛЕРНЫЕ КЛЕТКИ (сокращенно ЕКК=ЕК=NK-клетки) и l КИЛЛЕРНЫЕ КЛЕТКИ (К-клетки). Общей особенностью ЕК- и К-клеток является способность лизировать клетки-мишени без предварительной сенсибилизации, что необходимо Т-лимфоцитам-киллерам. Морфологически это лимфоциты большого размера с зернистой цитоплазмой. Дифференцируются из общей клетки предшественника лимфоцитов (LSC).
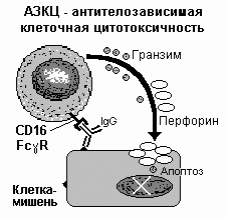 Естественные киллеры не зависят в своем развитии от вилочковой железы. Экспрессируют на своей поверхности рецепторы к интерферону-γ и интерлейкину-2 (ИЛ 2). Функционально они являются цитотоксическими клетками киллерами, но на NK нет антигенраспознающих рецепторов, которые обязательно присутствуют на Т-киллерах. Натуральных киллеров на клетку мишень наводят антитела IgG специфичные к мембранным антигенам клетки-мишени. Первоначально антитела связываются с антигеном на клетке, а затем с помощью Fc рецептора к IgG (FcγRIII) NK присоединяется к этому комплексу АТ - АГ-клетки-мишени. Функция ЕК-клеток в организме заключается в защите от развития опухолей, вирусов и др. Основными их маркерами являются CD16 и CD56. (FcγRIII по CD- номенклатуреэто CD16). Разрушение клетки-мишени ЕК осуществляет с помощью перфорина. Содержание ЕК (CD16+ клеток) у здоровых людей – 8 – 22%. Естественные киллеры не зависят в своем развитии от вилочковой железы. Экспрессируют на своей поверхности рецепторы к интерферону-γ и интерлейкину-2 (ИЛ 2). Функционально они являются цитотоксическими клетками киллерами, но на NK нет антигенраспознающих рецепторов, которые обязательно присутствуют на Т-киллерах. Натуральных киллеров на клетку мишень наводят антитела IgG специфичные к мембранным антигенам клетки-мишени. Первоначально антитела связываются с антигеном на клетке, а затем с помощью Fc рецептора к IgG (FcγRIII) NK присоединяется к этому комплексу АТ - АГ-клетки-мишени. Функция ЕК-клеток в организме заключается в защите от развития опухолей, вирусов и др. Основными их маркерами являются CD16 и CD56. (FcγRIII по CD- номенклатуреэто CD16). Разрушение клетки-мишени ЕК осуществляет с помощью перфорина. Содержание ЕК (CD16+ клеток) у здоровых людей – 8 – 22%.
К-клетки неоднородная группа клеток, несущая на своей поверхности рецепторы к Fc- фрагменту Ig G и способны к антителозависимой клеточной цитотоксичности. К ним относятся моноциты, нейтрофилы, макрофаги, эозинофилы, конечно НК и некоторые лимфоциты. Антителозависимая
клеточноопосредованная цитотоксичность (АЗКЦ) является своеобразным отражением связи между гуморальным и клеточным звеньями иммунной системы. Антитела выступают в роли «наводчиков» клеток-эффекторов на клетки-мишени, несущие чужеродные антигены.
Все лимфоциты (Т-, В-, ЕК- и К-клетки) обладают способностью к миграции и рециркуляции, что обеспечивает повсеместный контроль за размножением клеток собственного организма, а при проникновении чужеродного антигена —генерализированный иммунный ответ и сохранение иммунологической памяти об антигене.
Приложение 1
КЛАСТЕРЫ ДИФФЕРЕНЦИРОВКИ (CD-антигены) ЛЕЙКОЦИТОВ
В процессе дифференцировки на мембранах клеток системы иммунитета появляются макромолекулы – маркеры, соответствующие определенной стадии развития, морфологической дифференцировки клетки. Они получили название CD-антигенов (от английского – clusters of differentiation – кластеры дифференцировки). В настоящее время их известно более 200. С помощью поверхностных антигенных маркеров (дифференцировочных антигенов, CD) возможно определить направление развития, степень зрелости клеток, популяцию и субпопуляцию клеток, стадию их дифференцировки и активации. Дифференцировочные антигены, таким образом, служат специфическими маркерами. По таким антигенам дифференцируют в частности субпопуляции лимфоцитов и других иммунокомпетентных клеток.
· CD1 - a, b, c; его несут кортикальные тимоциты, субпопуляции В-клеток, клетки Лангерганса, является общим антигеном тимоцитов, белок, подобен антигенам 1класса гистосовместимости, ММ 49 КД.
· v CD2 - маркер всех Т-клеток, имеют также большинство ( 75%) ЕК, известны три эпитопа молекулы, один из которых связывает эритроциты барана (Е-рецептор); является адгезивной молекулой связывается с CD58 (LFA III), LFA IV, передает трансмембранные сигналы при активации Т-клеток; ММ 50 КД. Выявить этот антиген можно реакцией розеткообразования. Реакция Е-розеткообразования является показателем суммы клеток (Т-л, ЕК, LAK), несущих CD2-кластер. Таким образом, CD2 –антиген не является абсолютным маркером Т-лимфоцитов, так как присутствует и на других клетках.
· v CD3 – несут все зрелые Т-лимфоциты, обеспечивает передачу сигнала от Т-клеточного антигенспецифического рецептора (ТКР) в цитоплазму, состоит из пяти полипептидных цепей (γ, δ, ε, ι, ξ). ММ – 25 КД; антитела к нему усиливают или ингибируют функцию Т-клеток. Важный маркёр Т- лимфоцитов.
· v CD4 – маркер Т-хелперов, рецептор к вирусу иммунодефицита человека (ВИЧ), имеется на
некоторых моноцитах, клетках глии; трансмембранный гликопротеин, участвует в распознавании
антигенов, ассоциированных с молекулами II класса гистосовместимости (HLA-DR), ММ 59 КД. (Рецептор для АГ ГКГС класса ll).
· v CD5 – имеют зрелые и незрелые Т-клетки, трансмембранный гликопротеин, член семейства рецепторов – “мусорщиков”, как и CD6, является лигандом для CD72 на В-клетках, участвует в пролиферации Т- клеток. CD5 так же имеют В-1-лимфоциты – субпопуляция В-клеток, с преимущественной локализацией в брюшной и плевральной полостях. ММ 67 КД.
· CD6 – несут зрелые Т-клетки и частично В-клетки имеют все Т-клетки и тимоциты, часть В-клеток; входит в семейство «мусорщиков», ММ 120 КД.
· CD7 – имеют Т-клетки, ЕК (Fcμ рецептор IgM); ММ 40 КД.
· v CD8 – маркер цитотоксических Т-лимфоцитов, имеют некоторые ЕК, структура адгезии, вовлекается в распознавание антигенов при участии молекул гистосовместимости 1 класса, состоит из двух S-S цепей , ММ 32 КД. (Корецептор для комплекса АГ + ГКГС класса l).
· CD9 – несут моноциты, тромбоциты, гранулоциты, В-клетки фолликулярных центров, эозинофилы, базофилы, эндотелий, ММ 24 КД.
· CD10- имеют незрелые В-клетки (GALLA – антиген лейкозных клеток), часть тимоцитов, гранулоцитов; эндопептидазаэяяюя, ММ 100 КД.
· CD11a – несут все лейкоциты, молекула цитоадгезии, αL цепь интегрина LFA-1, ассоциирована с CD18; рецептор для лигандов: CD15 (ICAM-1), CD102 (ICAM-2) и CD50 (ICAM-3) молекул; отсутствует у больных с LAD-1 синдромом (синдром дефицита молекулы адгезии), ММ 180 КД.
· v CD11b – (CR3- или c3bi-рецептор) – несут моноциты, гранулоциты, ЕК, αМ цепь интегрина, ассоциирована с CD18молекулой; рецептор для лигандов: CD54 (ICAM-1), C3bi-компонента комплемента (CR3-рецептор) и фибриногена; отсутствует при LAD-1 синдроме: ММ 165 КД.
· v CD11c (CR4-рецептор) – имеют моноциты, гранулоциты, ЕК, активированные Т- и В-лимфоциты, αХ цепь интегрина (ассоциирована с CD18, является четвертым типом рецептора (CR4) для компонентов C3bi, C3dg комплемента; его лиганды– СD54 (ICAM-1), фибриноген; ММ 95/150 кД.
· CD13 – имеют все миелоидные, дендритные и эндотелиальные клетки, аминопептидаза N, рецептор для коронавируса, ММ 150 КД.
· v CD14 – имеют моноциты/макрофаги, гранулоциты, рецептор для комплексов ЛПС с ЛПС-
связывающим белком и для PI-молекул тромбоцитов; отсутствует у больных с пароксизмальной ночной гемоглобинурией (PNH), антитела к нему могут вызывать окислительный взрыв в моноцитах, ММ 55 КД.
· CD15 – (Lewis) – имеют гранулоциты, слабо экспрессируют моноциты, некоторые антитела к нему
подавляют фагоцитоз.
· CD15s – (sialyl-Lewis) – имеют миелоидные клетки, лиганд для CD62P (P-селектин), CD62E (E-селектин), CD62L (L-селектин), отсутствует у больных LAD-2.
· v CD16 – несут ЕК, нейтрофилы, некоторые моноциты, (низкоаффинный Fc-рецептор для IgG),
интегральный мембранный белок (Fcγ RIIIA) на ЕК и макрофагах, PI-связывающая форма (Fcγ RIIIB) на нейтрофилах, отсутствует у больных с PNH – пароксизмальной ночной гемоглобинурией.
· CD18 – имеют большинство лимфоидных и миелоидных клеток, молекула адгезии, β2 цепь интегрина LFA, ассоциирован с αCD11 a, b, c, отсутствует при LAD-1 синдроме, ММ 95 КД.
· v CD19 – (В4) – имеют пре-В и В-клетки, часть их рецепторного комплекса вовлекается в их активацию (сигнал трансдукции, ассоциирован с CD21 (CR2); ММ 95 КД. Важный маркёр В-клеток.
· v CD20 – (В1) – несут все В-клетки и дендритные клетки в фолликулах, участвует в активации через кальциевые каналы клеток, ММ 35 кДа.
· v CD21 – (CR2 рецептор, В2) - имеют субпопуляции В-клеток, некоторые тимоциты, Т-клетки, рецептор для С3d компонента комплемента и для вируса Эпштейна-Барра, участвует в регуляции активации комплемента (RCA) наряду с CD35, CD46 CD55 и в активации В-клеток. |
 Скачать 0.79 Mb.
Скачать 0.79 Mb.





